含磺酸基和氮氧自由基共聚合物的合成及性能研究*
朱军峰,拓 欢,朱 婷,高薇春,张万斌
(陕西科技大学 化学与化工学院 陕西省轻化工助剂化学与技术重点实验室,西安 710021)
0 引 言
二次电池正极材料的研究是当前新能源领域的一个热点问题,传统的正极材料多以无机金属氧化物为主,其电子转移受制于锂离子在电极中较慢的“嵌入”和“脱嵌”的动力学过程,限制了其能量密度的提升[1],且制备所需能量高及CO2排放量高的问题也限制了其工业化生产[2-3],有机自由基聚合物能够发生快速稳定的电子自交换反应同时具有环境友好性[4-5],因此作为一种新型高能量密度正极材料进入人们的视野。
自2002年聚(4-甲基丙烯酰氧基-2,2,6,6-四甲基哌啶氮氧自由基)(PTMA)作为正极材料首次应用于二次电池,人们发现这种自由基聚合物在充放电循环的过程中具有优异的倍率性能及循环稳定性,在电池、电子器件和存储领域有着潜在应用价值[6]。将带有离子活性基团的化合物以共聚合方式引入PTMA主链上,能够提供更多导电载流子(自由电子,正负离子或空穴)[7-8],更易传递电子,增加其导电性。苯乙烯磺酸钠是一种带有活性阴离子基团的化合物,其阴离子基团能够有效促进氧化态自由基被氧化,促进锂离子在聚合物/电解质界面的迁移,且苯环的共轭结构能够使游离态电子有效传输,从而增强氮氧自由基聚合物PTMA的导电性能,提升其作为有机电池电极材料的应用性[9-12]。
本文以苯乙烯磺酸钠作为电荷平衡的阴离子活性基团,通过无规共聚的方法得到共聚产物PTMA-co- PSS,对其进行结构表征,并将目标产物应用于锂离子电池正极材料,通过组装扣式电池测试并分析电化学性能[13]。该结果对改性自由基聚合物PTMA以及带离子侧基的氮氧自由基聚合物在二次电池电极中的应用研究具有一定指导意义。
1 实验部分
1.1 试剂与仪器
主要试剂:4-甲基丙烯酸-2,2,6,6-四甲基哌啶醇酯、苯乙烯磺酸钠、偶氮二异丁腈(AIBN,经乙醇重结晶后使用)、间氯过氧苯甲酸(mCPBA),购于上海麦克林生化科技有限公司;甲醇、正己烷、无水乙醇、四氢呋喃,N,N-二甲基吡咯烷酮,购于天津市科密欧化学试剂有限公司;以上试剂均为分析纯。
主要仪器:ADVANCEⅢ 400 MHz型核磁共振仪,德国Bruker公司;VECTOR-22型傅里叶红外光谱仪,德国Bruker公司;MaXisTOF型液相/质谱联用仪(HPLC-MS),德国Bruker公司;E500电子顺磁共振仪(EPR),德国Bruker公司;AXISSUPRA型X光电子能谱仪(XPS),英国Kratos公司;Waters 2695型凝胶渗透色谱仪,美国Waters公司;Parstat Mc型电化学工作站,美国Princeton公司。
1.2 实验方法
1.2.1 PTMPM-co-PSS的合成
将甲醇与水(8 mL,2/1,v/v)加入到10 mL Schlenk管中作为溶剂,将1.0 g(4.4 mmol) 4-甲基丙烯酸-2,2,6,6-四甲基哌啶醇酯、0.92 g(4.4 mmol)已重结晶过的苯乙烯磺酸钠和10.0 mg偶氮二异丁腈(AIBN)混合加入到Schlenk管中,依次用生胶和透明胶带对反应管进行密封操作,进行不少于3次冷冻-真空-解冻循环后,在65 ℃下搅拌反应10 h,将产物滴加到正己烷中,过滤收集沉淀,真空干燥12 h得到产物PTMPM-co-PSS(如图1)。

图1 PTMPM-co-PSS的合成Fig 1 Synthesis of PTMPM-co-PSS
1.2.2 PTMA-co-PSS的合成
用上步产物PTMPM-co-PSS(200 mg)溶解于6 mL无水乙醇中,再添加400 mg间氯过氧苯甲酸(mCPBA),在室温下持续搅拌12 h。将氧化后的产物滴加至NaCO3溶液中(质量分数为10%),静置分层,取上层有机相,滴加至正己烷中沉降3次,收集沉淀在真空中完全干燥,得到最终产物PTMA-co-PSS(如图2)。

图2 PTMA-co-PSS的合成Fig 2 Synthesis of PTMA-co-PSS
1.3 扣式电池组装及电化学性能测试
将合成的PTMA-co-PSS、乙炔黑和聚四氟乙烯按8:1:1的质量比混合研磨均匀,加入N,N-二甲基吡咯烷酮研磨至粘稠状,涂膜于铝箔上,放入真空干燥箱干燥12h后切片作为电池正极,以金属锂片作为负极,以1 mol·L-1LiPF6/EC+DMC(体积比为1∶1)混合溶液为电解液,在手套箱中组装成CR2025型扣式电池,在开路电位下测试电池电化学阻抗,电压值振幅为10 mV,频率范围100 kHz~0.1 Hz;在充放电电压范围为2.0~4.3 V,电流密度为200 mA·g-1下进行恒流充放电测试。
2 结果与讨论
2.1 PTMPM-co-PSS的1HNMR分析
将产物PTMPM-co-PSS以DMSO为氘代试剂测试核磁氢谱,参照文献数据分析[14],图3中7.41 ppm为苯环上靠近磺酸根基团的两个质子峰,6.67 ppm处的化学位移为侧链苯环上靠近主链的两个质子峰,4.98 ppm处为哌啶醇酯双键聚合后吸收峰,1.69 ppm处为亚甲基和次甲基的质子峰两种类型的质子峰重叠在一起,1.08 ppm处的宽峰为聚合物主链上哌啶四个甲基侧基的化学位移,化学位移在5.30~5.34 ppm与5.81~5.87 ppm处碳碳双键上亚甲基的质子吸收峰以及在6.67~6.77 ppm处碳碳双键上次甲基的质子吸收峰均消失,说明发生碳碳双键的聚合,证明4-甲基丙烯酸-2,2,6,6-四甲基哌啶醇酯与苯乙烯磺酸钠发生聚合反应,生成共聚物PTMPM-co-PSS。
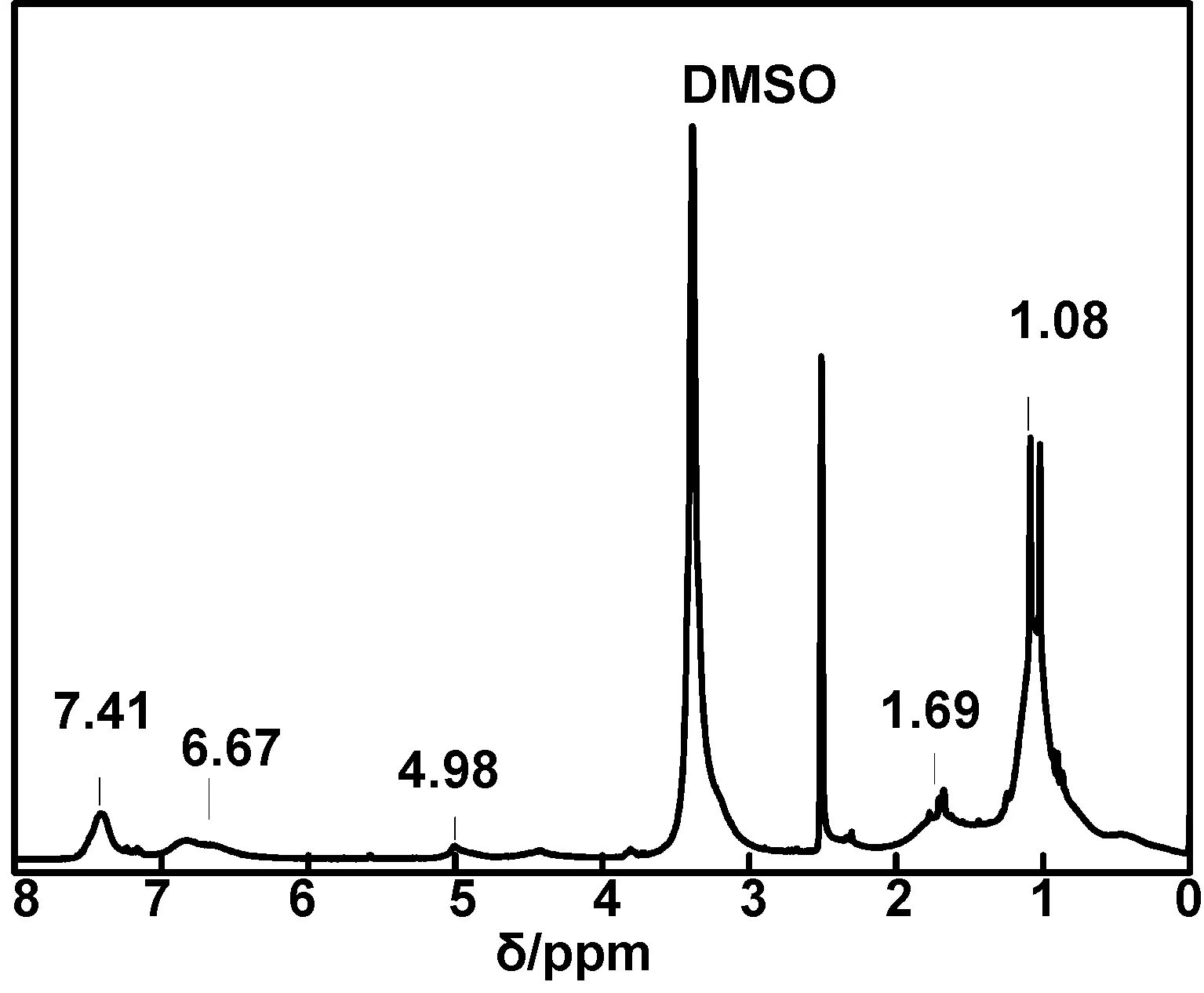
图3 PTMPM-co-PSS的核磁共振氢谱图Fig 3 HNMR of PTMPM-co-PSS
2.2 PMTMP-co-PSS和PTMA-co-PSS的FT-IR分析
使用KBr压片法进行傅立叶红外测试,如图4所示,3 480 cm-1处是仲胺基的伸缩振动吸收峰,2 980 cm-1是甲基的反对称伸缩振动及亚甲基的伸缩振动吸收峰,1 720 cm-1是酯(-COO)的伸缩振动吸收峰,1 600和1 480 cm-1是苯环上C=C的伸缩振动吸收峰,1 390 cm-1是甲基弯曲振动吸收峰,1 180 cm-1,1 040 cm-1是磺酸盐的反对称伸缩振动吸收及对称伸缩振动吸收峰,850 cm-1是苯环上C-H的二元取代(对位)面外弯曲吸收峰,以上主要特征结构可以证实合成的共聚产物应该为PTMPM-co-PSS。比较而言,PTMA-co-PSS的红外谱图也存在2970 cm-1处甲基的反对称伸缩振动,1 710cm-1处酯(-COO)的伸缩振动吸收峰,但3 500 cm-1附近仲胺基的伸缩振动吸收峰消失,说明被氧化成氮氧自由基,860 cm-1出现苯环上C-H的二元取代(对位)面外弯曲吸收峰。从以上主要特征结构可以判断出,PTMPM-co-PSS已经被氧化为PTMA-co-PSS[15]。

图4 PTMPM-co-PSS和PTMA-co-PSS的红外谱图Fig 4 FT-IR of PTMPM-co-PSS and PTMA-co-PSS
2.3 PMTMP-co-PSS和PTMA-co-PSS的XPS分析
因N原子不参与氧化反应,故可用氮信号变化分析PTMPM-co-PSS的氧化结果[16-17]。如图5(a)X光电子能谱全谱中可以清晰地看到N1s信号,此外,如图5(b)所示,N1s高分辨谱证实了氮的两种不同化学状态,较低结合能397.2 eV处应为哌啶环上N-H键结合能,随着氧化态增加,侧基氧化结合能上升,因此相比于氧化前的PTMPM-co-PSS,氧化后PTMA-co-PSS在399.6 eV处出现N-O·相关的信号峰,通过PTMA-co-PSS大分子链上的自由基N-O•对应的位点来进一步分析,可以证实PTMPM-co-PSS被mCPBA成功氧化成含有磺酸盐的自由基聚合物PTMA-co-PSS。
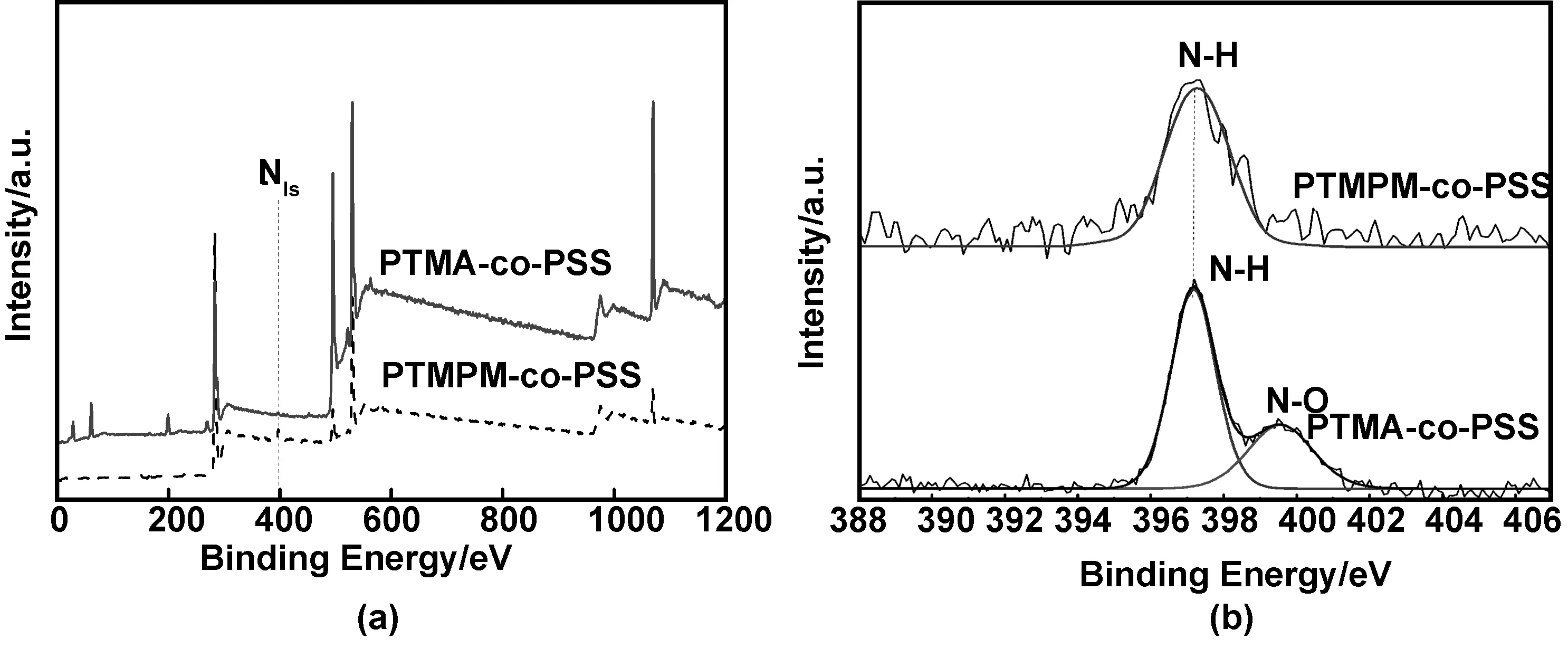
图5 PTMPM-co-PSS和PTMA-co-PSS的(a)X光电子能谱全扫描谱图和(b)N1s高分辨谱图Fig 5 XPS survey spectra and N1s region spectra of PTMPM-co-PSS and PTMA-co-PSS
2.4 PTMA-co-PSS的UV-vis分析
以氯仿作为溶剂,对PTMPM-co-PSS和PTMA-co-PSS进行紫外可见光谱的测试,从图6可知,相比于PTMPM-co-PSS,PTMA-co-PSS在400~450 nm处出现π-π*的紫外特征吸收峰,这与氮氧稳定自由基N-O·所呈现出来的橙红色有关,此处应为它的特征吸收峰[18-19],这也进一步说明共聚物PTMPM-co-PSS中的N-H被氧化为自由基聚合物PTMA-co-PSS中的稳定的N-O·。
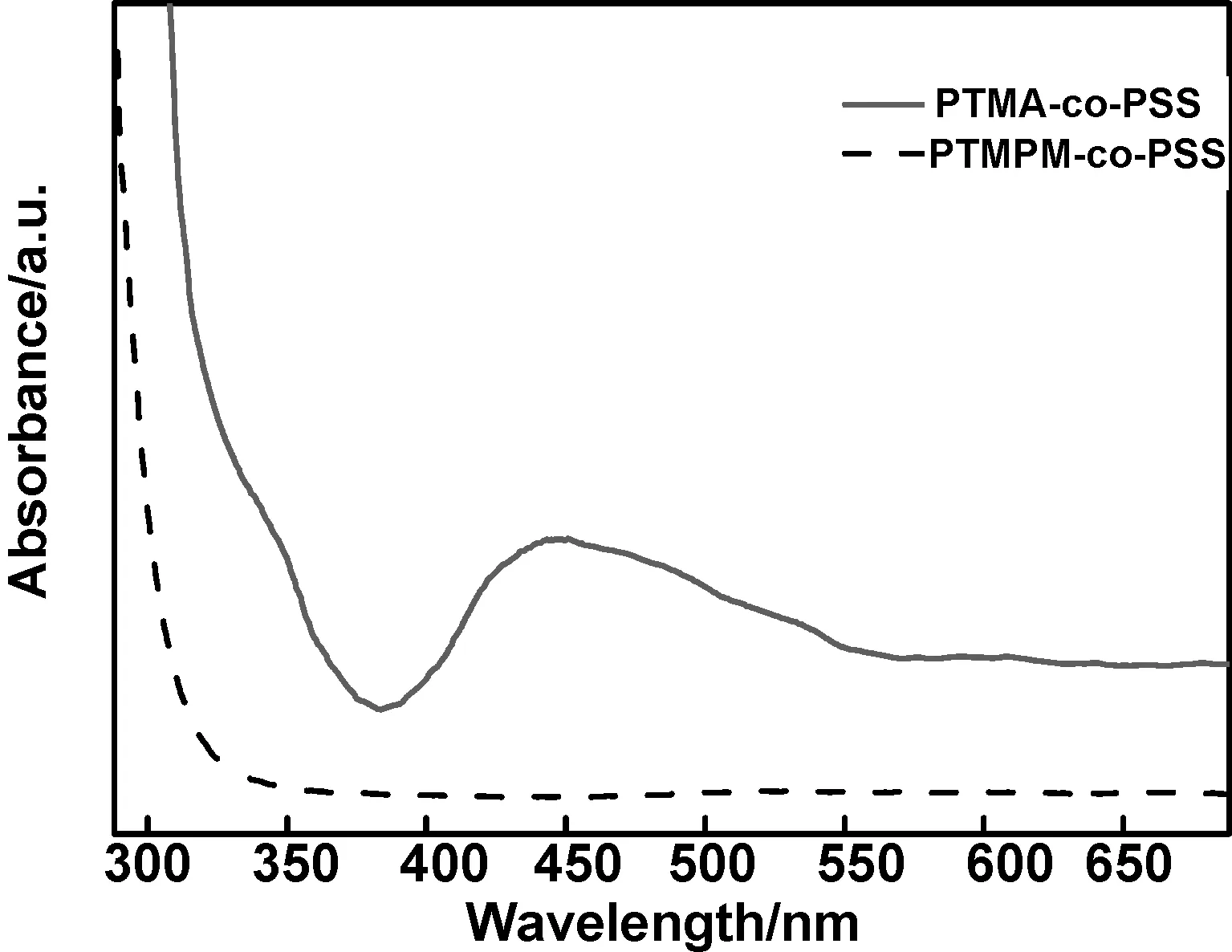
图6 PTMPM-co-PSS和PTMA-co-PSS的紫外可见光谱图Fig 6 UV-vis of PTMPM-co-PSS and PTMA-co-PSS
2.5 PTMA-co-PSS的EPR分析
电子顺磁共振是检验氮氧自由基存在与否最简便直观的一种方法,将样品溶于THF进行电子顺磁共振测试,从图7可以看出合成的共聚物PTMA-co-PSS的EPR信号与TEMPO信号峰基本一致,说明PTMA-co-PSS中已经存在氮氧自由基结构,信号稍有不对称可能是由于共聚后带磺酸盐基团的苯环结构使电子云发生偏移,对孤对电子产生了影响。同时由公式h=gβH可计算出PTMA-co-PSS的g值为2.0049,这与TEMPO的g值2.0056非常相近,由此可以进一步证明确实成功合成了含有氮氧自由基结构的共聚物PTMA-co-PSS。

图7 PTMA-co-PSS的电子顺磁共振光谱图Fig 7 EPR of PTMA-co-PSS
2.6 PTMA-co-PSS的GPC分析
为表征PTMA-co-PSS的相对分子质量及其分布,以THF为流动相对共聚物做凝胶渗透色谱测试,从图8可以看出GPC曲线呈单峰对称分布,且无肩峰存在,这说明体系中只有单一组分物质;从表1可以看出,PTMA-co-PSS的重均分子量Mw为1.67×104,数均分子量Mn为1.07×104,多分散性指数PDI为1.56,表明通过无规共聚合成的产物分子量分布较窄。

图8 PTMA-co-PSS的凝胶渗透色谱图Fig 8 GPC of PTMA-co-PSS

表1 自由基聚合物PTMA-co-PSS的分子量及其分布Table 1 Molecular weight and distribution of PTMA-co-PSS
2.7 PTMA-co-PSS的交流阻抗图分析
组装扣式电池并在开路电位下测量交流阻抗,图9为PTMA及PTMA-co-PSS作为正极活性材料在充放电前的交流阻抗谱图,交流阻抗图有低频区半圆和高频区斜线组成,同时高频区斜线趋近于竖直,低频区半圆与电极材料和电解质溶液之间的电荷转移电阻有关[15],经拟合计算,PTMA-co-PSS作为电极材料的电荷转移电阻168Ω,这说明PTMA-co-PSS的电化学转移阻抗较小,容易进行电化学反应,这是因为含有离子空穴的自由基聚合物得到有效活化了,同时也表明共聚物有较好的电荷传输动力学特征。
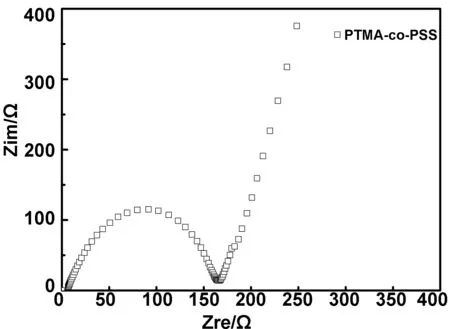
图9 PTMA-co-PSS的电化学阻抗分析图Fig 9 EIS of PTMA-co-PSS
2.8 PTMA-co-PSS的充放电容量及库伦效率分析
从图10中可以看到电池首次放电比容量为99.08 mAh/g,首次充电比容量为92.97 mAh/g,相应的首次库伦效率为93.83%,这可能是首次充放电时阴离子空穴尚未完全活化,在充放电循环50圈后,比容量为71.97 mAh/g左右,容量保持率74.95%,充放电循环100次后,比容量降到了67.50 mAh/g,容量保持率为70.83%,循环100次后库伦效率持续稳定且趋于100%,这说明阴离子空穴已经完全得到活化使得活性材料具备了很好的循环可逆性,同时PTMA-co-PSS的充放电容量亦高于PTMA充放电容量[20],表明在电池循环过程中活性材料PTMA-co-PSS具有较好的储锂性能和有优良的循环性能。

图10 PTMA-co-PSS的充放电循环性能和库伦效率图Fig 10 Charge and discharge cycling performance and coulombic efficiency of PTMA-co-PSS
3 结 论
以4-甲基丙烯酸-2,2,6,6-四甲基哌啶醇酯和苯乙烯磺酸钠为原料,通过内自由基聚合法合成了共聚物并氧化得到目标产物PTMA-co-PSS,通过1HNMR、FT-IR 等手段对所合成的产物进行表征,通过XPS、EPR、UV-vis等进一步确定了目标产物中N-O·存在。
通过对组装扣式电池,分析PTMA-co-PSS作为正极活性材料的电化学阻抗和充放电循环,证明相比于 PTMA-co-PSS作为正极材料电荷转移电阻为168 Ω,首次放电比容量为99.08 mAh/g,首次充电比容量为92.97 mAh/g,经过100次循环后容量稳定在67.50 mAh/g,保持率为70.83%,库伦效率接近100%,表明PTMA-co-PSS作为电极活性材料循环可逆性能良好,循环寿命稳定,在有机二次电池材料中具有潜在应用前景。

