金属化多级孔密胺材料的催化性能
刘恩华,张天琪,尹 健,张宇峰,4,孟建强
(1.天津工业大学 省部共建分离膜与膜过程国家重点实验室,天津 300387;2.天津工业大学 材料科学与工程学院,天津 300387;3.天津宝钢稀土研究院有限公司,天津 300300;4.天津城建大学 环境与市政工程学院,天津 300384)
现代社会对化石燃料的严重依赖导致了CO2的过量排放与全球气候变暖、威胁海洋生物生存等问题[1]。同时,CO2为可再生碳经济创造了可能性,它已被作为高效的单碳(C1)来源,大量用于生产有价值有机化合物,如甲酸、一氧化碳、循环碳酸盐等[2]。因此,有必要制定可行的CO2捕集和转化策略,以减少碳排放。采用具有亲和/浓缩CO2性能的材料,提高CO2浓度能够有效促进CO2的转化速率。具有高催化性能、合成方法简单、廉价的催化剂,对于CO2转化的应用尤为重要,因此需要高效且经济的催化剂生产以避免额外的CO2排放和能源成本。到目前为止,已经报道了多种功能材料,可以实现CO2捕获和/转化[3-5],包括胺溶液、离子液体、金属有机配和多孔材料等。其中,多孔材料因为其易分离且具有良好的催化再生性能而备受关注。例如,金属有机框架(MOFs)在过去10 年中由于其结构与功能的多样性而被广泛研究,应用于捕获和转化CO2。然而,MOF 的应用受到其稳定性以及其他问题的影响[6-8]。与MOF 类似,多孔有机聚合物(POPs)继承了其结构中各种官能化单体所提供的优异的物理和化学可调性;此外,强共价键保证聚合物的化学稳定性,具有高比表面积的多孔聚合物结合特定的催化位点,更适用于CO2捕获/转化[9-11]。研究表明,具有良好的CO2亲和性和高比表面积的多孔密胺(PMF)是理想的材料之一。
事实上,多孔PMF 聚合物已经研究多年。Deryło-Marczewska 等[12]通过使用气相二氧化硅作为硬模板来合成介孔PMF 树脂以引入多孔结构。Kailasam 等[13]报道了通过软模板法制备的介孔PMF 聚合物以形成多孔结构。然而,在这些工作中,所得到的聚合物由柔性交联分子链组成,具有低比表面积。Tan 等[14]通过形成刚性多孔有机骨架,制备了具有高比表面积的多孔PMF 聚合物。
此前,本课题组通过以三聚氰胺和多聚甲醛为反应单体,以二甲基亚砜(DMSO)为连续相溶剂、Isopar M 为分散相溶剂,泊洛沙姆F127 为稳定剂,通过高内相乳液聚合,一步法制备出具有微孔、介孔、大孔的多级孔结构材料[15]。但在高内相乳液制备过程中,需要额外加入大量长链烷烃作为内相乳液,不利于工业化生产。本文提出了一种简易的多孔密胺制备方法,吸附铜离子后,用于氧化苯乙烯与CO2的环加成催化反应。通过在三聚氰胺和多聚甲醛的共聚体系中加入致孔剂泊洛沙姆F127,利用水热法制备出了具有多孔结构的密胺材料,负载铜离子后作为环加成催化反应的催化剂,使其具有优秀的催化性能。
1 实验部分
1.1 主要试剂及仪器
主要试剂:三聚氰胺,分析纯,百灵威科技有限公司产品;多聚甲醛、醋酸铜、四丁基溴化铵、氧化苯乙烯、氘代氯仿(0.03 v/v TMS),均为分析纯,上海阿拉丁生化科技有限公司产品;泊洛沙姆F127,分析纯,西格玛奥德里奇(上海)贸易有限公司产品;甲醇、四氢呋喃、丙酮,均为分析纯,天津科密欧化学试剂有限公司产品。
主要仪器:0551-62921227 型水热釜,安徽科幂机械科技有限公司产品;SHZ-D 型循环水式真空泵,浙江黄岩求精真空泵公司产品;TGL-16C 型离心机,上海安亭科学仪器厂产品;SLM 型高温高压反应釜,北京世纪朗森实验仪器有限公司产品;Vector22 型傅里叶变换红外光谱仪、400M 型核磁共振仪,均为德国Bruker 公司产品;STA409PC 型热重分析仪,德国NETZSCH 公司产品;K-Alpha 型X 射线光电子能谱,美国Thermo Scientific 公司产品;S-4800 型场发射扫描电子显微镜、JEOL JEM-2100F 型高分辨透射电子显微镜,均为日本Hitachi 公司产品;3H-2000PM型比表面积测试仪,贝士德仪器科技有限公司产品;Perkinelmer 8300 型电感耦合等离子体质谱仪,铂金埃尔默股份有限公司产品。
1.2 Cu@PMF催化颗粒的制备
将4.62 g 的泊洛沙姆F127 和12 mL 的二甲基亚砜加入到250 mL 三口烧瓶中,70 ℃的温度下溶解1 h,然后加入 1.134 g 三聚氰胺(9 mmol)和 0.486 g 多聚甲醛(16.2 mmol),95 ℃加热 2 h。然后将其填入入水热釜(50 mL)中,旋紧后放在烘箱中,170 ℃的温度下加热72 h。聚合完成后,将固体样品在足量的四氢呋喃中搅拌6 h,抽滤后将样品在足量丙酮中搅拌6 h,抽滤后,将颗粒在120 ℃烘箱中干燥12 h,然后将颗粒加入到0.1 mol/L 的Cu2+的溶液中搅拌24 h,过滤后再用甲醇冲洗,再在80 ℃的烘箱中干燥6 h。
1.3 Cu@PMF颗粒的表征
1.3.1 红外(FT-IR)测试
将Cu@PMF 颗粒于80 ℃真空干燥6 h。用Vector22型红外光谱仪对其进行测试分析。
1.3.2 热重测试(TG)
将 Cu@PMF 颗粒于 80 ℃真空干燥 6 h。用STA409PC 型热重分析仪测试其热稳定性。氮气保护下,从 25 ℃升温到 800 ℃,升温速率为 20 ℃/min。
1.3.3 X 射线光电子能谱法(XPS)
用ThermoFisher K-Alphα 型X-射线光电子能谱仪对接枝改性前后的纤维素膜表面元素组成及相对含量进行分析。XPS 中的X 射线源采用K-Alkα(1 486.6 eV),扫描全谱图的测试能量范围是0~1 000 eV,样品分析深度可达到2 nm,其分析准确精度达到1%~2%。
1.3.4 颗粒形貌观测(SEM 和TEM)
用S-4800 型号场发射扫描电子显微镜观测Cu@PMF 颗粒的粒径和表面形貌。用JEOL JEM-2100F 型号高分辨透射电子显微镜观测Cu@PMF 颗粒的微孔结构。
1.3.5 比表面积测试仪
用3H-2000PM 型号比表面积测试仪测试Cu@PMF 颗粒的比表面积以及孔径分布。脱气条件为100 ℃,10 h。
1.3.6 液态氢谱核磁法(1H NMR)
环加成催化反应的转化率由液相1H NMR 测试计算得到。液相1H NMR 光谱由Bruker400 光谱仪记录,含有TMS 的 CDCl3用作内参照,CHCl3的残留 H 峰为7.26×10-6。根据制备的环氧标准曲线、峰面积比值可以计算得到产率。
1.4 环加成催化反应
1.4.1 高温高压催化反应
先将 CO2通入高温高压反应釜(50 mL)10 min 以排出其中空气,然后将16 mg 多级孔结构的密胺颗粒、15 mL 环氧丙烷和464 mg 四丁基溴化铵加入反应釜中,然后将CO2压力缓慢增加到2 MPa,初始压力表显示2 MPa,在停止通气后压力示数会有一定程度的降低,反应器设定搅拌速率150 r/min,温度为100 ℃。当反应器温度升至100 ℃,开始计时0.5 h,当反应结束后,将反应器取出放置在水中进行降温,降至室温后将残留CO2放出。用5 mL 离心管将反应后的混合物取出,在6 000 r/min 的离心机中离心30 min,取上层清液,用其测量反应转化率。产物用1,1,2,2-四氯乙烷作为内标,用液态氢谱核磁进行测试,得到产率。
1.4.2 常温常压催化反应
先将 CO2通入三口烧瓶(250 mL)10 min 以排出其中空气,然后将16 mg 多级孔结构的密胺颗粒、100 mL 环氧丙烷和464 mg 四丁基溴化铵加入三口烧瓶中,然后将充满CO2气体的气包连接上三口烧瓶以提供CO2气氛,反应搅拌速率设定为150 r/min,温度为25 ℃。反应55 h 后,停止搅拌,待催化颗粒沉淀后,取上层清液,用其测量反应转化率。产物用1,1,2,2-四氯乙烷作为内标,用液态氢谱核磁进行测试,得到产率。
2 结果与讨论
2.1 红外分析与热重分析
图1 为Cu@PMF 的红外分析图和热重分析图。
图1(a)是具有多级孔的密胺材料的红外光谱图,图1(a)中3 420 cm-1附近的宽峰是由于氨基的伸缩振动造成的,1 560 cm-1和1 350 cm-1附近的峰是由于N—H 键的弯曲振动峰和C—N 键的伸缩振动造成的,而2 925 cm-1和1 470 cm-1附近的峰主要成因是大量亚甲基的存在。这些结果表明了存在大量的胺基和三嗪基团,并成功合成了密胺材料。

图1 Cu@PMF 的红外分析图和热重分析图Fig.1 ATR-FTIR spectra and thermal gravimetric analysis of Cu@PMF
图1(b)为 Cu@PMF 的热重分析图,在氮气氛(TGA)下通过热重分析检测其热稳定性。其聚合温度在170 ℃,拥有较高的热稳定性,在200 ℃以下没有观察到催化剂材料的明显分解,在300 ℃开始分解,在360 ℃分解速度达到最高,在800 ℃仅剩20%左右的质量。其在200 ℃下的优异热稳定性表明Cu@PMF 适合作为环氧化物与CO2的环加成催化反应中的催化剂,因为其大量反应通常是发生在25~180 ℃之间,在该温度区间,催化剂不会进行热分解。
2.2 形貌分析
图2 为 Cu@PMF 的 SEM 和 TEM 图像。

图2 Cu@PMF 的的 SEM 和 TEM 图像Fig.2 SEM and TEM images of Cu@PMF
图2 直接证明了Cu@PMF 中存在孔隙,由SEM图像可以观测到介孔结构,泊洛沙姆F127 的加入,聚合完成后,致孔剂被洗脱,原本占据的位置即是介孔结构。这种孔隙结构对反应中的传质十分有利。
2.3 孔径分析
图3 为Cu@PMF 的氮气吸脱附曲线和孔径分布图。
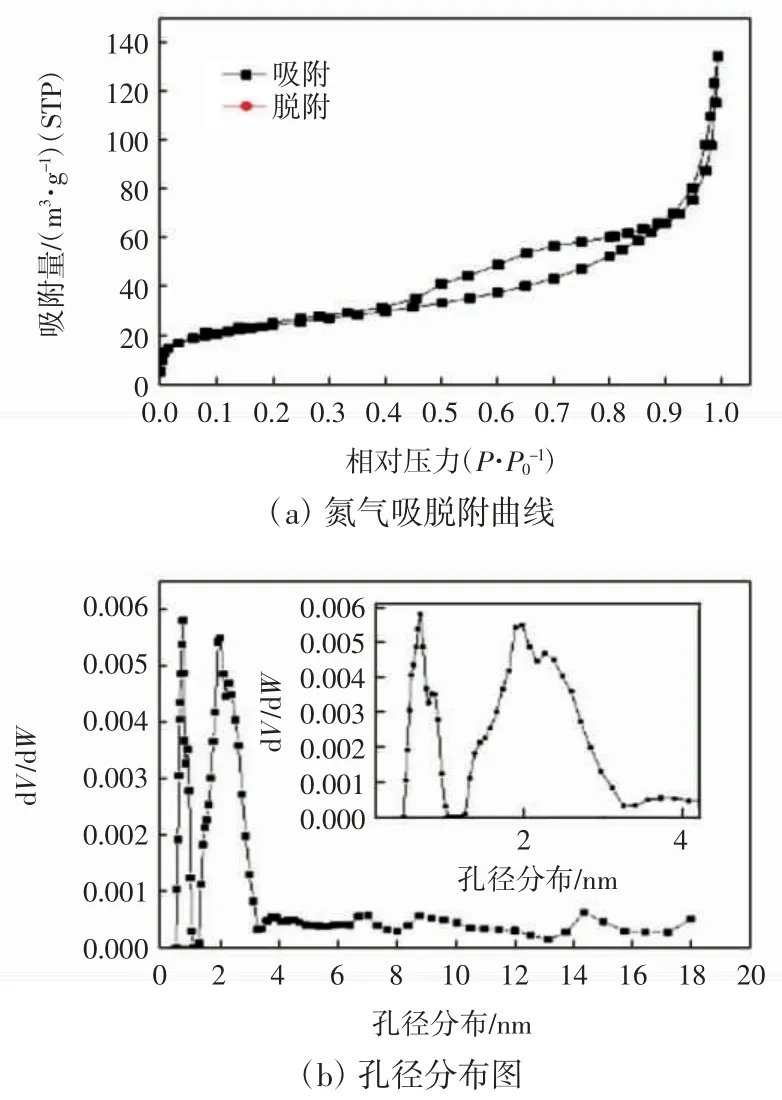
图3 Cu@PMF 的氮气吸脱附曲线和孔径分布图Fig.3 Adsorption and desorption isotherms of Cu@PMF pore size distribution curve of Cu@PMF
图3(a)为 Cu@PMF 在 77 K 条件下的 N2吸脱附曲线。由图3(a)观察到具有H3型的N2等温吸脱附曲线,并且出现了非常典型的IV 型磁滞回线。在P/P0<0.05 区域,微孔吸附引起N2吸收急剧增加,在0.05
2.4 元素分析
图4 为Cu@PMF 和PMF 的XPS 全谱图。由图4可知,Cu@PMF 在XPS 全谱图中主要由4 个发射峰,其对应的能量分别为288 eV、399 eV、540 eV、930 eV,它们分别代表 C1s、N1s、O1s、Cu2p3的发射峰。Cu@PMF 的谱图中,C—H、C=N、C—N 等键对应 288 eV 处的峰位;其在930 eV 处的峰位是Cu@PMF 独有的,对应吸附的铜离子。
2.5 催化性能分析
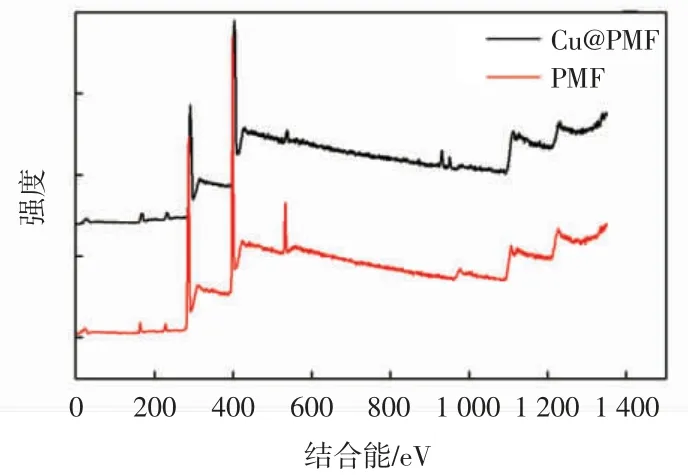
图4 Cu@PMF 和 PMF 的 XPS 分析图谱Fig.4 XPS spectra of Cu@PMF and PMF
将氧化苯乙烯、TBAB、催化剂加入到反应釜中,排除空气后,CO2加压到 2 MPa,加热 100 ℃,150 r/min搅拌。CO2一部分溶解于环氧丙烷,一部分与TBAB(四丁基溴化铵)形成氨基甲酸盐,TBAB 提高了CO2的溶解量。环氧丙烷被催化剂上的路易斯酸位点(铜离子)吸引活化,CO2被催化剂上的氨基基团吸引,靠近催化剂。此时,溶解于环氧的四丁基溴化铵电离出来的带负电溴离子,进攻环氧丙烷上的亚甲基(因为环氧的氧原子吸引电子,导致亚甲基带正电性,容易被带负电性的离子进攻),亚甲基开环后,CO2(由于碳原子被氧原子吸引电子,碳原子带正电性)的碳原子与开环后的环氧的氧原子结合,CO2进入其中,然后闭环形成碳酸酯,与催化剂分离[16-19],反应原理如图5 所示。
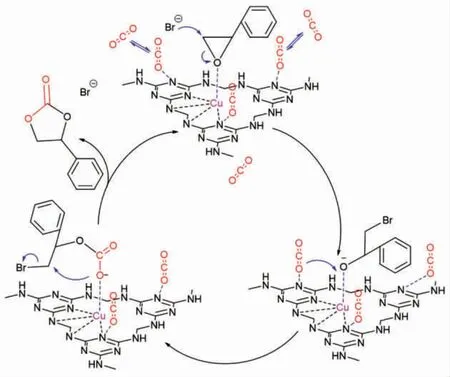
图5 环加成催化反应机理Fig.5 Proposed reaction mechanism of SO with CO2 catalyzed by Cu@PMF
在高温高压及S/C 值为13 000 条件下进行催化反应,得到表1 所示数据。由表1 可见,项目1 在压力2 MPa,温度100 ℃的条件下反应0.5 h,转化率达到57.1%,选择性为99%。项目2 中,将反应时间延长到2 h,转化率达到97.2%,选择性为99%。项目3 反应中,反应体系中不加入催化剂,由共催化剂单独催化反应,转化率达到16.1%。项目4 反应中,反应体系中不加入共催化剂,有催化剂单独催化反应,转化率为0.1%。Cu@PMF 在共催化剂的辅助下,对氧化苯乙烯的环加成反应有良好的催化性能。在常温常压条件下,催化反应的转化率较低,如项目5 所示,反应6 h,转化率为1.5%。
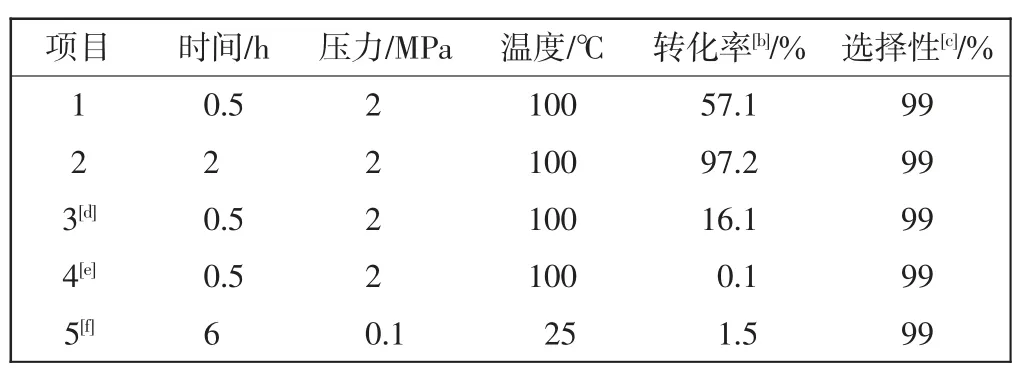
表1 氧化苯乙烯和CO2 的环加成反应[a]Tab.1 Cycloaddition reaction of styrene oxide with CO2[a]
环氧化合物的环加成催化反应为典型的吸热反应,在高温的条件下反应更易发生[21],但催化剂的反应活性也会随时间的变化而变化,因此寻找最合适的反应温度十分必要。如图6 所示,在Cu@PMF 和TBAB的二元体系中,氧化苯乙烯与CO2的环加成催化反应的最佳反应温度为100 ℃。在该温度条件下,催化剂活性最佳,拥有最好的催化性能。
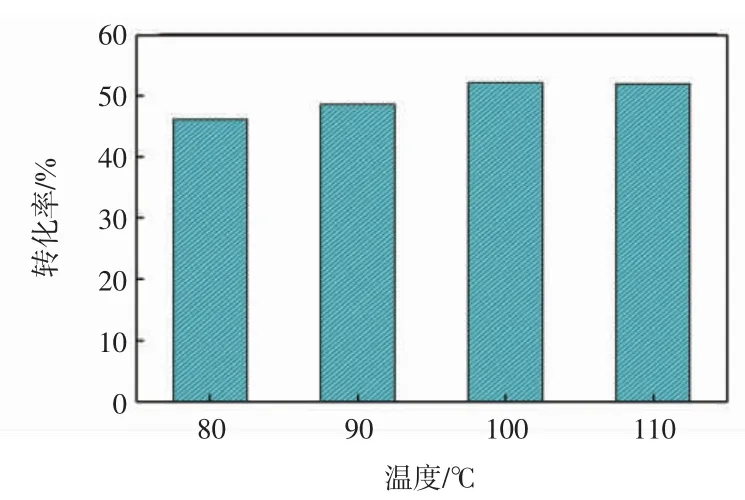
图6 Cu@PMF 在不同温度下的转化率Fig.6 Conversion of reaction at different temperature
3 结 论
将三聚氰胺和多聚甲醛溶于二甲基亚砜中,加入表面活性剂,采用水热法制备出具有微孔和介孔结构的密胺材料。比表面积为59 m2/g。在最佳反应温度100 ℃,压力 2 MPa 的条件下,Cu@PMF 在共催化剂的作用下,进行氧化苯乙烯的环加成催化反应,转化率达到97.2%。本研究采用简单的方法制备了一种高效率的聚合物多孔催化剂,将具有良好的工业应用前景。

