Pd-Pt NCNs电催化剂的制备及其甲醇氧化性能
张亚彬,李 娟,赵永男,余建国
(1.天津工业大学省部共建分离膜与膜过程国家重点实验室,天津 300387;2.天津工业大学材料科学与工程学院,天津 300387;3.天津工业大学环境科学与工程学院,天津 300387)
直接甲醇燃料电池(DMFC)具有能量转换效率高、便携性好、无有害排放等优点,是用于固定和便携式微型电器的非常有前景的电源[1]。然而,由于甲醇氧化反应的电极催化活性低、耐久性差、制造成本高等原因,DMFC 的大规模商业化应用受到限制,因此甲醇氧化电催化剂的选择显得尤为重要。近年来,具有高催化活性的阳极电催化剂受到了广泛关注[2-3]。
DMFC 的阳极电催化剂目前大多以Pt 为基础,但Pt 会强烈结合反应中的CO 中间体而引起催化剂中毒,造成甲醇氧化动力学缓慢且Pt 成本较高,自然资源有限[4]。为克服这些困难,科学家们已经研究了许多具有协同作用的Pt 基双金属材料(Pt-M),例如PtAu[5]、PtPd[6]、PtRu[7]等。在 Pt-M 催化剂中,Pt 与 Pd 因为晶格匹配度高且具有良好的混溶性而受到特别关注。此外,Pt-Pd 催化剂在高电位下比其他双金属催化剂更稳定[8-9]。研究表明,富Pd 的Pt-Pd NCs 催化剂还表现出高CO 耐受性。
引入先进的载体,如碳纳米管、碳球、石墨烯片、CeO2、TiO2等,可以极大地改善催化剂的分散性和稳定性[10]。最近,由于其多孔结构和高表面积,在导电基底如导电聚合物(CP)上分散金属颗粒引起了研究者们的兴趣[11]。聚合物基质既可用作纳米颗粒的载体,也可用作纳米颗粒的稳定剂,防止颗粒团聚[12]。聚合物稳定的钯纳米粒子作为电催化剂也引起了人们的广泛关注,Sowal 等[13]使用“原位聚合和复合形成方法”合成了聚合物负载的钯纳米颗粒,并证明了其在碱性介质中具有增强的甲醇氧化活性。
本文采用PVA 聚合物直接作为绿色还原剂和稳定剂,通过水热还原法制得Pd-Pt 纳米颗粒电催化剂,并系统优化了电催化剂的合成过程,探究其甲醇氧化性能。
1 实验部分
1.1 原料和仪器
原料:氯化钯、氯铂酸钾、聚乙烯醇、无水甲醇、氢氧化钾、稀盐酸、无水乙醇,均为分析纯,上海国药集团产品;20%商业Pt/C 和Nafion 溶液,阿拉丁公司产品;高纯氮气,天津市六方氮气厂产品;去离子水,自制。
仪器:JV2002 型电子分析天平、聚四氟乙烯反应釜,上海精密科学仪器有限公司产品;D8 DISCOVER型X 射线粉末衍射仪(XRD),BRUKER 公司产品;H-7650 型透射电子显微镜,日本日立公司产品;ECSAKAB 型 X 射线光电子能谱仪(XPS),英国 VG Scienctific 公司产品;磁力搅拌器、CHI660D 型电化学工作站,上海辰华仪器有限公司产品;玻碳电极、饱和甘汞电极、Pt 箔对电极,天津艾达有限公司产品;TG18G 型离心机,盐城凯特实验仪器有限公司产品。
1.2 催化剂的制备
采用恒温密闭水热还原的方法,首先将聚乙烯醇(PVA)固体(Mw≈120 000,水解度 97%)配制成 5%PVA 水溶液。称取 30 mg 氯化钯(PdCl2)固体溶于 15 mL去离子水中超声分散配制成2 mg/mL 氯化钯溶液。再量取质量浓度为7.51 mg/mL 的氯铂酸钾(K2PtCl6)溶液2.5 mL,在恒定搅拌下加入到15 mL 氯化钯水溶液(0.169 mmol)中来制备Pd-Pt 金属前体溶液。随后缓慢加入20 mL 新制备的聚乙烯醇(5%)溶液,分别通过少量滴加KOH 或稀HCl 溶液来调节反应混合物的pH 值。在持续搅拌600 min 后,反应溶液从淡黄色逐渐变为深褐色胶体溶液,在180 ℃水热反应6 h 后得到深黑色悬浮液。将深黑色悬浮液以11 000 r/min 离心处理10 min,再用乙醇和去离子水洗涤产物,此操作重复5 次以上以除去过量的金属前体和未反应的PVA。最终干燥后的黑色产物即为所需的Pd-Pt NCNs电催化剂。该催化剂中Pd 与Pt 的物质的浓度之比为4.4 ∶1,因此本文根据反应溶液不同的 pH 值(pH 值为6、8、10),将产物分别表示为 Pd4.4Pt1NCNs-1、Pd4.4Pt1 NCNs-2 和 Pd4.4Pt1NCNs-3。
为了考察掺入的Pt 含量对催化剂性能的影响,本文使用相同的方法,反应溶液pH 值为6 时合成了含有不同体积的质量浓度为7.51 mg/mL 的氯铂酸钾(K2PtCl6)溶液(2.5 mL 或 5.5 mL)的电催化剂,并依据物质的量浓度之比将产物分别命名为Pd4.4Pt1NCNs-1和Pd2Pt1NCNs-1。
1.3 催化剂的表征
采用X 射线粉末衍射仪(XRD)来分析样品的晶体结构,衍射角范围为30°~90°;通过透射电镜(TEM)来观察样品的结构形貌特征;采用X 射线光电子能谱(XPS)测试来分析样品的表面化学相和元素组成。
1.4 催化剂的电极制备和电化学性能测试
采用传统的三电极系统进行测试,测试的工作电极制备过程如下:将制备的催化剂超声分散在去离子水中形成2 mg/mL 均相溶液,取10 μL 催化剂混合物缓慢滴加到玻碳电极(GCE)上,并在环境温度下自然干燥12 h。电极表面的催化剂负载量优化为0.285 mg/cm2。然后将3 μL Nafion 溶液(5%)滴在电极表面上粘附住催化剂。使用循环伏安法(CV)来研究验证所制备的Pd-Pt 纳米颗粒的电催化响应。循环伏安(CV)测试的电位范围选择-0.9~0.3 V 和-0.2~0.96 V,扫描速率均为50 mV/s,甲醇氧化性能测试在1 mol/L KOH+1 mol/L CH3OH 溶液中进行,从而研究所得电催化剂的甲醇氧化活性。计时电流(CA)测试在-0.2V 下、1mol/LCH3OH+1 mol/L KOH 溶液中进行5 000 s。电解质溶液应在试验前在环境温度下用超纯氮气(N2)纯化20 min。
2 结果与讨论
2.1 Pd-Pt NCNs电催化剂的形貌分析与结构表征
2.1.1 XRD 分析
图1 所示为 Pd4.4Pt1NCNs-1 和 Pd4.4Pt1NCNs-2 的XRD 图谱。

图1 Pd4.4Pt1 NCNs-1(a)和 Pd2Pt1 NCNs-1(b)电催化剂的XRD 图谱Fig.1 XRD patterns of Pd4.4Pt1 NCNs-1(a)and Pd2Pt1 NCNs-1(b)electrocatalysts
由图1 中(a)和(b)可以看出,所合成的不同 Pd、Pt 摩尔比的 Pd4.4Pt1NCNs-1 和 Pd2Pt1NCNs-1 电催化剂均形成了面心立方(fcc)晶体结构。Pd4.4Pt1NCNs-1和Pd2Pt1NCNs-1 的XRD 图谱对应于面心立方(fcc)的Pt(JCPDS ∶04-0802)和Pd(JCPDS ∶46-1043)[14]。并且随着PdxPty NCNs 电催化剂中Pt 原子百分比的增加,所合成的Pd2Pt1NCNs-1 催化剂样品的XRD 图谱向更低的2θ 值偏移,证实了Pd 和Pt 形成Pd-Pt 合金[15]。根据 Debye Scherrer 方程[14]评估 Pd4.4Pt1NCNs-1 和Pd2Pt1NCNs-1 样品的平均微晶尺寸分别为5.6 nm 和6.8 nm。结果表明,Pd4.4Pt1NCNs-1 催化剂具有更小的颗粒尺寸。
2.1.2 TEM 分析
运用TEM 测试来研究所制备的Pd4.4Pt1NCNs-1,Pd4.4Pt1NCNs-2 和Pd4.4Pt1NCNs-3 电催化剂中金属颗粒的分散情况以及形态特征如图2 所示。

图2 Pd4.4Pt1 NCNs-1(a)、Pd4.4Pt1 NCNs-2(b)和Pd4.4Pt1 NCNs-3(c)的 TEM 图像Fig.2 TEM images of Pd4.4Pt1 NCNs-1(a),Pd4.4Pt1NCNs-2(b)and Pd4.4Pt1 NCNs-3(c)
由图2 可知,不同pH 值下所合成的Pd-Pt 纳米颗粒仍旧呈现纳米链网络状结构(NCNs),其中Pd4.4Pt1NCNs-1(图2(a))催化剂表面存在大量的 Pd 金属纳米颗粒和少量自成核的Pt 纳米颗粒。Pt 颗粒倾向于随机分散在PVA 表面上形成小颗粒,因为带负电的Pt金属前体(K2PtCl6)能够通过静电力与PVA 聚合物载体表面形成相当大的相互作用,所以一些Pt 金属前体可以自成核并生长在聚合物表面上形成小的Pt 纳米颗粒[16]。图2(a)中Pd-Pt 纳米粒子高度分散在少量PVA 聚合物薄层上而没有明显的颗粒聚集,并且颗粒总体分布较均匀,平均直径约为5.5 nm,与上述XRD测量结果一致。图2(b)中,反应溶液pH 值为8 时,所制备的Pd4.4Pt NCNs-2 催化剂中金属颗粒尺寸逐渐增大,平均直径约为9.8 nm 且小颗粒之间存在部分团聚的趋势。正如所料,从图2(c)中可以看到,当反应溶液pH 值为10 时,所制备的Pd4.4Pt1NCNs-3 催化剂中金属颗粒尺寸继续增大且分布不均匀,出现了大量的小尺寸金属纳米颗粒团聚在一起形成更大的球体被包覆在聚合物层中。此类现象会导致催化剂的比表面积和活性位点急剧减少,从而影响其电催化活性和稳定性。
2.1.3 XPS 分析
运用XPS 来确定所制备的Pd-Pt NCNs 电催化剂的表面元素组成和价态分布。各催化剂样品的Pd 3d和Pt 4f 光谱如图3 所示。
由图3 可知,Pt 4f 峰可以解卷积成对应于金属Pt 4f7/2和 Pt 4f5/2的双峰(71.8 eV 和 75.2 eV)[17]。在335.7 eV 和340.9 eV 处观察到的2 个峰可分别归因于Pd 3d5/2和Pd 3d3/2[18]。这些结果证实Pd 和Pt 前体已被PVA 成功还原成分散在少量PVA 薄膜上的Pd-Pt NCNs 电催化剂。Pd4.4Pt1NCNs-1、Pd4.4Pt1NCNs-2 和Pd4.4Pt1NCNs-3 电催化剂中 Pd、Pt、C 和 O 元素的含量如表1 所示。
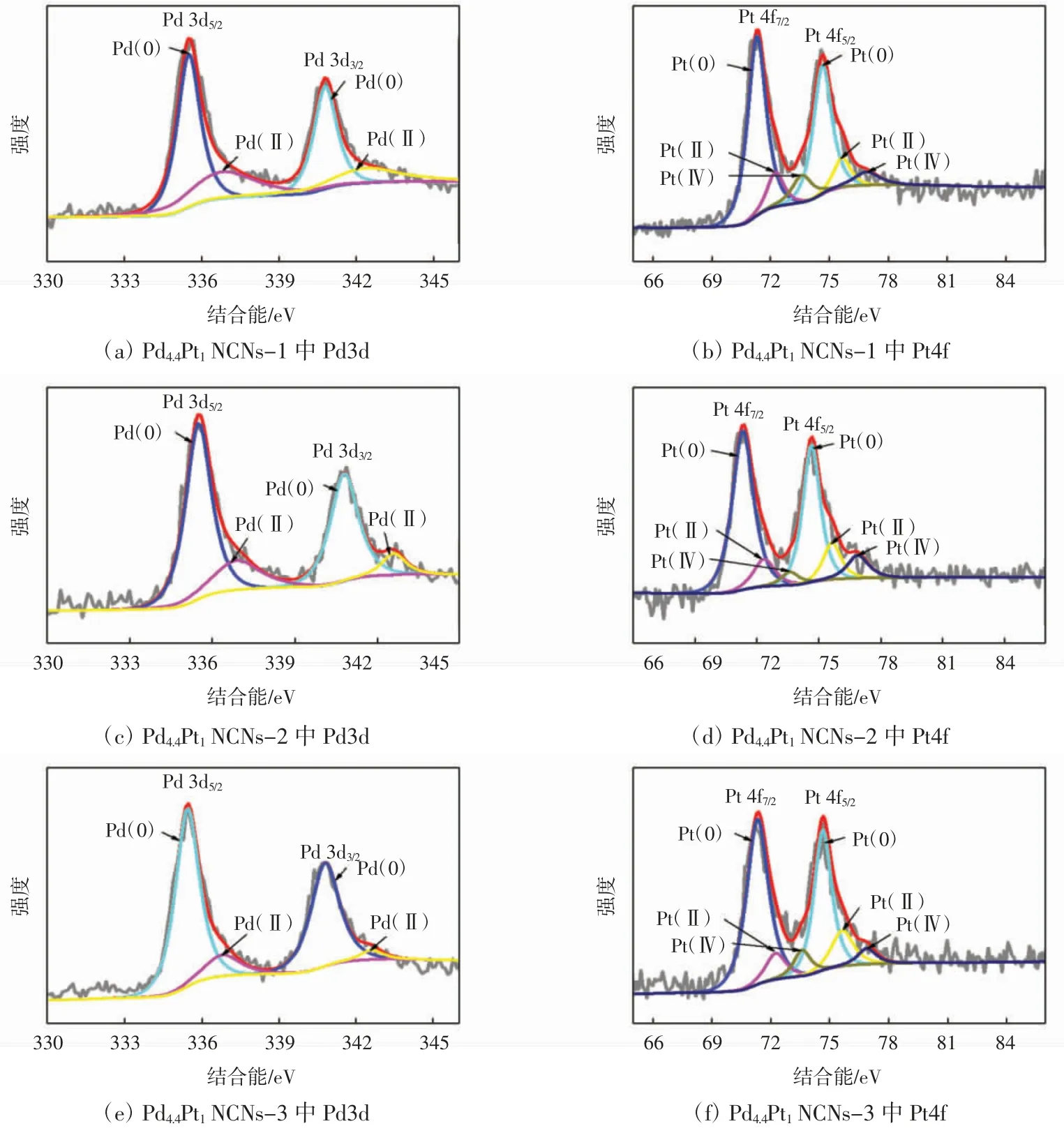
图3 Pd4.4Pt1 NCNs-1(a,b)、Pd4.4Pt1 NCNs-2(c,d)和 Pd4.4Pt1 NCNs-3(e,f)中 Pd 3d 和 Pt 4f 的 XPS 拟合图Fig.3 XPS fitting profiles of Pd 3d and Pt 4f of Pd4.4Pt1 NCNs-1(a,b),Pd4.4Pt1 NCNs-2(c,d)and Pd4.4Pt1 NCNs-3(e,f)

表1 Pd4.4Pt1 NCNs-1、Pd4.4Pt1 NCNs-2 和 Pd4.4Pt1 NCNs-3中 Pd、Pt、C 和 O 元素含量Tab.1 Contents of Pd,Pt,C and O in Pd4.4Pt1 NCNs-1,Pd4.4Pt1 NCNs-2 and Pd4.4Pt1 NCNs-3 %
由表1 可见,样品 Pd4.4Pt1NCNs-1、Pd4.4Pt1NCNs-2和Pd4.4Pt1NCNs-3 中的Pd 原子分数分别达到12.21%、7.76%和4.38%,Pt 原子分数分别为3.72%、2.65%和1.39%,可见Pd4.4Pt1NCNs-1 样品中含有最高的Pd 和Pt 含量。表2 总结了 Pd4.4Pt1NCNs-1、Pd4.4Pt1NCNs-2,Pd4.4Pt1NCNs-3 样品中Pd(0)、Pd(Ⅱ)、Pt(0)、Pt(Ⅱ)及Pt(Ⅳ)的元素价态含量。

表2 Pd4.4Pt1 NCNs-1、Pd4.4Pt1 NCNs-2 和 Pd4.4Pt1 NCNs-3中的 Pd(0)和 Pd(Ⅱ)的含量Tab.2 Contents of Pd(0)and Pd(Ⅱ)in Pd4.4Pt1 NCNs-1,Pd4.4Pt1 NCNs-2 and Pd4.4Pt1 NCNs-3 %
由表2 可以看出,所有催化剂样品中主要以金属Pd(0)和Pt(0)形式存在,此结果与之前的XRD 图谱一致。此外,Pd(0)和Pt(0)的含量随着反应溶液pH 值的减小而增加。Pd4.4Pt1NCNs-1 样品中Pd2+、Pt2+和Pt4+的含量最少,说明当溶液pH=6 时,绝大多数Pd2+和Pt4+被还原为Pd-Pt 金属纳米颗粒。上述研究结果表明,弱酸性条件更有利于合成具有纳米链网络状结构的Pd-Pt NCNs 电催化剂,其中大量的Pd-Pt 金属纳米颗粒良好地锚定在PVA 聚合物中,Pd-Pt NCNs 与少量PVA 薄膜之间的协同相互作用以及Pd 和Pt 的合金化效应,为催化剂的电催化反应提供了较大的比表面积和充足的活性位点,从而使其具备较高的催化氧化性能[19]。
2.2 Pd-Pt NCNs电催化剂的电化学性能研究
2.2.1 甲醇氧化性能分析
使用循环伏安法来评价Pd4.4Pt1NCNs-1、Pd4.4Pt1NCNs-2 和Pd4.4Pt1NCNs-3 电催化剂对甲醇氧化的电催化活性。图4 为在含有1 mol/L KOH 的氮气饱和溶液、-0.9~0.3 V(vs SCE)的电位范围内的测试结果。

图4 Pd4.4Pt1 NCNs-1、Pd4.4Pt1 NCNs-2 和 Pd4.4Pt1 NCNs-3催化剂的循环伏安图像Fig.4 Cyclic voltammograms of Pd4.4Pt1 NCNs-1,Pd4.4Pt1 NCNs-2 and Pd4.4Pt1 NCNs-3 catalysts
由图4 可知,与Pd4.4Pt1NCNs-2 和 Pd4.4Pt1NCNs-3相比,Pd4.4Pt1NCNs-1 的氢吸附/解吸和氧化钯还原区域的电流密度明显提高,表明随着反应溶液pH 值的降低,所制备的Pd-Pt NCNs 电催化剂的氧化峰和还原峰均显著增强。
Pd4.4Pt1NCNs-1、Pd4.4Pt1NCNs-2 和 Pd4.4Pt1NCNs-3电催化剂与20%商业Pt/C 在碱性溶液中的甲醇电氧化反应活性对比如图5 所示。
由图5 可以清楚地观察到,所有样品均有2 个甲醇氧化峰,正向扫描中的强电流峰值是甲醇氧化的特征。在更大的正电位下电流密度的降低是由Pt 和Pd氧化物的形成引起的,这阻碍了甲醇的进一步化学吸附。在-0.3 V 处的反向峰是由于负向扫描中Pt 和Pd 氧化物还原导致甲醇氧化的电催化表面发生再活化[20]。如图5(a)所示,Pd4.4Pt1NCNs-1 催化剂的峰电流密度为 482.14 A/g,高于 Pd4.4Pt1NCNs-2(398.61 A/g)和 Pd4.4Pt1NCNs-3(315.99 A/g)样品,几乎是 20%商业Pt/C(189.6 A/g)的 2.5 倍。
Pd4.4Pt1NCNs-1、Pd4.4Pt1NCNs-2、Pd4.4Pt1NCNs-3、Pd2Pt1NCNs-1 电催化剂和20%商业Pt/C 催化剂在1 mol/L KOH 溶液中的甲醇氧化峰电位、峰电流密度和If/Ib比值如表3 所示。

图5 Pd4.4Pt1 NCNs-1、Pd4.4Pt1 NCNs-2、Pd4.4Pt1 NCNs-3与20%商业Pt/C 的循环伏安图像Fig.5 Cyclic voltammograms of Pd4.4Pt1 NCNs-1,Pd4.4Pt1 NCNs-2,Pd4.4Pt1 NCNs-3 and 20%commercial Pt/C
由表3 可见,Pd4.4Pt1NCNs-1 具有更低的起始电位、最大的峰值电流密度和If/Ib 值。这些结果均表明弱酸性条件下合成的Pd4.4Pt1NCNs-1 电催化剂的甲醇催化氧化性能最佳。
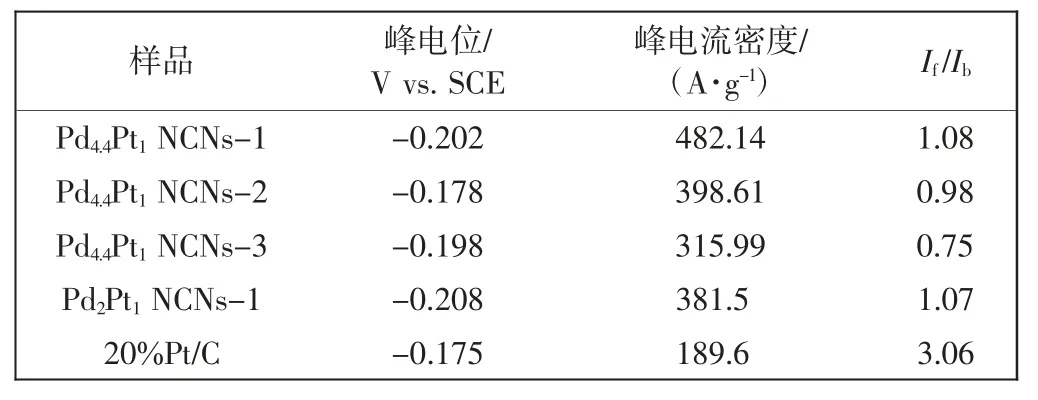
表3 Pd4.4Pt1 NCNs-1、Pd4.4Pt1 NCNs-2、Pd4.4Pt1 NCNs-3、Pd2Pt1 NCNs-1 和20%商业Pt/C 催化剂的甲醇氧化峰电位、峰电流密度和If/Ib 值Tab.3 Peak potentials,peak current density and If/Ib values of various Pd4.4Pt1 NCNs-1,Pd4.4Pt1 NCNs-2,Pd4.4Pt1 NCNs-3,Pd2Pt1 NCNs-1 and 20%commercial Pt/C catalysts for methanol oxidation
图6 所示为反应溶液pH 值为6 时制备的不同Pd/Pt 比的 Pd4.4Pt1NCNs-1、Pd2Pt1NCNs-1 电催化剂与20%商业Pt/C 在1 M KOH+1 M CH3OH 溶液中的循环伏安图像。
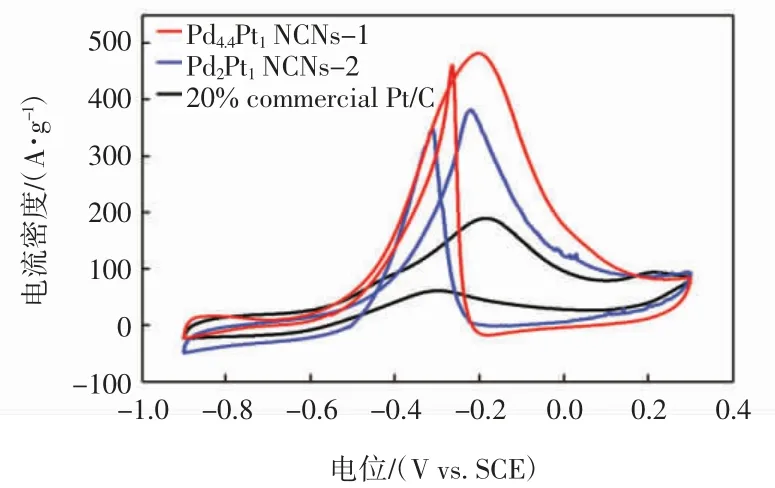
图6 Pd4.4Pt1 NCNs-1、Pd2Pt1 NCNs-1 和20%商业Pt/C催化剂的循环伏安图像Fig.6 Cyclic voltammograms of the Pd4.4Pt1 NCNs-1,Pd2Pt1 NCNs-1 and 20%commercial Pt/C catalysts
由图6 可知,Pd4.4Pt1NCNs-1 仍然具有最大的电流密度,因此Pd-Pt NCNs 在碱性环境中的最佳电催化活性可以通过优化Pd/Pt 比为4.4 ∶1 来实现。上述结果表明,Pd4.4Pt1NCNs-1 电催化剂的纳米链网络状结构以及Pd 与Pt 合金的协同效应可以为甲醇的电氧化提供优异的电催化活性。
2.2.2 循环稳定性分析
通过在催化剂电极上同时进行300 次连续电位扫描来检查Pd4.4Pt1NCNs-1 催化剂的稳定性,如图7 所示。
由图7 可知,Pd4.4Pt1NCNs-1 电催化剂的峰值电流密度在第200 圈时达到最大值,在第300 个循环后该催化剂的峰值电流密度仅减少6.7%,表明Pd4.4Pt1NCNs-1电催化剂在甲醇氧化反应中具有较高的稳定性。
2.2.3 计时电流分析

图7 Pd4.4Pt1 NCNs-1 电催化剂循环300 圈的循环伏安图像Fig.7 Cyclic voltammograms of Pd4.4Pt1 NCNs-1 electrocatalyst up to 300th cycle
为了进一步研究所合成的Pd-Pt NCNs 电催化剂的耐久性和抗中毒能力,在-0.2 V 下、1 mol/L CH3OH+1 mol/L KOH 溶液中进行5 000 s 计时电流测试,如图8 所示。
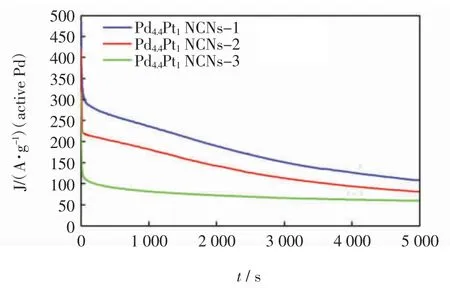
图8 Pd4.4Pt1 NCNs-1、Pd4.4Pt1 NCNs-2 和 Pd4.4Pt1 NCNs-3电催化剂的计时电流图像Fig.8 CA profiles of Pd4.4Pt1 NCNs-1,Pd4.4Pt1NCNs-2 and Pd4.4Pt1 NCNs-3 electrocatalysts
由图8 可知,最初由于催化剂表面上有许多活性位点,所有催化剂样品都具有较高的电流密度。大约20 s 后,由于吸附在活性位点上的CO 等中间碳质物质的形成,电流迅速衰减,阻止甲醇在电催化剂表面上进一步氧化。随后在30 min 内电流密度逐渐衰减,在后期阶段电流趋于稳定,表明催化剂具有良好的CO 耐受性。Pd4.4Pt1NCNs-1 电催化剂的最终电流密度(127.86 A/g)高于 Pd4.4Pt1NCNs-2(96.83 A/g)和Pd4.4Pt1NCNs-3(73.57 A/g),表明 Pd4.4Pt1NCNs-1 电催化剂在甲醇电化学氧化过程中具有更好的抗CO 中毒性和稳定性。
3 结 论
采用聚乙烯醇(PVA)作为绿色还原剂和稳定剂,通过水热还原法成功制备了纳米链网络状结构的Pd-Pt 纳米颗粒电催化剂(Pd-Pt NCNs)。通过调节反应溶液的pH 值和Pd、Pt 摩尔比制备了不同的Pd-Pt NCNs电催化剂样品,并研究了其甲醇氧化性能,结果表明:
当溶液pH 值为6、Pd/Pt 比值为4.4 时所制备的Pd4.4Pt1NCNs-1 电催化剂对甲醇氧化表现出了优异的催化活性和稳定性,其甲醇氧化峰值电流密度为482.14 A/g,约为 20%商业 Pt/C(189.6 A/g)的 2.5倍。

