玻璃体内注射抗血管内皮生长因子药物对糖尿病肾脏损害的影响
娄丽璇 涂远茂 张丽华 吴晓梅 周 云 朱淑华 杜孟茹 戴馨琳 谢红浪
由于血管内皮生长因子(VEGF)在维持内皮细胞功能包括肾小球及管周毛细血管系统中起重要作用,抗VEGF静脉治疗可能的不良反应如高血压、蛋白尿、血栓事件[1-2]现备受重视。VEGF也是糖尿病视网膜病变(DR)形成的关键因子,DR患者VEGF及受体表达升高,玻璃体内注射抗VEGF 药物可促进新生血管消退、减轻渗漏、减少新生血管形成,有效控制眼底病变[3],广泛用于增殖期糖尿病视网膜病变(PDR)、糖尿病性黄斑水肿(DME)及DR玻璃体术前辅助用药。既往认为[4-5]玻璃体内局部注射抗VEGF药物因局部应用且剂量小,不增加系统风险,但局部用药仍经循环系统清除[5],可导致VEGF系统抑制效应。糖尿病患者出现DR时多伴糖尿病肾病(DN)[6]及多种心血管并发症[7],因此DR患者抗VEGF治疗的潜在风险如蛋白尿、高血压、血栓事件更值得关注。
本文回顾性报道了9例玻璃体内注射抗VEGF类药物对糖尿病患者肾脏损害的影响,分析临床、病理特征和预后,以期为此类患者的诊治提供经验。
对象和方法
病例选择选取2016年6月至2019年9月在东部战区总医院国家肾脏疾病临床医学研究中心住院的糖尿病患者。入选标准:(1)经裂隙灯生物显微镜下眼底检查、散瞳后眼底照相确诊为DR;(2)接受玻璃体内注射抗VEGF药物治疗;(3)玻璃体内用药后1年内估算的肾小球滤过率(eGFR)较基线下降>25%[8],或血压升高即舒张压较基线升高持续>20 mmHg或降压药较基线增加1个以上[9]。
排除标准:(1)合并自身免疫疾病或其他继发性肾脏病;(2)同时应用中药偏方、非甾体类抗炎药(NSAID)等潜在肾毒性药物;(3)明确存在其他可能导致急性肾损伤的原因,如感染、血容量不足、大出血等;(4)恶性肿瘤患者。
临床资料及实验室检查(1)一般情况:患者年龄、性别、糖尿病病程、肾脏病程、高血压和降压治疗方案;(2)患者基线、玻璃体内用药前后及每个随访点血压水平;(3)24h尿蛋白定量、血清肌酐(SCr)、尿素氮、血清白蛋白、空腹血糖、糖化血红蛋白,eGFR采用EPI公式计算。
肾脏病理学检查部分患者行超声引导下经皮肾活检术,肾组织标本行光镜、免疫荧光及电镜检查,评价肾小球、肾小管间质及肾血管病变程度。
相关定义基线蛋白尿、SCr、血压、eGFR定义为玻璃体内抗VEGF治疗前3月内监测值。糖尿病病程、高血压病程、肾脏病程分别定义为自诊断糖尿病、发现血压升高、发现蛋白尿至玻璃体内抗VEGF治疗的时间。肾活检时间定义为自玻璃体内抗VEGF治疗至行肾活检时间。随访时间定义为玻璃体内用药后至末次随访。终末期肾病(ESRD)定义为eGFR<15 ml/(min·1.73m2)。
统计学方法统计分析采用《SPSS 19.0》软件。非正态分布计量资料用中位数(四分位数间距)表示。配对定量资料的统计分析采用配对资料的符号秩和检验。
结 果
基线资料9例患者的基线资料见表1。8 例为男性,中位年龄47.1(38,53)岁,中位糖尿病病程90(34~157.5)月,2型糖尿病8例,1型糖尿病1例。1例(患者1)仅伴高血压,1例(患者2)仅伴蛋白尿,其余7例基线均有蛋白尿和高血压。中位肾脏病程17.7(1.0,14.0)月。所有患者既往无心肌梗死及心功能不全史。DR分期均为Ⅲ~Ⅴ期,2例伴DME,患者1、2、6、7单次单眼注射,患者9单次双眼注射,患者3、4、5、8多次单眼注射。

表1 患者基线资料
DM:糖尿病;DR:糖尿病视网膜病变;HP:高血压;SP:收缩压;DP:舒张压;DN:糖尿病肾病;eGFR:估算的肾小球滤过率;DME:糖尿病性黄斑水肿
肾脏损害临床特征患者1用药1周后出现水肿、恶心,急性肾损伤(SCr峰值为327.1 μmol/L)、轻度贫血、血小板降低,血压升高,筛查抗核抗体、ENA多肽谱阴性,C3、C4、C3肾炎因子、补体H因子均正常,抗H因子抗体阴性,ADAMTS13 活性正常,ADAMTS13抗体阴性,冷球蛋白正常,胸部CT正常(表2、图1)。患者2表现为新发高血压,收缩压和舒张压分别较基线增加48 mmHg和24 mmHg,蛋白尿、SCr稳定。
另外7例基础同时伴蛋白尿及高血压的患者,3例常规复诊发现肾脏病进展,4例因水肿或水肿加重就诊,其中3例同时伴心功能不全。玻璃体内抗VEGF治疗后3~6月,6例患者出现蛋白尿较前升高,SCr较前上升。与单次给药者相比,多次给药者SCr呈持续加速升高趋势,伴心功能不全的患者肾功能恶化速度较则更快。患者5在35d内给予3次康柏西普治疗,1周后出现双下肢水肿和心功能不全,尿蛋白尿和SCr迅速升高。7例患者血压均较基线升高,多次用药患者血压上幅度高于单次用药者(表2、图1)。患者4用药后发生急性心肌梗死并置入支架2枚。
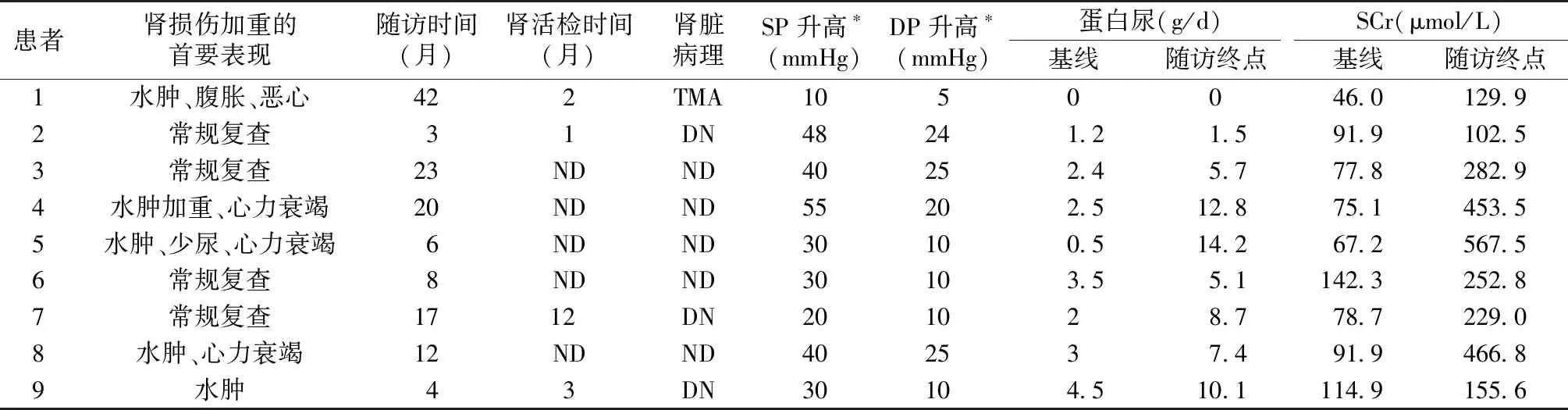
表2 玻璃体内注射抗血管内皮生长因子类药物治疗后随访
ND:未做;TMA:血栓性微血管病;DN:糖尿病肾病;SP:收缩压;DP:舒张压;*:玻璃体内注射后血压峰值与基线血压差值
肾组织活检病理特征4例行肾活检术。患者1病理表现血栓性微血管病(TMA),荧光染色IgM+弥漫颗粒状沉积于系膜区及血管袢,光镜见肾小球缺血皱缩、外周袢分层,小叶间动脉内膜增厚、水肿,内皮下疏松、内皮细胞增生、肿胀,见葱皮样改变,数处动脉闭锁,电镜见肾小球弥漫内皮下疏松伴系膜溶解,肾小球足细胞足突广泛融合(图2)。
其余3例患者肾脏病理均表现DN,光镜见肾小球系膜增生性病变伴结节形成,球性废弃(48.4%~61,9%),节段硬化(3.2%~9.5%),肾小管间质慢性病变(40%~60%),可见小动脉节段和全层透明变性、闭锁,小叶间动脉内膜增厚、弹力层增厚分层,3例均未见内皮下疏松及内皮肿胀。
治疗及预后患者中位随访时间14.9(4.5,21.5)月。9例患者均需增加降压药物种类或剂量以维持降压效果,其中5例(患者1、3、5、8、9)需3种及以上降压药。患者1经泼尼松15 mg/d,蛋白尿转阴,SCr降至130.0 μmol/L。患者2在随访中尿蛋白和SCr稳定。7例基础伴蛋白尿及高血压患者,中止抗VEGF治疗后SCr无下降趋势,蛋白尿均无缓解。尚无单次用药者进入ESRD,3例多次用药者进入ESRD,其中2例需维持性血液透析。
讨 论
本研究是迄今为止关于玻璃体内注射抗VEGF类药物治疗DR患者肾脏损害的影响最大样本的病案系列报道,发现DR患者在接受玻璃体内抗VEGF治疗后可能出现新发肾脏损害或基础肾损害的加速进展、血压升高,提醒临床医师警惕玻璃体内抗VEGF治疗的潜在肾脏风险。
现有研究认为[3,4,10],抗VEGF玻璃体内注射属局部用药,药物剂量明显低于静脉用药,不增加全身不良事件风险。但局部用药仍可进入血液循环抑制眼外脏器VEGF活性[11]。动物实验发现[12]玻璃体内注射阿柏西普后,药物可沉积于肾小球并降低肾小球局部VEGF水平。药代动力学及药效动力学研究[13-15]证实,玻璃体内注射雷珠单抗、阿柏西普、贝伐单抗后血药浓度可持续数天至1月达到半抑制浓度,多次给药后血药浓度数月内持续可测,循环VEGF水平也随之明显下降。因此玻璃体注药可能引起与静脉用药相似的全身效应。
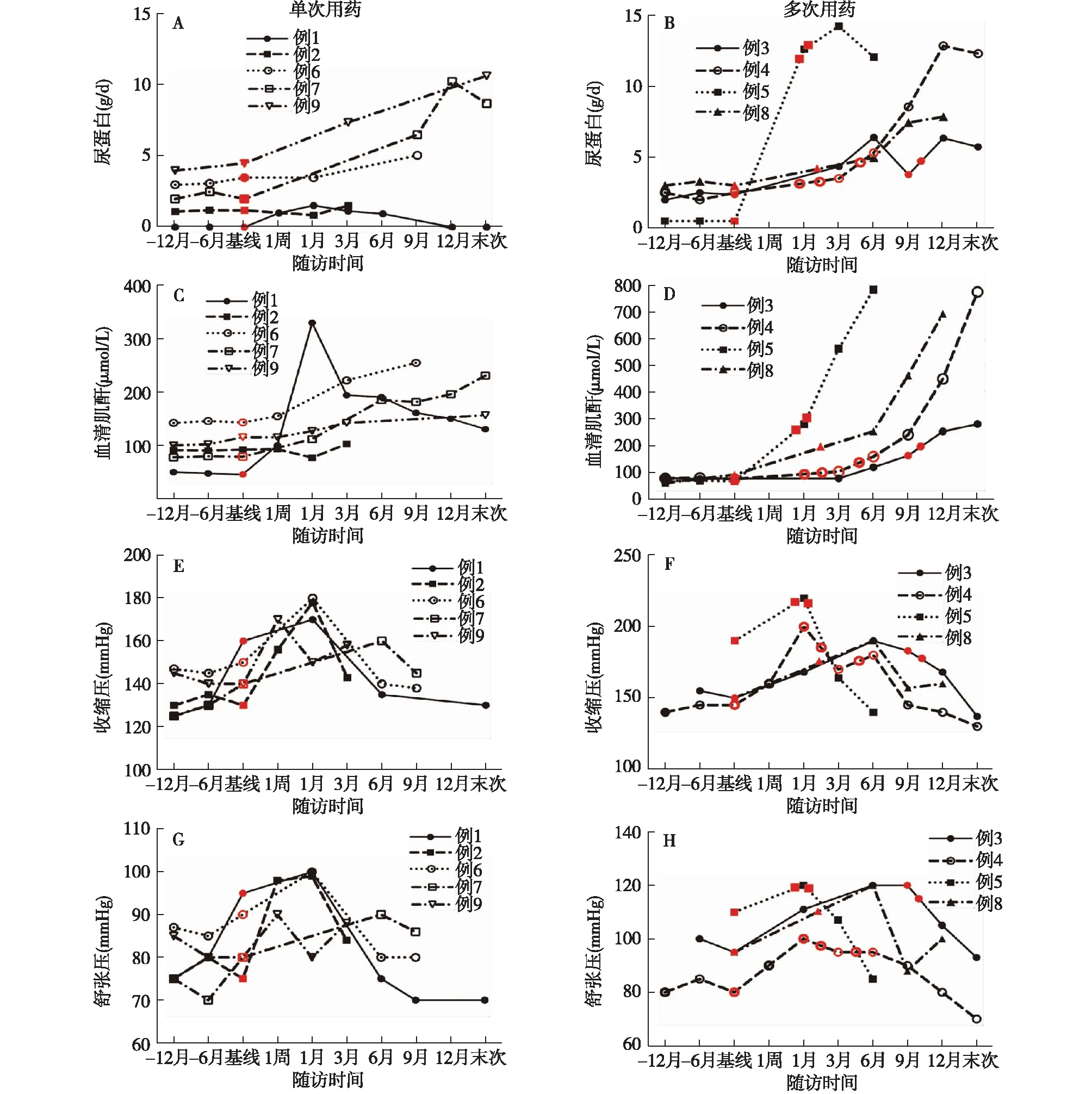
图1 玻璃体内抗VEGF治疗后尿蛋白、血清肌酐、血压变化
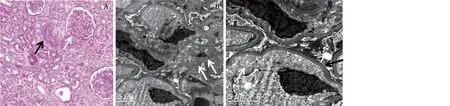
图2 患者1肾活检示血栓性微血管病样病变
抑制肾脏局部VEGF水平可减少正常内皮细胞数量,促进微血管损伤,诱发TMA[1]。Pelle等[16]报道首例基础伴高血压的患者玻璃体内抗VEGF治疗1月后出现TMA,本组1例基础仅伴高血压患者表现TMA,该2例患者临床均未查及明确继发因素,终止眼内抗VEGF注射后蛋白尿、肾功能明显改善,进一步支持为药物相关。
以往研究发现高血压患者玻璃体内注射抗VEGF类药物后更易出现血压升高[17],而早期临床实验倾向于排除严重高血压、肾功能损害的患者。DR患者多合并肾脏受累[6]、心血管并发症[7],抑制系统VEGF的风险可能更高。目前关于DR患者玻璃体内抗VEGF治疗后肾损害的个案报道[18-22],患者基础均伴蛋白尿和肾功能减退,用药后在原有病程基础上肾功能明显加速恶化,蛋白尿增加及血压升高,部分直接进入ESRD和透析治疗。本文中7例基础伴蛋白尿和高血压的患者肾脏损害特点与文献报道一致,同时我们发现连续给药后患者肾功能呈持续加速进展趋势,多次注射可能增加肾损伤风险。本研究中,多次用药患者血压升高幅度较单次用药患者大、心功能不全比例高,除了抗VEGF制剂本身肾毒性及重复用药打击,心功能不全、高血压可能是肾功能进展更为迅速的原因,但患者在纠正心力衰竭后并肾功能并无改善。本组基础伴蛋白尿的患者肾脏病理均符合DN,未见提示其他肾小球疾病的病理表现,临床医生如不追问眼内用药史,仅依据蛋白尿、SCr升高及病理表现,很容易忽视肾脏损害加重的诱因。循环VEGF水平降低,还可致新生血管形成受抑制、支循环建立受损,增加心肌缺血[11]及脑血管事件风险[23],本组1例患者多次用药后发生急性心肌梗死,除传统心血管危险因素外,药物可能是重要诱因。
本研究为回顾性研究,样本量小,从肾脏专科纳入已出现肾脏受累的患者。目前关于DR患者玻璃体内应用抗VEGF药物后短期及长期肾损伤的发生率、易感人群、疾病特点和对血压的影响仍需前瞻大样本研究进一步观察。Avery等[23]采用Meta分析揭示高危患者玻璃体内长期大剂量应用抗VEGF药物死亡率及脑血管风险均明显增加。Brown等[10]发现随访至36月,雷珠单抗0.5 mg/月与0.3 mg/月治疗DME效果相当,但大剂量组高血压、蛋白尿、血栓事件等严重不良事件明显升高。DR一般需要多次玻璃体内抗VEGF治疗,可持续抑制循环VEGF,DR患者尤其是DR晚期患者本身存在肾损害及心血管高风险,此类患者接受玻璃内抗VEGF治疗的剂量及疗程值得商榷,应注意早期识别可能的系统损伤以及时调整剂量,尤其是需要多次用药时,更要加强对可能发生的不良事件的监测和筛查。
小结:本研究通过回顾性分析发现,DR患者玻璃体内抗VEGF治疗后可能出现基础肾脏损害进展或新发肾脏损害、血压升高。因此我们建议所有接受玻璃体内抗VEGF治疗的患者在治疗前后密切监测蛋白尿、肾功能、血压的变化,关注可能的不良事件,尤其是需要多次用药者。

