高中电化学知识教学浅析
李茂炽
(湖北省襄阳市第四中学 441021)
电化学知识是高中化学重难点之一,是化学知识和前沿科技结合应用的热点,也是高考必考知识点,该部分内容不仅知识点多,题型也多种多样,主要考查内容包括原电池工作原理与应用、化学电池、电解原理与应用、电化学定量计算方法等.
一、电化学在高考中的地位
电化学是一类特殊的氧化还原反应,主要研究电极反应和能量变化两方面内容.在高考中占有非常重要地位.纵观近几年各地高考试题可以看出,试题形式多样化,考察内容包括新型电池结构解析(主要涉及高分子膜)、燃料电池、电极的判断以及方程式书写、离子迁移方向浓度变化等是高考命题热点.近几年高考命题常从生活实际着手,使学生在学习电化学基础上认识到化学学习与社会、科技、生活息息相关.
二、近几年高考试题分析

例1某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理如图,下列说法正确的是 ( ).
A.a为CH4,b为CO2

C.此电池在常温时也能工作
解析A.从电子流向可以确定左边电极是负极,所以a处通入甲烷,则右边是正极,从右侧出去的是氮气可以看出,b处通入的是空气(氧气作氧化剂),故A不正确;
C.此电池是用熔融碳酸盐作电解质,只能是在高温下进行工作,故C不正确;
正确答案:BD.
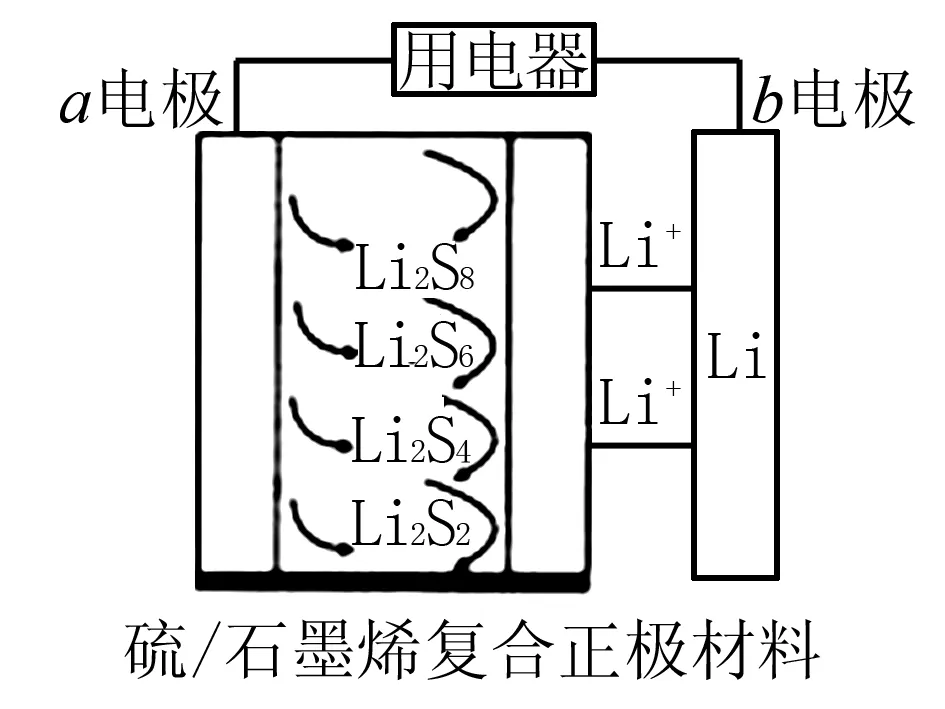

A.电池工作时,a是正极,外电路中流过0.02mol电子,负极材料减重0.14g
B.石墨烯的作用主要是提高电极a的导电性
C.当锂硫电池电极提供1mol电子时,则理论上铁电极增重32g
D.放电时,Li+向正极移动,在此电池中加入硫酸可增加导电性
解析A.a是正极,b极为负极,Li-e-=Li+转移0.02mol电子减重为0.02×7=0.14g,故A正确;B.石墨烯具有导电作用,它的使用能提高电极a的导电性,B正确;C.铁上镀铜,铜作阳极,阴极(铁极)发生反应:Cu2++2e-=Cu,转移1mol电子时,析出铜0.5×64=32g,C正确;D.硫酸能够与金属锂电极反应,不能构成原电池,D错误.正确答案:D.
例3有一种节能的氯碱工业新工艺,将电解池与燃料电池相组合,相关流程如下图所示(电极未标出),下列说法错误的是( ).
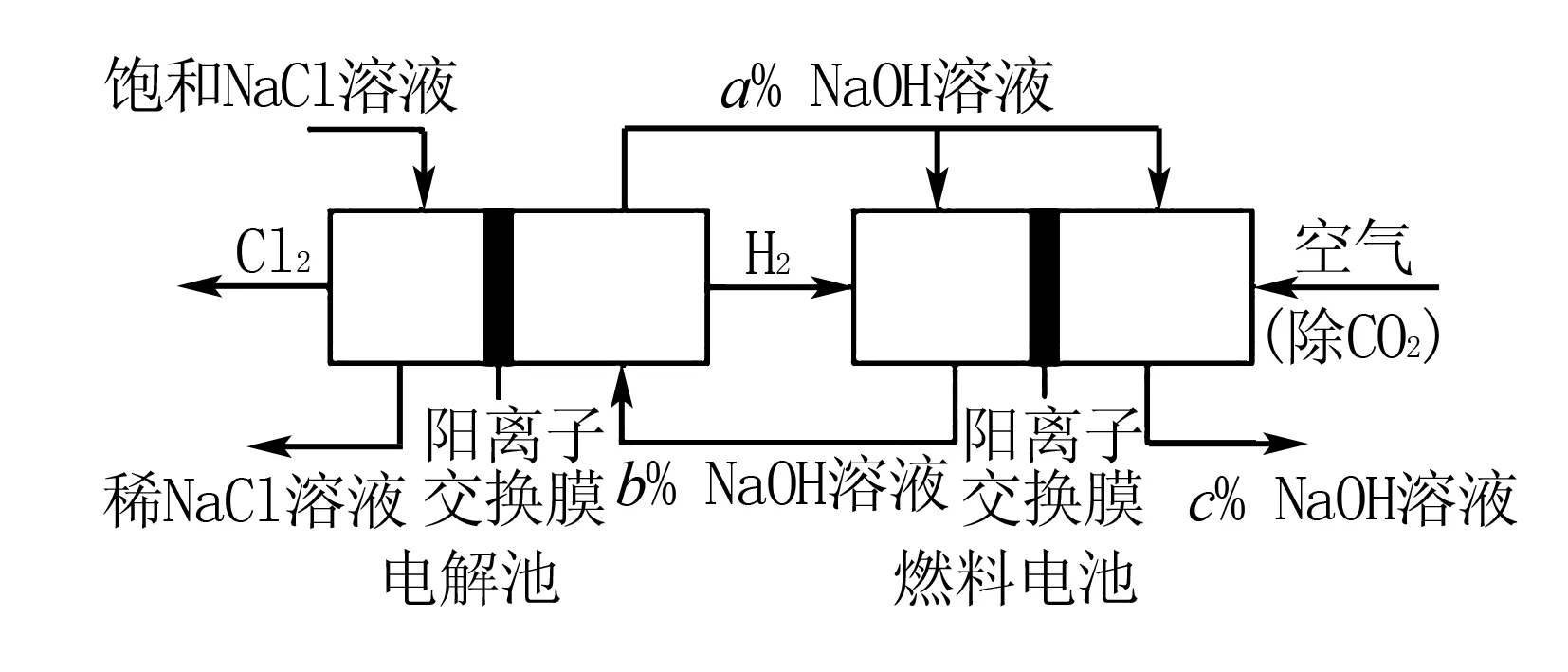

B.相同条件下,当电解池生成2L Cl2,理论上燃料电池应消耗1L O2
C.电解池中阳离子移动流向阴极池
D.溶液a、b、c的pH大小顺序为:a>b>c

三、新课教学和高考复习建议
电化学基础在高中化学中是教学重难点,因此教师在讲授新课时,要注意本章节内容与“溶液中离子平衡”、“氧化还原反应”相关知识构建联系,使其能够分析反应体系中微粒及其运动情况.此外,教师在讲授原电池和电解池工作原理时能够对一次性锌锰干电池与二次铅蓄电池以及燃料电池、电镀金属冶炼等进行分析,使学生不仅能够掌握电极反应和电池反应方程式,还能够体会到电化学与生产、生活密切相关,对人类进步和社会发展起着十分重要的作用.
在高考复习环节,教师要按照考纲要求强化学生对原电池(以Zn-Cu原电池为例)和电解池(电解CuCl2溶液为例)工作原理的掌握,使其熟练掌握电极和电池反应方程式书写方法,能够说出常见化学电源种类及工作原理,清楚地阐明金属发生电化学腐蚀原因,掌握金属腐蚀危害和预防金属腐蚀措施.学生要想做到以上几点就需要教师在高考复习过程中运用一定技巧,比如指导学生熟记基础知识和原电池模型及工作原理;通过类比原电池结构模型准确书写方程式,从有效练习高考经典习题中不断摸索此类型题目解题思路,提高解题速度.

