基于理性设计提高产微球茎菌AG1琼胶酶的热稳定性
郭玉淅 高 贺 倪 辉 ,2,3,4 姜泽东 ,2,3,4 肖安风 ,2,3,4 朱艳冰 ,2,3,4*
(1 集美大学食品与生物工程学院 福建厦门 361021
2 福建省食品微生物与酶工程重点实验室 福建厦门 361021
3 厦门市食品与生物工程技术研究中心 福建厦门 361021
4 厦门市南方海洋研究中心经济海藻资源化利用与深加工重点实验室 福建厦门 361021)
琼胶又称琼脂,是江蓠、紫菜和石花菜等红藻的细胞壁的亲水性多糖,由琼脂糖和琼脂胶组成[1]。琼脂糖是一种由D-半乳糖和3,6-内醚-α-L-半乳糖经 α(1→3)和 β(1→4)糖苷键交替连接而成的链状多糖,是形成凝胶的主要组分。琼脂胶是一种非凝胶组分,具有与琼脂糖类似的多糖链状结构,含有多种取代基,如硫酸酯、丙酮酸乙缩醛、甲基等。琼胶酶能催化水解琼脂糖分子内的糖苷键,产生琼胶寡糖。基于所催化糖苷键的类型差异,琼胶酶分为两大类:α-琼胶酶(E.C.3.2.1.158)和β-琼胶酶(E.C.3.2.1.81),前者作用于琼脂糖的α-1,3 糖苷键,产物是以 3,6-内醚-α-L-半乳糖为还原性末端的琼寡糖;后者作用于琼脂糖的β-1,4糖苷键,产物是以D-半乳糖为还原性末端的新琼寡糖[2-3]。琼胶寡糖水溶性好,易于为人体吸收,具有多种生理功能,如抑菌、抗氧化、抗癌、美白、保湿、益生元等[4-7]。琼胶酶作为一种重要的工具酶,可以制备琼胶寡糖,用于海藻多糖结构研究,水解琼脂糖凝胶并从中回收DNA和RNA,以及制备海藻单细胞和原生质体,被广泛应用于食品、制药和日用化工等领域。
琼胶酶主要存在于海洋微生物和一些海洋软体动物的消化道内[8]。琼脂的热溶液在43℃以下就能凝固形成凝胶[9]。琼脂溶液具有较高的黏度,其随着温度的降低逐渐增加。研究具有良好热稳定性的琼胶酶,对于琼胶的利用具有重要意义。
在先前的研究中,从产微球茎菌AG1(Microbulbifer sp.AG1)中克隆得到琼胶酶基因[10],它的GenBank登录号为KU049031。为获得热稳定性高的琼胶酶,本文采用理性设计方法获得琼胶酶突变体。
1 材料与方法
1.1 材料
1.1.1 菌株 含菌株AG1琼胶酶基因的重组质粒和大肠杆菌(E.coli)BL21由实验室保存;原核表达载体pGEX-6P-1为Novagen产品。
1.1.2 主要试剂 Taq DNA聚合酶、dNTPs、限制性内切酶BamHI和XhoI,为TaKaRa公司产品;T4DNA连接酶,Fermentas公司产品;柱式DNA胶回收试剂盒、质粒DNA小量纯化试剂盒,购买自天根生化科技(北京)有限公司;寡核苷酸引物的合成及核酸序列的测定均由华大基因(上海)股份有限公司完成;Glutathione sepharose 4B,GE Healthcare Life Sciences公司产品;琼脂糖,购于美国Hydragene公司;其余化学试剂均为国产分析纯产品。
1.1.3 主要仪器与设备 ZHWY-2102双层全温度恒温摇床,上海智城分析仪器制造有限公司;Mastercycler gradient PCR仪,德国Eppendorf公司;5810R冷冻离心机,德国Eppendorf公司;UV-5200紫外可见分光光度计,上海元析仪器有限公司;XMTD-8222数显恒温水浴锅,上海精宏实验设备有限公司。
1.2 方法
1.2.1 提高产微球茎菌AG1琼胶酶热稳定性位点的选取 使用PoPMuSiC-2.1在线分析工具[11](http://dezyme.com/)分析菌株AG1琼胶酶序列,在线计算琼胶酶每个突变氨基酸的去折叠自由能变化,选择去折叠自由能显著减少的氨基酸作为突变位点。经分析选择D136N作为突变位点,设计扩增D136N基因的引物,序列如表1所示。
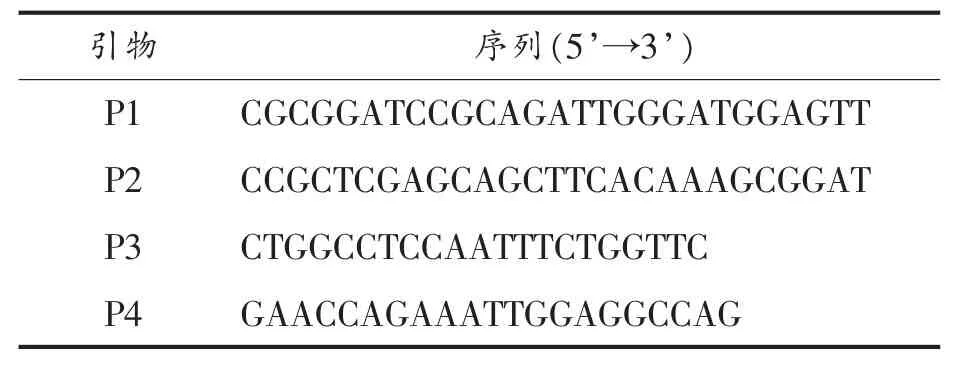
表1 突变体D136N的特异性引物Table1 The specific primers for mutant D136N
1.2.2 突变体D136N基因的获得 采用重叠延伸PCR获得突变体基因。分别以P1和P4、P2和P3为引物,以含有琼胶酶基因的重组质粒为模板,进行PCR,条件为95℃5 min预变性;94℃45 s,50℃45 s,72℃60 s,30 个循环;72℃延伸5 min,回收并纯化PCR产物。取上述两轮PCR纯化产物,加入引物P1和P2扩增全基因片断。最后回收并纯化PCR产物,获得突变体基因。
1.2.3 含突变体D136N基因重组质粒的构建 将突变基因和质粒PGEX-6P-1分别进行BamHI和XhoI的双酶切反应,酶切后的基因片段和表达载体进行连接反应后,转化至E.coli BL21感受态细胞,将其涂布于含氨苄青霉素的LB固体培养基。37℃过夜培养,选取菌落PCR阳性的克隆子,并进行测序,确认插入序列。
1.2.4 突变琼胶酶在大肠杆菌(E.coli)中的诱导表达与纯化 将含有突变体基因的阳性克隆单菌落37℃过夜培养,转接培养至OD600为0.8,加入IPTG至终浓度0.05 mmol/L,22℃诱导表达16 h后,4℃、5 000×g离心 20 min,弃上清,菌体用预冷的PBS缓冲液 (140 mmol/L NaCl,2.7 mmol/L KCl,10 mmol/L Na2HPO4,1.8 mmol/L KH2PO4,pH 7.3)重悬,在冰浴条件下超声破菌后,4℃、12 000×g离心20 min,获得的上清液即粗酶液。参照Glutathione sepharose 4B的使用说明书,采用亲和层析纯化重组蛋白。蛋白质的纯度及分子质量利用SDS-PAGE分析。利用BCA蛋白定量法进行蛋白质浓度测定。
1.2.5 琼胶酶活力的测定 酶活力测定采用DNS法[12]。取580 μL含 0.3%琼脂糖的50 mmol/L Tris-HCl缓冲液(pH 7.5),加入 20 μL 琼胶酶(质量浓度为0.5 mg/mL),60℃反应30 min后,沸水浴10 min终止反应。加入900 μL DNS试剂,混匀后沸水浴10 min,冷却后加蒸馏水定容至5 mL,于540 nm波长下测定吸光值。琼胶酶活力定义为,在上述条件下,每分钟能够水解底物释放1 μmoL还原糖(以D-半乳糖计)所需的酶量。
1.2.6 温度对琼胶酶的影响 分别在不同温度(30,40,50,60,70和 80℃)下检测酶的活力,并以最高酶活力为100%,研究酶的最适反应温度。将酶分别置于不同温度(40,50,60和70℃)下分别放置10~60 min后,测定酶的残余活力,以未经处理的酶活力为100%,研究酶的热稳定性。
1.2.7 pH对琼胶酶的影响 分别用不同pH缓冲液配置0.3%的琼脂糖底物溶液,并测定酶的活力,以最高酶活力为100%,研究酶的最适反应pH。所用的缓冲液为50 mmol/L C6H8O7-Na2HPO4缓冲液(pH 4.0~7.0),50 mmol/L Tris-HCl缓冲液(pH 7.0~9.0),50 mmol/L 甘氨酸-NaOH 缓冲液(pH 9.0~10.0)。将酶分别置于不同pH的缓冲液中,25℃放置1 h后,测定酶的残余活力,以未经处理的酶活力为100%,研究酶的pH稳定性。
1.2.8 动力学参数的测定 分别配制不同浓度的琼脂糖溶液 (0.1,0.15,0.2,0.3,0.4,0.6和 0.8 mg/mL),测定酶在不同底物浓度下的酶活力。利用Lineweaver-Burk双倒数作图法,计算酶的动力学参数,包括 Km,Vmax,kcat和 kcat/Km。
1.2.9 酶的结构分析 利用SWISS-MODEL进行琼脂酶的三维模建,使用PyMOL软件显示并分析酶的结构。
2 结果
2.1 温度对突变体D136N活性及稳定性的影响
在不同温度下测定酶的活力,结果(图1)显示,突变体D136N与野生型同样在60℃下表现出最大活力。突变酶在40~70℃的温度范围内呈现70%以上的相对活力,与野生型相比,突变体D136N在较低温度下表现出更高的酶活力。
酶的热稳定性分析结果见图2。突变体D136N在40,50和60℃热处理1 h后还能保持相对稳定,能够保持超过85%的活力。野生型在50和60℃处理1 h,能分别保持约66%和19%的相对酶活力。突变酶与野生型在70℃下温育10 min都基本失去活力。这些结果表明,突变体D136N相比野生型琼胶酶具有更好的热稳定性。
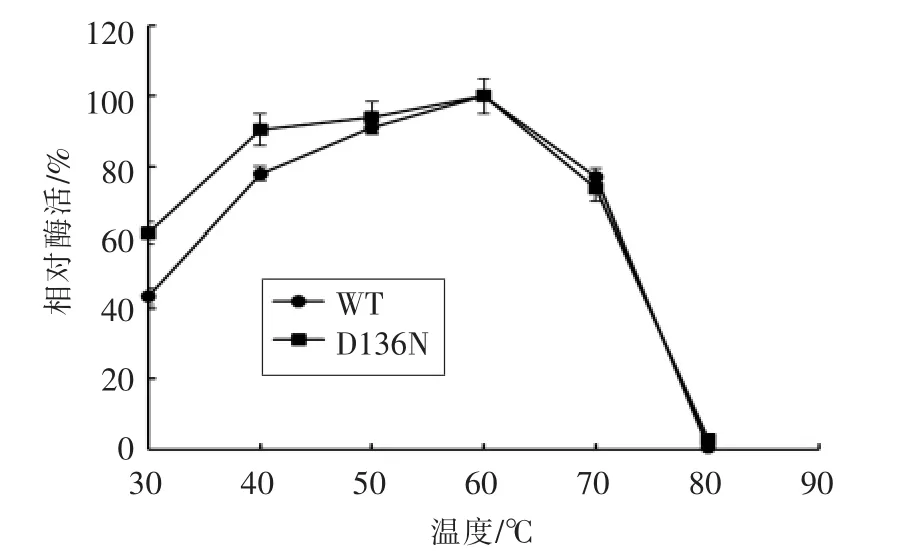
图1 突变体D136N和野生型琼胶酶的最适作用温度Fig.1 The optimum temperature of the mutant D136N and wild-type agarase
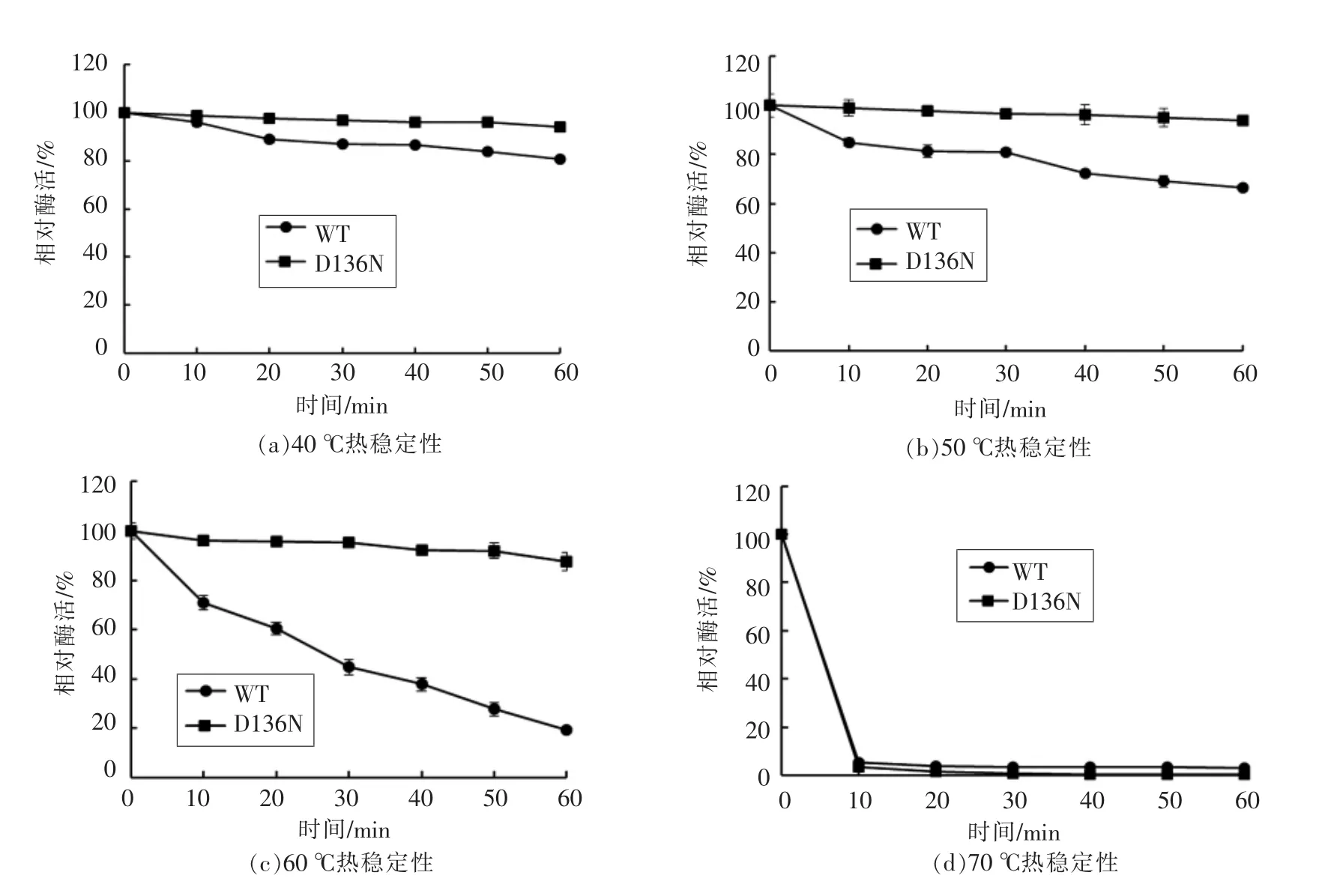
图2 温度对突变体D136N和野生型琼胶酶热稳定性的影响Fig.2 Effect of temperature on the thermostability of the mutant D136N and wild-type agarase
2.2 pH对突变体D136N活性及稳定性的影响
突变体D136N与野生型酶的最适反应pH均为7.5(图3a)。突变酶在pH 6.0~9.0之间保持了较高的活力,具有最高活力的60%以上,在pH 4.0和10.0条件下,酶活力基本丧失。pH稳定性分析结果(图3b)显示,与野生型酶相似,突变体D136N在pH 6.0~9.0范围内具有良好的稳定性,25℃处理1 h后仍能够保持高于80%的活力,但是在pH 10.0的条件下处理后酶稳定性迅速下降。

图3 pH对突变体D136N和野生型琼胶酶的活性(a)和稳定性(b)的影响Fig.3 Effect of pH on the activity (a) and thermostability (b) of the mutant D136N and wild-type agarase
2.3 突变体D136N的动力学参数
以琼脂糖为底物测定酶的动力学参数。结果如表2所示,与野生型相比,突变体D136N的Km值和kcat值增大,Vmax值略微增加,kcat/Km值降低。说明突变体D136N对琼脂糖的亲和能力下降,催化效率也有所降低。

表2 野生型和突变体D136N的动力学参数Table2 Kinetic parameters for wild-type enzyme and mutant enzyme of D136N
2.4 琼胶酶的结构分析
酶的结构分析显示,野生型琼胶酶的Asp136与Asn255形成两个氢键,与Tyr282形成一个氢键(图4a)。突变后的Asn136和Asn255形成3个氢键,与Tyr282形成一个氢键,还与Ala134形成一个氢键(图4b)。因此突变后的136位氨基酸能够与周围氨基酸形成更多的氢键。

图4 突变位点引起的氢键变化Fig.4 Hydrogen bonds changes caused by the mutant site
3 讨论
蛋白质的理性设计是在对蛋白质结构与功能认识的基础上,采用定点突变技术改变蛋白质中的个别氨基酸残基,使蛋白质的性质向着既定的方向改变[13-14]。本文基于理性设计,采用重叠延伸PCR技术,通过将Asp136突变为Asn136,获得热稳定性预计提高的突变体D136N。
将突变体D136N进行诱导表达和纯化,得到突变琼胶酶,并对其酶学性质进行研究。与野生型酶相比,突变体D136N对琼脂糖的亲和能力下降,催化效率也有所降低。突变酶的最适反应温度和最适反应pH与野生型相同。突变体D136N在pH 6.0~9.0范围内稳定,在 40,50和 60℃,该突变酶的热稳定性好于野生型酶。这些性质提高了该突变酶在工业应用上的价值,使其在实际生产应用中具有良好前景。
蛋白质的热稳定性与带电荷残基、疏水氨基酸残基、盐键、氢键、疏水相互作用等因素有关[15-18]。氢键是通过氢原子参与成键的特殊形式的化学键,是维持蛋白质结构的主要作用力之一。Zhu等[19]和Zhou等[20]通过定向进化获得了热稳定性的酶,对于这些酶突变位点的微观结构分析发现,突变体相较于野生型在突变位点附近都产生了新的氢键。本文中,相较于野生型酶,突变体D136N在136位的氨基酸形成的氢键增加2个。增加的氢键可能更有利于维持产微球茎菌AG1琼胶酶的结构,使其具有更好的热稳定性。
——以高中化学“氢键”的教学为例

