疏水改性黄原胶XG-C16溶液性能及微观结构探究
胡钰灵,全红平,黄志宇
(1.西南石油大学 化学化工学院,四川 成都 610500;2.西南石油大学 油气田应用化学四川省重点实验室,四川 成都 610500)
随着油气藏开发的不断深入以及对能源需求的日益增加,非常规油气资源已成为当前勘探开发的热点。聚合物驱是三次采油中的重要手段,目前常用的驱油剂有人工合成的部分水解聚丙烯酰胺和生物聚合物黄原胶两种[1-2]。但随着原油开采难度的增加,对驱油剂的要求越来越高,部分水解的聚丙烯酰胺中残留的未聚合的丙烯酰胺单体影响环境这一问题限制了其应用。因此,具有许多优良特性的黄原胶(XG)具有广泛的应用前景。黄原胶具有悬浮增粘性能、水溶性、耐酸碱等多种优良性能,但仍旧存在着高温下热氧化降解等问题[3-4],本文对其进行改性,以期望获得一种性能优良的驱油剂XG-C16。
1 实验部分
1.1 材料与仪器
黄原胶(纯度>99%),工业品;N,N-二甲基甲酰胺、氢氧化钠、8-苯氨基-1-萘磺酸铵、溴化钾、无水乙醇均为分析纯;1-溴代十六烷,化学纯;去离子水,自制。
DF-101S恒温加热磁力搅拌器;SGR循环水式真空泵;101-2A电热鼓风干燥箱;Bruker AVANCE III HD 400核磁共振波谱仪;HAAKE MARSIII高温高压流变仪;LS55荧光光谱仪;Phenom Pro扫描电子显微镜。
1.2 XG-C16的合成
合成路线见图1。

图1 XG-C16合成路线示意图Fig.1 Route used to synthesize XG-C16
将4.0 g XG在氮气保护下加至N,N-二甲基甲酰胺(DMF)溶液中,在搅拌下缓慢加入NaOH溶液,进行碱化,在反应温度60 ℃,缓慢滴加0.5 g 1-溴代十六烷,搅拌反应9 h,得到淡黄色产物。用乙醇洗涤3次,于50 ℃干燥24 h,得到淡黄色粉末状XG-C16。
1.3 分析方法
1.3.1 核磁共振分析 将少量XG和XG-C16分别溶于重水(D2O)中,使用核磁共振波谱仪对样品结构进行分析。
1.3.2 溶液性能测试 用高温高压流变仪对XG和XG-C16溶液性能进行测试,测试温度为25 ℃,剪切速率为7.34 s-1。
1.3.3 荧光分析 用荧光光谱仪,以8-苯胺-1萘磺酸(ANS)作为荧光探针,对不同浓度的XG溶液和XG-C16溶液进行分析,发射波长为380~690 nm。
1.3.4 扫描电镜分析 用扫描电镜观察XG溶液和XG-C16溶液的微观结构。溶液浓度分别为0.1%和0.3%。
2 结果与讨论
2.1 XG-C16的表征
XG和XG-C16溶液的核磁氢谱图见图2、图3。δ=4.70为溶剂D2O的质子峰。
由图2、图3可知,XG与XG-C16均出现a、b、c、d四个峰,其中δ=1.25和δ=2.10分别为丙酮酸和醋酸基的化学位移,δ=1.98~2.07为主链上大量 —OH的化学位移,δ=3.27~3.7为葡萄糖和甘露糖支链上 —OH的化学位移。


图2 XG的核磁氢谱图Fig.2 1H NMR spectra of the XG


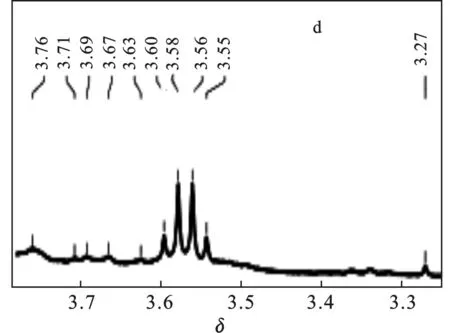
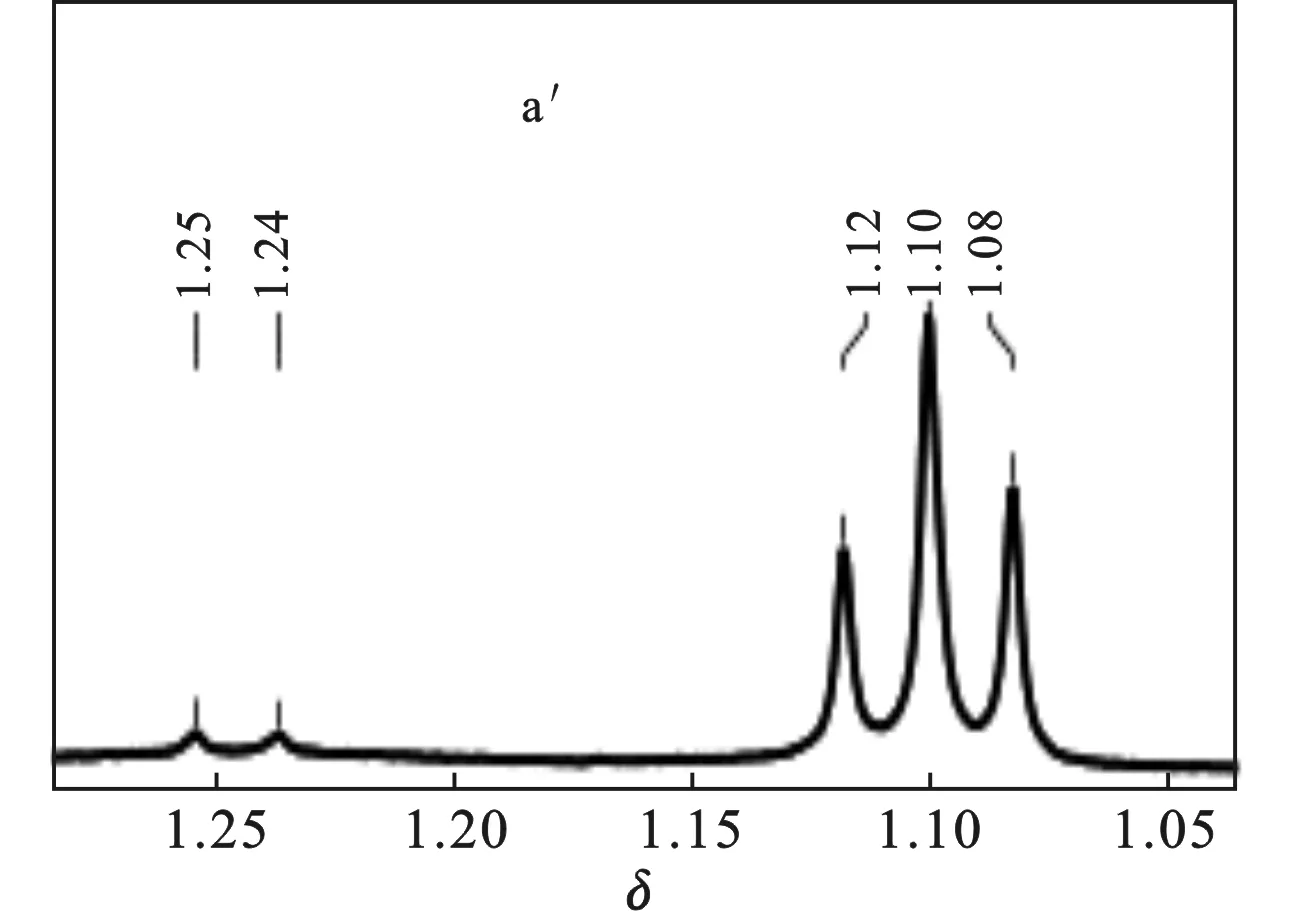
图3 XG-C16的核磁氢谱图Fig.3 1H NMR spectra of the XG-C16
对于XG-C16,可以观察到一些额外的峰(a′和d′),a′处出现的峰是接枝到主链上的长碳链所致,在δ=1.08~1.12处,δ=1.10和1.12为长碳链上的亚甲基中的质子化学位移,δ=1.08处为长碳链长甲基质子的化学位移;d′处出现的化学位移(δ=3.60)归因为化学改性引入的醚键。核磁氢谱分析表明XG-C16制备成功。
2.2 XG-C16临界缔合浓度测定
分别配制XG-C16质量浓度0.075%,0.1%,0.125%,0.15%,0.175%,0.2%,0.3%,0.4%,0.5%的水溶液,使用流变仪对溶液表观粘度进行测定,XG-C16浓度对其水溶液粘度的影响见图4。

图4 浓度对XG-C16溶液粘度的影响Fig.4 The influence of concentration on the viscosity of XG-C16
由图4可知,XG-C16溶液的表观粘度随聚合物溶液的浓度增加趋势为:在低浓度时缓慢增加,超过一定浓度时,粘度增长趋势出现拐点,增长速度突然上升,拐点对应的聚合物溶液质量浓度为0.16%[5],说明XG-C16的临界缔合浓度为0.16%。
2.3 XG-C16微观结构探究
2.3.1 ANS荧光测试 8-苯氨基-1-萘磺酸铵(ANS)作为荧光探针被广泛用于研究蛋白质等大分子组织的微观极性和分子结构,其波长会因为探针从极性介质转移到非极性介质时发生蓝移[6-8]。同时,ANS在水中最大发射波长为520 nm,而在疏水环境下以最大发射波长在460~480 nm之间[9-10]。所以ANS被用来检测由于结合聚合物的分子内/或分子间相互作用而产生的疏水微域的存在,ANS荧光探针测试结果见图5、图6。

图5 不同浓度下XG与XG-C16的ANS荧光光谱图Fig.5 The fluorescence spectra of ANS in XG and XG-C16 at different concentrations
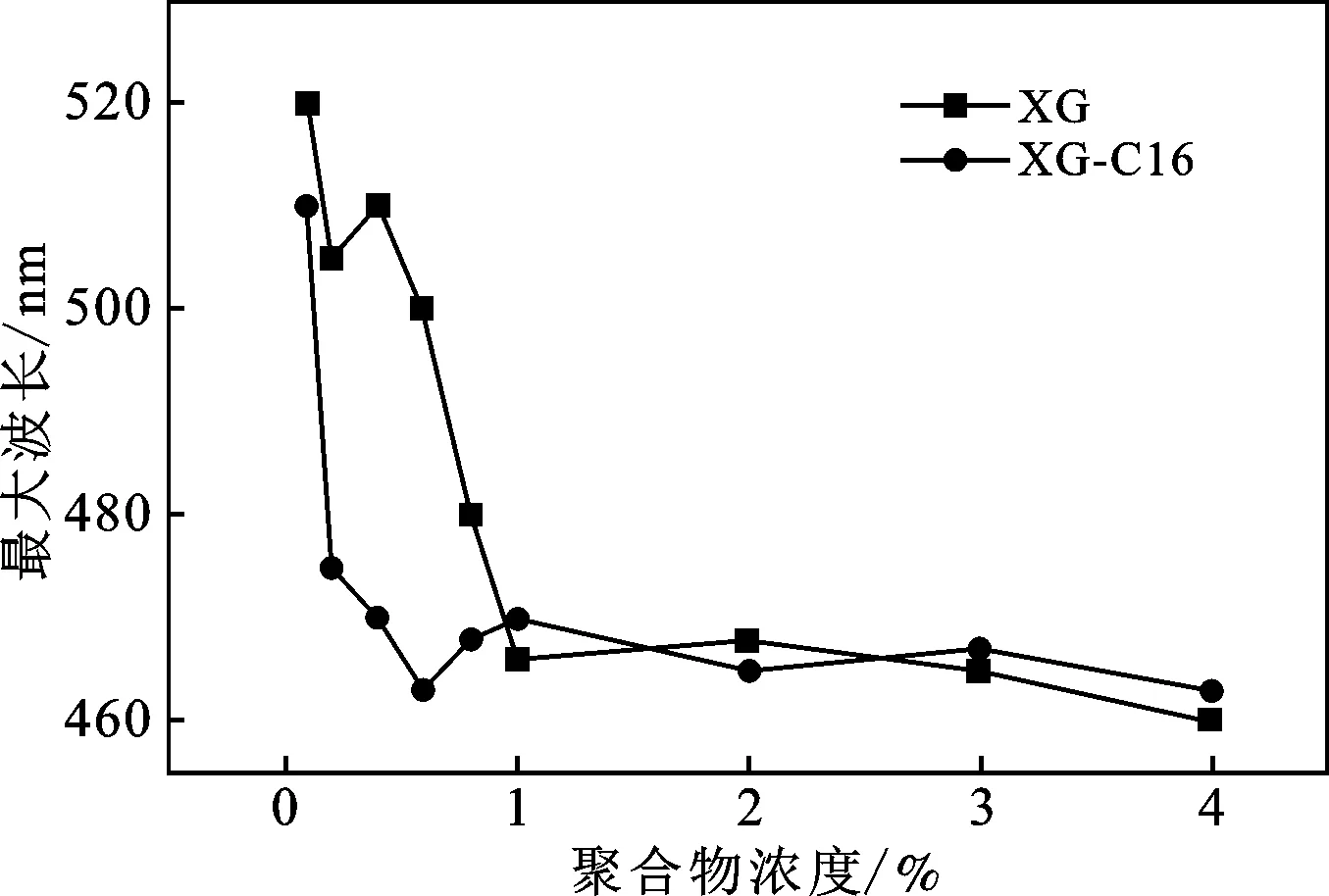
图6 ANS在不同浓度的XG和XG-C16溶液下的最大波长Fig.6 The maximal emission wavelength of ANS in different XG and XG-C16 concentrations
由图5可知,聚合物浓度增加时,XG和XG-C16溶液的荧光强度均有所增加,但XG-C16溶液中的荧光强度增加更明显。同时,随着两种黄原胶溶液浓度的增加,波长均出现蓝移现象。图6表示了黄原胶在不同浓度下ANS的最大发射波长的变化,在浓度为0~0.1%时,所有样品的最大发射波长都有相同的变化趋势,即从510~520 nm急剧减少至460~470 nm,聚合物浓度继续增大,最大波长变化不大,在465 nm处趋于稳定。这表明不管是哪种样品,当黄原胶浓度增大时,ANS均被更多疏水介质包围。
而对于XG溶液来说,溶液中的疏水微区应该来自于黄原胶分子上氢键水溶性聚合物水溶液性质的影响。分子中的氢键是黄原胶螺旋构象的起源,当静电斥力在高离子浓度下被屏蔽时,分子间的氢键形成黄原胶的三级结构(棒状刚性分子结合成空间大分子聚集体)。根据目前的荧光结果,XG溶液浓度高于0.8%后,即使黄原胶没有接枝疏水长链,黄原胶大分子也可通过分子间的氢键形成空间结构,保留疏水性,这解释了图5中未改性黄原胶溶液ANS荧光增加的原因。但对于XG-C16来说,最大发射波长降低对应的溶液浓度因为疏水长链的接枝,大大低于XG,说明疏水长链的引入并未对黄原胶稳定的分子结构造成破坏,同时降低了XG的缔合浓度,改善了黄原胶的其他溶液性能。
2.3.2 扫描电镜测试 根据测定的XG-C16的CAC值,取缔合前后的浓度值,分别配制浓度为0.1%和0.3%的XG和XG-C16的溶液。两种质量浓度的两种聚合物溶液的微观形态放大5 000倍后的图像见图7。

图7 CAC浓度前后XG与XG-C16溶液SEM图像Fig.7 SEM images of XG and XG-C16 before and after associationa.0.1%XG;b.0.3%XG;c.0.1%XG-C16;d.0.3%XG-C16
由图7a、图7c可知,聚合物浓度小于XG-C16缔合浓度(0.16%)时,XG与XG-C16溶液微观形态无明显差别,可以看到明显的棒状结构,这是由聚合物浓度小于CAC时聚合物溶液间无分子间作用,分子内缔合占主导地位,空间网状结构不明显;由图7b、图7d可知,随着聚合物浓度逐渐增大,XG与XG-C16均呈现空间网状结构形态。不同的是,对于XG而言,是由于分子间氢键作用使分子间的形成黄原胶的三级结构(棒状刚性结构结合成空间大分子聚集体),网状结构稀疏,对于XG-C16而言,是由于聚合物溶液浓度大于缔合浓度时,疏水长链缠绕结合,分子间缔合占主导地位,空间网状形态较XG更为致密和稳定。
2.4 XG-C16溶液抗温性能
根据测定的XG-C16的临界缔合浓度,配制浓度为0.1%和0.3%的XG和XG-C16的聚合物溶液,对其进行高温流变测试,结果见图8。


图8 浓度为0.1%(A)和0.3%(B)的XG与XG-C16溶液的抗温曲线Fig.8 High-temperature rheological curve of XG and XG-C16 at the concentration of 0.1%(A) and 0.3%(B)
由图8A可知,聚合物浓度低于CAC时,XG和XG-C16溶液在高温下粘度相差不大,测试前期,XG-C16溶液粘度甚至稍低于XG溶液,这是由于改性过程中,碱化剂会对黄原胶主链分子结构造成一定程度的破坏,但聚合物浓度较低,黄原胶分子未发生缔合,疏水作用对黄原胶溶液粘度贡献不明显。由图8B可知,聚合物浓度高于CAC时,XG-C16溶液中形成分子间缔合,测试前期,XG-C16溶液的粘度不稳定,当温度稳定后,XG-C16溶液粘度逐渐稳定且一直远远高于相同温度下XG溶液粘度[11]。对比两组数据可以看出,随着聚合物浓度增加,聚合物溶液的耐温性能增强,这是由于XG-C16含量越大,形成的空间网状结构越致密,越稳定,所以在高温下能保持更高的粘度,说明XG-C16拥有良好的抗温性能。
2.5 XG-C16溶液抗盐性能
2.5.1 盐加量对XG-C16溶液表观粘度的影响 配制质量浓度分别为0.1%和0.3%的XG和XG-C16溶液,逐渐加入NaCl,每次待NaCl完全溶解后,静止30 min,使用流变仪对溶液的粘度进行测定,NaCl含量对黄原胶溶液粘度的影响见图9。


图9 浓度为0.1%(a)和0.3%(b)的XG与XG-C16溶液的抗盐曲线Fig.9 NaCl resistance curve of XG and XG-C16 at the polymer concentration of 0.1%(a) and 0.3%(b)
由图9a可知,聚合物浓度为0.1%时,XG溶液粘度和XG-C16溶液粘度的变化趋势基本相同,聚合物在盐溶液中粘度先下降然后趋于稳定,这是由于黄原胶分子含有强极性基团,如羧基和羟基,盐溶液中的Na+和黄原胶侧链上的极性基团产生静电效应中和电荷,从而减少静电斥力,降低溶液的粘度。而当侧链的静电斥力相互作用降低后,侧链更容易与主链纠缠,对主链具有更好的保护作用,从而使聚合物溶液随盐浓度增加保持稳定。但对于XG-C16溶液而言,在0.1%的浓度下没有发生分子间缔合,并且化学改性没有改变黄原胶原有的结构,所以在NaCl溶液中XG-C16溶液粘度的变化机理与XG溶液相同,但改性中使用的碱化剂可以在一定程度上破坏黄原胶的纤维素主链,所以XG-C16在NaCl溶液中的最终粘度略低于未改性黄原胶溶液。
由图9b可知,聚合物浓度高于XG-C16临界缔合浓度之后,添加NaCl,两种溶液中均有一个初始粘度下降,但在XG-C16溶液中,溶液粘度随盐浓度增加先保持稳定,后又轻微上升,这可能由两方面的原因导致的:第一,溶液的极性随着盐的加入而增加,形成分子间疏水缔合,进而形成维网的趋势增强;第二,随着盐的加入,XG-C16的疏水部分的溶解度会降低,从而促进水中具有较大水动力体积的分子间聚集物的形成,提高了缔合度[12]。因此,由于长疏水链的存在,所以XG-C16在盐溶液中的粘度远远高于XG溶液,说明XG-C16具有较好的抗盐性。
2.5.2 XG-C16盐溶液的微观形貌 分别在浓度为0.1%和0.3%的黄原胶溶液中加入4%的NaCl,利用电子显微镜观察溶液微观形貌,结果见图10。
由图10可知,低浓度XG和XG-C16溶液未发生缔合,抗盐性差,浓度为0.3%的XG溶液,聚合物分子链中阴离子被Na+屏蔽,分子链卷曲,空间网状结构被破坏,故上述三种溶液中扫描电镜分析图中均只能看到一片盐结晶。对于缔合后的XG-C16溶液,由于引入了长链疏水链,在XG-C16溶液高浓度盐溶液中仍然能观察到较好的空间结构,保持较高的粘度,拥有较好的抗盐性能。
3 结论
(1)通过醚化反应将十六烷基接枝到黄原胶链的羟基上,得到疏水改性黄原胶XG-C16,临界缔合浓度为0.16%。
(2)ANS荧光探针测试表明,改性的条件下,黄原胶的主链保持了原有的有序刚性螺旋结构,但疏水长链的引入降低了XG的缔合浓度,使其具有更好的空间网状结构,相较于XG,XG-C16空间网状结构变得更加致密,这对提高黄原胶的耐温耐盐性能有积极影响。
(3)140 ℃下,0.3%的XG-C16溶液表观粘度(421 mPa·s)是相同浓度下XG溶液表观粘度的3.4倍,具有较好抗温性;5%的NaCl溶液中,0.3%的XG-C16溶液表观粘度为728 mPa·s,且仍能保持良好的空间网状结构,具有良好的抗盐性。

