硫酸介质中具表面活性噻唑衍生物的缓蚀性能研究
陈肖杰,胡志勇,朱海林,马雪梅,王京宝,万祎,李军,曹端林
(中北大学 化学工程与技术学院,山西 太原 030051)
酸洗是工业领域用于设备除垢的一种经济有效的方法,但是酸洗过程会发生氢脆现象[1]。因此,在酸洗时要加入缓蚀剂。苯并噻唑类缓蚀剂是一类阴极型缓蚀剂[2-3],能抑制反应析氢,对于各个工业部门中设备的水垢清洗具有重要意义。文献研究表明[4],改善缓蚀剂在金属表面的吸附性能,可以提高其对金属的缓蚀性能。基于此,本文对2-巯基苯并噻唑(MBT)进行改性使其具有表面活性,能够在碳钢界面定向吸附成膜,继而提高其对碳钢的缓蚀作用。
1 实验部分
1.1 试剂与仪器
具表面活性噻唑衍生物(BTC6T),实验室自制[5];浓硫酸,分析纯;45#碳钢(元素组成(质量分数%):0.5 C,0.37 Si,0.8 Mn,0.04 P,0.045 S,0.25 Cr,0.25 Ni,0.25 Cu,其余为Fe),由扬州市祥玮机械有限公司提供。
AL204电子天平;K100全自动表面张力仪;IM6/IM6E电化学工作站。
1.2 实验方法
1.2.1 表面张力测定 配制一系列不同浓度的BTC6T的硫酸溶液,利用全自动表面张力仪测定20 ℃时各溶液的表面张力γ,绘制γ-logC曲线。
1.2.2 静态失重 本实验所用45#碳钢试片规格为20 mm×10 mm×2 mm,腐蚀介质为 0.5 mol/L H2SO4溶液。分别在20,30,40 ℃的恒温条件下,将准备好的碳钢片悬挂在含不同浓度的缓蚀剂溶液中48 h,取出试片后用丙酮、无水乙醇清洗,冷风干燥后用电子天平称重,根据试片的失重计算其腐蚀速率及缓蚀率。
(1)
(2)
式中M0和M——分别表示腐蚀前后金属试片的重量,g;
A——试片的表面积,m2;
t——测试时间,h;
V0和V——分别表示碳钢在不添加缓蚀剂和添加不同浓度缓蚀剂的腐蚀液中的腐蚀速率,g/(m2·h);
η——缓蚀率,%。
1.2.3 电化学实验 电化学测试设备采用电化学工作站,采用传统的三电极体系,工作电极为45#碳钢(工作面积为1 cm2,其余部分用环氧树脂封装),参比电极为饱和甘汞电极(SCE),辅助电极为铂电极。
1.2.3.1 电化学阻抗谱扫描 测试前电极表面用水相砂纸(150#、400#、600#、800#、1 000#)将45#碳钢逐级打磨抛光至光亮,用丙酮、无水乙醇清洗后干燥,保鲜膜密封待用。开始阻抗谱扫描之前,先将工作电极放入测试电解液中进行开路电压扫描,待开路电压稳定后,外加振幅 5 mV 的正弦微扰电压信号,相对开路电位在 35 mHz~10 kHz 频率范围内自低频向高频扫描,测试温度为20 ℃。
1.2.3.2 动电位极化曲线扫描 极化曲线实验测试温度为20 ℃,扫描速率是 1 mV/s,扫描范围是相对开路电压-0.7~0.4 V。测定0.5 mol/L H2SO4溶液中含不同浓度缓蚀剂的45#碳钢的极化曲线,通过电化学工作站进行数据拟合得到电极反应的动力学参数。
2 结果与讨论
2.1 表面活性
通过表面张力测定方法研究2-巯基苯并噻唑衍生物(BTC6T)的表面活性,其在硫酸溶液中的表面张力随浓度的变化曲线γ-logC见图1。
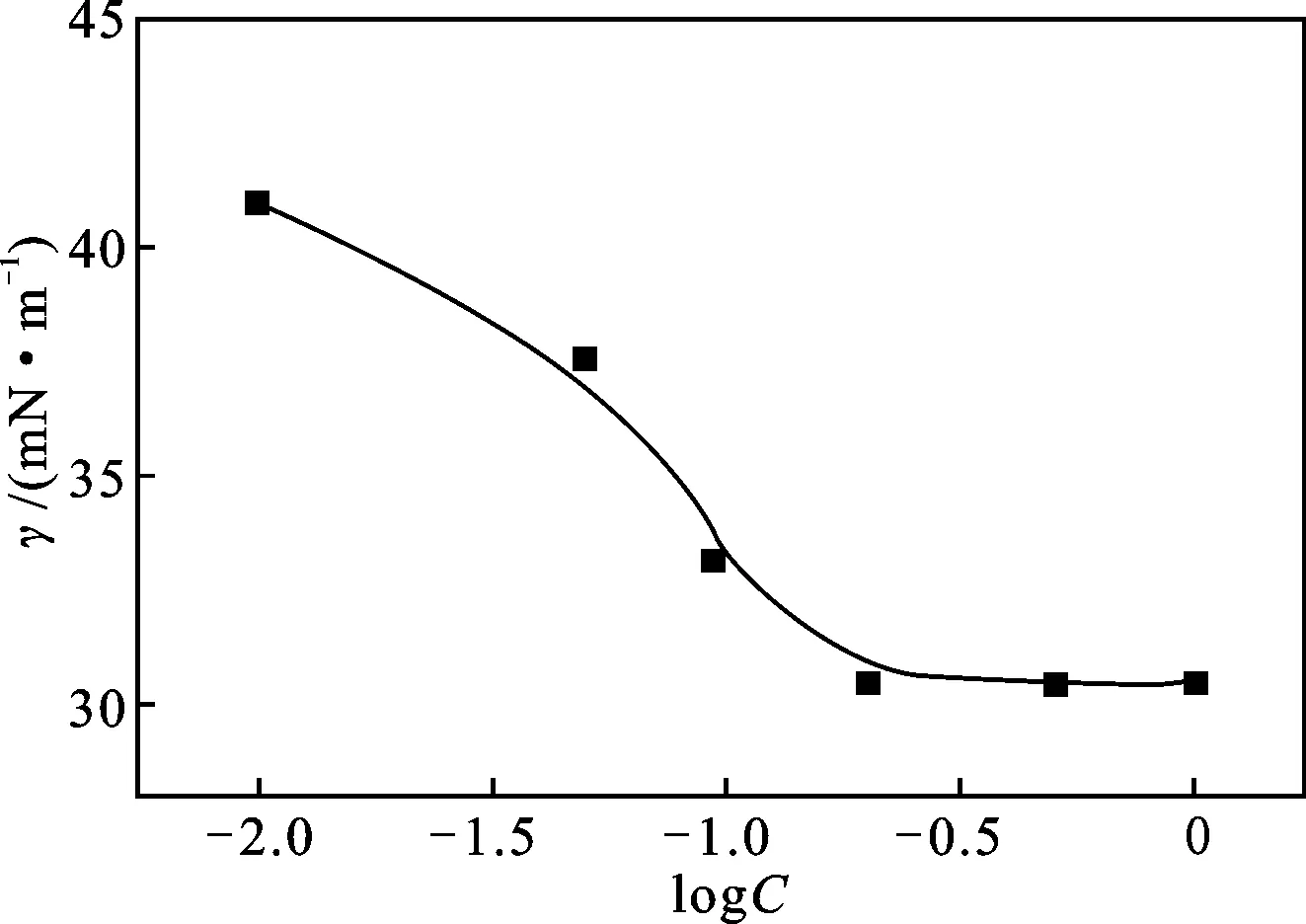
图1 BTC6T的γ-logC曲线(20 ℃)Fig.1 γ-logC curve of BTC6T at 20 ℃
由图1可知,随着BTC6T浓度的增大,其在硫酸溶液的表面张力先是显著下降而后基本保持不变,这主要是由于在BTC6T浓度较低时,随着BTC6T浓度的增加,其在溶液表面的聚集增加,溶液的表面张力骤减,而随着浓度的进一步增加,溶液表面聚集的分子越来越密集,表面张力降低越来越慢,当聚集达到饱和以后,表面张力降至最低,此时再增加BTC6T浓度,溶液表面张力将不再随其变化。表面张力达到最低时,溶液的浓度即为临界胶束浓度(cmc)。由图1可以得到,20 ℃时,BTC6T在0.5 mol/L 硫酸中的临界胶束浓度为0.22 mol/L,最低表面张力γcmc为30.45 mN/m。
2.2 静态失重
静态失重实验结果见图2。
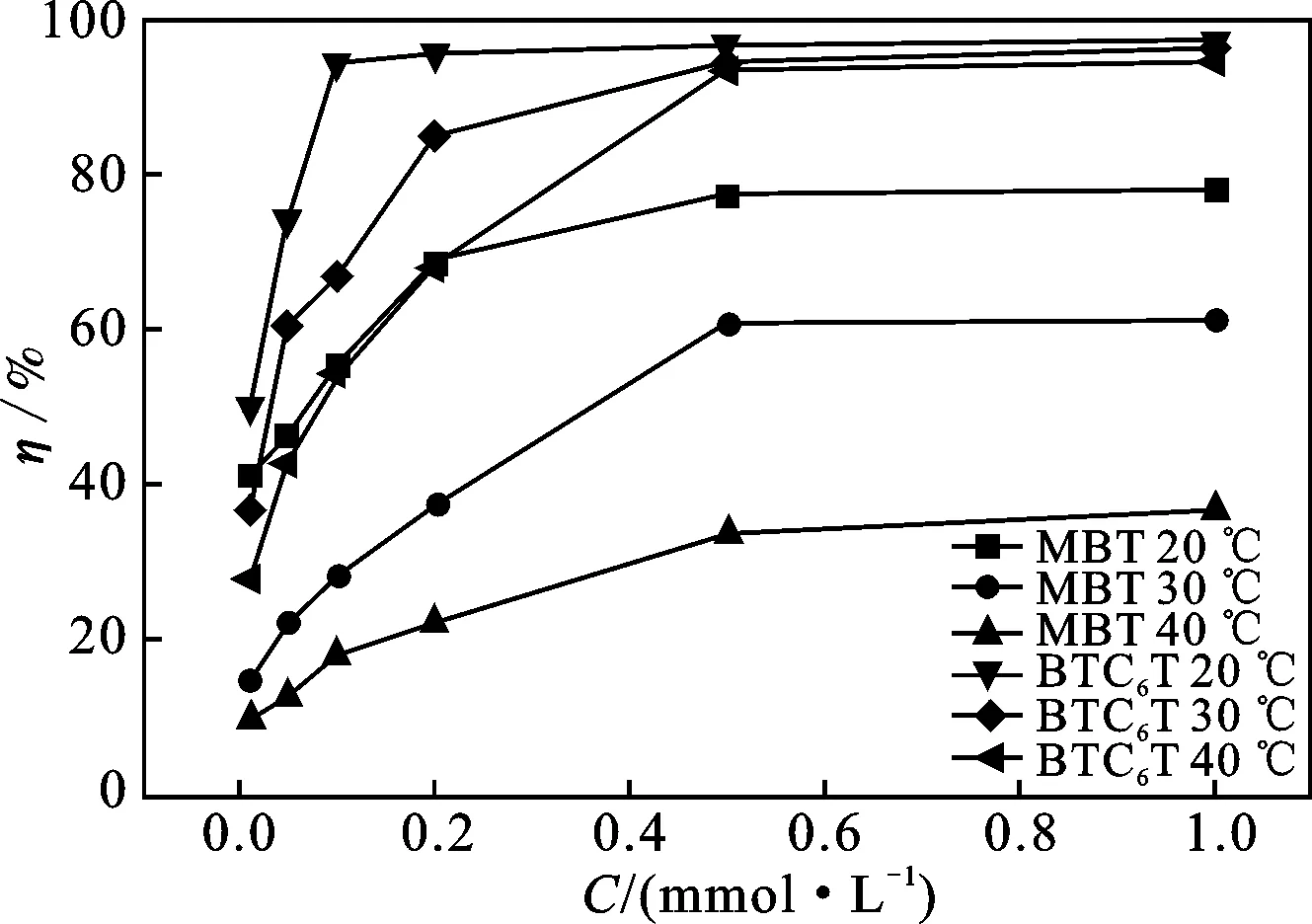
图2 不同温度条件下缓蚀率随MBT与BTC6T浓度的变化曲线Fig.2 Corrosion inhibition efficiency curves of MBT and BTC6T at different temperatures
由图2可知,MBT与BTC6T的缓蚀率均随着浓度的增加而增加,这主要是由于缓蚀剂在碳钢表面吸附形成致密的有机膜,随着缓蚀剂的用量增大,缓蚀剂分子在碳钢表面的覆盖度增加[6]。当两种缓蚀剂用量为0.50 mmol/L时,继续增加缓蚀剂的用量,缓蚀率不再有明显提升,这可能是由于碳钢表面具有有限的吸附量,当缓蚀剂用量达到一定程度时,缓蚀剂在碳钢表面的吸附趋于饱和[7]。因此,两个缓蚀剂最佳用量均为0.50 mmol/L。
由图2可知,MBT与BTC6T的缓蚀率均随着温度的升高而降低,这表明这两种缓蚀剂是温度依赖性缓蚀剂,这可能是由于温度升高导致分子热运动加剧[8],吸附的缓蚀剂从碳钢表面解吸,膜的致密性下降,导致缓蚀率减小。由此说明这两种缓蚀剂与碳钢表面之间存在物理吸附[6,9]。此外,BTC6T对硫酸介质中碳钢的缓蚀率受温度的影响比MBT小,说明BTC6T对热的稳定性优于MBT。
由图2还可知,以45#碳钢为试样,当腐蚀温度及缓蚀剂的用量一定时,BTC6T的缓蚀率远远高于MBT。这可能是由于在硫酸溶液中添加BTC6T后,硫酸溶液的界面张力得到显著的降低,从而促进了缓蚀剂在金属与溶液界面间的吸附。
2.3 电化学实验数据
2.3.1 电化学阻抗谱扫描 碳钢电极在添加不同浓度 MBT、BTC6T 的 0.5 mol/L 硫酸溶液中的电化学阻抗谱以 Nyquist 图的形式在图3中示出。

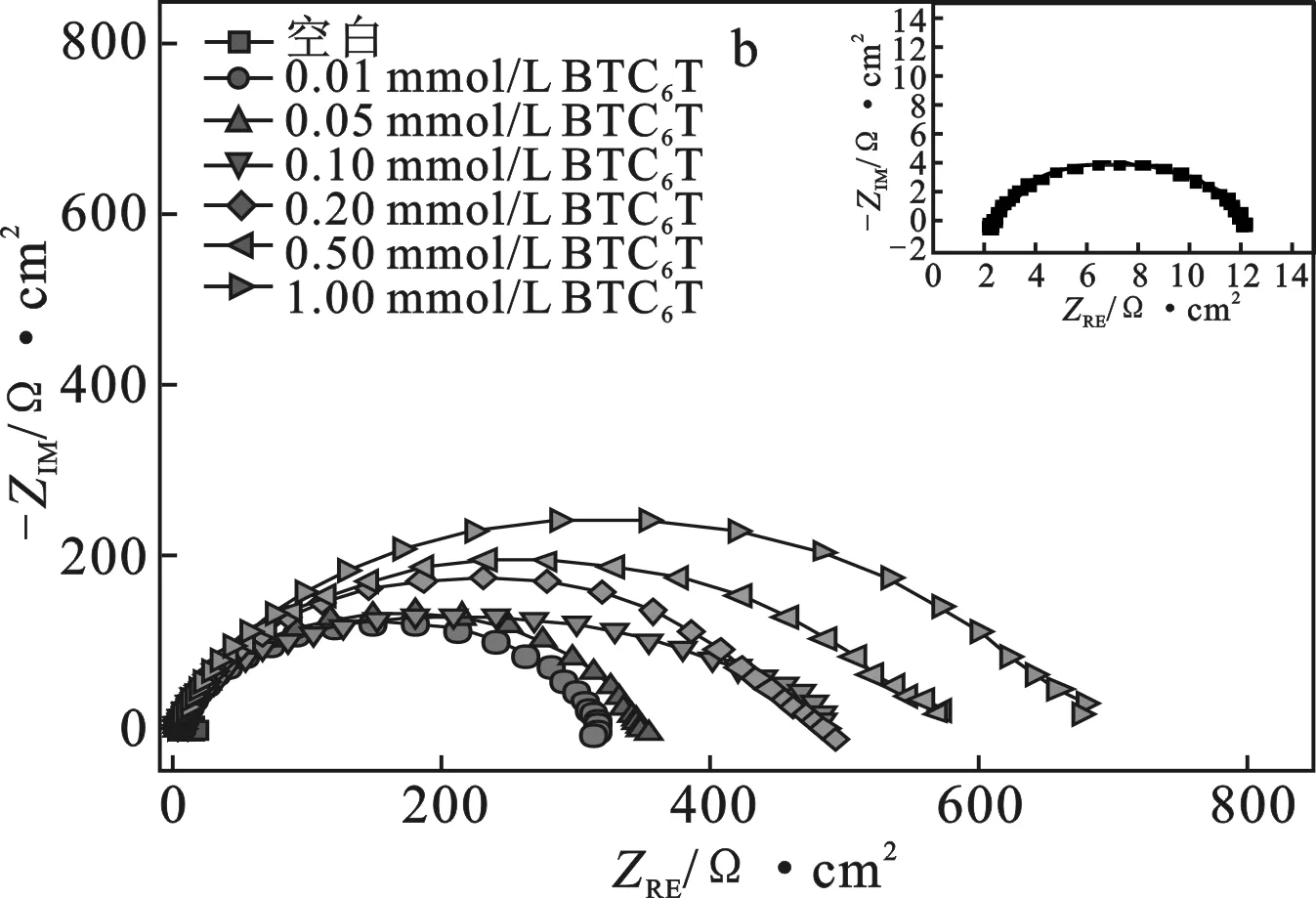
图3 碳钢电极在添加不同浓度MBT(a)及BTC6T(b) 的0.5 mol/L硫酸溶液中的电化学阻抗谱图Fig.3 Electrochemical impedance spectra of carbon steel electrode were added with different concentrations of MBT(a) and BTC6T(b) in 0.5 mol/L sulfuric acid solution
由图3可知,这两个 Nyquist 图在高频时都表现为一个近似半圆的容抗弧,且随着缓蚀剂浓度的增加,容抗弧的直径增大[10]。这可能是由于缓蚀剂分子能够吸附在碳钢电极表面,且随着浓度的增加,电极表面上吸附的缓蚀剂增多,导致腐蚀反应的阻力增大[11]。此外,两个 Nyquist 图在高频时不是完美的半圆,而是呈现凹陷的半圆形式,这主要归因于碳钢电极表面的不均匀性。
由图3a可知,添加缓蚀剂 MBT 后,腐蚀体系的界面阻抗特征发生明显变化,在低频端即将结束时又出现一个不明显的弧(感抗弧),这可能与碳钢电极表面吸附物质的弛豫过程有关[12],也可能是由于碳钢电极在低频下发生再溶解过程[13]。由图3b可知,添加缓蚀剂 BTC6T 后,腐蚀体系的界面阻抗特征并未发生明显变化[14-15],仅仅在高频处呈现一个凹陷的半圆(容抗弧)。
结合图3a和图3b发现,当两个缓蚀剂的添加量相同时,BTC6T 高频弧的直径明显大于 MBT,说明 BTC6T 的缓蚀效果优于 MBT,这与静态失重法测试结果一致。
2.3.2 动电位极化曲线 图4为碳钢电极在添加不同浓度 MBT(a) 及 BTC6T(b) 的 0.5 mol/L 硫酸溶液中的极化曲线。对应的拟合参数包括自腐蚀电位Ecorr、腐蚀电流密度Icorr、阴、阳极Tafel斜率(bc、ba)列于表1。

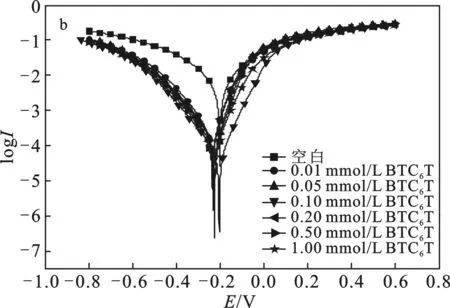
图4 碳钢电极在添加不同浓度MBT(a)及BTC6T(b) 的0.5 mol/L硫酸溶液中的极化曲线Fig.4 Polarization curves of carbon steel electrode were added with different concentrations of MBT(a) and BTC6T(b) in 0.5 mol/L sulfuric acid solution

表1 MBT与BTC6T极化曲线拟合数据Table 1 Fitting data of MBT and BTC6T polarization curve
由图4和表1可知,随着缓蚀剂 BTC6T 和 MBT 浓度的增大,体系的腐蚀电流密度均逐渐减小,缓蚀率增加,这可能是由于随着缓蚀剂浓度的增大,缓蚀剂分子在金属表面所形成的吸附膜越来越致密,保护金属表面不受腐蚀,从而提高缓蚀效果[16]。
由表1可知,添加缓蚀剂BTC6T和MBT后,腐蚀电位的最大位移值<85 mV,说明 BTC6T和MBT是混合型缓蚀剂[17]。由图4可知,BTC6T和MBT降低阴极腐蚀电流密度的趋势更明显,BTC6T和MBT是以阴极为主的混合型缓蚀剂[5]。此外,添加MBT后,阳极腐蚀电流密度增大,金属溶解反应加速,在硫酸介质中是一种危险的金属缓蚀剂;而对于BTC6T,阴、阳极腐蚀电流密度均减小,且 BTC6T 降低腐蚀电流密度的趋势更明显,说明BTC6T缓蚀效果比MBT好,这与静态失重及电化学阻抗谱测试结果一致。这可能是由于缓蚀剂BTC6T具有表面活性,利用其在碳钢表面的定向吸附,亲水基团与碳钢表面发生物理吸附或化学吸附,非极性基团在水溶液中起到疏水作用,因而提高了缓蚀效果[18]。
3 结论
通过表面张力测定研究了BTC6T在硫酸溶液中的表面活性,研究发现20 ℃时,BTC6T在0.5 mol/L 硫酸中的临界胶束浓度为0.22 mol/L,最低表面张力γcmc为30.45 mN/m。
通过缓蚀剂性能评价常用方法(静态失重、动电位极化曲线、交流阻抗谱)研究MBT与BTC6T在0.5 mol/L H2SO4溶液中对45#碳钢的缓蚀效果,所得结论如下。
(1)MBT和BTC6T对硫酸介质中碳钢的缓蚀率均随着浓度的增大而增大,且BTC6T对碳钢的缓蚀效果显著优于MBT。当BTC6T添加量为0.50 mmol/L,在腐蚀时间48 h、温度20 ℃的实验条件下,缓蚀率可达96.84%。
(2)MBT和BTC6T对硫酸介质中碳钢的缓蚀率随着温度的升高而降低,但BTC6T对热的稳定性优于MBT。
(3)MBT 和 BTC6T 是以阴极为主的混合型缓蚀剂。MBT 在酸性介质中是一种危险的金属缓蚀剂,而BTC6T 可以在金属表面发生定向吸附,从而提高缓蚀作用。

