Al-MCM-41 的制备及其对镉的吸附
刘 保,耿奔奔
(1.肥西县环境保护局,安徽 合肥231200;2.安徽馨源环保工程有限公司,安徽 合肥231200)
随着全球工业化的快速发展,环境中重金属污染越来越严重,目前已成为国内外学者的研究重点[1]。镉是一种具有极强毒性的重金属元素之一,其硫化物、卤化物、硝酸盐等均具有毒害作用,给人类健康和生态环境造成了巨大的威胁[2-3]。环境中镉主要来源于矿石冶炼、加工、电镀等过程中排放的废气及废水,同时农药、油漆、染料、玻璃等大量使用也会导致镉排放到环境中[4-5]。目前去除砷的常用方法有化学沉淀法、离子交换法、氧化还原法和吸附法等[6-8]。其中吸附法具有高吸附量、高选择性、吸附速率快、吸附剂廉价易得等优点,在镉污染治理方面具有优势[9-10]。
吸附法是利用吸附剂对镉离子的选择吸附能力,是废水中去除镉的一种方法。常用的吸附剂包括活性炭、废弃物、天壤矿物、金属氧化物和合成材料等[11-13],其中介孔材料具有吸附量大、结构稳定、再生性能好等优点,在环境领域已得到广泛应用[14-16]。Soltani 等[17]合成了MCM-41 及经过氨基修饰的M-MCM-41,并应用于水溶液中Cd(Ⅱ)的去除,结果表明,Cd(Ⅱ)在M-MCM-41上的吸附符合PSO 动力学模型,为化学吸附,在25 ℃下的最大吸附容量为46.73 mg/g。Wanchai 等[18]成功合成了SDS 功能化MCM-41 介孔材料,其对Cd(Ⅱ)具有较强的吸附能力,吸附过程能在30 min 内达到平衡,符合二级吸附动力学方程,且该吸附剂在经过6 次循环后的吸附容量是原始材料吸附容量的70%,具有良好的再生性能。本研究水热合成法制备MCM-41 及铝改性Al-MCM-41 介孔材料,并将其应用于Cd(Ⅱ)的去除,考查其对Cd(Ⅱ)的吸附性能。
1 实验部分
1.1 实验原料
十六烷基三甲基溴化铵(C19H42BrN,CTAB)、氯化铝(AlCl3)、氢氧化钠(NaOH)等均为分析纯,购自上海国药集团化学试剂有限公司;粉煤灰取自合肥某生物滤料厂。粉煤灰的化学组成成分及XRD 图谱分别如表1 及图1 所示。
由表1 和图1 可看出,粉煤灰含有丰富的硅铝成分,其中二氧化硅质量百分含量为55.16%,氧化铝质量百分含量为35.79%。粉煤灰所含的晶体主要为莫来石(Al6Si2O13)相和刚玉(Al2O3),且在25~35°衍射角区域出现了宽大的衍射特征峰,说明粉煤灰含有大量的玻璃体,适合作为硅铝源制备介孔材料。
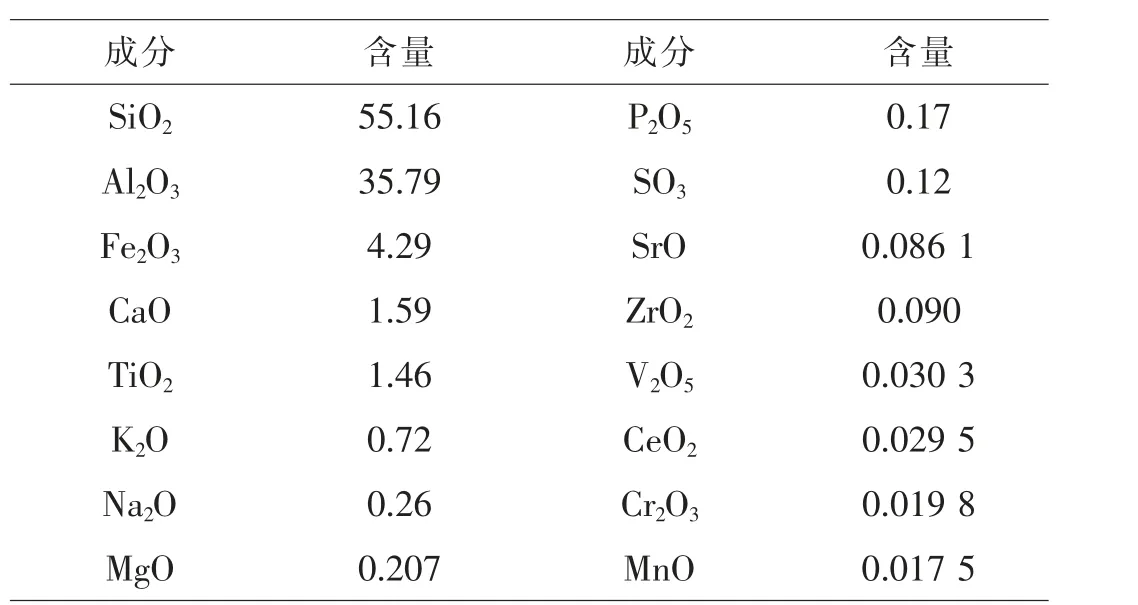
表1 粉煤灰化学成分分析(wt%)

图1 粉煤灰XRD 图
1.2 硅源的提取
配制浓度为7 mol/L 的NaOH 溶液,向溶液加入一定量的粉煤灰,粉煤灰与NaOH 溶液的质量比为1∶8,将混合物置于三口烧瓶中,放在恒速磁力搅拌器上反应5 h,温度为80℃,反应结束后将混合液冷却至室温,离心、抽滤,得含硅上清液,作为原料合成MCM-41。
1.3 MCM-41 的制备
以十六烷基三甲基溴化铵(CTAB)为模板剂,取1.0 g 氢氧化钠溶于200 mL 水中,加入4.85 g 的CTAB,在38 ℃条件下磁力搅拌0.5 h 至液澄清,剧烈搅拌下逐滴加入提取的硅源,混合溶液继续搅拌2 h,反应过程中溶液pH 保持在10 左右,将所得白色凝胶转入聚四氟乙烯晶化反应釜中,110 ℃条件下晶化36 h;取出冷却至室温,过滤、洗涤、干燥,得MCM-41 原粉;将其置于马弗炉中升温至550 ℃,焙烧8 h,得MCM-41 介孔材料。
1.4 Al-MCM-41 的制备
以十六烷基三甲基溴化铵(CTAB)为模板剂,氯化铝(AlCl3)为铝源,在合成过程中直接添加含有金属铝的溶液。取1.0 g 氢氧化钠溶于200 mL 水中,加入4.85 g 的CTAB,在38 ℃条件下磁力搅拌0.5 h 至液澄清,剧烈搅拌下依次加入硅源和氯化铝(AlCl3)溶液,混合溶液继续搅拌2 h,反应过程中溶液pH 保持在10 左右,将所得白色凝胶转入聚四氟乙烯晶化反应釜中,110 ℃条件下晶化36 h;取出冷却至室温,过滤、洗涤、干燥,得Al-MCM-41 原粉;将其置于马弗炉中升温至550 ℃,焙烧8 h,得Al-MCM-41 介孔材料。
1.4 样品表征
采用D8ADVANCE 型X 射线衍射(XRD)、ASAP-2020 型比表面积与孔隙度吸附仪、NANO SEM430 型扫描电子显微镜等表征和分析介孔分子筛的结构和形貌。
1.5 静态吸附实验
称取一定量的吸附剂于一系列250 mL 锥形瓶中,向锥形瓶中倒入100 mL 的Cd2+溶液,用1 mol/L 的NaOH 溶液和HCl 溶液调节pH,在恒温振荡器中振荡一段时间,转速为150 r/min。静置一段时间后取上清液,采用TAS-986 型原子吸收分光光度计测定溶液中Cd2+浓度。Cd2+的吸附量和去除率计算公式如式(1~2)所示:

式中:Qe为平衡吸附容量,mg/g;η 为去除率,%;C0为Cd2+的初始浓度mg/L;Ce为Cd2+吸附平衡时的浓度mg/L;V 为溶液体积,mL;m 为吸附剂投加量,g。
2 结果与讨论
2.1 结构表征
2.1.1 X 射线衍射
图2 是为粉煤灰制备介孔材料MCM-41 和Al-MCM-41 的XRD 谱图。从图2 可看出,两种样品在小角范围内出现了3 个明显的特征峰,在2θ 为2.3°附近有1个强烈的衍射峰,该峰对应于介孔分子筛(100)晶面;在4.0°~4.3°范围内出现2 个衍射峰,分别对应于(110)和(200)晶面,属于典型的介孔结构的特征峰,说明该样品具有长程有序的二维六方介孔结构[19-20]。
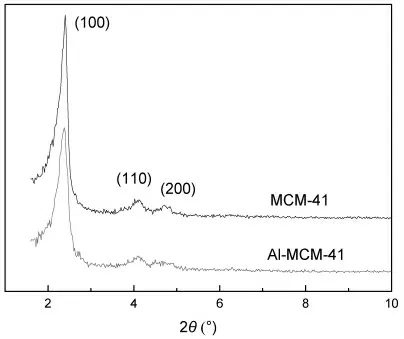
图2 MCM-41 和Al-MCM-41 的XRD 图
2.1.2 比表面积及孔结构分析
介孔材料MCM-41 和Al-MCM-41 的N2吸附脱附等温线和孔径分布如图3 所示。从图3 可看出,两种样品的等温线类型属于典型的Ⅳ型曲线[21],即介孔材料吸附曲线。由BJH 公式计算得出MCM-41 和Al-MCM-41的比表面积分别为1 008.51 m2/g 和782.3 m2/g,孔容分别为0.95 cm3/g 和0.89 cm3/g,孔径分别为2.56 nm 和3.27 nm。Al 离子负载后,占据了介孔材料中的部分孔道,从而导致其比表面积和孔容降低。

图3 MCM-41 和Al-MCM-41 的N2 吸附/脱附曲线
2.1.3 红外光谱(FTIR)
MCM-41 和Al-MCM-41 的红外分析谱图(FTIR)如图4 所示,由图4 可看出,在461 cm-1处的吸收峰是硅氧四面体中Si-O 的弯曲振动峰,在798 cm-1和1 080 cm-1处的吸收峰是硅氧四面体中Si-O-Si 之间的对称伸缩振动和非对称伸缩振动,1 620cm-1处的吸收峰是吸收水变角振动吸收,3 402cm-1处的吸收峰是Si-OH的振动峰[22]。

图4 MCM-41 和Al-MCM-41 的红外光谱图
2.2 静态吸附实验
2.2.1 吸附剂投加量对Cd2+的影响
图5 是MCM-41 和Al-MCM-41 投加量对Cd2+吸附性能的影响。Cd2+的浓度为100 mg/L,溶液pH 值为7,温度为25 ℃,反应时间24 h。由图5 可知,随着吸附剂投加量的增加,Cd2+的去除率不断上升,当吸附剂投加量小于0.35 g/L 时,吸附速率较快,当吸附剂投加量大于3.5 g/L 时,吸附曲线趋于平缓,这是因为随着吸附剂的增加吸附位点也增加,Cd2+吸附去除率上升,当吸附剂投加量增加到一定程度后,吸附剂吸附位点饱和,已将Cd2+吸附完全,吸附去除率不再上升。同时,从图中还发现,经铝改性后的Al-MCM-41 对Cd2+的去除率大于MCM-41,因此后续实验采用Al-MCM-41 吸附剂。
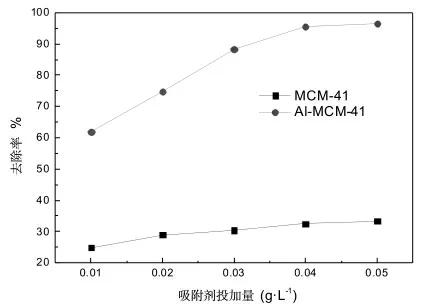
图5 MCM-41 和Al-MCM-41 的用量对吸附性能的影响
2.2.2 pH 对Cd2+的影响
图6 是pH 对Al-MCM-41 吸附Cd2+的影响,Cd2+的浓度为100 mg/L,吸附剂投加量为0.35 g/L,温度为25℃,反应时间24 h。由图6 可知,当pH 值小于3 时,Cd2+的吸附量较低,随着pH 值的增大,Cd2+的吸附量逐渐升高,pH=8 时,吸附量可达到27.57 mg/g,当pH 大于8 之后,Cd2+的吸附量趋于平衡。这主要是因为当pH<3 时,溶液呈酸性环境,存在大量H+与Cd2+竞争吸附位点,当pH>8 时,溶液呈碱性环境,Cd2+水解能力增强,同时与Al-MCM-41 表面硅羟基结合的H+会发生离解,使其表面活性位点增加,因此Cd2+的吸附量升高[23]。

图6 pH 值对Al-MCM-41 吸附Cd2+的影响
2.2.3 温度对Cd2+的影响
图7 是反应温度对Al-MCM-41 吸附Cd2+的影响,Cd2+的浓度为100 mg/L,温度分别为5℃、10℃、15℃、20℃、25℃、30℃、35℃,溶液pH 值为7,吸附剂投加量为0.35 g/L,反应时间为24 h。由图7 可看出,随着温度的增加,Cd2+的吸附量逐渐增加,当温度大于30 ℃时,Cd2+的吸附量不再继续增加,温度对Cd2+的吸附影响较小,最佳反应温度为25℃。

图7 温度对Al-MCM-41 吸附Cd2+的影响
2.2.4 吸附动力学
图8 是Al-MCM-41 对Cd2+的吸附动力学实验结果,Cd2+的浓度分别为50 mg/L、100 mg/L、150 mg/L,溶液pH 值为7,吸附剂投加量为0.35 g/L,温度为25 ℃。由图8 可看出,随着时间的增加,Cd2+的吸附量逐渐增加。当反应时间小于4 h,吸附量上升速度较快,4 h 之后,吸附量上升较少且速率较慢,趋于平缓。同时,Cd2+的浓度增大,相应的吸附量也增大,分别为13.50 mg/g、27.57 mg/g、39.78 mg/g。

图8 Cd2+的吸附动力学
采用准一级动力学模型和准二级动力学模型分析Al-MCM-41 对Cd2+的吸附动力学过程,准一级动力学和准二级动力学方程如式(3)和式(4)所示[24-25]:

式中:qt为t 时吸附剂的吸附容量,mg/g;k1为准一级吸附动力学常数,1/min;qe为反应平衡时吸附剂的吸附容量,mg/g;k2为准二级动力学速率常数,g/mg·min;t 为反应时间,min。

图9 Cd2+的吸附动力学
图9 是Al-MCM-41 对Cd2+的吸附动力学模拟结果,Cd2+的浓度分别为50 mg/L、100 mg/L、150 mg/L 时,准一级动力学方程相关系数分别为0.988、0.986、0.989,准二级动力学方程相关系数分别为0.996、0.996、0.999,均大于准一级动力学方程相关系数,说明准二级动力学方程能够更好地描述Al-MCM-41 对Cd2+的吸附动力学过程。
3 结论
(1)以粉煤灰为原料提取硅源,以十六烷基三甲基溴化铵作为模板剂,氯化铝为铝源,采用水热合成法制备了MCM-41 及Al-MCM-41 介孔材料。MCM-41 和Al-MCM-41 均具有稳定的二维六方介孔结构,铝的添加增大了介孔材料的孔容和比表面积,降低了材料孔径。
(2)将MCM-41 及Al-MCM-41 介孔材料应用于Cd2+的吸附,研究发现,经过铝改性的Al-MCM-41 对Cd2+的吸附去除率比MCM-41 高63%,且随着Al-MCM-41 投加量的增加,Cd2+的吸附去除率逐渐增大,最佳投加量为0.35 g/L。
(3)pH 值对Al-MCM-41 吸附Cd2+的影响较大,在碱性环境下,Al-MCM-41 对Cd2+吸附能力大于酸性环境,这是因为酸性环境下存在大量的H+与Cd2+竞争吸附位点,pH=7 时,Cd2+的吸附容量最大,为27.57 mg/g。温度对Al-MCM-41 吸附Cd2+的影响较小,当温度大于25 ℃时,Cd2+的吸附容量趋于平衡。
(4)从Al-MCM-41 对Cd2+的吸附动力学相关系数来看,三种初始浓度条件准二级动力学方程相关系数均大于0.99,而准一级动力学方程相关系数均小于0.99,说明准二级动力学方程能够更好地描述Al-MCM-41对Cd2+的吸附动力学过程。
(5)铝的添加提高了介孔材料对Cd2+的吸附能力,说明Al-MCM-41 是一种高效的除镉吸附剂,具有良好的发展前景。

