·Cl引发3种环状含有NH结构有机化合物的大气转化机制及动力学
刘聪,马芳芳,付自豪,谢宏彬,陈景文
大连理工大学环境学院,工业生态与环境工程教育部重点实验室,大连 116024
大气氯自由基(·Cl)与有机污染物具有强的化学反应活性。一般来说,·Cl与很多大气有机污染物的反应速率常数比羟基自由基(·OH)高一个数量级[1-5]。过去一直认为·Cl主要存在于沿海地区,通过卷入海盐的多相反应生成[2,6-9]。考虑到·Cl和·OH的浓度以及大气氧化能力[10-12],·Cl对有机污染物的转化贡献大约是·OH的10%~100%。更重要的是,2010年Thornton等[13]发现,在美国内陆地区氮氧化物与无机氯化合物反应能生成·Cl的前体物ClNO2。此后该前体物在其他国家(如加拿大、德国、英国和中国)的内陆地区也陆续被检出[14-18]。·Cl在内陆地区的发现表明,·Cl对有机污染物的转化可能起着比以前更为重要的作用。最近的研究发现,在区域尺度上,·Cl对烷烃转化的贡献强于·OH[19]。此外,·Cl引发有机污染物的转化可能导致与·OH引发反应不同的大气归趋及环境风险[20-21]。因此,亟待关注·Cl引发有机污染物的大气转化。
含有NHx(x = 1, 2)结构的有机化合物是一类潜在的大气污染物。目前,在大气中已检测出了160种含有NHx(x = 1, 2)结构的有机化合物,如脂肪胺、芳香胺、酰胺、哌嗪(PZ)、吗啉(MOR)、哌啶(PIP)、吡咯烷(PYR)和氨基酸等[22-23]。被大气中的·OH和·Cl等氧化剂氧化是这些物质去除的主要途径[24-25]。在众多的氧化产物中,N中心自由基可以和NO反应形成致癌性的亚硝胺[20,26],增加环境风险。因此,在含有NHx(x = 1, 2)结构的有机化合物的风险评价中,N中心自由基成为最被关注的一类产物。很多研究表明,·Cl与NHx(x = 1, 2)基团能够形成特殊的相互作用[27],导致·Cl引发含有NHx(x = 1, 2)结构有机化合物的大气氧化是形成N中心自由基的主要途径之一。
近年来,·Cl引发含有NHx(x = 1, 2)结构有机化合物的大气转化引起了科研工作者的广泛关注。已有研究表明,·Cl可引发简单的链状含有NHx(x = 1, 2)结构的有机化合物(如甲胺(MA)、二甲胺(DMA)和乙醇胺(MEA))的大气氧化反应[12,20],该反应中,NHx(x = 1, 2)基团与·Cl能够形成独特的两中心三电子键(2c-3e键)[27],这使得·Cl夺取N—H的H生成N中心自由基成为反应的主要路径。然而,对于链状含有NHx-键结构的p-π共轭有机化合物的研究发现[28],并不是所有的含有NHx(x = 1, 2)结构有机化合物与·Cl反应都会生成N中心自由基。这些研究表明·Cl引发含有NHx(x = 1, 2)结构有机化合物反应生成N中心自由基具有结构依赖性。因此,为了综合地评估含有NHx(x = 1, 2)结构的有机化合物的大气归趋及环境风险,为将来建立·Cl引发含有NHx(x = 1, 2)结构有机化合物反应的结构活性关系提供数据支撑,需要深入研究·Cl引发不同结构的含有NHx(x = 1, 2)结构的有机化合物的大气转化机制和动力学。
在大气中检测出的160种含有NHx(x = 1, 2)结构的有机化合物中,环状含有NH结构的有机化合物是重要的一类。然而,目前大多数研究主要集中在·Cl引发链状含有NHx(x = 1, 2)结构的有机化合物的转化,很少关注环状含有NH结构的有机化合物。唯一研究的环状含有NH结构的有机化合物是笔者最近报道的环状二胺PZ[26]。大气中检出的环状含有NH结构的有机化合物还包括MOR、PIP和PYR等,它们主要用于工业溶剂,以及药物、杀菌剂和杀虫剂的合成等[29-31],其中PIP和MOR在颗粒相中也有检出[32]。作为笔者对·Cl引发环状含有NH结构的有机化合物转化研究的延续,本文研究·Cl引发MOR、PIP和PYR的大气转化机制及动力学。
1 计算方法(Computational methods)
1.1 全局极小点的确定
由于MOR、PIP和PYR在气相中具有不同的构型,因此,在研究·Cl引发三者的反应机制前,需要确定MOR、PIP和PYR在大气中最稳定的构型,即全局极小点。为了得到足够的构型,本文选用从头算分子动力学(AIMD)模拟方法来获得3种模型化合物的一系列构型。AIMD模拟使用TURBOMOLE程序[33],在BLYP-D/def2-SV(P)理论计算水平下进行。温度设置为500 K,模拟时间为10 ps,步长为2 fs[34]。使用VMD软件筛选获得的全部构型,分别在M062X/6-31+G(d,p)和M062X/6-311+G(3df,2p)计算水平下对筛选出来的结构进行优化和单点能计算,该计算在Gaussian 09软件包中进行[35]。最后选择具有最低吉布斯自由能的结构作为全局极小点来进行反应机制和动力学的研究。最稳定构型如图1所示。
1.2 电子结构计算
电子结构优化和能量计算均使用Gaussian 09软件包[35]。在所有反应路径中,反应物、反应前络合物、过渡态、反应后络合物和产物的结构优化和频率计算在MP2/6-31+G(d,p)计算水平下进行。通过内禀反应坐标(IRC)计算进行过渡态验证,确认其连接指定的反应物和产物。单点能在CCSD(T)/6-311+G(2df,2p)水平下进行计算。每个物质的能量通过公式(1)获得:
E = ESP+ Ecorr
(1)
式中:ESP为CCSD(T)/6-311+G(2df,2p)计算水平下的单点能;Ecorr为MP2/6-31+G(d,p)计算水平下的零点校正能。考虑到自旋轨道耦合效应,对孤立的·Cl进行校正(0.8 kcal·mol-1)[12]。使用自然键轨道(natural bond orbital, NBO)计算反应前络合物中每个原子的电荷[36]。
1.3 动力学计算
使用MultiWell-2014.1软件包[37-38]进行动力学计算。基于MP2/6-31+G(d,p)水平下优化的结构和CCSD(T)/6-311+G(2df,2p)水平下的能量,得到态密度和体系的反应能垒,使用Rice-Ramsperger-Kassel-Marcus (RRKM)理论计算反应速率常数[39]。主方程的能量格子设置为每10 cm2000,并连续执行到85 000 cm-1。选择N2作为反应体系的浴气[34]。

图1 MP2/6-31+G(d,p)水平下优化得到的MOR、PIP、PYR以及·Cl引发反应中重要络合物和过渡态的结构注:MOR表示吗啉,PIP表示哌啶;PYP表示吡咯烷;“RCm-n”和“TSm-n”分别表示反应中的反应前络合物和过渡态;“m”和“n”分别表示不同的反应和不同的物质。白色 = H原子;灰色 = C原子;蓝色 = N原子;红色 = O原子;绿色 = Cl原子。长度单位为0.1 nm。Fig. 1 Optimized structures of MOR, PIP, PYR, important pre-reactive complexes and transition states involved in the ·Cl initiated reactions at the MP2/6-31+G(d,p) level of theoryNote: MOR, PIP and PYP stand for morpholine, piperidine and pyrrolidine, respectively. The symbols “RCm-n” and “TSm-n” denote the pre-reactive complexes and transition states involved in the reactions, respectively; “m” and “n” denote different reactions and species, respectively. White = H-atoms, grey = C-atoms, blue = N-atoms, red = O-atoms and green = Cl-atoms. The distances is shown in 0.1 nm.
采用Gilbert等[40]和Joback等[41]的经验方法计算络合物的Lennard-Jones (LJ)参数。N2与反应活性中间体的碰撞转移速率通过一次下降指数模型来描述,模型的平均转移能量为200 cm-1。使用弥散的长程过渡态理论(long-range transition state theory with a dispersion force potential)计算反应络合物形成的反应速率常数[42]。在所有反应速率常数计算中,考虑隧道效应[43]。总的反应速率常数k(T)通过公式进行计算:
k(T) = k∞(T)(1-反应物)
(2)
式中:k∞(T)是化合反应的高压极限速率常数,反应物是反应物的产物分支比。
2 结果与讨论(Results and discussion)
2.1 ·Cl引发反应的反应机理
·Cl与有机化合物的反应机制主要包括氢夺取和加成到不饱和键2种类型。由于MOR、PIP和PYR是饱和分子,因此,在·Cl引发3种环状含有NH结构的有机化合物的反应中,只能发生氢夺取反应,包括·Cl夺取—CH2—(垂直位置和平伏位置)和—NH上的H原子。由于3个物质都具有Cs对称性,因此,3个引发反应需要考虑的氢夺取位点分别减少为—CH2—CH2—NH—(MOR);—CH2—CH2—CH2—NH— (PIP) 和—CH2—CH2—NH— (PYR)。优化的结构,如反应物、重要络合物和过渡态,如图1所示;·Cl与MOR、PIP和PYR的反应势能面如图2所示。可以看出,每条反应路径都经过反应前和反应后络合物。由于环状反应物不是平面分子,因此,夺取平面上下两侧的氢会经过不同的反应前络合物。其中·Cl引发MOR反应中,存在一个O…Cl相互作用的反应前络合物(RC1-1)。通过反应能垒(Ea)可以看出,在·Cl引发MOR、PIP和PYR反应中,·Cl通过过渡态TS1-5、TS2-6和TS3-4夺取N—H的H比夺取C—H的H更容易发生。因此,从动力学角度来看,生成N中心自由基(MOR-N、PIP-N和PYR-N)是最可行的反应路径。这与·OH引发MOR的反应不同(主要生成C中心自由基),与·Cl引发MA、DMA、MEA和PZ反应相似[12,20,26],而与·Cl引发酰胺的反应不同[28]。此外,我们对比了·Cl引发MOR、PIP和PYR反应中夺取N—H的H的过渡态结构,发现,N—H键键长并没有明显的伸长,分别为0.1042、0.1044和0.1046 nm;Cl—H键键长分别为0.1909、0.1904和0.1914 nm,这表明·Cl与3种环状含有NH结构有机化合物反应的最可行路径的过渡态是类反应物过渡态。此外,我们发现,除了没有找到过渡态的2个位点,·Cl与—CH2—的垂直位置的H反应的能垒低于对应的平伏位置的H(TS1-1< TS1-2、TS1-4< TS1-3、TS2-2< TS2-3、TS2-5< TS2-4、TS3-3< TS3-2),因此,·Cl夺取垂直H应该比夺取平伏H更容易。这与我们之前研究的·Cl与PZ的反应类似[26]。需要指出的是,尽管做了很多的尝试,我们仍然没有找到·Cl夺取PIP和PYR中与—NH相邻的—CH2—中垂直位置H的过渡态。根据前人·Cl引发链状含有NHx(x = 1, 2)结构有机化合物反应的研究[12,20,26],我们假设·Cl夺取—CH2—上的H不会与夺取NHx上的H产生竞争。因此,缺失的数据不会影响本研究的结论。
从图2可以看出,与·Cl引发链状含有NHx(x = 1, 2)结构有机化合物(如MA、DMA和MEA)反应相似,·Cl引发3种环状含有NH结构的有机化合物生成N中心自由基的反应路径会经过一个稳定的反应前络合物(RC1-2、RC2-2和RC3-2)。由于·Cl与NH基团形成了独特的2c-3e键,从而导致·Cl与3种环状含有NH结构有机化合物反应时,夺取N—H的H更容易。通过计算反应前络合物的NBO电荷可知,RC1-2、RC2-2和RC3-2中Cl原子上的电荷分别为-0.32 e、-0.34 e和-0.33 e,表明3个反应前络合物均属于电荷迁移络合物[44]。此外,通过比较MOR、PIP和PYR的气相碱度发现[45],3个反应前络合物的稳定性顺序(RC2-2> RC3-2> RC1-2)与3个环状含有NH结构有机化合物的气相碱度的顺序(PIP > PYR > MOR)一致,表明具有较强气相碱度的含有NHx(x = 1, 2)结构有机化合物具有较强的供电子能力,能够增加反应前络合物中2c-3e键的强度。
2.2 ·Cl引发反应的动力学
使用主方程方法,在298 K和1 atm下,计算得到·Cl引发MOR、PIP和PYR反应的总反应速率常数(kCl)分别为5.010-10、5.110-10和4.910-10cm3·molecule-1·s-1,与·Cl引发MA (2.910-10cm3·molecule-1·s-1)、DMA (3.910-10cm3·molecule-1·s-1)、MEA (3.610-10cm3·molecule-1·s-1)和PZ (4.710-10cm3·molecule-1·s-1)的反应速率常数值接近[12,20,26]。如图3所示,在230~330 K温度范围内,计算的kCl值随温度增加而增加,表明kCl具有正的温度依附性。同时,我们也计算了3个反应的产物分支比。结果发现,在298 K和1 atm下,·Cl引发MOR、PIP和PYR反应生成N中心自由基(P1-3、P2-5和P3-3)的分支比()分别为98.97%、99.64%和98.89%,表明引发反应的主要产物是N中心自由基。此外,从图3可以看出,N中心自由基的值随温度上升略有降低,其他产物的值随温度增加而增加,但仍然很低,可以忽略。因此,以上结果再次证明,在大气条件下,·Cl引发3个环状含有NH结构的有机化合物的反应主要形成N中心自由基。
3 环境意义(Implications)
和之前·Cl引发MA、DMA、MEA和PZ的研究类似[12,20,26],由于2c-3e键及电荷迁移络合物的生成,·Cl夺取N—H的H生成N中心自由基是·Cl引发MOR、PIP和PYR反应的最佳反应路径。在298 K和1 atm下,计算的kCl分别为5.010-10(MOR)、5.110-10(PIP)和4.910-10(PYR) cm3·molecule-1·s-1。在这3个环状含有NH结构的有机化合物中,只能找到·OH引发MOR和PIP的反应速率常数(kOH)和MOR的产物分支比[46]。通过这些数据计算·Cl和·OH引发反应的准一级反应速率常数比(kCl[·Cl]/kOH[·OH],[·Cl]和[·OH]分别为·Cl和·OH的浓度)来评价·Cl和·OH对于MOR和PIP转化的贡献。在海洋边界层,[·Cl]大约为[·OH]的1%~10%,计算得到·Cl对MOR和PIP转化的贡献分别是·OH的2.6%~26%和6.9%~69%。结合·OH引发MOR反应生成MOR-N中心自由基的产物分支比(10%)[46],计算得到·Cl引发MOR生成MOR-N中心自由基的贡献(kCl[·Cl]×N,·Cl)/(kOH[·OH]×N,·OH),其中,N,·Cl和N,·OH分别表示·Cl和·OH引发反应中N中心自由基的产率)是·OH的25%~250%。这些结果表明·Cl在MOR、PIP的转化和MOR-N中心自由基生成中起着重要作用。本文的研究结果为将来建立·Cl引发含有NHx(x = 1, 2)结构有机化合物反应的结构-活性关系、全面地评估含有NHx(x = 1, 2)结构有机化合物的大气归趋和环境风险提供数据支持。
致谢:感谢大连理工大学超算中心给予的计算资源支持。

图2 ·Cl引发MOR(A)、PIP(B)和PYR(C)反应的势能面注:“Rm”、“RCm-n”、“TSm-n”、“PCm-n”和“Pm-n”分别表示反应物、反应前络合物、过渡态、反应后络合物和产物。“m”和“n”分别表示不同的反应和不同的物质。Fig. 2 Schematic free energy surfaces for the MOR + ·Cl (A), PIP + ·Cl (B) and PYR + ·Cl (C) reactionsNote: The symbols “Rm”, “RCm-n”, “TSm-n”, “PCm-n” and “Pm-n” denote the reactants, pre-reactive complexes, transition states, product complexes and products involved in the reactions, respectively. “m” and “n” denote different reactions and species, respectively.
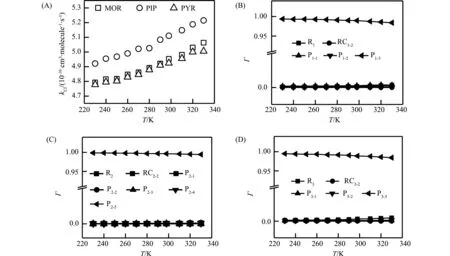
图3 在230~330 K范围内·Cl引发MOR、PIP和PYR反应的速率常数(kCl)的变化(A),以及·Cl引发MOR(B)、PIP(C)和PYR(D)反应生成Rm、RCm-n和Pm-n的产物分支比()的变化注:“Rm”、“RCm-n”和“Pm-n”分别表示反应中反应物、反应前络合物和产物,“m”和“n”分别表示不同的反应和不同的物质。Fig. 3 Variation of reaction rate constants (kCl) for the reactions of MOR, PIP, and PYR with ·Cl in the temperature range of 230~330 K (A); Variation of branching ratios () for the formation of Rm, RCm-n, and Pm-n for the reactions of MOR + ·Cl (B), PIP + ·Cl (C), and PYR + ·Cl (D) at 1 atmNote: “Rm”, “RCm-n”, and “Pm-n” denote the reactants, pre-reactive complexes and products involved in the reactions, respectively; “m” and “n” denote different reactions and species, respectively.

