微生物法测定婴幼儿配方食品中生物素的不确定度评估
商迎辉 章丽娜 李梦洁 赵范范 刘馨君 魏 俊 黄汉昌 劳凤学
(北京市生物活性物质与功能食品研究院 北京联合大学功能因子与脑科学研究院生物化学工程学院 北京 100191)
生物素(Biotin)又称维生素 B7、维生素 H,是一种水溶性B族维生素,由含有一个硫原子的脲基环和一条戊酸的侧链组成,目前已知8种异构体。天然存在的D-生物素具有活性,为哺乳动物5种生物素依赖性羧化酶的辅酶,在催化糖原异生,氨基酸分解代谢和脂肪酸合成中起关键作用。生物素还通过共价键与组蛋白结合,在调节基因稳定性和表达中起重要作用[1]。
生物素缺乏症(Biotin deficiency)以皮肤、黏膜和神经系统损害为主[2]。生物素主要来源于酵母、花椰菜、坚果类、蛋黄、肝脏和肾脏。人体肠道内细菌可合成一些生物素,一般情况下极少缺乏。然而,由于婴幼儿肠道功能较弱,需在婴幼儿食品中强化生物素,以避免生物素缺乏症的发生[3]。
生物素测定方法有微生物法、同位素稀释法、比色测定法、荧光测定法、化学分光法、薄层色谱法、气相色谱法、高效液相色谱法、液相色谱质谱联用法、滴定分析法、动力学电位法、蛋白质耦合法、竞争耦合化学分光法、酶标记竞争耦合法、薄层层析法、毛细管电泳法、动物试验法、酶联免疫吸附法、微分脉冲伏安等。其中微生物法是最灵敏和应用最广泛的方法,是美国官方分析化学家协会(AOAC)推荐方法,也是美国、中国等国家的官方指定方法[3]。
我国食品安全国家标准GB 5009.259-2016规定了食品中生物素的测定方法,然而该方法操作繁杂,微生物生长的不确定性强,影响因素较多。按照 CNAS-CL07:2011要求,本研究按照食品安全国家标准GB 5009.259-2016规定的方法对婴幼儿配方食品中生物素含量进行测定,依据JJF1059.1-2012和GB/Z22553-2010对测定过程中影响检验结果的各个分量进行评估,并给出扩展不确定度[4-7]。
1 材料与方法[4]
1.1 主要材料与试剂
试样:生物素定值样品婴幼儿谷粉(婴幼儿配方食品)QC-RP-010中国检验检疫科学研究院测试评价中心。
菌种:植物乳杆菌(Lactobacillus plantarum),中国科学院微生物研究所CGMCC 1.0485。标准品:生物素(标准品,纯度 99.6%,批号:100291-201303),中国食品药品检定研究院。
培养基及试剂:生物素测试肉汤(批号:5056924),美国BD公司;MRS琼脂培养基(批号:150702),北京陆桥生物技术有限公司;氢氧化钠(分析纯,批号:20120201)、无水乙醇(分析纯,批号:20150527),北京化工厂;超纯水。
1.2 仪器与设备
高压蒸汽灭菌锅,日本Tomy公司;BSP-250生化培养箱,上海博讯实业有限公司医疗设备厂;BSA124S电子天平(精度0.1 mg),赛多利斯科学仪器(北京)有限公司;MS105DU电子天平(精度0.01mg),瑞士MettlerTodedo公司;UV2450紫外/可见光分光光度计,日本岛津公司。
1.3 样品处理与试验方法
1.3.1 样品处理与稀释 准确称取适量样品(约含 0.2~0.5 μg生物素)精确至 0.001 g,于 250 mL三角瓶中。加入硫酸溶液100 mL,121℃水解30 min,冷却后用氢氧化钠溶液调节pH至(4.5±0.2)。定量转到250 mL容量瓶中,用水定容,充分混合。用滤纸过滤,弃去最初的几毫升。吸取滤液5 mL,加入约20 mL水,用氢氧化钠溶液调pH为(6.8±0.2),定量转到 100 mL容量瓶中,用水定容。
1.3.2 测定 按照GB 5009.259-2016《食品安全国家标准食品中生物素的测定》6.4~6.7节要求,制备试样系列管、标准系列管、灭菌、接种、培养和测定。
1.4 标准曲线的绘制
以生物素含量(ng)为横坐标,OD550nm为纵坐标,绘制标准曲线。
1.5 样品稀释液中生物素含量计算
按GB 5009.259-2016《食品安全国家标准食品中生物素的测定》6.7.2节要求计算。
1.6 样品中生物素含量计算
按GB 5009.259-2016标准中6.7.2节要求计算,见式(1)。

2 结果与分析
2.1 不确定度来源分析[8-11]
根据整个试验过程,通过微生物法测定生物素含量,主要由测量重复性、试样称量及稀释、标准物质称量及标准溶液配制、标准曲线拟合、紫外分光光度计测量偏差等引入的不确定度。
2.2 测量不确定度评估
2.2.1 测量重复性引入的不确定度[12-13]按照GB 5009.259-2016对定值样品的生物素含量进行8次平行测定,结果见表1。重复测量产生的不确定度属于A类不确定度。

表1 样品生物素含量测定结果Table1 Result of the repeated measurements
按贝塞尔公式(式2)计算出试验标准差:

按GB 5009.259-2016,日常检测做 2个平行,检测结果取平均值,2次重复测试引入的不确定度,见式(3)。

相对标准不确定度,见式(4)。

2.2.2 样品称量及稀释引入的不确定度
2.2.2.1 样品称量引入的不确定度 用电子天平准确称取样品1.5002 g,即1500.2 mg,天平精度为0.1 mg,根据天平检定证书,最大重复性误差为0.2 mg,当0≤m≤50 g时,示值误差为0.2 mg。采用矩阵分布,包含因子k为,按B类不确定度评定,标准不确定度,见式(5)。

合成标准不确定度,见式(6)。
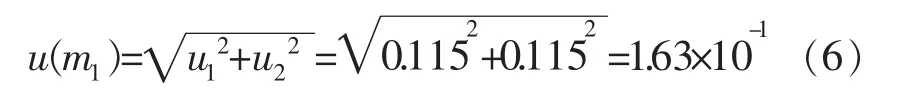
样品称量时的相对不确定度,见式(7)。

2.2.2.2 样品稀释引入的不确定度[14-15]样品前处理和稀释过程中使用了250,100 mL容量瓶,5 mL单标线吸量管,这些玻璃器具的校准和室温对液体体积的影响,可导致生物素含量测定的偏差。根据最大允许误差,按均匀分布处理,包含因子k为计算不确定度分量,见式(8)。

相对不确定度见式(9)。

因此,各玻璃量具在稀释过程中引入的不确定度见表2。

表2 样品稀释时玻璃量具校准引入的不确定度Table2 Uncertainties for measuring glasses’calibration in sample
合成玻璃器具校准引入的不确定度分量见式(10)。

实验室温度变化介于(20±5)℃,水的膨胀系数为2.1×10-4/℃,按照矩形分布,k为,温度产生的标准不确定度见式(11)。

相对标准不确定度见式(12)。

合成实验室温度变化引入的玻璃器皿相对不确定度分量见式(13)。

2.2.2.3 样品称量和稀释引入的不确定度的合成

2.2.3 标准物质及标准溶液配制引入的不确定度[16]
2.2.3.1 标准品引入的不确定度 根据生物素标准品说明书,其纯度p=(100±0.4)%,按B类不确定度评定,区间的半宽度为0.004,按均匀分布处理,包含因子为则标准品引入的不确定度见式(15)。

2.2.3.2 标准品称量引入的不确定度 用电子天平准确称取生物素标准品100.23 mg,所用天平精度为0.01 mg,根据天平检定证书,当0.01≤m≤5 g时,示值误差为0.01 mg,最大重复性误差为0.04 mg。采用矩阵分布,包含因子为按B类不确定度评定,标准不确定度见式(16)。

合成标准不确定度见式(17)。

标准品称量时的相对不确定度见式(18)。

2.2.3.3 标准溶液配制引入的不确定度 标准溶液配制过程中使用了 1 000,500,250,100 mL 容量瓶,5,1 mL单标线吸量管,其中5,1 mL单标线吸量管和100 mL容量瓶各使用2次,这些玻璃器具的校准和室温对液体体积的影响,可导致标准溶液配制的偏差。根据2.2.2.2节相关公式计算出玻璃器具校准引入的相对不确定度,具体见表3。

表3 标准溶液配制时玻璃器具校准引入的不确定度Table3 Uncertainties for measuring glasses’calibration in standard solution preparation
合成玻璃器具校准引入的不确定度分量见式(19)。

温度产生的标准不确定度见式(20)。
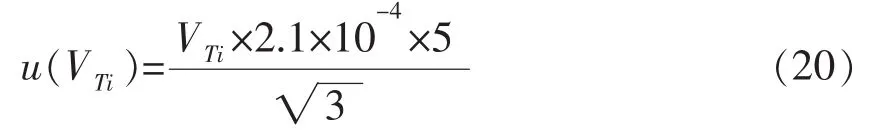
相对标准不确定度见式(21)。

合成实验室温度变化引入的玻璃器皿相对不确定度分量见式(22)。
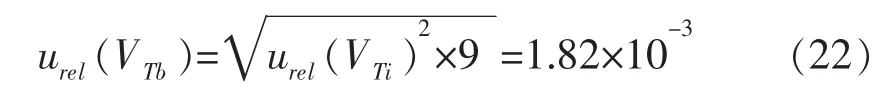
2.2.3.4 标准物质及标准溶液配制引入的不确定度的合成

2.2.4 标准曲线拟合引入的不确定度[9]按照按GB 5009.259-2016中6.2.4节,标准系列管取8个生物素含量点,每个含量点做3个平行,试验数据见表4。
根据标准曲线数据表,标准系列管吸光值残差的标准差见式(24),式(25)。

表4 标准曲线数据表Table4 Data sheet of standard curve
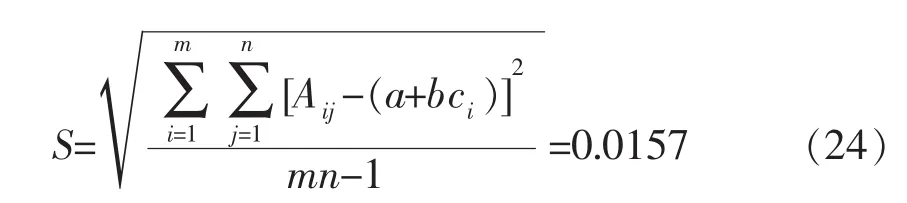
式中,Aij-(a+ci)——生物素量为ci时,仪器测得的吸光值与按标准曲线计算的理论吸光值差值;m——生物素含量点数;n——每个点测量次数。

式中,Ci——标准系列管中各生物素含量;——标准系列管各管生物素含量平均值。
按照GB 5009.259-2016中6.2.1节,试样系列测试管中加入的试样稀释液量取4个点,每个点做3个平行,测得各管吸光值,依据标准曲线查得的各试样测试管中生物素含量见表5。

表5 试样测试管中生物素含量Table5 The biotin content of sample testing tubes
标准曲线拟合引入的不确定度见式(26)。

相对不确定度见式(27)。

2.2.5 紫外-可见分光光度计引入的不确定度
依据检定证书,紫外-可见分光光度计的透射比示值误差为0.5%,按均匀分别处理,k为由紫外-可见分光光度计测量偏差引入的相对不确定度见式(28)。

2.3 合成不确定度的计算
综上,试验过程中,影响检验结果的各个因素引入的相对标准不确定度,见表6。

表6 不确定度分量表Table6 The heft of uncertainty
综合各不确定度分量,合成标准不确定度,计算婴幼儿谷粉中生物素含量测定的相对不确定度见式(29)。
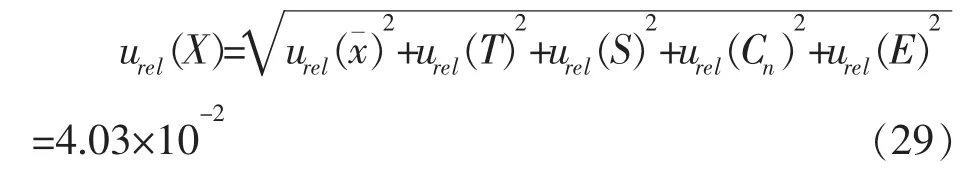
样品测定平均值为32.49 μg/100 g,则生物素定值样品婴幼儿谷粉测定的不确定度见式(30)。

2.4 扩展不确定度
测定结果按正态分布估计,置信水平为95%时,包含因子k=2,扩展不确定度可由合成标准不确定度乘以包含因子获得,则u=2×1.31 μg/100 g=2.62 μg/100 g。本次测定的生物素定值样品婴幼儿谷粉的生物素含量为(32.49±2.62)μg/100 g。
3 结论
按照GB 5009.259-2016《食品安全国家标准食品中生物素的测定》标准,测定生物素定值样品婴幼儿谷粉中生物素含量,并对测定过程进行不确定度评估。结果显示,测量不确定度主要来源于标准曲线拟合,其次是由重复测量引入的,而这两个过程都和微生物因素密切相关,分析认为微生物因素对样品生物素测定中的不确定度有非常大的影响。GB 5009.259-2016食品中生物素测定的原理为生物素是植物乳杆菌必需营养素,在生物素测定培养基中,植物乳杆菌的生长与生物素含量呈线性关系,测试过程中微生物影响不易估计,可粗略用基于试验及最终结果的重复性的标准偏差来表征[17],也可通过计算拟合不确定度来评估微生物因素引入的不确定度[18]。
——人-时间资料率比分析与SAS实现

