复方丹参滴丸在大鼠体内代谢产物的分析
郭洪梅,苏振宇,高诗凯,杜 岩,季 帅,汤道权∗
(1.徐州医科大学附属市立医院,江苏 徐州 221004;2.徐州市第一人民医院,江苏 徐州 221004;3.徐州医科大学药学院,江苏 徐州 221004)
复方丹参滴丸由丹参、三七、冰片3 味药材组成,临床上主要用于冠心病、高血脂等心血管疾病的治疗,同时在脑梗死、肝纤维化、慢性肺心病等疾病中也表现出较好的疗效[1],丹参酮、酚酸、三萜皂苷是其主要成分[2]。目前,关于复方丹参滴丸化学成分和质量控制的研究已有大量报道,但其药效物质基础仍不明确,对于这个含有成百上千种成分的中药复方而言,能被吸收入血的才有可能是真正发挥作用的。因此,研究复方丹参滴丸口服给药后血液中代谢产物,是阐明其活性物质基础,以及其配伍原理和作用机制的重要环节[3]。
近年来,对复方丹参滴丸单味药(丹参或三七)或其所含单体成分(丹参素、丹参酮Ⅰ、丹参酮ⅡA、丹酚酸A 等)的代谢研究较多,已有多位学者进行了报道[4-6]。然而,中药是一个复杂体系,由于化合物之间的相互作用,导致这些单味药或单体成分各自的代谢轮廓并不能代表在复方中的代谢情况。目前,关于复方丹参滴丸全方的代谢研究较少,仅有的几篇大多是针对其中少数几种主要成分[7-8],不能代表整个复方,而且尚无对其入血成分全面的分析鉴定。
随着液质联用技术的不断发展,其快速、高效、准确的特点在体内外复杂成分分析方面有着明显优势,逐渐成为中药体内代谢研究的有效手段[6]。本实验采用超高效液相色谱和四极杆飞行时间质谱(UPLC-qTOF/MS)法,对复方丹参滴丸灌胃大鼠后的入血成分进行鉴定,为该复方药效物质基础研究提供依据。
1 材料
1.1 仪器 Agilent 1290 UPLC 色谱仪、Agilent 6550 qTOF 质谱仪(美国Agilent 公司);XW-80A微型涡旋仪(上海沪西分析仪器厂);AB265-S 电子分析天平(瑞士梅特勒-托利多公司);5417R 台式高速冷冻离心机(德国Eppendorf 公司)。
1.2 试药 复方丹参滴丸(天津天士力制药集团有限公司)。丹参酮Ⅰ、二氢丹参酮Ⅰ、丹参酮ⅡA、丹参素、丹酚酸B、阿魏酸、原人参二醇、咖啡酸、丹酚酸A、人参皂苷Rg1对照品(四川省维克奇生物科技有限公司);原儿茶酸、人参皂苷Rb1、三七皂苷R1、原儿茶醛、迷迭香酸对照品(上海阿拉丁试剂有限公司)。甲醇、乙腈、甲酸为色谱纯(美国MREDA 公司)。
1.3 动物 清洁级雄性SD 大鼠,体质量(250±20)g,购于徐州医科大学实验动物中心,实验动物生产许可证号SCXK2018-0016。大鼠饲养于徐州医科大学实验动物中心,室内温度20~26 ℃,相对湿度40%~70%,明暗12/12 h。
2 方法
2.1 药物混悬液制备 精密量取滴丸3 429 mg,研磨后转移至50 mL 量瓶中,生理盐水定容至刻度,超声10 min,即得(68.58 mg/mL)。
2.2 生物样品采集及处理 15 只大鼠给药前禁食12 h,自由饮水,按275 mg/kg 剂量(相当于临床剂量的4 倍)灌胃给予混悬液,每天1 次,连续21 d,最后1 次给药后0、0.25、0.5、1、1.5、2、3、4、6、8、10、12、24 h 眼底静脉丛取血各0.4 mL,置于肝素处理的离心管中,3 000 r/min离心10 min,上清液合并,加4 倍量甲醇沉淀蛋白,涡旋混匀30 s,12 000 r/min 离心10 min,上清液氮气吹干,残渣用100 μL 甲醇复溶,涡旋30 s,0.22 μm 微孔滤膜过滤。
2.3 对照品溶液制备 精密称取丹参素、阿魏酸、咖啡酸、迷迭香酸、丹酚酸A、丹酚酸B、原儿茶醛、原儿茶酸、三七皂苷R1,人参皂苷Rb1、人参皂苷Rg1、原人参二醇、丹参酮ⅡA、二氢丹参酮Ⅰ、丹参酮Ⅰ对照品适量,甲醇溶解定容,0.22 μm微孔滤膜过滤,即得,。
2.4 分析条件
2.4.1 色谱 Poroshell 120 SB-C18色谱柱(2.1 mm×100 mm,2.7 μm);流动相乙腈-水(含0.1% 甲酸);梯度洗脱(0~1 min,10%~15% 乙腈;1~5 min,15%~28% 乙腈;5~12 min,28%~30% 乙腈;12~17 min,30%~65% 乙 腈;17~25 min,65%~66%乙腈;25~30 min,66%~80%乙腈;30~35 min,80%~90%乙腈);柱温35 ℃;体积流量0.2 mL/min;进样量2 μL。
2.4.2 质谱 ESI 电喷雾离子源;正负离子扫描模式;干燥气温度200 ℃,体积流量14 L/min;毛细管电压3.5 kV;雾化器压力35 psi(1 psi=6.895 kPa);鞘气温度275 ℃,体积流量11 L/min;碎裂器电压135 V;碰撞能量10~30 eV。
3 结果
3.1 UPLC-qTOF/MS 分析 总离子流图见图1,通过MassHunter 软件中的EIC Manager、Formula Calculator、Mass Calculator、消除背景峰等数据处理功能,结合相应对照品及参考文献中的保留时间,一级、二级质谱信号,共分析得到85 种入血成分,其中原型成分23 种,代谢产物62 种,具体见表1~2;负离子模式下检测到59 种,主要包括酚酸、三萜皂苷类及其代谢产物;正离子模式下检测到26 种,主要包括丹参酮及其代谢产物,其中3 种为首次报道。在23 种原型成分中,15 种结构与对照品比对后得到确认,分别是原儿茶酸(7)、阿魏酸(9)、原儿茶醛(11)、咖啡酸(13)、丹酚酸A(27)、丹参素(29)、三七皂苷R1(30)、丹酚酸B(36)、迷迭香酸(39)、人参皂苷Rb1(49)、原人参二醇(54)、人参皂苷Rg1(55)、二氢丹参酮Ⅰ(79)、丹参酮Ⅰ(81)、丹参酮ⅡA(83)。

图1 样品总离子流图Fig.1 Total ion current chromatograms of samples
3.2 酚酸及其代谢产物鉴定 表1 显示,灌胃给药后在血浆中检测到咖啡酸、迷迭香酸、丹酚酸D、阿魏酸、丹参素、丹酚酸A、原儿茶酸、丹酚酸B、原儿茶醛、异阿魏酸10 种酚酸类成分原型及其代谢产物,其中8 种结构与对照品比对后得到确认,同时检测到丹参中的一种微量成分丹酚酸F的原型,其一相代谢方式主要为甲基化、羟基化,偶尔发生水解、去羟基化等反应;二相代谢方式主要为葡萄糖醛酸化、硫酸酯化,偶尔产生甘氨酸结合物。下面以丹参素为例,介绍其代谢过程及产物鉴定方法。
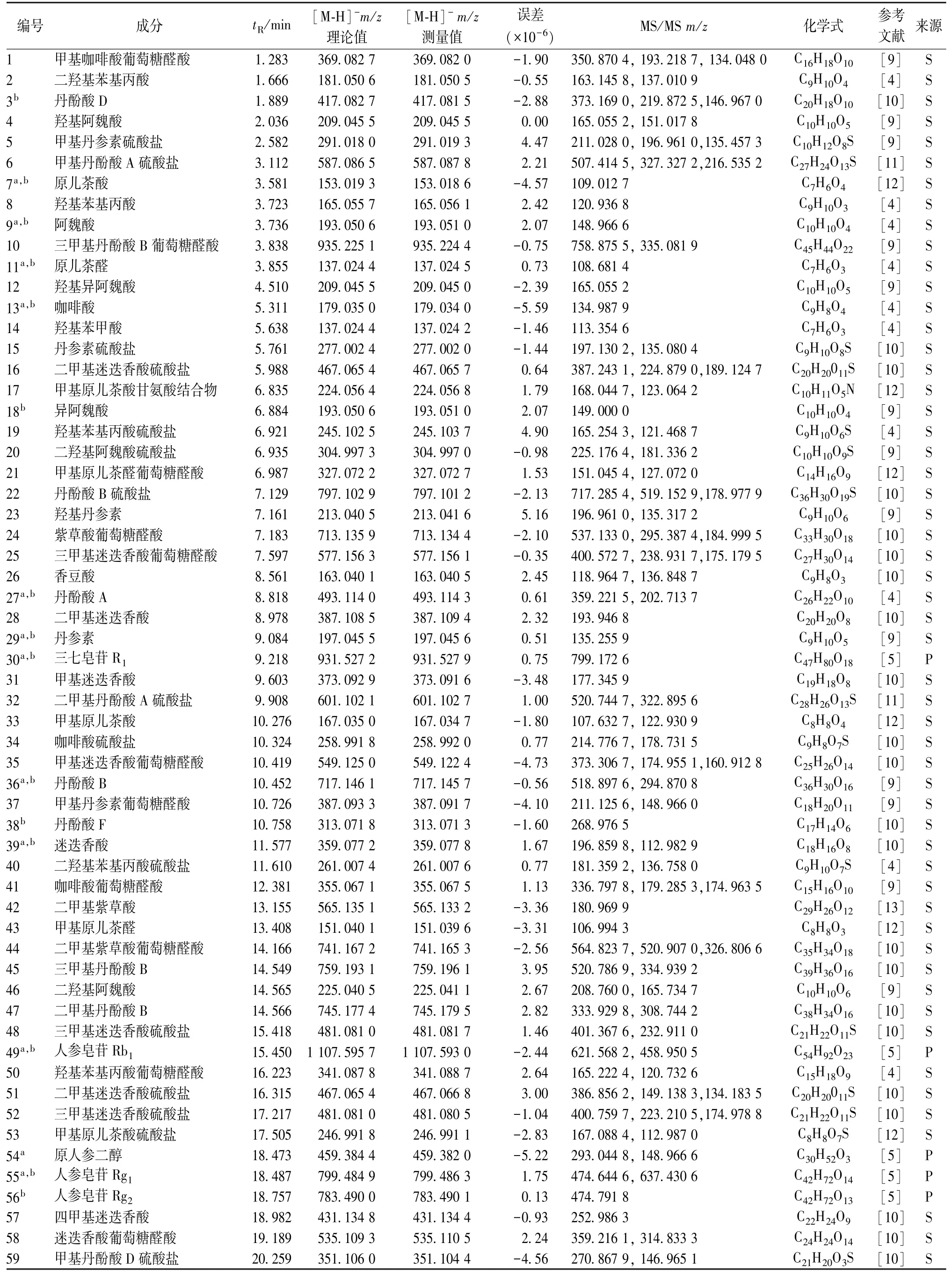
表1 大鼠血浆中代谢产物(负离子模式)Tab.1 Metabolites in rat plasma(negative ion mode)

表2 大鼠血浆中代谢产物(正离子模式)Tab.2 Metabolites in rat plasma(positive ion mode)
本实验中除了检测到丹参素(29)原型外,还检测到其4 个代谢产物,分别为甲基丹参素硫酸盐(5)、丹参素硫酸盐(15)、羟基丹参素(23)、甲基丹参素葡萄糖醛酸(37)。其中,29的[M-H]-分子离子峰是m/z197.045 6,表明分子式为C9H10O5,二级质谱显示一个主要的碎片离子为m/z135.255 9,是丹参素分子失去一个羧基(-CO2)、一分子水(-H2O)后的特征碎片,其保留时间与质谱信息、对照品完全一致,确认为丹参素;23 的[M-H]-分子离子峰是m/z213.041 6,表明分子式为C9H10O6,比丹参素多一个氧原子,在二级质谱中脱去一个羟基产生m/z196.961 0(对应于丹参素的分子离子峰),同时产生丹参素特征碎片离子m/z135.317 2,与文献[9]报道一致,故鉴定为羟基丹参素;15 的[M-H]-分子离子峰是m/z277.002 0,表明分子式为C9H10O8S,比丹参素分子量多了80 Da,二级质谱显示一个脱去硫酸盐(-SO3)的特征碎片m/z197.130 2(对应丹参素分子离子峰),同时也可观察到丹参素特征碎片离子m/z135.080 4,与文献[10]报道一致,故鉴定为丹参素硫酸盐;5 的[M-H]-分子离子峰是m/z291.019 3,表明分子式为C10H12O8S,在二级质谱图中脱去一个SO3分子而产生硫酸盐特征碎片m/z211.028 0,同时可进一步脱去甲基(-14 Da)而产生m/z196.961 0(对应于丹参素分子离子峰),故鉴定为甲基丹参素硫酸盐;37 的[M-H]-分子离子峰是m/z387.091 7,表明分子式为C18H20O11,在二级质谱图中失去176 Da,表明是一个葡萄糖醛酸化产物,产生的碎片离子m/z211.125 6 与甲基丹参素相同,同时可发生与丹参素相同的裂解(丢失一个羧基、一分子水)而产生m/z148.966 0,与文献[9]报道一致,故鉴定为甲基丹参素葡萄糖醛酸。MS/MS 谱图见图2。

图2 各成分MS/MS 谱图Fig.2 MS/MS spectra for various constituents
3.3 三萜皂苷及其代谢产物鉴定 灌胃给药后,仅在血浆中检测到三七皂苷R1(30)、人参皂苷Rb1(49)、人参皂苷Rg1(55)、人参皂苷Rg2(56)4 个原型,其中3 个与对照品比对后得到确认,另外还检测到1 个水解后的代谢产物原人参二醇,在负离子模式下有较好的质谱响应。其中,30的精确[M-H]-分子离子峰是m/z931.527 9,丢失一个木糖分子(-132 Da)而产生的m/z799.172 6 是其主要碎片;49 在负离子模式下可加上一分子甲酸而产生 [M-H]-分子离子峰m/z1 107.593 0,可连续水解失去多个葡萄糖而产生碎片m/z621.568 2、皂苷元m/z458.950 5;55 的[M-H]-分子离子峰是m/z799.486 3,同样可连续丢失2 个葡萄糖而产生m/z637.430 6、苷元m/z474.644 6;56 的 [M-H]-分子离子峰是m/z783.490 1,表明分子式为C42H72O13,可丢失一分子葡萄糖、一分子鼠李糖而产生苷元m/z474.791 8。另外,原人参二醇(54)的[M-H]-分子离子峰是m/z459.382 0,在较高碰撞能量下可发生开环裂解而产生碎片m/z293.044 8、148.966 6,与文献[5]报道一致,故鉴定为皂苷元原人参二醇[5]。
3.4 丹参酮及其代谢产物鉴定 灌胃给药后,在血浆中检测到26 种丹参酮,分别是丹参酮Ⅰ、丹参酮ⅡA、丹参酮ⅡB、二氢丹参酮Ⅰ原型及其代谢产物,同时还发现含有量较低的丹参新醌A、丹参酸甲酯、紫丹参甲素A、丹参酮Ⅵ原型,其中3 个结构与对照品比对后得到确认。此外,3 个丹参酮类代谢产物,即丹参酮ⅡB硫酸盐(65)、二羟基丹参酮ⅡA葡萄糖醛酸(66)、丹参酮ⅡA硫酸盐(74)为首次报道。该类成分在体内的代谢转化方式较多,主要包括一相代谢羟基化、呋喃环裂解、加氢还原、甲氧基化等反应,以及二相代谢的葡萄糖醛酸化、硫酸酯化等,下面以丹参酮ⅡA为例,介绍其代谢转化方式及产物鉴定方法。
化合物83 的高分辨[M+H]+分子离子峰是m/z295.132 9,表明分子式为C19H18O3,在二级质谱图中可看到m/z276.851 6、249.134 4,是丹参酮ⅡA相继丢失一分子H2O、一分子CO 后的特征碎片,其保留时间和质谱裂解方式与对照品完全一致,故鉴定为丹参酮ⅡA;化合物80 的[M+H]+分子离子峰是m/z471.162 3,表明分子式为C25H26O9,在二级质谱中丢失176 Da(葡萄糖醛酸单元)而产生m/z295.110 3,同时能进一步裂解产生丹参酮ⅡA的特征碎片m/z249.091 3,与文献[17]报道一致,故鉴定为ⅡA 葡萄糖醛酸[17];化合物74 推测为丹参酮ⅡA硫酸盐,为首次报道;化合物75的[M+H]+分子离子峰是m/z311.127 4,分子式为C19H18O4,比丹参酮ⅡA多了一个氧原子,在二级质谱图中有丢失H2O、CO 后的特征碎片m/z292.964 0、m/z249.149 8,根据文献鉴定为羟基丹参酮ⅡA;化合物77 的[M+H]+分子离子峰是m/z327.120 3,表明分子式为C19H18O5,比丹参酮ⅡA多了两个氧原子,在二级质谱图中有连续丢失H2O、CO 后的特征碎片m/z311.743 3、277.120 9、264.961 5,与文献[16]报道一致,故鉴定为二羟基丹参酮ⅡA;化合物66、70 的 [M+H]+分子离子峰分别是m/z503.154 2、487.161 5,均可丢失一个葡萄糖醛酸单元(176 Da),根据所产生苷元的精确分子量和质谱裂解方式,鉴定两者分别是二羟基丹参酮ⅡA葡萄糖醛酸、羟基丹参酮ⅡA葡萄糖醛酸[15],其中前者为首次发现。
3.5 其他成分及其代谢产物鉴定 灌胃给药后,在大鼠血浆中检测到了含有量较高的丹参酮ⅡB(63),它一部分来自于原型成分吸收入血,而另一部分是由丹参酮ⅡA经羟基化后得到的代谢产物[15-16],并且可进一步发生一相、二相代谢反应。本实验共检测到3 个与丹参酮ⅡB直接相关的代谢产物,分别是二羟基丹参酮ⅡB(67)、丹参酮ⅡB硫酸盐(65)、丹参酮ⅡB葡萄糖醛酸(61)。鉴于此,丹参酮ⅡA的代谢途径可归纳为图3。
4 讨论
UPLC-qTOF/MS 不仅具有分析速度快、选择性强、准确度好、灵敏度高的特点,而且能提供丰富的碎片离子信息,精确鉴定代谢产物,已广泛应用于生物样品的体内代谢研究,故本实验建立该方法分析大鼠灌胃复方丹参滴丸后血浆代谢产物。为了与临床长期用药保持一致,选择连续灌胃21 d以使其体内代谢产物及其浓度变化达到稳态,考虑到不同代谢产物在体内的达峰时间有所差异,在最后1 次给药后收集24 h 内不同时间点的血浆样品,以期检测到更多代谢产物,同时采用正负离子相结合的qTOF/MS 模式,使得不同类型化合物均有更强的质谱响应信号,从而提高了方法灵敏度。

图3 丹参酮ⅡA可能的代谢途径Fig.3 Possible metabolic pathways for tanshinoneⅡA
结果表明,复方丹参滴丸代谢产物主要来源于丹参中酚酸和丹参酮,以及三七中三萜皂苷类。其中,酚酸、丹参酮生物利用度较高,在体内可被广泛检测到,并能发生多种一相、二相代谢反应而生成多个代谢产物,以羟基化、甲基化、葡萄糖醛酸化、硫酸酯化产物为主;三萜皂苷吸收较弱,仅在体内检测到4 个原型和1 个代谢产物,进而证实丹参化合物是复方丹参滴丸主要入血成分。
通过查阅文献发现,与大鼠灌胃单味药(丹参或三七)或单体成分(丹参素、丹参酮Ⅰ、丹参酮ⅡA、丹酚酸A 等)比较,灌胃复方丹参滴丸后相关成分代谢产物可能会发生变化。例如,文献报道给予丹参提取物后在血浆中可检测到隐丹参酮及其代谢产物[4],而本实验仅检测到隐丹参酮代谢产物,并未发现原型,其原因可能是复方丹参滴丸各单味药之间的相互作用改变了相应药物代谢酶活性,从而增加了隐丹参酮代谢,使其全部转化为代谢产物;给予丹参素后在血浆中可检测到代谢产物甲基丹参素[19],而本实验并未检测到甲基丹参素,却发现大量甲基丹参素硫酸盐(5)和甲基丹参素葡萄糖醛酸(37),表明复方丹参滴丸其他组成药物加速了甲基丹参素二相代谢。另外,代谢产物变化的原因还有可能是本实验条件与文献报道有所差异,具体还需作进一步研究。

