大鼠体内白藜芦醇胶束的药代动力学研究*
张纯刚,于琛琛,康 宁,唐静雅
(1.辽宁中医药大学,辽宁 大连 116600; 2.大连医科大学附属第一医院药剂科,辽宁 大连 116011)
白藜芦醇(RESV)是天然的非黄酮类多酚化合物,主要来源于葡萄、花生、桑椹等,是肿瘤的化学预防剂[1],也是降低血小板聚集,预防和治疗动脉粥样硬化、心脑血管疾病的化学预防剂[2],广泛应用于保健品、医药和食品等领域。其水溶性低、稳定性差,生物利用度低,在光、热和氧化剂条件下不稳定,易被氧化降解,在一定程度上限制了其应用[3]。因此,开发安全性高、稳定性好的新剂型来提高白藜芦醇的稳定性、水溶性和生物利用度,具有重要临床意义[4]。因其低溶解度、高渗透性,按生物药剂学分类为Ⅱ类化合物,其生物利用度主要取决于体外溶出速度[5]。胶束在溶液中,两亲性共聚物可自行组装成特定的超分子有序聚集体,形成一种稳定、澄清的液体制剂,有助于增加药物的溶解度,提高生物利用度。本研究中根据白藜芦醇的性质和疏水特性,以泊洛沙姆188为载体,将其制成胶束,以提高白藜芦醇的水溶性、稳定性,并使其半衰期延长,提高生物利用度,扩大其临床应用。并以原料药为参比制剂,探讨白藜芦醇胶束在大鼠体内的药代动力学过程。现报道如下。
1 仪器、试药与动物
仪器:岛津LC-2010A型色谱仪(岛津色谱工作站,UV检测器);AY220型电子分析天平(SHTMADZU公司);TGL-16 g型高速离心机(上海安亭科学仪器厂);DAS 3.0软件(中国药理学会数学药理专业委员会);Vortex-5型涡旋混合器(海门市其林贝尔仪器制造有限公司)。
试药:白藜芦醇对照品(含量为98%,南京森贝伽生物科技有限公司,批号为111535-201502);白藜芦醇原料药(武汉远成赛创科技有限公司);卡马西平对照品(含量为99%,上海哈灵生物科技有限公司,批号为100142-201605);白藜芦醇胶束(自制);乙腈(色谱纯,天津科密欧科技有限公司)。
动物:取 SD 大鼠 12只,雄性,体质量为(250±20)g,由辽宁中医药大学实验动物中心提供,动物使用许可证号为 SCXK(辽)2015-0001。
2 方法与结果
2.1 溶液制备
取白藜芦醇对照品10.2 mg,精密称定,置250 mL棕色容量瓶中,加甲醇溶解并稀释至刻度,摇匀,制成质量浓度为40.8 μg/mL的白藜芦醇对照品贮备液。
精密称取白藜芦醇对照品10.0 mg,精密称定,与上述同法操作,制成质量浓度为40.0 μg/mL的白藜芦醇质量控制贮备液。
取卡马西平对照品10.1 mg,精密称定,置10 mL容量瓶中,加甲醇溶解并稀释至刻度,摇匀,即得1.01 mg/mL卡马西平贮备液。精密量取卡马西平贮备液,加甲醇稀释得质量浓度为25 μg/mL的内标溶液[6]。以上溶液均于4℃冰箱保存,备用。
2.2 色谱条件
色谱柱:AgilentExtendC18柱(150mm×4.6mm,5μm);流动相:乙腈 -水(30 ∶70,V/V);流速:1.0 mL/min;进样量:30 μL;检测波长:320 nm;柱温:室温。
2.3 血浆样品处理[6]
取血浆100 μL,置2 mL离心管中,依次加入10 μL甲醇,10 μL 内标溶液,50 μL 0.5% 醋酸,200 μL 乙腈,涡旋混合 60 s,离心 10 min(12000 r/min),取 100 μL上清液置进样容器中,取30 μL进样分析。
2.4 方法学考察
专属性考察:分别取6只大鼠空白血浆,除以甲醇(内标溶液的溶剂)替代内标溶液外,其余按2.3项下方法操作,得大鼠空白血浆样品色谱图(图1 A);另取空白血浆、白藜芦醇样品和内标,及第1只大鼠单次给药后0.5 h的血浆样品,按2.3项下方法操作,得模拟样品及实际样品色谱图(图1 B和图1 C)。结果白藜芦醇的保留时间为3.86 min,内标的保留时间为7.25 min,空白血浆中的内源性物质和代谢物不干扰白藜芦醇样品和内标(卡马西平)的测定。
标准曲线考察和定量限确定:取标准贮备液适量,加空白血浆稀释成质量浓度为 10,20,51,102,204,510,1020,2550 ng/mL 的系列血浆样品,其余按 2.3项下方法操作,同一质量浓度进行双样本分析,记录色谱图。以血浆中待测物浓度(C,ng/mL)为横坐标、待测物与内标物的峰面积比值(A)为纵坐标,采用加权最小二乘法进行回归运算,得直线回归方程[7]。结果白藜芦醇质量浓度在10~2550 ng/mL范围内与峰面积线性关系良好,血浆样品的典型标准曲线回归方程为Y=0.0057X+0.1068,r=0.9982(n=8),最低定量限(LLOQ)为质量浓度10 ng/mL,可满足SD大鼠体内白藜芦醇测定的要求。
精密度和准确度试验:精密量取质量控制贮备液适量,加空白血浆稀释成质量浓度为低、中、高质量浓度(25,400,2040 ng/mL)的质量控制(QC)样品溶液各 6份,连续测定3 d,除少加甲醇10 μL外,其余按2.3项下方法操作,分别考察日内和日间精密度。结果见表1。可见,方法的准确度与精密度均符合生物样品分析的要求。
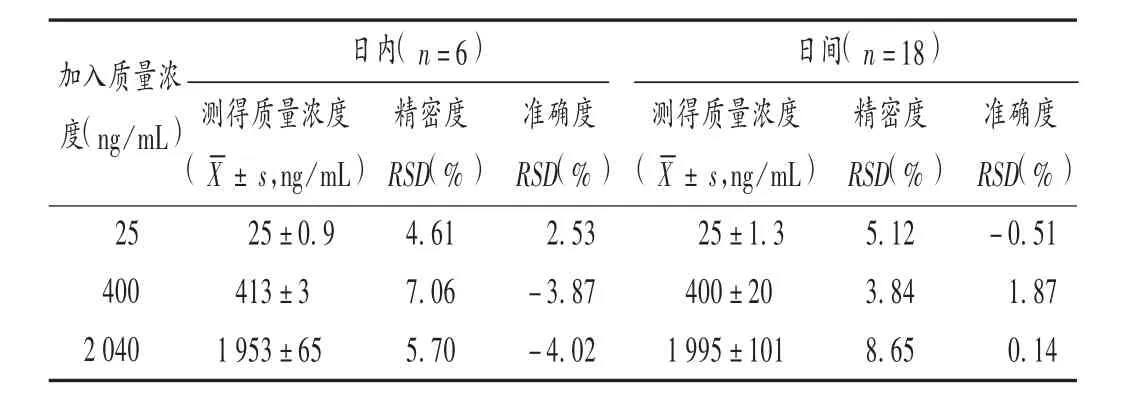
表1 大鼠血浆中白藜芦醇的准确度和精密度试验结果
提取回收率:取空白血浆100 μL,加入白藜芦醇系列质量控制溶液10 μL,配制白藜芦醇低、中、高质量浓度(25,400,2040 ng/mL)的 QC 样品溶液,除少加甲醇10 μL外,其余按2.3项下方法操作,每一质量浓度进行6样本检测,得白藜芦醇相应峰面积,记为A;同时,另取6只大鼠的空白血浆100 μL,除以甲醇10 μL代替相应内标卡马西平的体积外,其余按2.3项下方法操作,再加入相应浓度和体积的白藜芦醇标准溶液和内标溶液,涡流混合,进样分析,每个质量浓度进行3样本分析,得白藜芦醇相应峰面积,记为B。以A与B的平均值计算白藜芦醇的提取回收率,白藜芦醇在3个质量浓度的血浆样品提取回收率分别为98.13%,97.59%,104.22% (n=3)。依法测得内标的提取回收率为101.19%,RSD均在 ±15%以内(n=3)。

图1 血浆中白藜芦醇和卡马西平的典型高效液相色谱图
稳定性试验:精密量取质控贮备液适量,用空白血浆稀释成低、中、高质量浓度(25,400,2040 ng/mL)的质量控制样品溶液,分别考察白藜芦醇血浆样品在室温放置2 h、白藜芦醇血浆样品经沉淀蛋白后进样室温(4℃)放置24 h、白芦藜醇血浆样品-20℃经历3次冷冻-解冻循环和-20℃冰冻30 d的稳定性(相对偏差均在±15%内)。3个质量浓度未处理,于室温放置2 h测定含量准确率(RE% )分别为 5.43% ,8.69% ,-5.50%;白藜芦醇血浆样品经沉淀蛋白后于室温(4℃)放置 24 h测得含量 RE%分别为 3.13%,-4.91%,1.04%;反复冻融3次测得含量RE%分别为3.42%,-1.51%,2.89%;-20℃冰冻30 d的稳定性测得含量RE% 分别为 1.20% ,-6.68% ,3.39%(RSD均在 ±15%内,n=3)。结果表明,白藜芦醇血浆样品在上述条件下稳定性符合要求。
2.5 分析方法在药代动力学中的应用
2.5.1 给药方案与样品采集
取雄性SD大鼠12只,随机分为A组和B组,各6只。实验前禁食12 h,自由饮水,次日晨,A组灌胃白藜芦醇胶束(20 mg/kg),B组灌胃白藜芦醇原料药(20 mg/kg)。分别于给药前(0 h)和给药后 0.083,0.167,0.25,0.33,0.5,0.75,1,1.5,2,4,6,8,12 h 于眼底静脉丛采血约200 μL,置预先标记好的肝素钠抗凝管中,4000 r/min离心3 min,分离上层血浆,血浆样品置-20℃冰箱保存,待测。
2.5.2 统计学处理
2.5.3 药代动力学研究
实际生物样品测定过程中,同时配制低(25 ng/mL)、中(400 ng/mL)和高(2040 ng/mL)质量浓度的 QC 样品,根据当日标准曲线计算未知样品和QC样品浓度。经测定,12只大鼠分别口服白藜芦醇胶束和原料药后获得平均血浆药物质量浓度-时间曲线见图2,主要药代动力学参数见表2。
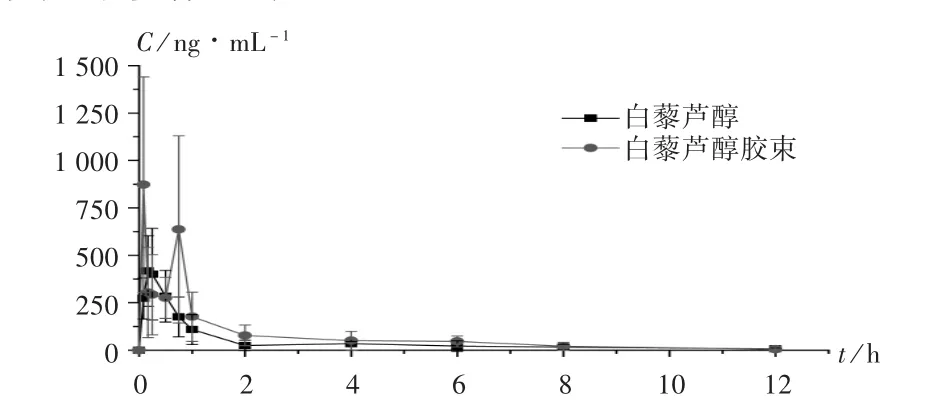
图2 白藜芦醇在大鼠体内的平均血浆药物浓度-时间曲线对比图
表2 大鼠体内白藜芦醇主要药代动力学参数比较(± s,n=6)
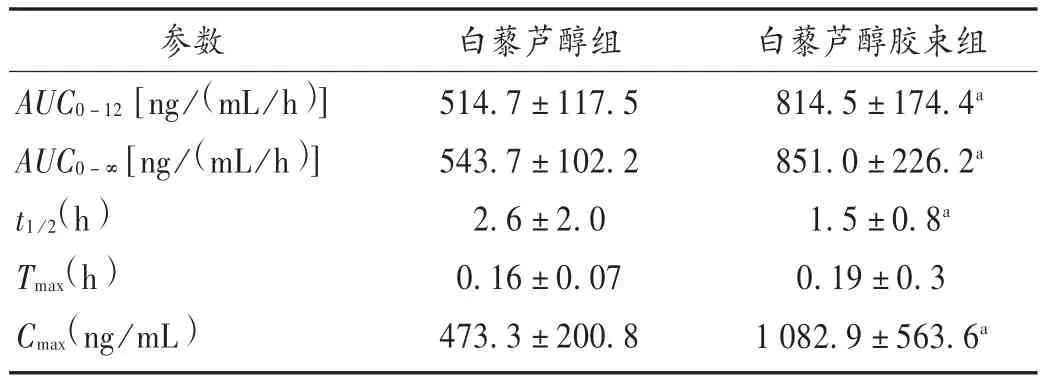
表2 大鼠体内白藜芦醇主要药代动力学参数比较(± s,n=6)
注:与白藜芦醇组比较,aP<0.05,AUC0-12为 0-12 h下药 -时曲线下面积;t1/2为生物半衰期;Tmax为达峰时间;Cmax为最大血药浓度。
参数AUC0-12 [ng/(mL/h)]AUC0- ∞ [ng/(mL/h)]t1/2(h)Tmax(h)Cmax(ng/mL)白藜芦醇组514.7 ± 117.5543.7 ± 102.22.6 ± 2.00.16 ± 0.07473.3 ± 200.8白藜芦醇胶束组814.5 ± 174.4a 851.0 ± 226.2a 1.5 ± 0.8a 0.19 ± 0.31082.9 ± 563.6a
大鼠分别灌胃白藜芦醇原料药及白藜芦醇胶束后,白藜芦醇分别在5 min和15 min左右血药浓度达峰,说明白藜芦醇胶束在大鼠体内迅速吸收入血。RESV原料药组最大血药浓度(Cmax)为(473.3 ±200.8)ng/mL,白藜芦醇胶束组为(1082.9 ±563.6)ng/mL,提高了 2 倍多(P<0.05)。与原料药组相比,胶束组可较快达到有效浓度。与白藜芦醇原料药组相比,白藜芦醇胶束组0~12 h内药-时曲线下面积(AUC0-12)是白藜芦醇原料药组的 1.58倍(P<0.05),即白藜芦醇组和相对生物利用度为158%。
3 讨论
本研究中采用热熔挤出制剂法制备由功能性辅料泊洛沙姆188与白藜芦醇组成的药物制剂,优于传统固体分散体。以泊洛沙姆188为载体将白藜芦醇制成胶束后能显著提高白藜芦醇在大鼠体内的生物利用度。
口服制剂出现双峰的可能原因如下。1)由于胃按一定时间排空,药物分成2次达到小肠,造成药物先后入血,出现双峰;2)药物在胃肠道的2个部位吸收,有快有慢,因而出现双峰;3)肝-肠循环即经胆汁或部分经胆汁排入肠道的药物,在肠道中又重新被吸收,经门静脉又返回肝脏;4)制剂原因,如含有速释成分和缓释成分;5)脂溶性药物吸收后,迅速分布到组织中,在血液中药物代谢到一定程度后,又出现二次入血[8]。由于原料药组并未出现双峰现象,仅白藜芦醇胶束组出现双峰现象,故可排除机体本身的因素,如吸收部位和肝肠循环。故考虑制剂的原因可能性较大。此制剂又并未含有速释和缓释双成分,即排除此因素。白藜芦醇胶束组出现双峰现象的原因可能为胶束在胃中析出,排空进入肠中后再次被吸收[7-8],待进一步研究。

