硼替佐米致多发性骨髓瘤患者急性肺损伤1例并文献复习
郝 丹,孙志强
(南方医科大学深圳医院血液科,广东深圳 518000)
蛋白酶体抑制剂硼替佐米是临床上广泛用于治疗多发性骨髓瘤(multiple myeloma,MM)的一类新药,使得该病疗效得到极大的提高,但由此带来的一些发生率低甚至罕见的不良反应,如急性肺损伤(acute lung injury,ALI),由于其具有潜在的高致命性,病情进展迅速,病死率高,在临床引起广泛关注。本文通过对1例初诊MM患者应用硼替佐米后迅速出现严重肺损伤的处理,同时进行相关文献复习,探讨其发生时间、糖皮质激素用量及后续诊疗策略,旨在引起临床医生对硼替佐米所致不良反应的关注和警惕。
1 临床资料
患者,男,50岁,因“头晕、乏力进行性加重”于2017年12月19日就诊于当地医院。既往有吸烟史30余年,高血压病史5个月,无过敏史。血常规:白细胞(WBC)4.08×109/L,血红蛋白(Hb)55 g/L,血小板(PLT)93×109/L;血生化:总蛋白132.30 g/L,清蛋白23.00 g/L,总胆红素56.10 μmol/L,尿素11.71 mmol/L,肌酐265 μmol/L,钙 1.51 mmol/L。胸部数字化X线成像(DR):双肺纹理增粗。心脏彩超:心脏射血分数(EF) 69%,主动脉瓣及肺动脉瓣口血流速度偏高,肺动脉压增高,左心室增大,左、右心房大小临界高值。CT显示:肝、胆、脾、胰横断位平扫未见明显异常,右肺中叶、双肺下叶炎症。左肺上叶下舌段、下叶少许肺大疱。腰椎磁共振成像(MRI):多发腰骶椎改变,考虑MM并L4及S1椎体病理性骨折。2017-12-24骨穿:骨髓有核细胞增生活跃,成熟红细胞呈缗钱状排列,骨髓瘤细胞占62.20%。流式细胞分析:浆细胞约16.40%,其免疫表型为CD38(++),CD138(+)部分,CD19(-),CD56(+),CD117(-),CD200(-),细胞内免疫球蛋白Lambda轻链限制性表达。血清免疫球蛋白及轻链定量:IgA 0.06 g/L,IgG 149.33 g/L,IgM 0.33 g/L,Kappa轻链(κ)0.57 g/L,Lambda轻链(λ) 10.61 g/L。尿游离轻链定量:κ 20.62 mg/L,λ 2 057 mg/L,κ/λ:0.01;荧光原位杂交(FISH):IgH/成纤维细胞生长因子受体3(FGFR3)融合基因(+); IgH基因重排(+);CKS1B(1q21)基因(+);未检测到p53(17p13.1)基因缺失,检测到cep17,p53基因数目异常;乙型肝炎病毒检查:HBsAg(+),HBeAb(+),HBcAb(+)。确诊:(1)MM(IgG-λ型,D-S分期Ⅲb期,ISS分期Ⅲ期);(2)乙型病毒性肝炎。综合分析评估后,无治疗禁忌证,按《中国MM诊治指南(2017版)》推荐,拟予PAD方案(硼替佐米1.30 mg/m2第1、4、8、11天,多柔比星40 mg第1天,地塞米松40 mg第1-4天、第9-12天)治疗。在2017年12月有30日第1次应用硼替佐米后患者出现咳嗽、胸闷、气喘,痰中带血丝,予地塞米松40 mg静脉滴注,患者不适症状未缓解。因出现前述症状,未用多柔比星。2017年12月31日出现咳血性痰,且血痰逐渐增多,以鲜血为主,胸闷、气喘、呼吸困难明显加重,停地塞米松,予以吸氧、止血、输血支持及亚胺培南西司他丁钠(1 g,每8小时1次)经验性抗感染治疗等。血气分析显示:pH 7.34,二氧化碳分压(PaCO2)26.40 mm Hg ,氧分压(PaO2) 52.00 mm Hg ,血氧饱和度(SaO2)84.00%;2018年1月2日胸部CT:双肺多发肺泡积血,见图1。痰培养:肺炎克雷伯菌亚种。但对症治疗后效果仍欠佳,急诊转本院。查体:体温36.9 ℃,脉搏105次/分,呼吸21次/分,血压133/74 mm Hg,浅表淋巴结未明显触及。全身皮肤黏膜无出血点及瘀斑等。双肺听诊闻及广泛湿啰音。心腹未见明显异常,双下肢无水肿。C反应蛋白(CRP)>160 mg/L;血常规:WBC 9.10×109/L,中性粒细胞绝对值(ANC)8.30×109/L,Hb 69 g/L,PLT 53×109/L;β2微球蛋白(β2-MG)15.47 mg/L。降钙素原(PCT)>100 ng/mL;血气分析:pH 7.417,PaCO227.80 mm Hg,PaO257.70 mm Hg,SaO270.10%;予注射用甲泼尼龙琥珀酸钠80 mg静脉滴注,并继续给予亚胺培南西司他丁钠抗感染治疗,次日患者症状较前稍有缓解,未再咳血痰,偶有痰中带血丝。复查血气分析:pH 7.437,PaCO224.70 mm Hg,PaO267.20 mm Hg,SaO272.30%,甲泼尼龙琥珀酸钠(80 mg)应用7 d后逐渐减量至停用,连续痰培养未见阳性致病菌。病情逐渐趋于稳定,复查胸部CT提示双肺渗出逐渐吸收(图2)。目前已先后给予RCD方案(来那度胺+环磷酰胺+地塞米松)化疗两个周期,耐受良好。

图1 该患者2018年1月2日胸部CT
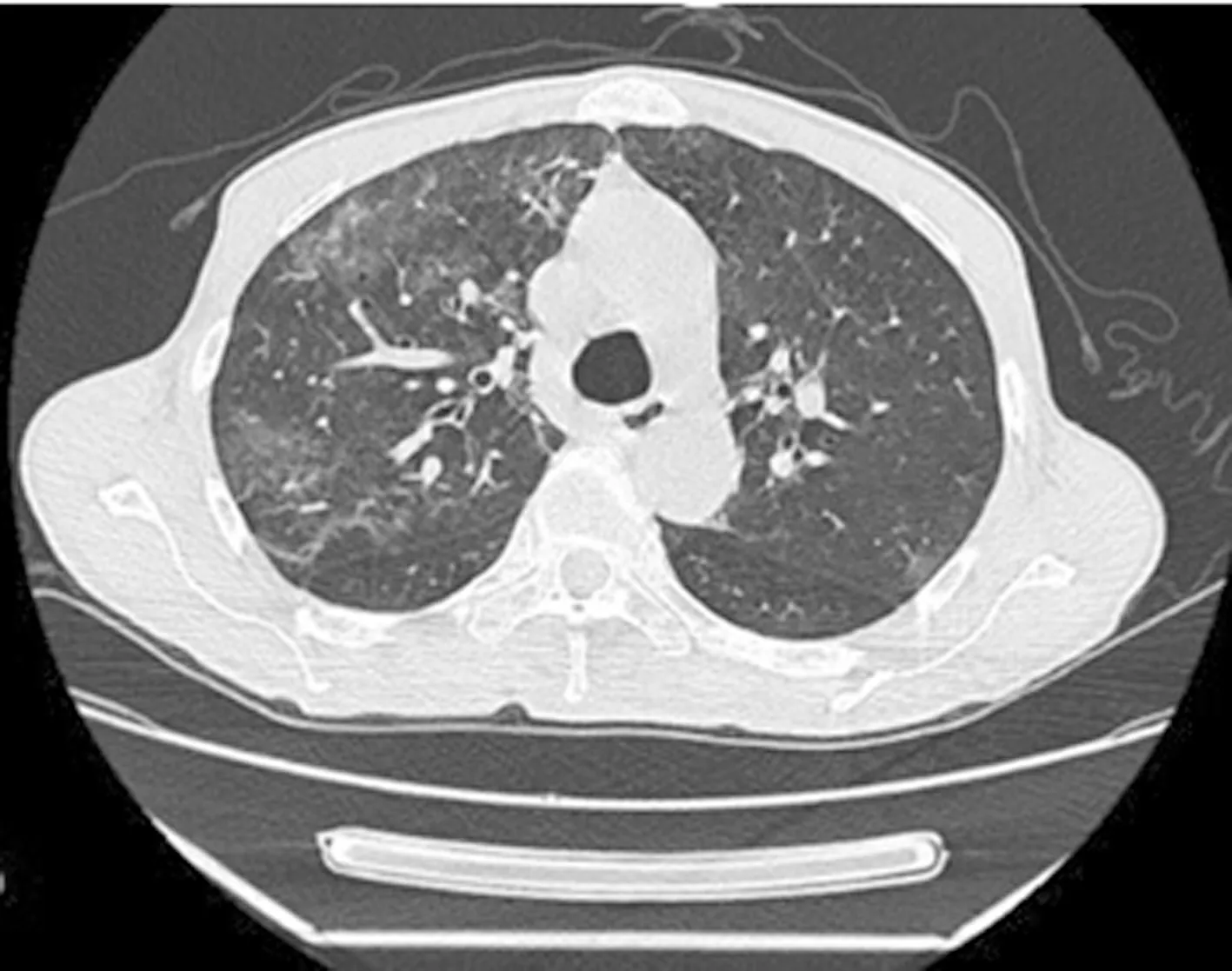
图2 治疗1个月复查胸部CT
2 讨 论
硼替佐米是目前MM一线治疗的主要药物之一,为一种可逆性的26S蛋白酶体抑制剂[1-2],可以克服MM的不良预后。硼替佐米的常见不良反应有恶心、腹泻、食欲缺乏等胃肠道症状,以及周围神经病变和血小板减少等[3]。ALI是近年来受到关注的主要不良反应之一,其具有潜在的高致命性,往往进展迅速,病死率高。
硼替佐米所致ALI主要表现为急性呼吸窘迫综合征及弥散性肺泡出血两种形式,后者报道例数较少[4]。弥散性肺泡出血主要表现为咯血、贫血、弥散性肺部浸润影及急性呼吸衰竭[5]。本例患者用药后即出现咳嗽、胸闷及咳血痰,影像学证实为广泛肺泡出血,考虑硼替佐米所致ALI。
硼替佐米所致ALI的发生率及严重性,国内外均有少量报道。MIYAKOSHI等[6]报道了13例患者应用硼替佐米后,有4例出现严重的肺损伤,其中2例死亡,发生率为30.7%,病死率为15.4%。2011年MUKAI H等[7]回顾分析了3 556例使用硼替佐米治疗的患者资料,相关肺损伤的发病率为2.33%。2014年YOSHIZAWA等[8]分析了1 010例病例资料,在复发难治MM人群中,硼替佐米诱导的ALI的发生率约为4.5%,病死率为0.5%。2008年国内报道了2例复发MM患者接受硼替佐米联合地塞米松治疗过程中出现严重肺损伤病例[9]。侯建等[3]报道该院106例MM患者中5例(4.7%)出现与硼替佐米相关的严重肺损伤,予糖皮质激素等治疗均无效,最终死亡。关于硼替佐米致MM患者ALI的发生时间,目前报道不一致。有报道显示ALI多发生于反复应用硼替佐米后,首次应用后亦可发生[10-12]。程军等[13]总结国内外33例硼替佐米致肺损伤病例发现,肺损伤多发生在硼替佐米用药后14 d内,最长为用药后161 d,且发病早的患者病死率相对较高。本例患者ALI发生于用药数小时后,较为少见。
是否有基础肺部疾病更易发生ALI,程军等[13]在33例硼替佐米致肺损伤病例中,有25例患者无基础肺部疾病。本文患者为中年男性,既往仅有吸烟史,无明确的肺部基础疾病,用药前无发热及咳嗽、咳痰,因而支持药物所致ALI的诊断。药物所致ALI的处理,需及时停药并给予激素治疗,一般多采用大剂量激素[14]。本例患者予以甲强龙 80 mg治疗后,肺出血及呼吸困难症状缓解相对迅速,治疗有效。该病例提示采用偏小剂量激素亦能取得良好疗效,避免大剂量激素可能所致的不良反应,可为日后进一步探讨及研究激素用量提供依据。
多年来硼替佐米致ALI发病机制尚不明确,多数学者认为核因子κB(NF-κB)参与其中[15]。NF-κB在骨髓瘤细胞的存活、增殖和耐药过程中发挥重要作用,硼替佐米停药会激活NF-κB系统,促使多种炎性因子表达增加,从而造成肺损伤[16-17]。但硼替佐米停药到激活炎性因子的时间不能确定,因此无法解释ALI发生时间跨度大的原因。对于硼替佐米致ALI有待更深入的机制研究。
总之,在应用硼替佐米治疗前应全面评估患者有无治疗禁忌证,尤其需注意有无肺部基础疾病,严密观察临床症状,如有无发热、胸闷、憋喘及呼吸困难等。及时的病原学检查也很有必要,在无法获得病原学支持下,同时考虑药物相关肺损伤时,应尽早给予糖皮质激素联合抗感染治疗,必要时予呼吸支持,争取迅速缓解症状,挽救患者生命。

