高分辨固体核磁共振法分析聚3-己基噻吩∶苝二酰亚胺衍生物的共混结构
舒婕 唐丹丹 王宁


摘要:苝二酰亚胺(PDI)衍生物是异质结太阳能电池中可替代\[6,6]-苯基-C61-丁酸甲酯(PCBM)的受体材料。本研究选取了两种不同化学结构的PDI衍生物作为研究体系,分别命名为PDI和PDI,采用高分辨固体核磁共振技术,探讨了PDI衍生物在与聚3-己基噻吩(P3HT)共混前后其分子聚集态结构的变化。发现PDI和PDI的纯净物体系中,分子均通过π-π作用形成了有序的堆叠结构,且PDI的有序度高于PDI。在分别与P3HT共混后,两种共混物表现为两相分离的结构。其中,PDI在与P3HT共混后,其晶区的有序度降低,但分子的堆叠结构没有变化;而PDI在与P3HT共混后,其晶区的有序度保持不变,但分子的堆叠结构发生了变化。通过Back-to-Back(BaBa)边带技术可以定量检测出PDI分子间酰胺位CH氢原子间的距离为3.66。依据13C-1HFSLG-HETCOR谱图的相关信息,发现两组分的界面区中,PDI的酰亚胺取代基位于P3HT噻吩环的屏蔽区。此外,使用REREDOR技术定量检测了两种PDI衍生物在与P3HT共混前后分子基团的局部运动性。研究发现,在与P3HT共混后,PDI的分子局部运动性没有变化,而PDI的分子局部运动性降低。本研究揭示了两种PDI衍生物在与P3HT共混前后的分子聚集态结构,总结了适用于研究PDI衍生物共混体系的固体核磁共振技术方案,用于表征分子的聚集态结构、组分相容性及分子基团的局部运动性能。
关键词:苝二酰亚胺;固体核磁共振;聚集态结构;相容性;聚3-己基噻吩
1引言
異质结(Bulkheterojunction,BHJ)有机太阳能电池(Organicsolarcells,OSCs)材料一般包括聚合物电子给体和富勒烯衍生物的电子受体,近年来,聚3-己烷基噻吩(P3HT)和\[6,6]-苯基-C61-丁酸甲酯(PCBM)的共混体系(P3HT:PCBM)受到高度关注[1~3]。其中,PCBM受体材料具有合适的电子能级和较高的电子迁移率,是目前效果最好的n型(受体)光伏材料。然而,其在可见光区几乎没有吸收,这限制了P3HT:PCBM相关器件的光电转化效率的进一步提高[4]。而苝二酰亚胺(PDI)衍生物在可见光区有较高的摩尔吸收系数,且作为n型(受体)光伏材料具有很高的电子迁移速率。此外,苝二酰亚胺衍生物的LUMO能级与PCBM相似,且HOMO能级很低,这些特点使PDI衍生物成为异质结太阳能电池中可替代PCBM的受体材料[5~10]。PDI分子之间具有很强的π-π相互作用,使PDI形成稳定的分子聚集态结构,因而表现出较高的电子移速率。然而,强的π-π作用致使聚集结构的尺寸较高,一般可达微米级,超出了OSCs材料中激子有效的迁移程。这阻碍了激子到达给受体界面的效率和解离率,降低了OSCs的性能[9,10]。因而,通过对PDI分子结构的修饰来控制PDI衍生物分子的聚集态结构和尺寸是提高OSCs性能的关键。对PDI分子结构的修饰主要集中在酰胺位和桥位[11~14],通过对取代基结构的改变或寡聚结构的设计与合成,可以在不同程度上提高相关OSCs的性能。结构的变化调控了分子在共混材料中的聚集态结构,包括共混物中PDI衍生物的分子堆叠结构、结晶度、PDI衍生物分子与给体分子的相容性及界面结构等,而这些结构性质影响着OSCs的光电性能[15,16]。由此可见,为了深入理解苝二酰亚胺化学结构对材料宏观性能影响机理,需要表征给、受体分子的聚集态结构及组分分子的相容性等微观信息,总结苝二酰亚胺分子化学结构、共混物中分子的聚集态结构及共混材料宏观性能的关系,从而正确地引导对于PDI化学结构的修饰。
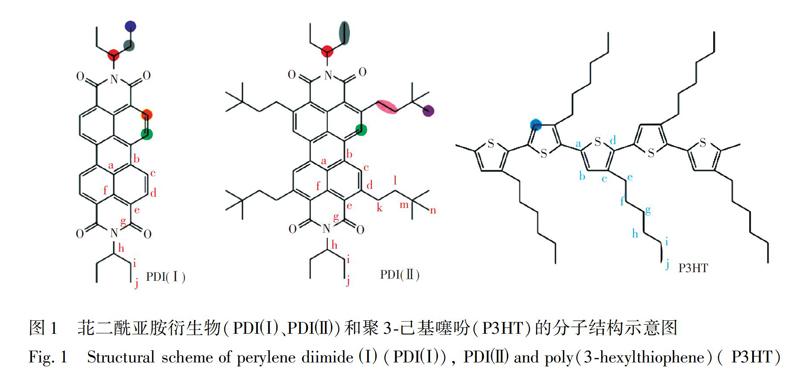
目前,表征BHJs材料的技术主要有原子力显微镜(AFM)和透射电镜(TEM)等[17,18]。这些技术可以在纳米尺度上表征共混材料的形貌特征,但很难实现分子尺度上结构及动力学信息的检测。近年来,随着硬件水平的逐步提高和脉冲序列技术的持续发展,高分辨固体核磁共振技术(Solid-statenuclearmagneticresonance,SSNMR)已成为研究材料体系结构和分子动力学行为的重要手段[19,20]。在高速魔角旋转(Magicanglespin,MAS)条件下,结合多脉冲去耦技术和多量子耦合重聚技术,研究者常可获取原子核间距离、分子聚集态结构、分子间相互作用、相尺寸以及分子局部运动性等定量或定性的信息。研究工作所涉及的体系包括液晶材料、共轭聚合物、多孔材料以及工业聚合物等[19,21,22]。然而,对于PDI衍生物材料的SSNMR研究鲜有报道。基于此,本研究采用SSNMR技术研究了两种苝二酰亚胺衍生物(分别命名为PDI和PDI,化学结构见图1)和聚3己基噻吩(P3HT)在共混前后的分子聚集态结构及共混物中组分的相容性。通过采集二维1H-1H双量子-单量子相关谱(2D1H-1HDQ-SQ)、1H-1H双量子边带谱(2D1H-1HDQsidebandpatterns)和二维13C-1H异核相关谱(2D13C-1HfrequencyswitchedLee-Goldburgheteronucleardipolar-correlationspectroscopy,FSLG-HETOCR)等谱图,对比研究了PDI和PDI的分子聚集态结构,并探讨了PDI∶P3HT和PDI∶P3HT共混物中组分的相容性及界面结构。此外,本研究使用13C{1H}rotor-encodedrotationalechodoubleresonance(REREDOR)技术,定量表征了两种PDI衍生物在与P3HT共混前后分子局部基团的运动性,探讨了PDI衍生物分子桥位结构改性对其分子聚集态结构的影响。本研究为同类共混体系的微观结构研究提供了可供参考的固体核磁共振研究方法。
2实验部分
2.1仪器与试剂
固体核磁共振2D1H-1HDQ-SQ实验、一维13C{1H}交叉极化实验(1D13C{1H}CP,Crosspolarization)和2D13C-1HFSLG-HETCOR实验[25]所使用的仪器为AVANCEⅢHD400WB固体核磁共振波谱仪(德国布鲁克公司),配有H/F/XDVT魔角探头,支持3.2mm外径的固体核磁样品管。SSNMR2D1H-1HDQsidebandpatterns实验[26]和3C{1H}REREDORsidebandpattern实验[27]所使用的仪器为AVANCEⅢ850固体核磁共振波谱仪(德国布鲁克公司),配有2.5mmH/XDVT双通道探头。
PDI和PDI样品为实验室合成样品,由原德国马普高分子所的FrédéricLaquai教授提供。合成方法参见文献\[23,24]。聚3-己基噻吩(P3HT,侧链等规度≥98%,Sigma-Aldrich公司);邻二氯苯(光谱纯,≥99%,北京伊诺凯科技有限公司)。固体核磁实验所使用的PDI∶P3HT和PDI∶P3HT共混物样品均通过溶剂挥发制备而成。
2.2实验方法
2.2.1测试样品的制备固体核磁实验所使用的PDI∶P3HT和PDI∶3HT共混物样品均通过溶剂挥发制备而成。首先,PDI衍生物和P3HT以质量比为1∶1共混溶于80℃的邻二氯苯中,制备成30mg/mL溶液。待样品全部溶解后,将溶液转移到培养皿中,静置于常温空气中,使溶剂自然挥发12h,再放置于真空干燥箱中,在80℃的真空环境下干燥12h,以去除残余的溶剂。最后,样品装入固体核磁样品管,并置于150℃环境退火处理1h。为了保证与共混体系实验条件的一致性,固体核磁实验所使用的PDI、PDI和P3HT样品采用同样的溶剂挥发制备而成。样品先在80℃溶于邻二氯苯中,制备成30mg/mL溶液。在常温空气中,自然挥发12h,在80℃的真空环境下干燥12h,去除残余的溶剂。最后,样品装入固体核磁样品管,并置于150℃环境退火处理1h。
2.2.2固体核磁共振实验及参数SSNMR2D1H-1HDQ-SQ實验、1D13C{1H}CP实验和2D13C-1HFSLG-HETCOR实验[25]所使用的魔角旋转速率均为18kHz,交叉极化接触时间均为2ms。2D1H-1HDQ-SQ实验使用RN序列对双量子信息进行激发与重聚[28]。在直接维和间接维的采样阶段,实验均使用Edumbo技术对1H原子核进行同核去偶[29]。实验的魔角旋转速率为18kHz。1D13C{1H}CP实验的采样次数为4096次,每次采集信号前的弛豫等待时间为3s。2D13C-1HFSLG-HETCOR实验的采样次数为2048次,t1维的采样点数为32。2D1H-1HDQsidebandpatterns实验使用BaBa序列激发双量子信号[30],魔角旋转速率为25kHz。一个转子周期(40μs)内的采样点数为20个。实验的累加次数为16次。13C{1H}REREDOR实验的魔角旋转速率为25kHz,一个转子周期内的采样点数为20个,实验信号的累加次数为3072次。所有的边带谱都通过使用Matlab程序进行拟合,得到1H-1H之间或1H-13C之间的偶极耦合常数值。
1H和13C的化学位移以四甲基硅烷为标准,通过使用金刚烷(Admantane,1H:δiso=1.85ppm,13C:δiso=38.484)作为二次标样进行化学位移定标[31,32]。
3结果与讨论
3.1PDI衍生物、P3HT及其共混物的分子聚集态结构研究

SSNMR2D1H-1HDQ-SQ可以半定量地提供刚性分子内及分子间的原子核空间距离的信息。通常,较短的DQ激发时间(<40μs)内所检测到的相关峰说明了相应的原子核之间的距离应小于4[26]。图2A和2B为两种PDI衍生物的2D1H-1HDQ-SQ谱,图中相关峰的指认参考图1化学结构中的颜色标记。对比PDI和PDI的谱图发现,两种衍生物的2D1H-1HDQ-SQ谱中都检测到芳香区的氢原子核的相关信息,且谱峰清晰可辨。其中,PDI分子d位氢原子之间的相关峰(橙色-橙色)可确定来源于分子间的两个d氢原子的相互作用。上述谱图信息说明两种PDI衍生物都形成了有序的分子聚集态结构。此外,与PDI相比,PDI的谱峰分辨率更高,且与烷烃取代基的相关信号更强,而PDI的烷烃区域有明显的F1维噪音。对于2D1H-1HDQ-SQ技术,谱中相关信息的强弱依赖于氢原子核之间偶极耦合强度,对于局部运动性较强的体系,其氢原子核间的偶极耦合强度较低,相关峰的信噪比较差。由于烷烃区域的氢原子密度与芳香区相比较高,因而局部运动性较高的烷烃基团往往在F1维表现出明显的噪音信号。结合PDI和PDI的谱图特征可推断,PDI的分子堆叠结构更规整,而PDI的烷烃取代基运动性较强。综合考虑两种分子的结构特点可推测,由于PDI桥位的烷烃取代基表现出较高的局部运动性,因而会带动PDI分子芳香区的局部震荡。与之相反,PDI分子的桥位没有取代基,且酰胺位取代基的结构与PDI相同,因此分子的局部运动性较弱,分子堆叠结构更加规整。





4结论
对比PDI和PDI的固体核磁实验数据可见,桥位烷基的修饰改变了PDI衍生物的分子堆叠结构及芳香区基团的局部运动性。此外,分子化学结构的改变也同时影响了PDI衍生物分子在与P3HT共混后的分子聚集态结构。通过对多种SSNMR谱图的解析发现,2D1H-1HSQ-DQ技术可提供有关分子π-π堆叠结构和氢原子核间空间距离的信息。结合烷烃区的谱峰峰型,可以定性推断侧链的局部运动性。此外,2D1H-13CHETOCR实验可以用于检测共混体系中组分的相容性。对于相分离的共混物,2D1H-13CHETOCR还有望提供两相界面区的分子局部结构信息。结合使用异核偶极耦合调制的边带谱技术,如13C{1H}REREDOR技术,可以通过对分子基团的局部运动性的定量表征,以进一步验证有关SSNMR结构分析的实验结论。
References
1DangMT,HirschL,WantzG.Adv.Mater.,2011,23(31):3597-3602
2MüllenK,PisulaW.J.Am.Chem.Soc.,2015,137(30):9503-9505
3LuLY,ZhengTY,WuQH,AlexanderMS,ZhaoDL,YuLP.Chem.Rev.,2015,115(23):12666-12731
4LinYZ,LiYF,ZhanXW.Chem.Soc.Rev.,2012,41(11):4245-4272
5LiC,WonnebergerH.Adv.Mater.,2012,24(5):613-636
6KozmaE,CatellaniM.DyesPigments,2013,98(1):160-179
7TangCW.Appl.Phys.Lett.,1986:48(2):183-185
8KammV,BattagliarinG,HowardIA,PisulaW,MavrinskiyMV,ChenL,MüllenK,LaquaiF.Adv.Energ.Mater.,2011,1(2):297-302
9LiuZT,ZhangLH,ShaoM,WuY,ZengD,CaiX,DuanJS,ZhangXL,GaoX.ACSAppl.Mater.Interfaces,2018,10(1):762-768
10WangLH,ChenLC,XiaoY.J.Mater.Chem.C,2017,5(48):12816-12824
11KotowskiD,LuzzatiS,ScaviaG,CavazziniM,BossiA,CatellaniM,KozmaE.DyesPigments,2015,120:57-64
12ZhongY,TrinhMT,ChenRS,WangW,KhlyabichPP,BharatK,XuQZ,NamCY,SfeirMY,BlackC,SteigerwaldM,LooYL,XiaoSX,NgF,ZhuXY,NuckollsC.J.Am.Chem.Soc.,2014,136(43):15215-15221
13ZhangXL,JiangB,ZhangX,TangAL,HuangJH,ZhanCL,YaoJN.J.Phys.Chem.C,2014,118(42):24212-24220
14HUXiao-Lian,SHIMin-Min,ZUOLi-Jian,FULei,DAIShu-Lie,CHENHong-Zheng.ActaChimicaSinica,2011,69(6):673-679
胡小鏈,施敏敏,左立见,傅磊,戴树洌,陈红征.化学学报,2011,69(6):673-679
15YangXY,XuWL,ZhengF,LiuJQ,HaoXT.Phy.D.Appl.Phys.,2016,49(25):255502-255509
16SunJP,HendsbeeAD,DobsonAJ,WelchGC,HillIG.Org.Electron.,2016,35:151-157
17ZhangX,LuZH,YeL,ZhanCL,JB,ZhaoY,HuangJH,ZhangSL,LiuY,ShiQ,LiuYY,YaoJN.Adv.Mater.,2013,25(40):5791-5797
18LiMG,WangL,LiuJG,ZhouK,YuXL,XingRB,GengYH,HanYC.Phys.Chem.Chem.Phys.,2014,16(10):4528-4537
19HansenMR,GrafR,SpiessHW.Chem.Rev.,2015,116(3):1272-1308
20BakhmutovVI.Solid-StateNMRinMaterialsSciencePrinciplesandApplications,2012,CRCPress,BocaRaton,USA
21ZhangTT,YuanY,CuiX,YinHN,GuJL,HuangH,ShuJ.Polym.Sci.Pol.Phys.,2018,56(9):751-761
22ShuJ,DudenkoD,EsmaeiliM,ParkJH,PunireddSR,ChangJY,BreibyDW,PisulaW,HansenMR.J.Am.Chem.Soc.,2013,135(30):11075-11086
23NoldeF,PisulaW,MüllerS,KohlC,MüllenK,Chem.Mater.,2006,18:3715-3725
24KammV,BattagliarinG,HowardIA,PisulaW,MavrinskiyA,ChenL,MüllenK,LaquaiF.Adv.EnergyMater.,2011,1(2):297-302
25RossumBJV,ForsterH,GrootHJMD.J.Magn.Reson.,1997,124(2):516-519
26SchnellI,SpiessHW.J.Magn.Reson.,2001,151(2):153-227
27SaalwachterK,SchnellI.Solid.State.Nucl.Mag.,2002,22(2-3):154-187
28CarravettaM,MattiasE,ZhaoX,BrinkmannA,LevittMH.Chem.Phys.Lett.,2000,321(3-4):205-215
29SakellariouD,LesageA,HodgkinsonP,EmsleyL.Chem.Phys.Lett.,2000,319(3-4):253-260
30FeikeM,DemcoDE,GrafR,GottwaldJ,HafnerS,SpiessHW.J.Magn.Reson.,1996,122(2):214-221
31HayashiS,HayamizuK.Chem.Soc.Jpn.,1991,64(2):685-687
32MorcombeCR,ZilmKW.J.Magn.Reson.,2003,162(2):479-486
33NieuwendaalRC,RoHW,GermackDS,KlineRJ,ToneyMF,ChanCK,AgrawalA,GundlachD,VanderHartDL,DelongchampDM.Adv.Funct.Mater.2012,22(6):1255-1266
34NieuwendaalRC,SnyderCR,KlineRJ,LinEK,VanderHartDL,DeLongchampDM.Chem.Mater.2010,22(9):2930-2936

