长期口服托伐普坦治疗心力衰竭患者1例
1 病例简介
患者男性,35岁,因“间断活动后胸闷、气促30年,双下肢水肿2年,加重20 d”入院。患者30年前于当地医院诊断为“先天性心脏病、主动脉瓣狭窄”,22年前行主动脉瓣机械瓣置换术(AVR)+右冠状动脉-主动脉根部旁路移植术,术后活动耐量正常,规律服用华法林抗凝。2年前患者劳累后出现胸闷气促、干咳,伴夜间阵发性呼吸困难及双下肢水肿,诊断为“心力衰竭”,规律口服培哚普利、倍他乐克、螺内酯、氢氯噻嗪、地高辛、华法林等药物。之后患者反复出现胸闷、气促,20 d前因双下肢水肿加重,尿少,伴夜间阵发性呼吸困难及干咳就诊。既往有吸烟史,已戒烟,否认家族性遗传病史。体格检查:双肺未闻及干湿性啰音,心界向左侧扩大,心率70次/min,心律绝对不齐,S1强弱不等,脉搏短绌,主动脉瓣听诊区可闻及3/6级收缩期吹风样杂音及舒张期机械瓣音,双下肢轻度水肿,每日尿量700~800 mL。实验室检查结果见表1。心电图示心房颤动,偶发室性早搏,ST-T改变,室内传导阻滞。床旁胸片示心脏扩大,主动脉根部致密影(术后改变),双侧胸腔积液,右侧较多(见图1A)。胸部CT示心脏扩大,双肺淤血,双侧胸腔积液,右侧为著(见图2A)。超声心动图示左房前后径78 mm、左室舒张末期内径61 mm、右房大小正常、右室前后径27 mm,左室射血分数(LVEF)32%,主动脉瓣机械瓣狭窄,二尖瓣、三尖瓣中量反流,心功能减低,肺动脉高压(估测肺动脉压59 mmHg)。主动脉CT血管成像(CTA)示主动脉瓣区金属瓣,瓣周主动脉根窦部管壁增厚、钙化,升主动脉右侧壁局部囊袋状突起,升主动脉横径30 mm;心脏扩大,以左房室为著;双侧少量胸腔积液,以右侧为著。冠状动脉造影、双侧颈动脉及双下肢血管超声未见异常。入院诊断:(1)先天性心脏病、主动脉瓣机械瓣置换术后、主动脉瓣狭窄、冠状动脉旁路移植术(CABG)后、心脏扩大、心律失常、心房颤动、心力衰竭、心功能Ⅲ级[纽约心脏病协会(NYHA)分级];(2)肺动脉高压;(3)高胆红素血症;(4)肝功能异常。
入院后给予患者口服托拉噻米40 mg/d,托伐普坦 15 mg/d治疗,连续使用3个月。患者胸闷气促症状好转,双下肢水肿消失,可耐受日常活动量,6 min步行实验>500 m。每日平均尿量均>1 500 mL,负平衡>500 mL,体质量逐渐下降至68 kg,见图3。复查胸片示双肺淤血明显吸收,胸腔积液较前减少,见图1B。复查胸部CT示右侧胸腔积液较前减少,见图2B。复查超声心动图示LVEF 40%(见表2),与用药前比较有升高,达到心外科手术要求,遂行主动脉瓣下增生隔膜切除术、二尖瓣置换术(MVR)及三尖瓣成形术(TVP)。术后患者胸闷气促及双下肢水肿好转,6 min步行试验=350 m。
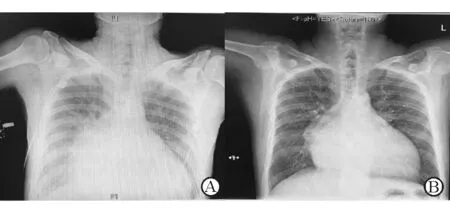
注:A为治疗前胸片;B为治疗后胸片,肺淤血吸收,胸腔积液量减少
图1 托伐普坦治疗前后胸片对比
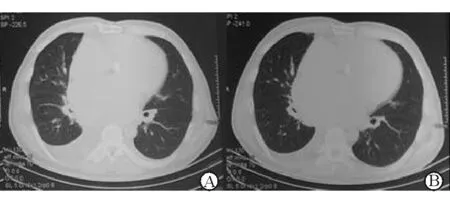
注:A为治疗前胸部CT;B为治疗后胸部CT,肺淤血吸收,右侧胸腔积液量减少
图2 托伐普坦治疗前后胸部CT对比
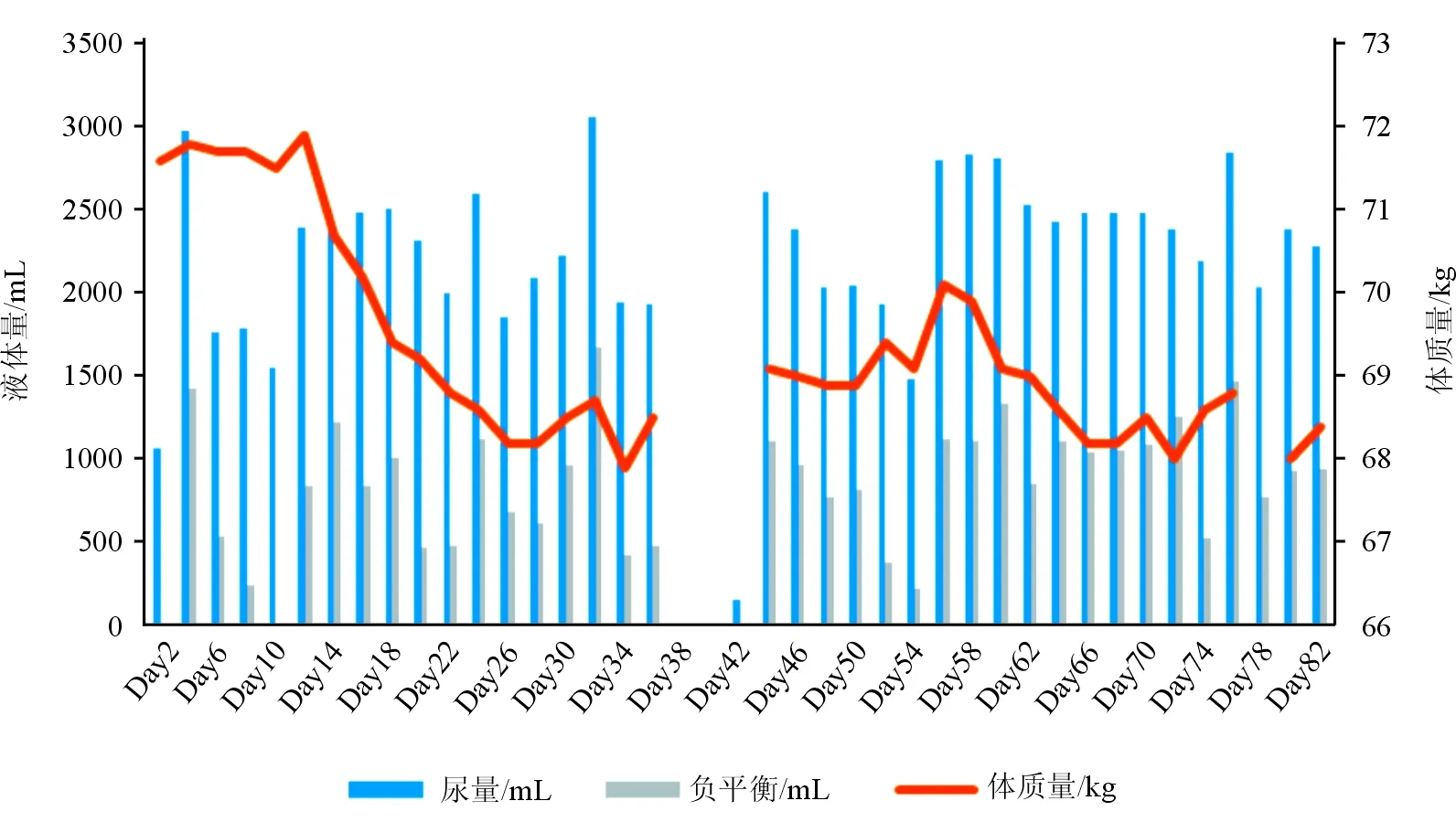
图 3 托伐普坦治疗期间尿量及体质量变化
表1 托伐普坦治疗前后生化指标变化

项目GGT/U·L-1Tbil/μmol·L-1Dbil/μmol·L-1肌酐/μmol·L-1尿酸/μmol·L-1血清钾/mmol·L-1血清钠/mmol·L-1NT-proBNP/pg·L-1治疗前21130.717.4588853.95138.33425治疗后8620.811.0984743.75141.12200
注:GGT为γ-谷氨酰转移酶;Tbil为总胆红素;Dbil为直接胆红素;NT-proBNP为N末端脑钠肽前体
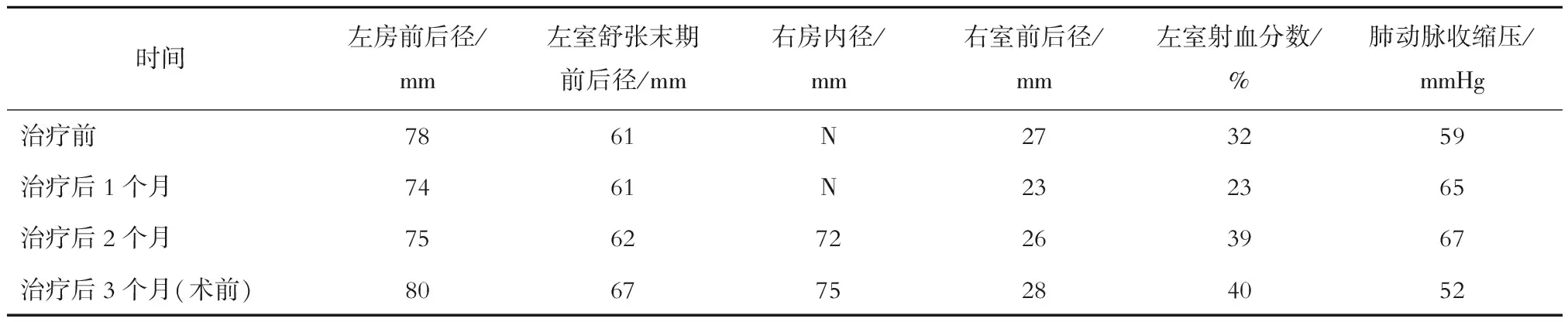
表2 托伐普坦治疗前后超声心动图指标变化
注:N表示正常,无具体数值
2 讨论
利尿剂作为改善心力衰竭症状的基本药物,在临床上已经使用50多年,效果肯定,但长期大量使用不仅会造成利尿剂抵抗,而且会激活体内神经内分泌系统,加重肾脏损害,导致电解质紊乱,从而形成心功能衰竭和肾功能衰竭的恶性循环[1],因此,有必要寻求更为安全有效的利尿剂。
精氨酸加压素(AVP)又称血管加压素、抗利尿激素(ADH),是丘脑视上核和室旁核的大型神经内分泌细胞合成并在神经垂体(垂体后叶)中贮存的肽类激素。目前已知的AVP受体有V1a、V1b和V2,AVP与肾脏集合管表面的V2受体结合,激活水通道蛋白2(AQP2),促进自由水的重吸收,同时激活表皮钠通道(ENaC),选择性调节钠的重吸收[2]。AVP水平升高可能是心力衰竭患者病情加重的原因。托伐普坦是选择性AVP-V2受体拮抗剂,与V2受体的亲和力是天然AVP与V2受体结合的1.8倍,是AVP与V1a受体亲和力的29倍。托伐普坦竞争性与V2受体结合,阻断AVP的作用,增加了水,特别是自由水的排泄[3]。
多项临床观察已证实,短期使用托伐普坦可以明显增加心力衰竭患者的尿量,降低体质量,减轻呼吸困难及肺淤血,改善心力衰竭症状,有效缩短住院时间[4-6]。2003年,美国30个医疗中心对托伐普坦使用25 d的随机对照试验证实,慢性心力衰竭患者在不严格限水且长期使用袢利尿剂的基础上分别加用30 mg/d、45 mg/d、60 mg/d托伐普坦,用药第1天即可显著降低体质量(-0.79±0.99)kg,(-0.96±0.93) kg,(-0.84±0.02) kg(P均<0.001),明显增加24 h尿量(3.9±0.6)L/24 h, (4.2±0.9)L/24 h,(4.6±0.4)L/24 h(P均<0.001),改善水肿,纠正低钠血症,对心率、血压、血钾或肾功能均没有显著影响[7]。EVEREST研究[8]中将2 072例使用托伐普坦(30 mg/d)60 d以上的心力衰竭患者与2 061例对照组患者对比,中位随访时间9.9个月,结果表明托伐普坦可以减轻心力衰竭患者的体质量并维持血钠正常水平,且作用持续时间较长,但对长期病死率及心力衰竭复发率无明显影响。
目前,临床上仍然缺乏长期使用托伐普坦的经验,用药时间最长的研究是METEOR研究[9],连续使用托伐普坦1年后,与治疗前比较,心力衰竭患者左室容积并无明显缩小,但患者的全因死亡率和再住院率明显降低。
2012年4月,英国药品和健康产品管理局曾发出警告:托伐普坦可导致血钠快速升高并引发严重神经症状,严重者可引起渗透性脱髓鞘甚至死亡。所以用药期间应动态监测患者的血钠水平,特别是对于血钠<120 mmol/L以及有渗透性脱髓鞘综合征风险(如低氧、酗酒、营养不良)的患者,建议将纠正血钠的速度控制在前1~5 h≤6 mmol/L,后6~12 h≤8 mmoL/L的范围内[10]。同时,用药期间应注意患者是否有因尿量突然增多而出现有效循环血量不足、低血压及脱水等情况。2013年1月,美国食品药品管理局曾警告托伐普坦存在严重并且可能致命的肝损伤风险,急性肝衰竭患者可能需要肝移植,建议有潜在肝病的患者不服用此药,并限定使用时间不超过30 d。如果出现肝功能异常,或伴有肝功能受损的症状和体征,如疲劳、厌食、恶心呕吐、右上腹不适、发热、皮疹、黄疸、尿色深等症状,应立即停止使用托伐普坦,并尽快进行肝功能检查。该警告基于一项1 445例常染色体显性多囊性肾病患者参与的为期3年的Ⅲ期、多中心、双盲、安慰剂、对照临床试验。该试验中,托伐普坦的每日最大剂量(上午90 mg和下午30 mg)已超过适应证中批准用于低钠血症治疗的60mg最大日剂量,其中有3例接受托伐普坦治疗的患者出现了谷丙转氨酶(ALT)显著升高,并伴随有临床意义的血清总胆红素升高,停止用药后肝功能均得到恢复[11]。托伐普坦临床前的动物实验表明导致肝脏病变的机制可能与肝脏代谢酶相关。托伐普坦主要通过肝脏(CYP3A4)代谢,据此认为肝损伤的程度与作用的强度和作用时间长短相关,肝硬化患者的肝脏更容易受损。但目前在肝硬化的临床试验中并未发现托伐普坦有肝损伤,上市后的安全性报告中也无明确肝损伤报告。
本例患者连续使用托伐普坦15 mg/d,共3个月,是尝试长期持续小剂量使用托伐普坦的典型病例,治疗期间主要的不良反应为口干,均为轻中度,患者可耐受,未发生其他严重不良事件。对本例患者随访的结果表明,心力衰竭患者在常规使用利尿剂的基础上长期加用小剂量托伐普坦安全有效,不影响血钠、血钾等电解质水平,未激活肾素-血管紧张素-醛固酮系统(RAAS)和交感-肾上腺髓质系统,不影响心率、血压及肝肾功能。该患者用药前存在心力衰竭合并肝功能轻度异常,用药过程中严密监测肝功能变化,配合使用保肝药物,肝功能不但没有继续恶化,反而随着心功能的改善而得以恢复,取得满意的治疗效果,托伐普坦能否改善长期预后尚需进一步大样本的临床观察。

