室管膜下区受侵对脑胶质瘤预后的影响*
彭世义 李艳萍 涂子为 李国庆
胶质瘤是常见的颅内原发肿瘤,手术治疗是重要的治疗手段,手术切除程度是影响患者生存的主要原因[1-2]。瘤床复发是主要的失败模式,但有部分患者,即便是低级别脑胶质瘤,也可能较早出现颅内播散,原因可能与肿瘤干细胞迁徙有关[3]。位于侧脑室壁外5 mm 范围内的室管膜下区(subventricular zone,SVZ)及海马齿状回颗粒下层(SGZ)是成人脑内两大干细胞池。有报道[4-5]胶质瘤干细胞与神经干细胞有相似的分子通路、PTEN 抑癌基因的失活以及相同的基因表型,因此神经干细胞被认为是胶质瘤干细胞的重要来源。有小样本的文献报道[2,6-7]SVZ 受累是影响总生存及无进展生存的不良预后因素,也有研究[8]认为SVZ 受累不是胶质瘤的预后影响因素。本研究回顾性分析江西省肿瘤医院175 例胶质瘤患者,根据术前MRI 检查SVZ 是否受侵分为受侵组(SVZ+)和未受侵组(SVZ-),探讨SVZ 受侵对脑胶质瘤患者预后影响,为合理治疗提供依据。
1 材料与方法
1.1 一般资料
通过病案检索收集江西省肿瘤医院2010年1月至2015年7月收治的胶质瘤患者共202 例,其中27例手术后未复查,2 例未手术,无多次手术患者,3 例术前影像资料不全,因此共175例资料完整的患者纳入分析。病案信息包括年龄、性别、术前病灶部位、大小、水肿程度、术后病理、术后是否放疗、放疗与手术间隔时间、放疗剂量、是否化疗。根据术前MRI中肿块与SVZ 关系(SGZ 与SVZ 颞角邻近,故未单独列出SGZ 是否受侵),如增强病灶(高级别胶质瘤)或T2 FLAIR异常区(低级别脑胶质瘤)与侧脑室壁最短距离<5 mm 为SVZ(+),反之为SVZ(-)(图1,2)。根据患者术后第1 次MRI(因为资料较早,多数患者未在术后72 h 行MRI 检查)与术前MRI 比较确定手术切除程度,无残存病灶为手术全切,有任何残存病灶为部分切除,活检特指立体定向活检。
1.2 方法
所有患者均经手术治疗,并取得病理证实。术后放疗采用CT与MRI融合勾画靶区。对于低级别胶质瘤,采用脑胶质瘤诊疗规范标准[9],肿瘤区(gross tumor volume,GTV)为术腔及MRI FLAIR 异常区,亚临床区(clinical tumor volume,CTV)为GTV外扩1.0~2.0 cm 并做适当修正(如骨、大脑镰等自然屏障),计划靶区(plan tumor volume,PTV)为CTV 外扩0.3 cm,给予54 Gy/27 次。对于高级别胶质瘤,采用MD Anderson 癌症中心勾画标准[10],GTV 为MRI T1 增强灶及术腔,CTV1 为GTV 外扩0.5 cm,CTV2 为GTV 外扩2.0 cm 并做适当修正(如骨、大脑镰等自然屏障),PTV1、PTV2分别在CTV1、CTV2外扩0.3 cm,PTV1给予60~66 Gy/28~30次;PTV2给予50 Gy/28次,采用调强放疗技术。
同期化疗为替莫唑胺75 mg/(m2·d),自放疗开始至放疗结束;辅助化疗为替莫唑胺150~200 mg/(m2·d),连续5 d,每4周1次。
1.3 生存时间及复发的定义
放疗结束及以后每2~3 个月复查MRI 检查,疗效评估采用RANO 标准[11]。总生存时间为确诊之日至末次随访时间或死亡时间;无进展生存时间为确诊之日至末次随访时间或首次复发时间或死亡时间。肿瘤复发定义为动态影像学检查出现新发病灶,或原病灶进展;复发灶中心与原发病灶之间距离在2.0 cm以内为瘤床复发,超过2.0 cm为远处复发。
1.4 统计学分析
应用SPSS 19.0软件进行统计学分析,采用Kaplan-Meier法计算本组患者总体生存率和无进展生存率,采用Log-rank检验进行单因素预后分析,采用Cox回归模型进行多因素分析,复发模式与SVZ受累的相关性采用χ2检验,P<0.05为差异具有统计学意义。
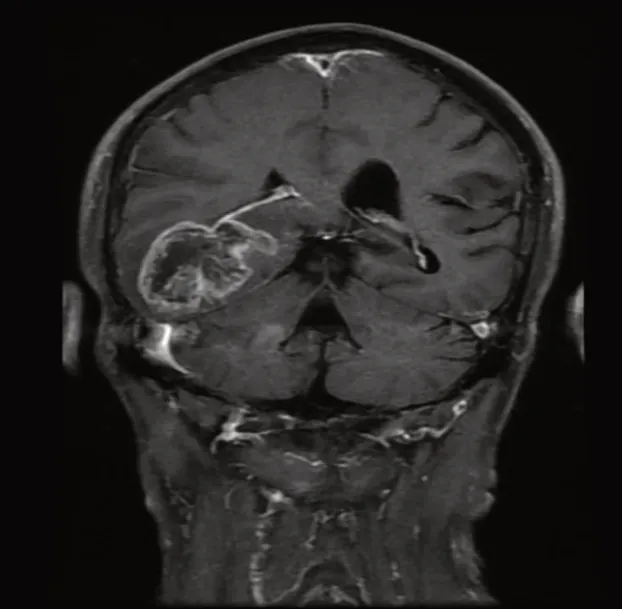
图1 SVZ受侵

图2 SVZ未受侵
2 结果
2.1 SVZ(+/-)两组患者临床特征及生存情况
75例患者在初诊时出现SVZ受侵。SVZ(+)组患者的手术全切率低(P<0.001),病灶更大(P<0.001),Ⅳ级患者更多(P=0.018);而在年龄、性别、病灶数目、水肿程度、是否放疗及化疗方面差异无统计学意义(表1)。替莫唑胺辅助化疗超过6 个周期5 例,其中SVZ(+)组4 例。全组中位随访时间63 个月,死亡82例,其中SVZ(+)组47例,5年总生存率(overall survival,OS)及无进展生存率(progression-free survival,PFS)分别为42.2%、37.5%;SVZ(+)组5年OS 及PFS分别为20.9%、15.3%,SVZ(-)组为57.1%、44.1%(P<0.001,P=0.002),生存曲线见图3,4。
单因素分析显示年龄(P=0.035)、是否单发(P<0.001)、SVZ 受侵(P<0.001)、水肿程度(P=0.008)、病理分级(P<0.001)、是否全切(P<0.001)、是否化疗(P=0.001)是影响OS 的预后因素。而是否单发(P=0.002)、SVZ 受侵(P=0.002)、水肿程度(P=0.030)、病理分级(P<0.001)、是否全切(P<0.001)是影响PFS的预后因素。多因素分析显示水肿程度、病理分级、是否全切是影响OS及PFS的预后因素(表2,3)。
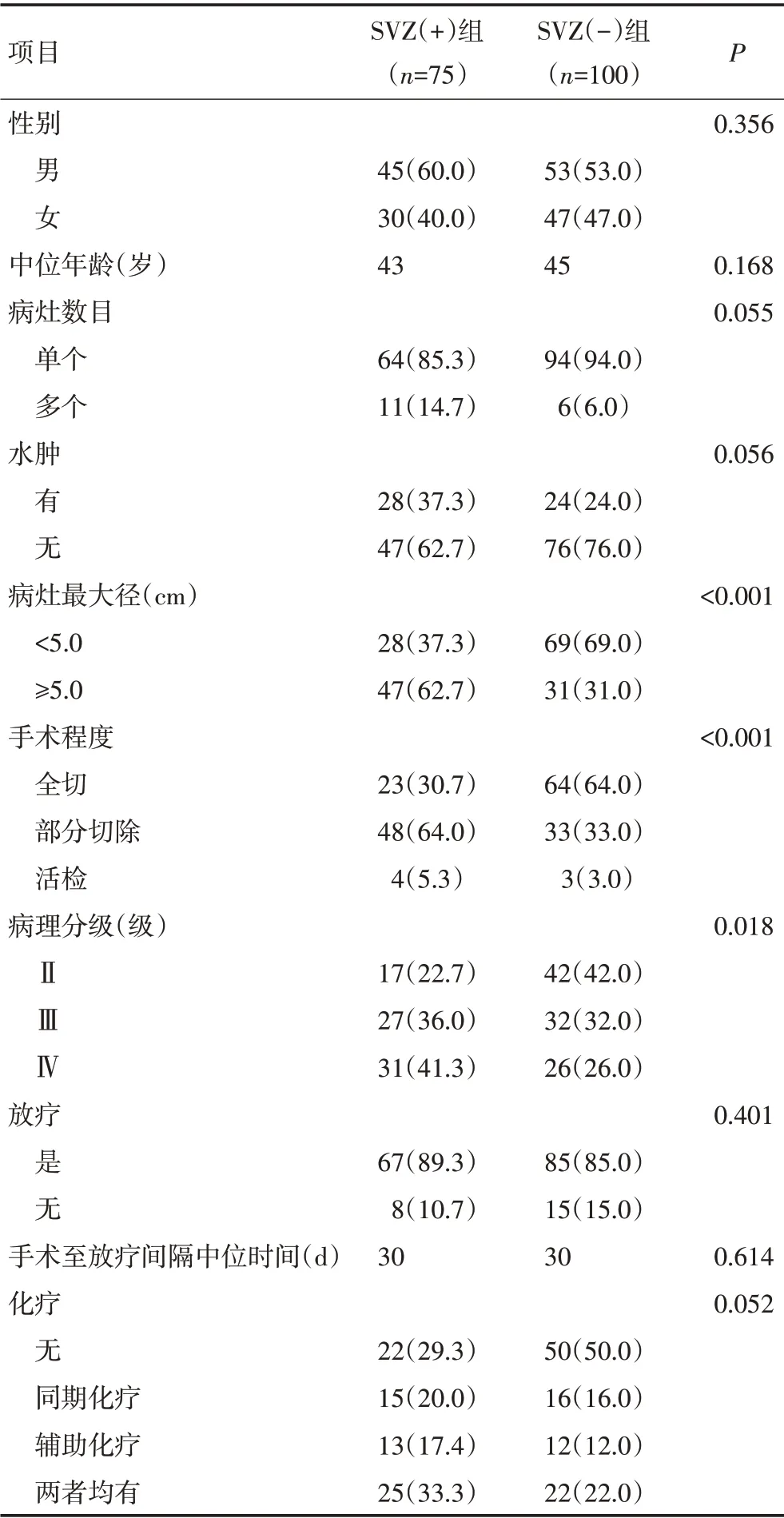
表1 175例胶质瘤患者临床特征 n(%)
2.2 复发情况
全组共89 例出现复发,单纯瘤床区复发66 例,单纯远处复发19例,4例同时存在瘤床区及远处复发(图5~7),总复发率为50.9%;其中SVZ(+)组总复发率为62.7%,SVZ(-)组为42.0%(P=0.007);SVZ(+)组远处复发率为21.3%,而SVZ(-)组为7.0%(P=0.004)(表4,5)。

图3 全组患者的OS和PFS曲线比较
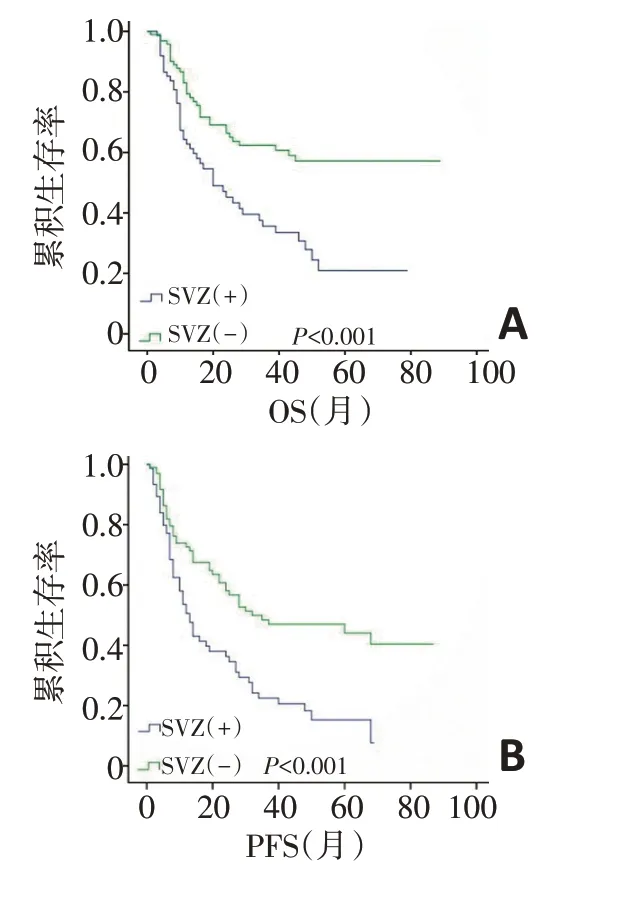
图4 SVZ(+/-)两组患者的OS和PFS曲线比较

表2 影响OS、PFS的单因素分析
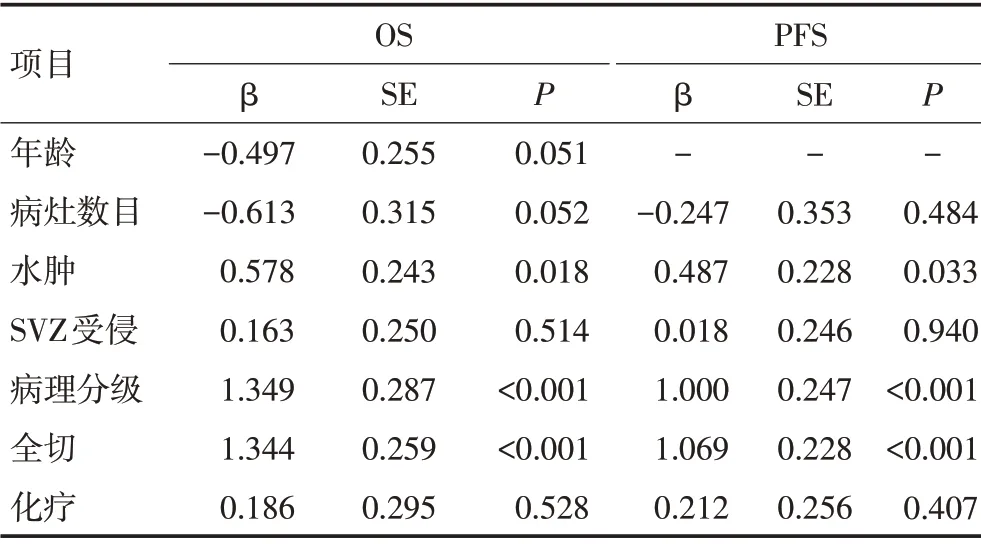
表3 影响OS、PFS的多因素分析

图5 瘤床区复发

图6 远处播散(第四脑室)
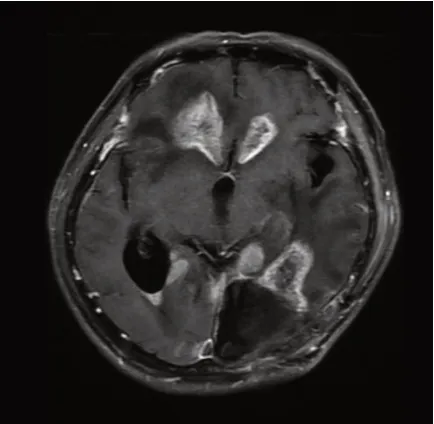
图7 瘤床复发及远处播散

表4 两组患者是否出现复发的比较 n(%)

表5 两组患者复发部位的比较 n(%)
3 讨论
本研究单因素分析显示SVZ 受侵是影响胶质瘤OS 和PFS 的不良预后因素,75 例SVZ(+)患者的5年OS及PFS分别为20.9%和15.3%,而SVZ(-)组分别为57.1%和44.1%(P<0.001,P=0.002)。原因可能与SVZ受侵患者的病灶通常位置更深,手术难以切除干净,且发生在SVZ 区肿瘤与胶质母细胞瘤关系更为密切有关。本研究显示SVZ(+)组的手术全切率明显低于SVZ(-)组。且多因素分析显示,手术是否全切、病理分级是影响OS 及PFS 的独立预后因素。Liu 等[12]报道143例低级别胶质瘤,其中115例SVZ受侵,全切率仅28.0%(P<0.001)。有报道[6,12-15]更高的病理分级、大病灶以及多灶是影响胶质瘤预后的不良因素。本研究同样发现在SVZ(+)组存在更多的高级别胶质瘤患者以及病灶最大径≥5.0 cm 的患者(P=0.018,P<0.001),初诊时多灶也更常见(P=0.055)。
Ho等[16]报道92例胶质母细胞瘤,术后接受替莫唑胺同期放化疗及辅助化疗,脑室周肿瘤的中位OS、PFS 分别为17.5 个月和5.7 个月,而非脑室周肿瘤达23.3个月和8.9个月(P=0.005)。Liang 等[17]也报道了类似结果,中位随访60.2个月,36例SVZ受侵患者中位OS 为18.6 个月,未受侵患者为26.4 个月(P=0.005),包括年龄、KPS 评分、切除程度、肿瘤大小、SVZ是否受侵在内进行多因素分析,SVZ受侵仍然是影响OS 的不良预后因素。对于低级别胶质瘤,Liu等[12]结果同样显示SVZ未受侵患者的OS优于受侵患者(P=0.027)。
有研究[4-5]认为胶质瘤干细胞起源于神经干细胞。肿瘤干细胞具有自我更新、无限繁殖、多向分化、迁移以及对放化疗抗拒的特性,这也是肿瘤发生复发及转移的主要原因[3,18-19]。本组共89 例患者出现复发,SVZ 受侵组总的复发率62.7%,而未受侵组为42.0%(P=0.007),远处复发率分别为(21.3%vs.7.0%,P=0.004)。原因一可能与SVZ区富含更多的胶质瘤干细胞,对术后放化疗抗拒,以及肿瘤干细胞沿血管周间隙迁移至远处,并形成转移灶[20]。Lim等[14]根据胶质瘤病灶与SVZ和大脑皮层之间关系,将肿瘤分为4 型:Ⅰ型为肿瘤累及SVZ 和皮层,Ⅱ型为肿瘤累及SVZ,未累及皮层,Ⅲ型为肿瘤未累及SVZ,但累及皮层,Ⅳ型为肿瘤未累及SVZ 和皮层;发现SVZ 受侵患者的复发率和远处复发率均更高。另一原因可能与手术中打通侧脑室,残留的肿瘤细胞脱落进入脑脊液,并随脑脊液循环播散至远处。Roelz 等[21]报道239 例高级别胶质瘤患者,137 例患者术中打通侧脑室,25 例患者出现软脑膜播散,而102 例未打通侧脑室的患者,仅2 例出现软脑膜播散,认为手术侵入侧脑室增加了软脑膜播散风险。
有报道[14-15,22-24]针对SVZ区给予合适的放疗剂量可改善OS 及PFS。Mathew 等[25]认为同侧接受大于56 Gy 的剂量未改善OS 及PFS。Adeberg 等[22]研究中,同侧SVZ接受超过40 Gy能明显改善胶质母细胞瘤患者的PFS(P=0.013)。但也有研究证实SVZ 区剂量与PFS 之间无关[26]。目前正在进行的两项临床研究(NCT02177578 和NCT02039778)有望回答是否给予SVZ区照射能带来生存获益。
本研究也存在一些缺陷:1)SVZ组的手术全切率更低以及包含更多的Ⅳ级患者,而手术切除程度、病理分级均是影响OS、PFS的独立预后因素。2)本文为回顾性研究且未开展分子检测,仅少数患者进行MGMT启动子甲基化、IDH1/2、1p19q杂合性缺失的检测,所以在分析时未就此方面进行比较。3)肿瘤的复发主要依靠影像检查的判断,而非病理检查。但是,在本组患者中仍观察到在单因素分析中SVZ受侵是影响胶质瘤OS、PFS的不良预后因素,SVZ受侵增加总的复发概率和远处复发概率。然而,是否将SVZ区作为放疗靶区仍需进一步研究。

