如意金黄散外敷治疗术后早期炎性肠梗阻的效果观察
姚柳青 王燕 陈昭硕 陈秀梅
(福建省肿瘤医院,福建 福州 350014)
肠梗阻是腹部手术后常见的并发症,但术后早期炎性肠梗阻(early postoperative inflammatory small bowel obstruction,EPISBO)易被忽视。炎性肠梗阻是由腹部手术创伤或腹腔内炎症等导致肠壁水肿和渗出,形成的一种机械性和动力性同时存在的肠梗阻,以粘连性肠梗阻多见,占术后肠梗阻的80%~90%[1,2],多发生在腹部手术后 2 周内,保守治疗效果好。目前保守治疗方法包括:禁食、持续胃肠减压、全肠外营养、维持水电解质和酸碱平衡,及时纠正低血钾,同时辅以生长抑素及小剂量激素,必要时抗感染治疗及甘露醇保留灌肠等[3],但如误诊为机械性肠梗阻而予以手术治疗,术后可能出现梗阻不能缓解甚至加重,同时因多次手术而致肠瘘、腹腔感染或因大部分肠管被切除发生短肠综合征,严重者甚至引起全身多器官功能衰竭死亡[4]。我院自2015年8月至2017年8月,在常规治疗的基础上联合如意金黄散外敷的方法治疗术后早期炎性肠梗阻患者,现报告如下。
1 资料和方法
1.1 一般资料 60 例患者中男 38 例,女 22 例,年龄41~86 岁。原发病:肝癌 22 例,胃癌 19 例,结直肠癌15 例,腹膜后肿瘤2 例,胃肠道间质瘤2 例,所有患者术后均有一过性的排气及少量排便; 出现腹胀33例;恶心、呕吐 11 例;轻度腹痛 7 例;发热 10 例。无典型的机械性完全性肠梗阻征象,均符合术后早期炎性肠梗阻的诊断标准[1-3]。按随机数字表法将患者分为治疗组和对照组各30 例,两组性别、年龄、术后至发病时间、手术类型比较,差异无统计学意义(P>0.05),具有可比性。见表1。
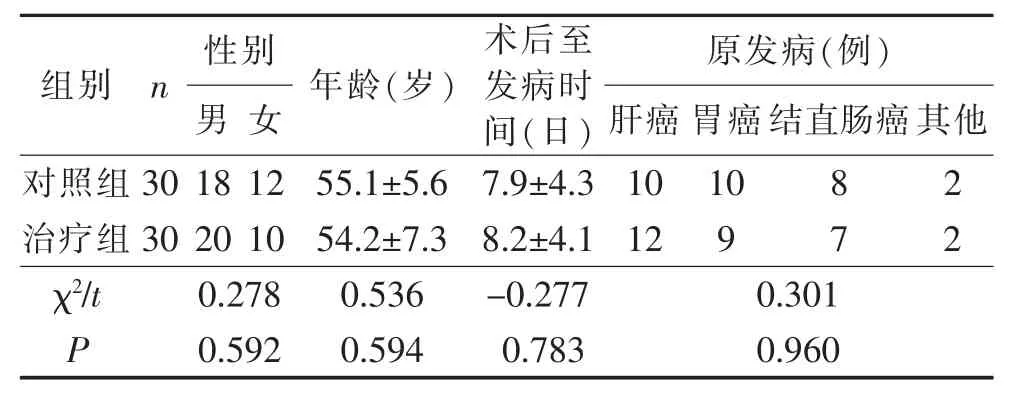
表1 两组患者基线资料比较
EPISBO 的诊断标准: ①有近期腹部手术史,尤其是有短期反复手术史,术中有广泛分离粘连病史。手术后的5~7 日,往往已排气、排便,进食后再出现梗阻,且症状逐渐加重;②有呕吐,腹胀,停止排气、排便等肠梗阻表现,腹痛一般较轻;③肠鸣音较少或消失,偶闻及气过水音;④立卧位腹部平片见小肠多处不同程度积气积液,偶见结肠积气; ⑤全腹轻压痛,腹部质韧,未扪及肿物;⑥消化道造影见肠管均匀扩张,肠蠕动减弱,CT 扫描见病变区肠壁水肿增厚,边界不清,肠腔积气;⑦排除机械性肠梗阻和继发于吻合口瘘、电解质紊乱等原因造成的肠麻痹。
1.2 治疗方法
1.2.1 基本治疗 两组常规禁食、持续胃肠减压、维持水电解质酸碱平衡、全肠外营养支持。总热卡为30~35 kcal/kg,60%为脂肪供能,40%为葡萄糖供能。应用奥曲肽(善宁)0.3 mg 加45 mL 生理盐水中用微量泵静脉泵入,每12 h 更换。同时甲强龙40 mg 加生理盐水 100 mL 静脉滴注,1 次/日,连续应用 3 日。
1.2.2 中药外敷 治疗组加用中药如意金黄散,取1袋(12 g)如意金黄散加入蜂蜜搅拌成糊状,均匀涂抹于无伤口敷料覆盖的前腹壁(上至肋弓,下至耻骨联合,两侧至腋前线),厚度3 mm,上盖两层纱布,外盖塑料保鲜膜(冰箱用保鲜膜即可),以防水分蒸发而降低疗效,每次 1~2 h 左右,每 6 h 使用 1 次,连续应用7 日。用药过程中观察患者腹部症状和局部皮肤情况。
1.2.3 评价方法 观察两组患者治疗后肠鸣音恢复时间、肛门排气时间、住院时间的差别。
1.2.4 统计学方法 数据以均数±标准差表示,采用SPSS 17.0 统计软件处理,计量资料用t 检验,计数资料用卡方检验,P<0.05 有统计学意义。
2 结果
两组治疗后肠鸣音恢复时间、肛门排气时间及住院时间比较见表2。
表2 两组患者术后各项指标比较()
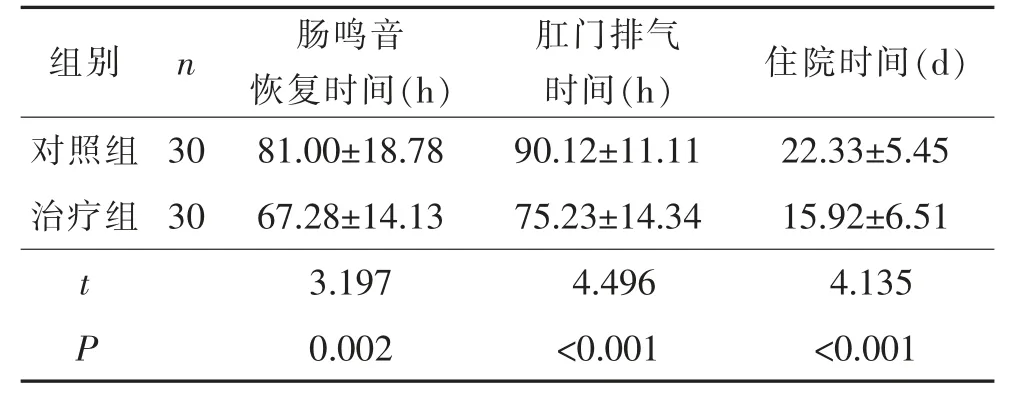
表2 两组患者术后各项指标比较()
组别 n 肠鸣音恢复时间(h)肛门排气时间(h) 住院时间(d)对照组 30 81.00±18.78 90.12±11.11 22.33±5.45治疗组 30 67.28±14.13 75.23±14.34 15.92±6.51 t 3.197 4.496 4.135 P 0.002 <0.001 <0.001
3 讨论
EPISBO 发生的主要原因是腹部手术创伤和腹腔内炎症。腹部手术创伤指术中分离肠管致外膜受损,长时间肠管外露以及其他因手术操作所造成的肠管损伤。腹腔内炎症主要是指术中腹腔内积血、积液或术后创面渗出导致无菌性炎症物质残留的情况[5],不包括术后吻合口瘘、胆瘘导致的腹腔感染。EPISBO 既有机械性因素,又有肠动力障碍。临床症状以腹胀为主,腹痛相对较轻,肠梗阻的症状及体征十分典型,但较少发生绞窄性肠梗阻,部分患者术后有一过性的排气及少量排便。因本病是由手术创伤及腹腔内炎症造成的肠壁缺血、水肿、蠕动减弱,是小肠的一种炎性生理改变,再次手术不仅不能有效地解除梗阻,反而会因分离粘连而进一步加重肠管的损伤,增加创面,术后可能出现梗阻不能缓解甚至加重[6]。EPISBO 患者因肠道内积气、积液,肠管扩张明显,肠腔压力高,肠黏膜屏障功能受损,容易出现肠菌移位,更有甚者出现肠道血供障碍,进一步加重肠腔内毒素吸收;同时机体持续过度应激反应,释放大量炎性因子入血,出现全身炎症反应综合征(SIRS),严重者可导致多器官功能障碍综合征(MODS)[7]。
目前EPISBO 的治疗主要包括禁食、持续胃肠减压、全肠外营养,及时纠正水、电解质及酸碱平衡紊乱。通过营养支持治疗,能够纠正低蛋白血症,减轻肠壁水肿,改善肠壁血供障碍,促进肠道功能的恢复。奥曲肽的应用可以抑制胃肠道消化液的分泌,降低肠腔内压力,减轻肠管扩张、缺血,减少肠黏膜屏障的破坏; 同时还能抑制胰岛素样生长因子I 的合成,抑制T 细胞对炎症的反应,并可阻止胶原的合成。另外小剂量激素具有确切的减轻全身炎症反应和促进肠壁水肿消退的作用[8]。在疾病后期,随着炎症的消退和渗出液的吸收,肠蠕动逐渐增强。此时,在明确肠鸣音好转的情况下,可适当给予肠动力药物,以促进肠道运动功能的恢复,加快解除梗阻[9]。
临床上目前广泛应用芒硝外敷治疗EPISBO。芒硝主要化学成分为含水硫酸钠,外敷腹壁可于局部形成高渗环境,透过腹壁吸收腹腔渗液,减轻肠壁水肿[10]。但外敷芒硝术后护理不易:一方面,芒硝单次用量较大,腹部手术后外敷芒硝腹壁压迫感明显,而且装芒硝的布袋过重导致患者下床活动受影响; 另一方面,芒硝使用后渗水硬结,布袋需频繁更换且容易导致床单、被褥浸湿,给患者及其家属带来不便的同时还增加了伤口感染的风险。
如意金黄散源于明代陈实功所著 《外科正宗》,为 《中国药典》2015年版一部收载品种,由黄柏、大黄、姜黄、白芷、天花粉、陈皮、厚朴、天南星等十味中药配伍组成。其中,黄柏燥湿泻火解毒为主;大黄解毒凉血祛瘀;姜黄破血通经,消肿止痛;白芷、天花粉解毒、消肿、排脓;陈皮、厚朴行滞消肿;苍术燥湿辟秽;天南星燥湿散结,消肿止痛;甘草泻热解毒。全方有清热解毒、燥湿化痰、消肿止痛、围聚之功效[11]。
相比于芒硝,如意金黄散与蜂蜜混合同样可于局部形成高渗环境,减轻肠壁水肿,而外敷使用时厚度仅3 mm,加之外盖保鲜膜,不仅更换方便且不影响患者下床活动。而对于金黄散消肿止痛的作用临床上也常见报道。胡文伟[12]采用如意金黄散外敷联合抗生素治疗阑尾周围脓肿,结果显示腹痛缓解时间、肿块消失时间、血常规达到正常时间、住院时间均缩短。于云[13]运用如意金黄散治疗186 例急性单纯性胰腺炎,患者的腹痛、发热、呕吐及血清淀粉酶、尿淀粉酶均有明显好转,说明金黄散对胰腺炎具有明显的消炎、消肿、止痛作用。张远哲等[14]研究发现如意金黄散可下调疮疡大鼠局部皮肤TNF-ɑ、IL—l 及IL-8 的表达,其清热解毒的功效可能与炎症递质的释放减少有关。
本例研究中,对EPISBO 患者金黄散外敷腹壁,治疗组患者的肠鸣恢复时间、肛门排气时间、住院时间均明显短于对照组(P<0.05),其原因可能与金黄散减少腹腔炎性渗出,减轻肠壁水肿,降低肠腔内压力,改善胃肠黏膜屏障功能,预防肠道细菌移位等因素有关。
由此可见,如意金黄散外敷结合常规治疗,能够有效缓解术后早期炎性肠梗阻患者的临床症状,促进炎性物质的吸收及肠蠕动功能的恢复,是辅助治疗EPISBO 的一种疗效可靠、安全的方法,使用方便,价格低廉,而且无明显副作用,值得临床推广。但在非手术治疗期间,需要严密观察病情变化,一旦出现绞窄性肠梗阻或肠穿孔等病情恶化的迹象,应及时手术治疗。

