吉西他滨联合顺铂治疗复发或转移性晚期鼻咽癌的临床研究
练英妮 毛进星 陈玉兰 欧庆莲 曾志坚

【摘要】 目的:評价吉西他滨联合顺铂治疗复发或转移性晚期鼻咽癌的临床效果和不良反应。方法:将174例复发或转移性晚期鼻咽癌患者随机分为试验组和对照组,各87例,试验组采用吉西他滨联合顺铂,对照组采用5-氟尿嘧啶联合顺铂。检测两组循环肿瘤细胞,评价与化疗效果和预后的关系。结果:试验组临床总有效率为72.4%,对照组为52.9%,试验组临床总有效率明显高于对照组(P<0.05)。对照组恶心呕吐、口腔黏膜反应等发生率均明显高于试验组(P<0.05),化疗后血小板抑制情况较对照组严重(P<0.05)。化疗开始前后,循环肿瘤细胞呈阳性率由71.8%逐步下降至12.1%,差异有统计学意义(P<0.001)。试验组的无病生存和总生存均优于对照组,差异均有统计学意义(P<0.05),Cox多因素回归分析,结果显示转移、化疗后循环肿瘤细胞状态以及化疗方法是晚期鼻咽癌患者的独立预后因子。结论:吉西他滨联合顺铂治疗复发或转移晚期鼻咽癌效果较好,循环肿瘤细胞检测可作为评估化疗效果和预后的有效指标。
【关键词】 吉西他滨; 顺铂; 复发或转移性晚期鼻咽癌; 临床疗效
【Abstract】 Objective:To evaluate the clinical efficacy and adverse reactions of gemcitabine combined with cisplatin in the treatment of recurrent or metastatic advanced nasopharyngeal carcinoma.Method:174 cases of recurrent or metastatic nasopharyngeal carcinoma were randomly divided into the experimental group and the control group,87 cases in each group.The experimental group used Gemcitabine combined with Cisplatin,and the control group used 5-Fluorouracil combined with Cisplatin.Circulating tumor cells were detected by immunomagnetic enrichment and fluorescence,the relationship with efficacy and prognosis was analyzed.Result:The clinical effective rate of the experimental group was 72.4%,the control group was 52.9%,the efficiency of the experimental group was significantly higher than that of the control group(P<0.05).The incidence of gastrointestinal reaction and oral mucosa reaction of the control group were significantly higher than those of the experimental group(P<0.05),while the platelet inhibition after chemotherapy of the experimental group was more serious than that of the control group(P<0.05).After chemotherapy,the positive rate of circulating tumor cells decreased from 71.8% to 12.1%,and the difference was statistically significant(P<0.001).The disease-free survival and overall survival of the experimental group were superior to the control group,and the differences ere statistically significant(P<0.05).The results of Cox multiple factors regression analysis showed that metastasis,circulating tumor cells and chemotherapy were the independent prognostic factor of the progression-free survival and overall survival in patients with advanced nasopharyngeal carcinoma.Conclusion:Gemcitabine combining with Cisplatin in the treatment of recurrent or metastatic advanced nasopharyngeal carcinoma has a better curative effect,and circulating tumor cell detection can be used as an effective indicator to evaluate the efficacy and prognosis of chemotherapy.
【Key words】 Gemcitabine; Cisplatin; Recurrent or metastatic advanced nasopharyngeal carcinoma;Clinical effect
First-authors address:First Peoples Hospital of Zhaoqing City,Zhaoqing 526000,China
doi:10.3969/j.issn.1674-4985.2019.12.001
鼻咽癌是一种常见的恶性肿瘤,全球范围内每年大约有86 000例新增患者,5 000例患者死于鼻咽癌[1]。早期或局部晚期鼻咽癌主要采用放疗或放化疗协同使用,5年生存率约为85%[2]。但是,有一部分人在诊断时就出现了远处转移,亦有放疗后复发的患者。复发或转移性鼻咽癌患者预后较差,中位生存期仅20个月左右[3]。目前,5-氟尿嘧啶联合顺铂是国内外常用的化疗方案,但此方案反应率为40%~65%,有效持续时间较短,副作用发生频繁,且往往难以耐受[4]。吉西他滨是一种核苷酸类似物,通过抑制DNA的合成,产生抗肿瘤的效果,常用于乳腺癌、胰腺癌和非小细胞肺癌。近期报道的2期临床试验结果显示,吉西他滨可用于治疗鼻咽癌,且疗效显著,并可以耐受不良反应[5-7]。本研究旨在评估吉西他滨联合顺铂治疗复发或转移性晚期鼻咽癌的临床效果和不良反应情况,为治疗晚期鼻咽癌提供临床依据。现报道如下。
1 资料与方法
1.1 一般资料 收集2012年3月-2017年3月本院肿瘤科收治的174例复发或转移晚期鼻咽癌患者。纳入标准:病理确诊为原发性鼻咽癌;治疗后复发或转移晚期鼻咽癌,至少有一处可以测量的病灶;复发或转移后尚未接受系统性治疗;肝肾功能正常;预计生存期大于半年者。排除标准:既往接受吉西他滨联合顺铂治疗者;精神与认知异常者;合并其他恶性肿瘤者。采用随机数表法将纳入本研究的患者分为试验组和对照组,每组87例。同时,考虑到患者年龄跨度较大的问题,而年龄的不均衡可能影响研究结果,故本研究将年龄作为平衡因素进行随机分组。174例患者中,男121例,女53例;年龄29~72岁,中位年龄55岁;肺部转移95例,肝转移83例,骨转移69例,其他部位22例(患者可无远处转移,或者单发转移,或者多发转移);循环肿瘤细胞阳性125例,阴性49例。该研究已经伦理学委员会批准,患者知情同意并签署知情同意书。
1.2 治疗方法 试验组采用吉西他滨联合顺铂的GP方案,对照组采用顺铂联合5-氟尿嘧啶的PF方案。
试验组GP方案:吉西他滨[生产厂家:齐鲁制药(海南)有限公司,批准文号:国药准字H20113286,规格:1.0 g/瓶]在化疗第1天和第8天静脉注射(30 min内滴完),剂量为1 000 mg/m2,顺铂(生产厂家:齐鲁制药有限公司,批准文号:国药准字H20023461,规格:20 mg/支)在化疗第1天静脉注射(约3 h),剂量为80 mg/m2。对照组PF方案:顺铂在化疗第1天静脉注射(约3 h),剂量为80 mg/m2,完成以后行静脉5-氟尿嘧啶(生产厂家:上海旭东海普药业有限公司,批准文号:国药准字H31020593,规格:10 mL︰0.25 g/支)持续滴注,持续96 h,剂量为4 000 mg/m2。以上治疗药物原则上按全量给药,但根据患者实际情况可允许总量10%的浮动。治疗持续最少4个疗程,最多6个疗程,每疗程21 d。非疾病进展,或出现不可耐受的毒副作用,一般不考虑停药。
1.3 观察指标与评定标准 (1)该研究的疗效评价标准采用WHO制定的实体瘤疗效评价标准,根据患者的体格检查和治疗后的影像学资料,将疗效分为完全缓解(CR)、部分缓解(PR),稳定(SD)及进展(PD),臨床总有效(RR)=CR+PR。同时,本研究还测定了上述患者化疗前后循环肿瘤细胞的变化,以深入研究鼻咽癌患者的疾病进展程度,探索更为直观地反映两种化疗方案临床疗效的方法。以上评价会在每2个疗程进行一次,如果患者达到CR或者PR则需在4个疗程后进行确认。(2)不良反应按照WHO抗癌药物急性及亚急性毒性反应分度标准为依据,重点监测血象、胃肠道生化指标及肾功能,根据实验室检查结果分为0~Ⅳ级。治疗开始后,每3个月对患者进行生存状态的随访,直至患者参加研究的12个月后或者死亡(不分先后顺序)。
1.4 统计学处理 采用SPSS 19.0软件对所得数据进行统计分析,计数资料以率(%)表示,等级资料进行秩和检验处理,生存分析采用Kaplan-Meier法,生存差异采用Log-Rank检验,进行多因素Cox分析。以P<0.05为差异有统计学意义。
2 结果
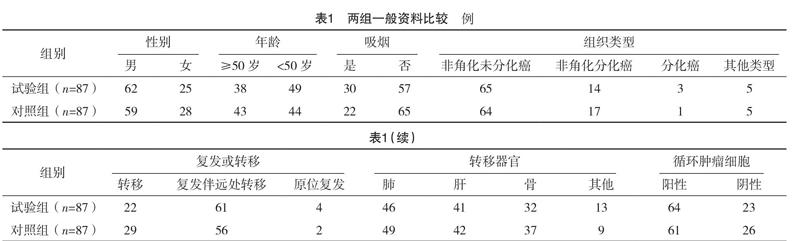
2.1 两组一般资料比较 两组性别、年龄、吸烟与否、组织类型、复发或转移情况、转移器官、循环肿瘤细胞状态等一般资料比较,差异均无统计学意义(P>0.05),见表1。
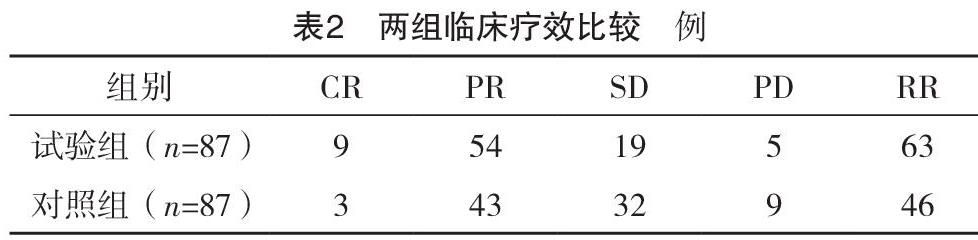
2.2 两组临床疗效比较 试验组临床总有效率为72.4%,对照组为52.9%,试验组临床总有效率明显高于对照组(字2=7.098,P=0.008),见表2。化疗开始前,125例(71.8%)患者循环肿瘤细胞呈阳性,化疗过程中循环肿瘤细胞阳性率逐步下降,至患者完成规定周期的化疗后,仅21例(12.1%)患者呈阳性,化疗前后比较差异有统计学意义(P<0.001)。其中CR阳性0例,PR阳性2例,SD阳性6例,PD阳性13例。
2.3 两组不良反应比较 两组均未出现严重不良反应,以至于停止化疗。对照组恶心呕吐、口腔黏膜反应等发生率明显高于试验组(P<0.05),而试验组化疗后血小板抑制情况比对照组严重(P<0.05),两组肝肾功能指标比较差异无统计学意义(P>0.05),见表3。
2.4 两组预后比较 根据随访情况,对两组患者进行了生存分析,结果显示试验组的无病生存和总生存均优于对照组,差异均有统计学意义(P=0.027、0.006<0.05),见图1。进一步采用Cox多因素回归分析,结果显示转移、化疗后循环肿瘤细胞状态及化疗方法是晚期鼻咽癌患者的独立预后因子,见表4。
3 讨论
鼻咽癌是头颈部常见的恶性肿瘤,以我国南方最为高发,欧美罕见。早期患者的5年生存率可达80%以上,而发生转移或复发的中晚期鼻咽癌的5年生存率仅30%左右,因此中晚期鼻咽癌的合理治疗对改善患者的预后尤为关键。复发或转移性鼻咽癌对化疗敏感,但其持续有效时间较短,预后较差[4]。5-氟尿嘧啶联合顺铂是国内外常用的化疗方案,但此方案反应率为40%~65%,反应时间较短,胃肠副作用较大,一部分患者不能耐受。吉西他滨作为一种广谱抗实体肿瘤的核苷类药物,临床效果好,已成为目前抗肿瘤一线药物。Zhang等[8]在一项2期临床试验中使用吉西他滨单药治疗鼻咽癌,结果显示总有效率为43.8%,一年生存率为67.0%,由此可见吉西他滨抗鼻咽癌的效果值得肯定。近年来,也有一批临床试验采用吉西他滨联合其他药物协同治疗鼻咽癌。其中,Wang等[6]在一项早期的临床试验中就曾用吉西他滨联合顺铂治疗鼻咽癌,获得的总有效率为42.7%,1年生存率为67.0%。Chan等[9]利用吉西他滨联合奥沙利铂治疗鼻咽癌的总有效率52.0%,一年生存率33.9%。Chen等[10]用吉西他滨联合长春瑞滨治疗铂类药物抵抗的晚期鼻咽癌患者,亦获得了37.7%的总有效率,5.2个月的无进展生存时间。以上研究均表明吉西他滨单药或者联合用药治疗鼻咽癌均具有较好的疗效。
本研究采用GP方案治疗复发或者转移的晚期鼻咽癌,结果显示总有效率为72.4%,中位无进展生存时間为10.3个月,优于PF方案。化疗毒副作用方面,两组均未出现严重的不良事件,总体来说可以耐受完成规定疗程的化疗,对照组恶心呕吐、口腔黏膜反应等发生率均明显高于试验组(P<0.05)。此外,两组骨髓抑制发生率相近,约为50%。生存分析结果显示,试验组的无病生存和总生存均优于对照组(P<0.05),Cox多因素分析显示肿瘤转移情况和化疗方案(GP方案)可作为无病生存和总生存的独立预后因素。
本研究还将循环肿瘤细胞作为一个独立的观察指标。循环肿瘤细胞常被用于评价肿瘤患者复发转移及预后分析[11-16],目前常用的方法有细胞计数法和核算检测法[17-22]。本研究采用的细胞计数法,化疗开始前,125例(71.8%)患者循环肿瘤细胞呈阳性,化疗过程中循环肿瘤细胞阳性率逐步下降,至患者完成规定周期的化疗后,仅21例(12.1%)患者呈阳性,化疗前后比较差异有统计学意义(P<0.05)。Cox多因素分析显示循环肿瘤细胞还可以作为无病生存和总生存的独立预后因素。因此,在临床应用中可以作为化疗效果和预后的一个指导参数。
综上所述,吉西他滨联合顺铂治疗复发或转移的晚期鼻咽癌疗效较好,患者副反应较小,能够耐受,临床应用可使患者获益。此外,循环肿瘤细胞检测可作为评估化疗效果和预后的有效指标。
参考文献
[1] Ferlay J,Soerjomataram I,Dikshit R,et al.Cancer incidence and mortality worldwide:sources,methods and major patterns in GLOBOCAN 2012[J].Int J Cancer,2015,136(5):E359-386.
[2] Blanchard P,Lee A,Marguet S,et al.Chemotherapy and radiotherapy in nasopharyngeal carcinoma:an update of the MAC-NPC meta-analysis[J].Lancet Oncol,2015,16(6):645-655.
[3] Tang L Q,Chen Q Y,Fan W,et al.Prospecti ve study of tailoring whole-body dual-modality fluorodeoxyglucose positron emission tomography/computed tomography with plasma Epstein-Barr virus DNA for detecting distant metastasis in endemic nasopharyngeal carcinoma at initial staging[J].J Clin Oncol,2013,31(23):2861-2869.
[4] Jin Y,Shi Y X,Cai X Y,et al.Comparison of five cisplatin-based regimens frequently used as the first-line protocols in metastatic nasopharyngeal carcinoma[J].J Cancer Res Clin Oncol,2012,138(10):1717-1725.
[5] Ma B B,Tannock I F,Pond G R,et al.Chemotherapy with gemcitabine-containing regimens for locally recurrent or metastatic nasopharyngeal carcinoma[J].Cancer,2002,95(12):2516-2523.
[6] Wang J,Li J,Hong X,et al.Retrospective case series of gemcitabine plus cisplatin in the treatment of recurrent and metastatic nasopharyngeal carcinoma[J].Oral Oncol,2008,44(5):464-470.
[7] Ngan R K,Yiu H H,Lau W H,et al.Combination gemcitabine and cisplatin chemotherapy for metastatic or recurrent nasopharyngeal carcinoma:report of a phase Ⅱ study[J].Ann Oncol,2002,13(8):1252-1258.
[8] Zhang L,Zhang Y,Huang P Y,et al.PhaseⅡclinical study of gemcitabine in the treatment of patients with ad-vanced nasopharyngeal carcinoma after the failure of platinum-based chemotherapy[J].Cancer Chemother Phar-macol,2008,61(1):33-38.
[9] Chan A T,Ma B,Tung S,et al.Biweekly gemcitabine and oxaliplatin(GEMOX)in first-line metastatic or recurrent nasopharyngeal carcinoma(NPC)-an early report[J].J Clin Oncol,2007,25(18):6071-6074.
[10] Chen C,Wang F H,Wang Z Q,et al.Salvage gemcitabine vinorelbine chemotherapy in patients with metastatic nasopharyngeal carcinoma pretreated with platinum-based chemotherapy[J].Oral Oncol,2012,48(11):1146-1151.
[11] Joosse S A,Gorges T M,Pantel K.Biology,detection,and clinical implications of circulating tumor cells[J].EMBO Mol Med,2014,7(1):1-11.
[12] Masuda T,Hayashi N,Iguchi T,et al.Clinical and biological significance of circulating tumor cells in cancer[J].Mol Oncol,2016,10(3):408-417.
[13] Ferreira M M,Ramani V C,Jeffrey S S.Circulating tumor cell technologies[J].Mol Oncol,2016,10(3):374-394.
[14] Song Y J,Ji L,Yang L.Advances in techniques for Detecting circulating tumor cells[J].Chin J Clin Oncol,2012,39(22):1859-1863
[15]董苗苗,王芳,孫国平.吉西他滨联合顺铂与氟尿嘧啶联合顺铂方案治疗晚期鼻咽癌疗效和不良反应的Meta分析[J].安徽医药,2017,21(7):1325-1330.
[16]王帆,易军.吉西他滨联合顺铂治疗远处转移性鼻咽癌的效果观察[J].中国当代医药,2016,23(30):72-74.
[17]袁晔.吉西他滨联合顺铂同期放化疗治疗中晚期鼻咽癌疗效观察[J].现代中西医结合杂志,2015,24(36):4081-4082.
[18]饶胜.细胞因子诱导杀伤细胞回输联合吉西他滨和顺铂治疗鼻咽癌放疗后肝肺转移瘤的效果及机制分析[J].吉林医学,2015,36(5):834-835.
[19]纪荣佳,管凯,庄建发,等.吉西他滨联合奈达铂化疗后序贯行姑息性放疗治疗复发性鼻咽癌的疗效及不良反应分析[J].医学综述,2017,23(11):2285-2288.
[20]胡少轩,何小慧,董梅,等.吉西他滨联合异环磷酰胺对铂类方案化疗失败的晚期鼻咽癌患者的疗效及安全性评价[J].中华肿瘤杂志,2015,37(8):632-636.
[21]高天生,范小玲,李庚,等.吉西他滨联合奈达铂化疗后序贯行姑息性放疗治疗复发性鼻咽癌的临床疗效分析[J].临床合理用药杂志,2015,8(24):38-40.
[22]张华,梁剑苗,冯卫能,等.吉西他滨联合奥沙利铂治疗复发性鼻咽癌的疗效[J].中国肿瘤临床与康复,2015,22(10):1203-1205.
(收稿日期:2018-10-26) (本文编辑:程旭然)

