高效液相色谱法检测三氯蔗糖的方法比较
李 桑 陈星蓉 汪玉玲 廖素溪
(广东省食品检验所 广东广州 510435)
1 前言
随着社会经济不断发展,人民生活水平在不断提高,对吃的需求不仅限于温饱,对食品的质量要求也越来越高。随着食品行业迅猛发展,作为最受欢迎的饮料已经成为了其中的佼佼者,甜味剂也应运而生。甜味剂种类较多,按其来源可分为天然甜味剂和人工合成甜味剂。天然甜味剂有甜菊糖、甘草、甘草酸二钠、甘草酸三钾和甘草酸三钠等;人工合成甜味剂有糖精、糖精钠、环己基氨基磺酸钠、天门冬酰苯丙氨酸甲酯、阿力甜等。葡萄糖、果糖、蔗糖、麦芽糖、淀粉糖和乳糖等糖类物质,虽然也是天然甜味剂,但因长期被人食用,且是重要的营养素,通常视为食品原料,在我国不作为食品添加剂。
三氯蔗糖又名三氯半乳蔗糖[1]、蔗糖素、4,1,6-三氯-4,1,6,-三脱氧半乳型蔗糖,是一种白色或近白色结晶性粉末的蔗糖衍生物,其甜度约为蔗糖的600 倍,口味纯正,没有任何异味或苦涩味,甜味特征曲线几乎与蔗糖重叠,具有很好的溶解性和稳定性,又兼具低热量、高甜度的特点。相比高热量、低甜度的食品添加剂[2]——食糖,三氯蔗糖越来越普遍用于饮料中,被认为是当今最理想的甜味剂。但三氯蔗糖对人体健康也可能产生一些危害[3],所以我国对三氯蔗糖的添加有一定的限量[4]。
食品中三氯蔗糖测定方法包括离子色谱法[5-7]、高效液相色谱法[8-14]、气相色谱-质谱法(GC-MS)[15]、液相色谱法(LC-MS)[16]、红外光谱法[17]等。各种方法有各自特点,精度和准度也存在一定差别,依据具体的实际条件和要求可选择不同的三氯蔗糖的测定方法,目前以高效液相色谱法为主。经大量实际实验发现,现有的食品安全国家标准GB 22255—2014《食品中三氯蔗糖(蔗糖素)的测定》[18]中对于饮料中的三氯蔗糖的测定,具有检测过程长、灵敏度低、实验试剂毒副作用大等缺点。实验试剂的毒副作用尤其需要注意,对其使用、回收及处理等都需要严格的要求。对于如何降低或消除实验试剂的毒副作用,一直是科研工作者的研究热点。同时,随着人们环保意识的提高,亟待开发出更为绿色环保的检测技术。孙晓娟等比较了蒸发光散色检测器和示差检测器在检测中的应用[19]。有关高效液相色谱法检测三氯蔗糖的方法中,毒副作用试剂的替代还未见报道。
本研究对GB 22255—2014 规定的食品中三氯蔗糖(蔗糖素)的测定方法进行了改进,使用了不同类型的色谱柱进行检测,对仪器分析条件进行了优化,通过比较不同色谱柱的检测条件,提供了更为绿色环保的检测方法。
2 材料与方法
2.1 仪器与试剂
岛津高效液相色谱仪(配RID-20A 示差折光检测器,岛津企业管理(中国)有限公司);MS 105DU分析天平(瑞士 METTLER TOLEDO 公司);KQ-500B型超声波清洗器(昆山市超声仪器有限公司);AutoEVA-60 氮吹仪(美国 Reeko 公司)。
Oasis HLB 固相萃取柱(美国 Waters 公司)(200 mg,类型为N-乙烯基吡咯烷酮和二乙烯苯亲水亲脂平衡型填料),使用前依次用4 mL 甲醇、4 mL水活化;0.45 μm 滤膜(美国 Agilent Technologies 公司)。
三氯蔗糖标准品(纯度为98.8%,北京曼哈格生物科技有限公司);乙腈、甲醇(色谱纯,德国默克股份两合公司);甲醇、磷酸氢二钾(分析纯,广州化学试剂厂)。
2.2 实验方法
2.2.1 色谱条件
国标方法:C18 反相色谱柱(4.6mm×150mm,5μm,日本GL Sciences 公司);柱温:35℃;检测池温度:35℃;进样量:20 μL;流速:1.0 mL/min,流动相:乙腈:水=89∶11(V:V)。
方法一:C18 反相色谱柱(4.6 mm×150 mm,5 μm,日本GL Sciences 公司);柱温:35℃;检测池温度:35℃;进样量:20 μL;流速:0.8 mL/min,流动相:甲醇:0.125%磷酸氢二钾=40:60(V:V)。
方法二:Hi-Plex H 色谱柱(300 mm×7.7 mm,美国安捷伦科技有限公司);柱温:65℃;检测池温度:35℃;进样量:20 μL;流速:0.8 mL/min,流动相:超纯水。
2.2.2 标准溶液配制
标准储备液:精确称取三氯蔗糖标准品0.100 g于10 mL 容量瓶中,用超纯水溶解完全后,定容至刻度,浓度约为10 mg/mL,放入2~8℃箱中储存备用,保质期6 个月。
2.2.3 标准工作曲线绘制
分别精确移取三氯蔗糖标准储备液稀释成以下浓度:20 mg/L、50 mg/L、100 mg/L、200 mg/L、400 mg/L,进样量为 20 μL。以浓度(X,mg/L)为横坐标,峰面积(Y,mV·min)为纵坐标,绘制标准工作曲线。
2.2.4 样品前处理方法
精确称取5 g(精确到0.001 g)试样,置于25 mL塑料离心管中,加入5 mL 超纯水稀释,涡旋混合器上震荡 30 min,以 3 000 r/min 离心 10 min。取全部上清液移入预先活化的固相萃取柱,控制液体流速为1 滴/s,柱上液面为2 mm 左右时,加入1 mL 的超纯水,继续保持液体流速不超过1 滴/s,至柱中液体完全排出后,用3 mL 甲醇洗脱,收集甲醇洗脱液。将洗脱液置于氮吹仪中吹干,残渣用1.00 mL 流动相溶解,溶液过0.45 μm 滤膜,滤液为制备的试样溶液,备用。
3 结果与分析
3.1 色谱条件的比对
在之前的预实验中,已经优化了C18 反相色谱柱的实验条件,验证了方法一的实验不仅能够达到国家标准要求,且更为省时、节约试剂[20]。
本次实验主要对比不同色谱柱条件下的实验结果。检测色谱图详见图1,阳性样品回收率实验结果详见表1,阴性样品回收率实验结果详见表2。
由图1(a)、(b)可以看出,方法一与方法二在三氯蔗糖标准溶液浓度为20 mg/L 时均有良好的响应值,且方法一的出峰时间较快。
通过t 检验两种方法得出的阳性样品浓度差异无统计学意义(P>0.05)。根据表1可以看出,两种方法在样品的加标回收率均在95%以上,具有良好的回收率。
在阴性样品中加入浓度2.5 g/kg 的三氯蔗糖标准溶液,根据表2可以看出,两种方法在样品的加标回收率均在95%以上,具有良好的回收率。
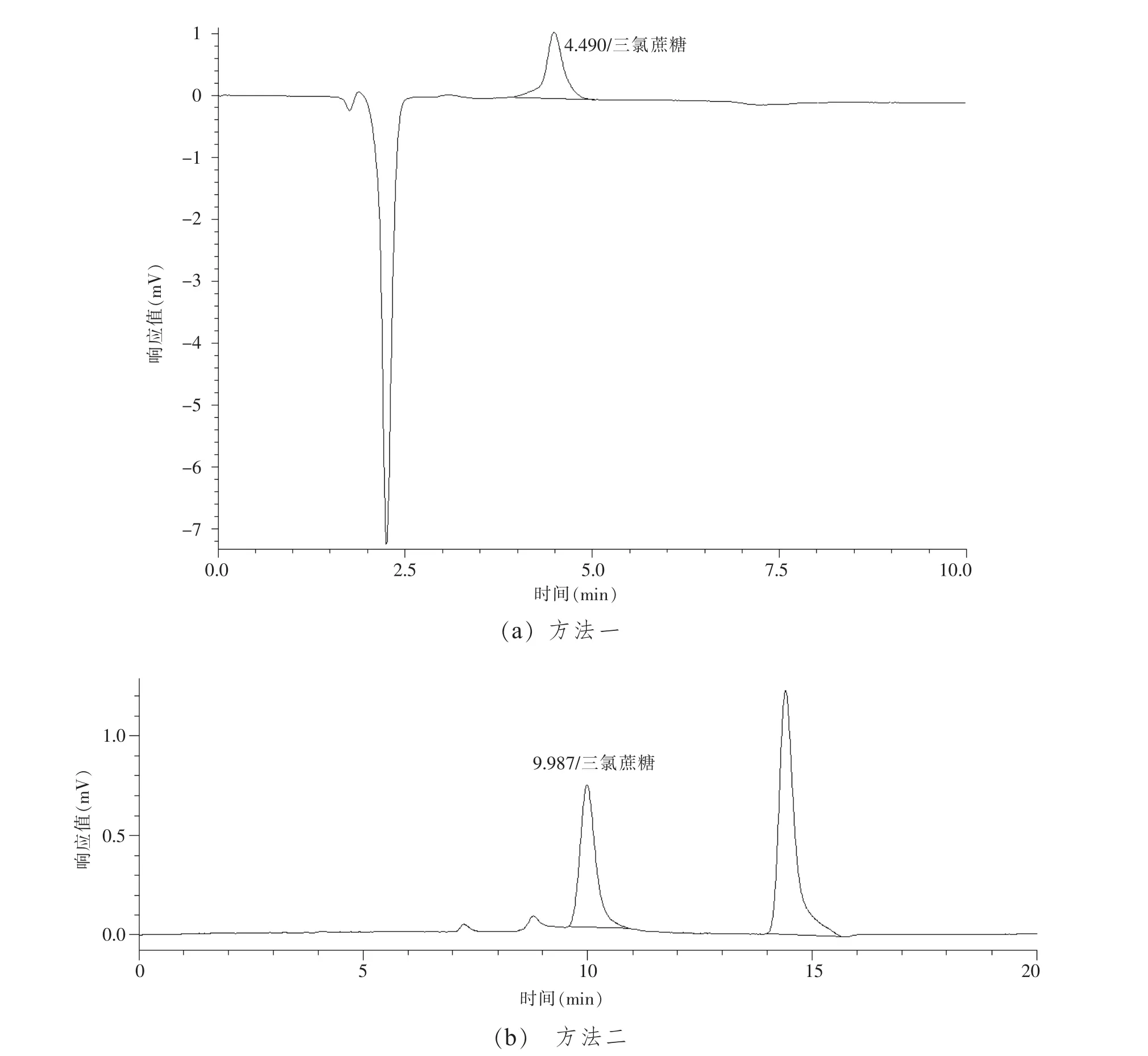
图1 三氯蔗糖标品色谱图

表1 饮料(阳性样品)中三氯蔗糖加标回收率试验(n=4)

表2 饮料(阴性样品)中三氯蔗糖加标回收率试验(n=4)
3.2 检出限及定量限
三氯蔗糖加标浓度为2.5 mg/L 的阴性样品,称样量为5 g、进样量为20 μL 时,方法一的检出限为0.000 5 g/kg,方法二的检出限为0.000 5 g/kg,均低于国标方法中的检出限0.002 5 g/kg,可以满足测定的需要。
3.3 精密度试验
对同一含量样品进行6 次测定,方法一与方法二的相对标准偏差RSD 分别为0.2%、0.1%。
如图2所示,三氯蔗糖的浓度与峰面积呈良好的线性关系,浓度(X,mg/L)为横坐标,峰面积(Y,mV·min)为纵坐标,方法一的回归方程为Y=930.3X+201.1,相关系数为 0.999 9,线性范围 20~400 mg/L;方法二的回归方程为Y=906.4X-727.0,相关系数为1,线性范围 20~400 mg/L。
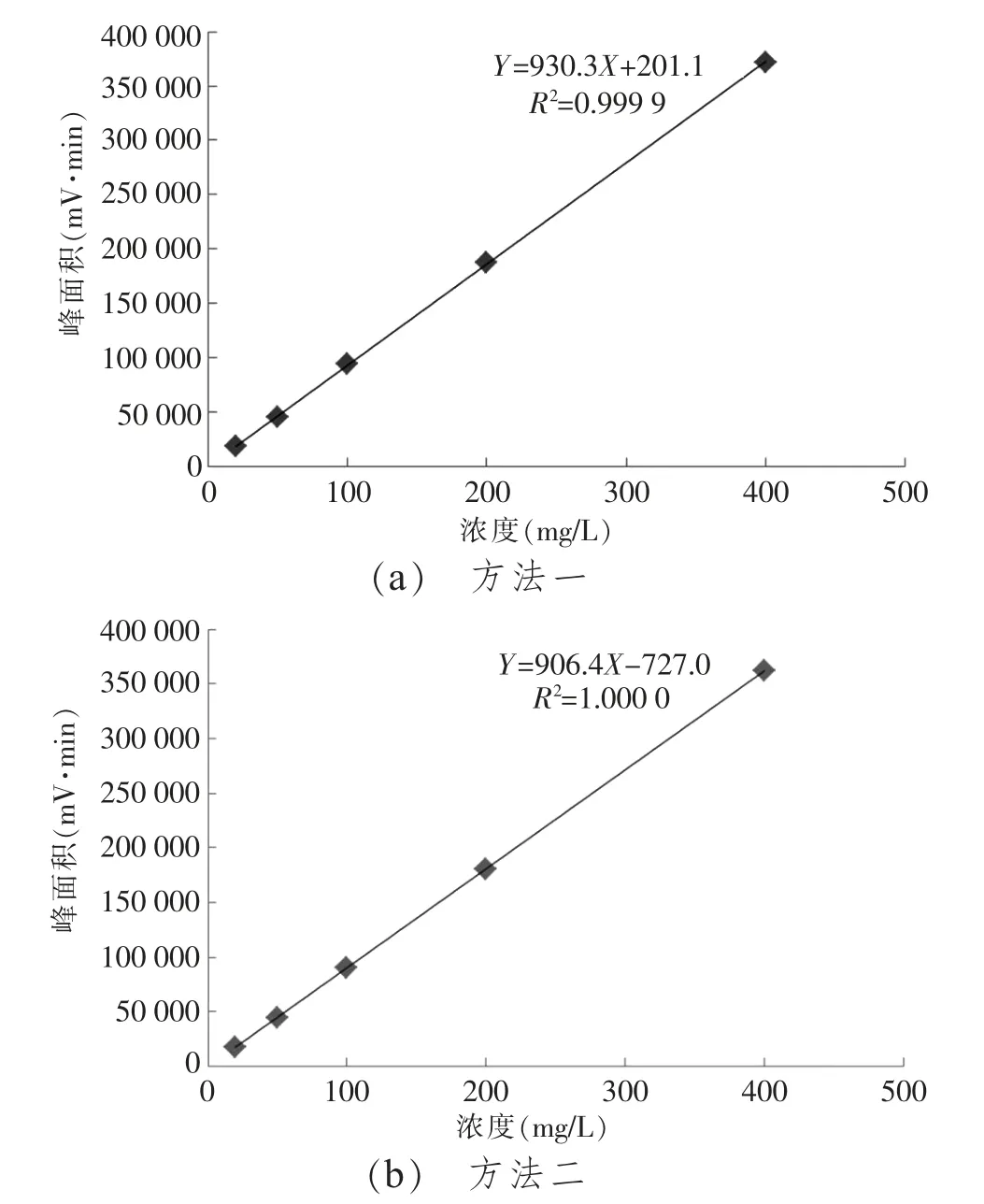
图2 线性试验结果图
4 结论
本研究中采用的两种非国标方法检测饮料中的三氯蔗糖,操作稳定,在精密度、准确度、检出限等方面都能完全满足日常分析的需要,与国家检测标准及一些学者[21,22]的研究结果相比,加快了分析速度,提高了灵敏度。方法一用甲醇代替乙腈,毒性和成本都有所降低;加入了盐,稳定性得到了提高,加快了检测器的平衡,节约了流动相的使用,检测效率提高,与甘宾宾等的研究结果一致,适合日常大量的饮料样品检测工作;与陈晓霞等[23]的研究相比,降低了柱温与检测温度,降低了对色谱柱的损耗,延长了色谱柱的使用寿命。方法二使用了与王桂华等研究中同样的水性色谱柱,使用超纯水作为流动相较易配制,但出峰时间较晚,较为浪费试剂。从有益于环保的角度出发,使用水柱的废液相较于有机相废液更易处理,且节约了金钱成本。读者可以就自己的实际情况选择适合自己的方法进行试验。
往后的工作,可以继续深究两种方法是否能够运用到其他类型样品的检测,也可以继续优化前处理方法,减少整个实验周期的时间,提高检测效率。

