GST pull-down联合LC-MS/MS筛选柑橘抗溃疡病转录因子CsBZIP40的互作蛋白
窦万福,祁静静,胡安华,陈善春,彭爱红,许兰珍,雷天刚,姚利晓,何永睿,李强
GST pull-down联合LC-MS/MS筛选柑橘抗溃疡病转录因子CsBZIP40的互作蛋白
窦万福,祁静静,胡安华,陈善春,彭爱红,许兰珍,雷天刚,姚利晓,何永睿,李强
(西南大学/中国农业科学院柑桔研究所,重庆 400712)
CsBZIP40是一个与溃疡病抗性相关的转录因子,本研究旨在筛选转录因子CsBZIP40在响应柑橘溃疡病菌(subsp.,)侵染过程中的互作蛋白,对CsBZIP40的互作网络进行分析,为柑橘抗溃疡病的分子育种提供理论依据。采用GST pull-down技术筛选柑橘在溃疡病菌侵染过程中CsBZIP40的互作蛋白。首先,构建带有GST标签的CsBZIP40蛋白融合表达载体,经IPTG(异丙基硫代半乳糖苷)诱导表达、纯化后获得GST-CsBZIP40融合蛋白作为诱饵蛋白;然后,将GST-CsBZIP40融合蛋白固定在谷胱甘肽亲和磁珠上,用固定在亲和磁珠的GST-CsBZIP40诱饵蛋白与接种溃疡病菌或LB培养基后柑橘叶片总蛋白进行孵育,与GST-CsBZIP40诱饵蛋白结合的蛋白复合物洗脱收集后进行SDS-PAGE凝胶电泳验证。将验证成功的样品洗脱液进行液相色谱串联质谱(LC-MS/MS)检测,鉴定出未侵染和侵染状态下CsBZIP40的互作蛋白,将检测到的蛋白利用甜橙基因组数据库进行注释,筛选出在溃疡病菌侵染过程中与CsBZIP40特异结合的蛋白,并进行GO、KEGG和互作网络分析。过表达的转基因植株表型正常,与对照植株无明显差异。过表达的转基因植株溃疡病抗性评价中病斑面积、病情指数均显著小于野生型植株,分别为野生型的45%和54%。以该转基因植株为材料成功提取出侵染溃疡病菌后和未接种溃疡病菌状态下的柑橘叶片总蛋白。成功构建出GST-CsBZIP40诱饵蛋白表达载体,诱导表达纯化出GST-BZIP40诱饵蛋白。利用GST-CsBZIP40诱饵蛋白从侵染溃疡病菌后柑橘总蛋白和未接菌柑橘总蛋白中成功钓取蛋白,并用LC-MS/MS检测。经过比对、注释和筛选,在柑橘溃疡病菌侵染过程中与GST-BZIP40特异结合的蛋白有53个,这些蛋白参与多个分子功能和通路。在这53个蛋白中,有6个蛋白(Cs1g02310、Cs3g05280、Cs3g23950、Cs6g13880、Cs7g12130、orange1.1t04973)可能与植物抗病性密切相关。数据库中已经证明53个蛋白中44个与CsBZIP40有直接或间接的互作关系。溃疡病菌侵染过程中有53个蛋白与CsBZIP40互作,根据注释6个蛋白与植物抗病性密切相关,这些蛋白可能在提高柑橘生物胁迫抗逆性方面发挥着重要的作用。
柑橘;柑橘溃疡病;柑橘溃疡病菌;BZIP;GST pull-down;互作蛋白
0 引言
【研究意义】柑橘产业在中国具有重要的经济地位,而病害严重影响着柑橘产业的健康发展。柑橘溃疡病(citrus bacterial canker,CBC)是主要的病害之一,它是一种由柑橘黄单胞杆菌柑橘亚种(subsp.,)所引起的检疫性细菌病害[1]。传统的防治方法具有环境污染、毁园、效果差、成本高等弊端,且无法根治[2]。培育优良抗性品种是解决柑橘溃疡病危害的有效途径,而通过分子育种方法培育抗性品种是控制柑橘溃疡病最为经济、有效、环保的方法。挖掘有潜力的候选基因是分子育种的重要基础,CsBZIP40是一个与溃疡病抗性相关的转录因子[3],可通过与具有转录激活作用的结构域相互作用调控下游相关基因的表达[4]。对CsBZIP40调控机理的研究首先需要明确该转录因子是否与其他蛋白互作共同发挥功能,因此,筛选CsBZIP40响应柑橘溃疡病菌侵染过程中的互作蛋白很有必要。【前人研究进展】大部分的转录因子无法单独调控基因的表达,一般情况下,几个转录因子同时直接或间接地与顺式作用元件结合,才能调控下游基因的表达[5]。转录因子间形成多聚体或与其他蛋白质因子形成调控复合因子时首先是转录因子的聚集,由一个转录因子招募与其共同作用的转录因子,然后结合通用转录因子和RNA聚合酶形成启动子复合物,开启基因的转录。一个转录因子是否能够促进基因的转录,必须有相关蛋白同时出现,而且这个转录因子必须处于能够与其他转录因子结合的状态[5],一些基因在调控网络中参与多条途径。转录因子在植物抵抗病原菌的反应中起重要作用[6-7],比如会通过识别不同的顺式作用元件,影响多种基因的表达,响应生物胁迫[8-9]。BZIP蛋白在抵抗病害、调节植物抗性应答方面发挥着重要的作用,过表达和的转基因植株可以提高对木薯枯萎病的抗性[10],干扰表达水稻中的BZIP转录因子TGA2.1使水稻对稻瘟病抗性明显增强[11]。GST pull-down是一种体外筛选与已知蛋白相互作用的未知蛋白的经典技术[12-13],广泛应用于互作蛋白的研究中。Akiyama等[14]将稻瘟病抗性相关的碱性几丁质酶基因RC24和苜蓿-1,3-葡萄糖酶基因-1,3-Glu同时导入水稻中,利用GST pull-down技术从水稻中分离出一个抗稻瘟病蛋白的互作蛋白;赵文等[15]应用GST pull-down技术对抗病蛋白PID2的早期响应蛋白进行了探索,得到31个蛋白在感病状态下特异结合;林生等[16]使用GST pull-down技术钓取出侵染下SoSGT1的7个响应蛋白。【本研究切入点】CsBZIP40为笔者实验室验证的与柑橘抗溃疡病相关的转录因子,为了研究其生物学功能,构建了过表达载体并转化柑橘获得了转基因植株,可作为研究CsBZIP40的功能和柑橘溃疡病菌侵染过程中CsBZIP40的互作蛋白和分子机理的试验材料。但CsBZIP40在柑橘体内发挥作用的分子机理尚不清晰。【拟解决的关键问题】通过对溃疡病菌侵染过程中CsBZIP40互作蛋白的挖掘,从蛋白质层面探明CsBZIP40在调控柑橘对溃疡病抗性过程中发挥功能的关键因子,为进一步研究CsBZIP40的调控网络和分子机理打下基础,并为抗溃疡病分子育种提供参考依据。
1 材料与方法
试验于2018年在西南大学/中国农业科学院柑桔研究所完成。
1.1 材料与试剂
试验植物材料为过表达的晚锦橙植株叶片。供试溃疡病菌是西南大学柑桔研究所保存的亚洲种A株系。植物总RNA提取、胶回收、反转录和质粒提取采用AIDLAB公司的相关试剂盒;实时荧光定量PCR(real-time fluorescent quantitative PCR,qRT-PCR)使用BIORAD公司的荧光染料;T-A克隆试剂和pGEMT easy载体购自TaKaRa公司;PGEX-4T-1载体、克隆菌株Top10和BL21(DE3)原核表达菌株购于南京德泰生物。
1.2 CsBZIP40过表达植株柑橘溃疡病抗性评价
使用引物(FCsBZIP40-1:TAACCAAGAAGGACCTG CTTTTGAT,RCsBZIP40-1:CTTTTCTTGTGATGGTTTT GCATCT)鉴定转基因菌株。阳性菌株提取叶片总RNA并反转录,根据基因特异性区域和柑橘内参基因设计定量PCR引物(FCsBZIP40-2:AGTTCCCTTTGGGCATCTCG,RCsBZIP40-2:ACCATT TGCAGATCCGTCGT,Factin:CATCCCTCAGCACCTT CC,Ractin:CCAACCTTAGCACTTCTCC),并用qRT-PCR检测的表达量,相对表达量采用2-ΔΔCt法(ΔCt=CtCsBZIP40-CtActin)计算,使用Excel进行数据统计分析并绘图。于液体LB培养基中培养柑橘溃疡病菌至OD600nm为0.5,菌液进行离心并用LB培养基重悬后分装备用;采集的叶片清洗并用75%的酒精消毒后放入超纯水中冲洗,置于超净台;以叶脉为中心进行针刺,六针为一组,每侧两组;用移液器点样溃疡病菌菌液,每针孔点样1 μL。然后将柑橘叶片的叶柄用浸湿的脱脂棉包裹,石蜡带密封于培养皿,于28℃恒温光照培养箱中培养(16 h光照/8 h黑暗)。对照组用LB代替溃疡病菌菌液,其他操作保持一致。分别在0、1、3、5 d取样。部分叶片点菌后培养10 d拍照,用Image J V1.47软件统计病斑面积(mm2)。按照病斑面积将病情分为0—7共8级,以字母R表示病斑面积,0级(R≤0.25 mm2),1级(0.25 mm2<R≤0.5 mm2),2级(0.5 mm2<R≤0.75 mm2),3级(0.75 mm2<R≤1 mm2),4级(1 mm2<R≤1.25 mm2),5级(1.25 mm2<R≤1.5 mm2),6级(1.5 mm2<R≤1.75 mm2),7级(R>1.75 mm2);根据公式计算病情指数:DI=100×Σ(各级病斑数×相应级数值)/(病斑总数×最大级数)[17]。
1.3 GST-CsBZIP40融合蛋白载体构建、表达与纯化
以锦橙cDNA为模板,上游引物FCsBZIP40-3:ATGGCGAGTCACA GAATTGG(带HI酶切位点),下游引物FCsBZIP40-3:TCA AAAGTTCGAGAAATGAT(带I酶切位点),进行PCR扩增的CDS序列;PCR产物连接T载体后转化大肠杆菌DH5;用HI和I酶切质粒和表达载体PGEX-4T-1,将线性化的载体和基因片段连接并转化大肠杆菌Top10感受态;提取阳性菌株质粒转化到BL21(DE3)中培养至菌液OD值为0.6,加入0.2 mmol∙L-1IPTG诱导,置于15℃摇床诱导表达;全菌采用50 mmol∙L-1Tris,150 mmol∙L-1NaCl(pH 8.0)缓冲液(含1% Triton X-100,1 mmol∙L-1DTT,1 mmol∙L-1PMSF)超声波裂解,同时以50 mmol∙L-1Tris,150 mmol∙L-1NaCl(pH 8.0)缓冲液平衡GST亲和层析磁珠,之后用含40 mmol∙L-1GSH的平衡缓冲液洗脱目标蛋白,并收集洗脱组分进行SDS-PAGE检测;收集纯度浓度相对较高的样品,将其透析到1×PBS(pH 7.8),5% Glycerol中,透析结束后用0.22 μm过滤器过滤,分装并保存于-80℃。采用Bradford法测定蛋白浓度,用R250染色的SDS-PAGE判断纯度。
1.4 柑橘总蛋白提取
取1 g柑橘叶片(分别接种溃疡病菌和LB),充分研磨后加入1 mL裂解液(50 mmol∙L-1Tris-HCl,50 mmol∙L-1NaCl,1 mmol∙L-1EDTA,1% Triston X-100,1 mmol∙L-1DTT,1 mmol∙L-1PMSF,pH 8.0)重悬叶片组织;4℃冰浴30 min,期间每隔5 min混匀一次,利用超声波破碎仪在冰浴中破碎叶片组织(750W,超声6s,间隔1s,超声20次);用高速冷冻离心机(12 000r/min)离心20min,取上清。取50 μL上清加50 μL 2×点样缓冲液沸水浴5min,12 000r/min离心2min,取上清进行SDS-PAGE。
1.5 GST pull-down反应
(1)取3个EP管标号为①、②、③,分别加入100 μL GST-磁珠到①、②、③管中,用1 mL PBS润洗3次。将150 μg的GST-CsBZIP40诱饵蛋白(标号6)加入到①号管中,150 μg GST标签蛋白(标号1)加入到②号管中,③号管中不做处理,将①、②、③号管中分别加入PBS补至600 μL并混合均匀,4℃层析柜孵育结合2 h;(2)将①、②号管离心后分别用PBS+1% Triton X-100洗3次,再用PBS洗3次,两个管中分别取出50 μL GST-CsBZIP40诱饵蛋白和GST-磁珠的混合物(标号2)、GST标签蛋白与GST-磁珠的混合物(标号7)进行SDS-PAGE验证;(3)分别向上述①、②、③号管剩余的GST-磁珠中同时加入150 μg的溃疡病菌侵染后柑橘叶片总蛋白(标号11),并用PBS补足液体到600 μL左右,以便蛋白之间能充分结合,4℃层析柜孵育结合2 h,离心后收集流出液体进行SDS-PAGE验证(①、②、③号管流出液体收集后标号8、3、12);(4)分别用PBS+1% Triton X-100洗3次,再用PBS洗3次,收集第1次的洗杂液备用,①、②、③号管洗杂液收集标号9、4、13)。然后用BBI(还原型谷胱甘肽GSH)洗磁珠,收集洗脱液进行SDS-PAGE验证(①、②、③号管洗脱液收集后标号10、5、14);(5)将上述标号1-14的液体分别加入50 μl 2×点样缓冲液沸水浴5 min,12 000 r/min离心2 min,取上清采用SDS-PAGE进行检测(泳道与收集标号一致)。未侵染溃疡病菌柑橘GST pull-down试验总蛋白换为未感病柑橘总蛋白即可,其他操作相同。
1.6 LC-MS/MS分析
将样品送至南京德泰生物有限公司进行LC-MS/MS分析,质谱结果用在线软件MaxQuant V1.5检索数据库[18],获取在溃疡病菌侵染过程中与CsBZIP40特异结合的蛋白序列、分子量等信息,进行后续信息学分析。
1.7 生物信息学分析
将溃疡病菌侵染过程中特异表达的蛋白用在线软件OmicsBean(http//www. omicsbean.cn)从分子功能方面进行GO富集分析和KEGG[19]信号通路富集分析。KEGG数据库以文献为基础,表示分子相互作用和反应的网络通路数据,包括比较全面的代谢通路图谱。STRING[20]是一个用来共享已知或预测的蛋白相互作用的数据库,用STRING(https://string-db.org)在线软件进行蛋白互作验证。
2 结果
2.1 过表达植株鉴定与评价
过表达植株表型正常,与对照植株无明显差异(图1-A)。以全基因组DNA为模板进行PCR,在1 000 bp和500 bp有两条植株特征条带出现,分别为扩增自基因组和转入的外源基因,在750 bp有一条模糊条带可能是柑橘基因组中的非特异性扩增结果(图1-B)。qRT-PCR检测发现表达量在转基因植株中表达量相比野生型高出70倍(图1-C)。转基因柑橘叶片接种溃疡病菌10 d后接种LB的叶片无菌斑生成,而接种溃疡病菌的叶片均有溃疡菌斑出现。同野生型相比,过表达植株的柑橘叶片发病轻,表现出一定的抗病性(图1-D)。对病斑面积进行统计显示过表达叶片上的病斑面积小于野生型叶片上的病斑面积,仅为野生型的45%(图1-E)。病情指数结果显示,转基因的病情指数植株明显低于野生型叶片上的病情指数,仅为野生型的54%(图1-F)。上述结果表明过表达的柑橘对溃疡病具有较高的抗性。
2.2 GST-CsBZIP40诱饵蛋白载体构建、表达与纯化
PCR扩增的编码序列(图2-A),用HⅠ和Ⅰ酶切的编码序列和PGEX-4T-1表达载体,酶切产物连接获得融合表达载体PGEX-CsBZIP40(图2-B)。双酶切验证表达载体确认目的片段插入无误(图2-C)。重组表达载体转化大肠杆菌Top10菌株,培养并提取质粒后转化BL21(DE3)表达菌株,IPTG诱导表达GST-CsBZIP40诱饵蛋白,结果表明在0.2 mmol·L-1IPTG诱导和15℃培养条件下上清液中的GST-CsBZIP40蛋白表达比较均一且表达量稳定,融合蛋白分子量82 kD(图3-A)。通过GST琼脂糖凝胶亲和层析纯化GST- CsBZIP40诱饵蛋白(图3-B)。随后对纯化的GST- CsBZIP40诱饵蛋白进行质检,浓度为0.214 mg·mL-1(图3-C),纯度为90%(图3-D)。

A:过表达CsBZIP40转基因植株表型Phenotypes of CsBZIP40 overexpression lines。B:转基因植株系中CsBZIP40的阳性检测The positive detection of CsBZIP40 in transgenic lines;M:marker;1:阳性检测条带Positive detection band。C:过表达CsBZIP40的相对表达量The relative expression of overexpressed CsBZIP40。D:接种溃疡病菌的转基因植株和野生型对照叶片 Disease spots of transgenic lines and the wild-type (WT) inoculated with LB and Xcc。E:接种溃疡病菌的转基因植株和野生型对照病斑面积 Lesion area of transgenic lines and the wild-type inoculated with Xcc;F:接种溃疡病菌的转基因植株和野生型对照病情指数 Disease index of transgenic lines and the wild-type inoculated with Xcc
2.3 GST pull-down
成功提取接种溃疡病菌和未接种溃疡病菌柑橘叶片总蛋白,然后将这两组总蛋白分别与结合在GST-磁珠上的GST-CsBZIP40诱饵蛋白进行孵育,收集流出、洗杂、洗脱液体,上样泳道编号与方法介绍中一致(图4)。SDS-PAGE结果显示GST-CsBZIP40诱饵蛋白能够与GST-磁珠亲和,吸附在GST-磁珠上的融合蛋白能够从柑橘总蛋白中成功钓取蛋白,扣除GST标签蛋非特异性吸附的条带后,仍然有差异条带,说明GST-CsBZIP40蛋白能够从柑橘总蛋白中获得有相互作用的未知蛋白,可以将洗脱样做LC-MS/MS检测,做进一步确认分析。
2.4 LC-MS/MS检测
质谱得到的GST-CsBZIP40的结合蛋白除去GST蛋白对照组鉴定的蛋白后,共鉴定到53个潜在的直接或间接相互作用的蛋白。这53个蛋白在柑橘溃疡病菌侵染过程中与CsBZIP40直接或间接结合。用软件MaxQuant V1.5检索数据库获得蛋白的序列信息。使用甜橙基因组数据库[21]对这些蛋白进行注释,注释出植物广谱抗性相关蛋白(Cs1g02310)、转录因子(Cs3g23950)、抗病蛋白(Cs3g05280)和活性氧代谢相关蛋白(Cs6g13880)等(表1)。这些蛋白可能与CsBZIP40共同起作用以提高柑橘对溃疡病的抗性。其中,NPR蛋白(Cs1g02310)为已经报道过的明确与BZIP40有相互作用的蛋白,证明本试验得到的结果可信[22]。
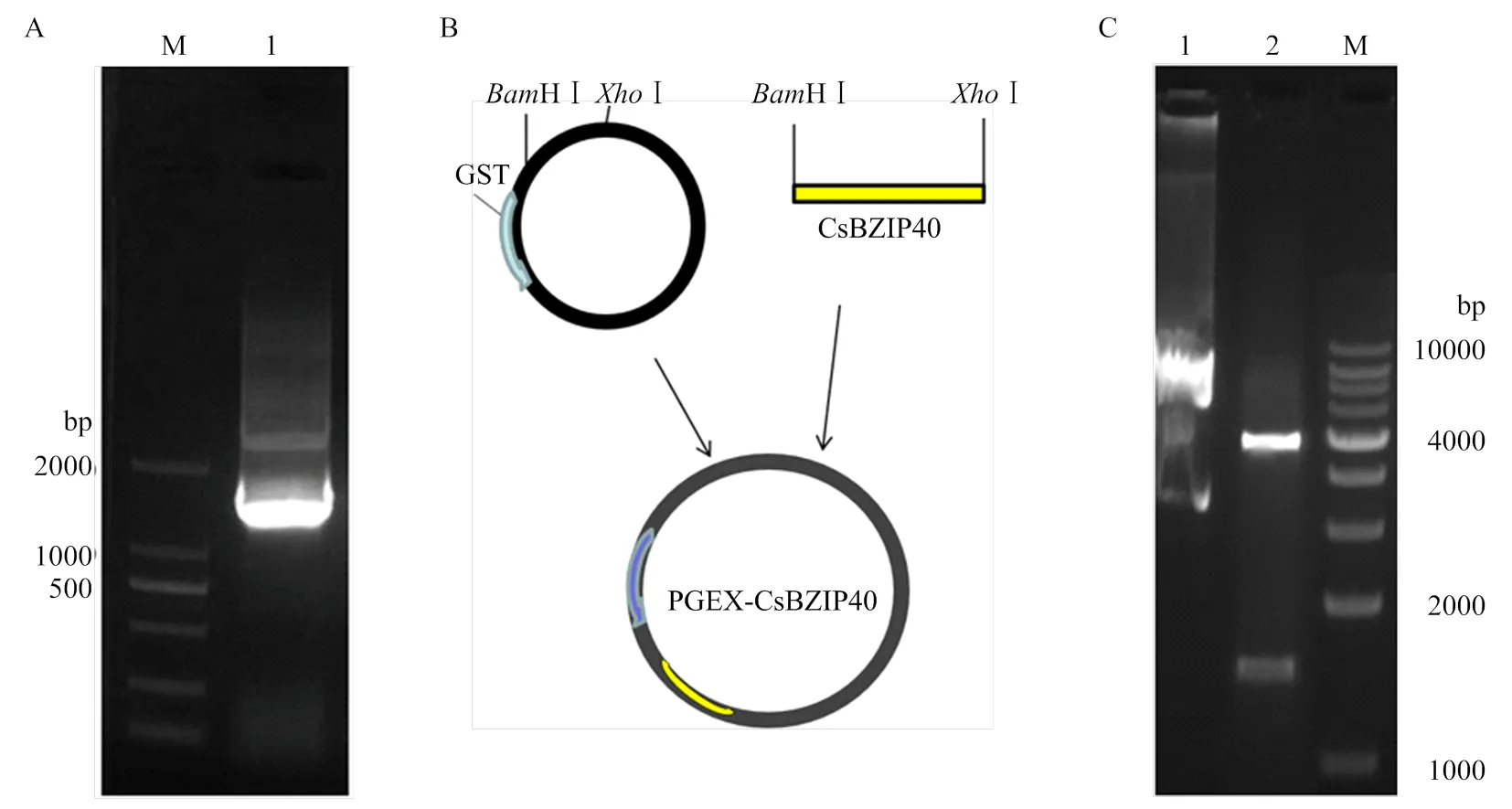
A:CsBZIP40的PCR扩增PCR amplification of CsBZIP40;M:2000 bp分子量标记2000 bp molecular marker;1:扩增产物,约1 530 bp amplified product, about 1 530 bp。B:CsBZIP40-GST融合表达载体的构建Construction of CsBZIP40-GST fusion expression vector。C:融合表达载体的酶切验证Enzymic digestion of CsBZIP40-GST vector;1:完整质粒条带the complete plasmid band;2:CsBZIP40-GST;M:10 000 bp分子量标记10 000 bp molecular marker
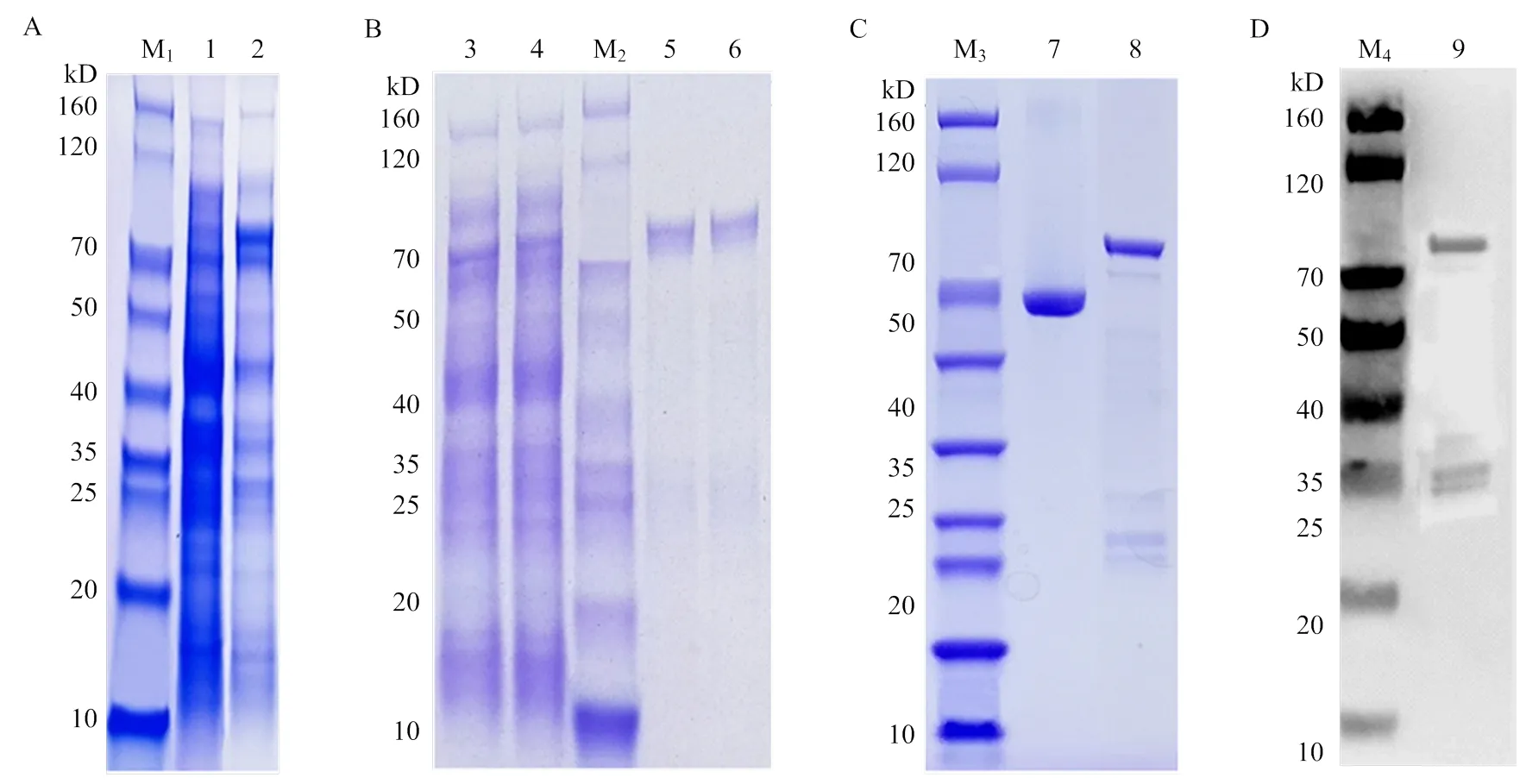
A:GST-CsBZIP40融合蛋白表达 Expression of GST-CsBZIP40;M1:Marker;1:无IPTG诱导表达对照Expression of GST-CsBZIP40 without IPTG;2:15℃加IPTG诱导表达IPTG and 15℃induced expression。B:诱饵蛋白纯化Bait protein purification;3:全菌破碎离心后上清supernatant after centrifugation;4:上清同GST孵育后流出液supernatant after incubation with GST;M2:Marker;5、6:40 mmol∙L-1洗脱GST-CsBZIP40 40 mmol∙L-1 eluent GST-CsBZIP40。C:诱饵蛋白纯化后浓度检测Concentration detection after purification of bait protein;M3:SDS-PAGE Marker;7:标准BSA standard BSA;8:GST-CsBZIP40。D:诱饵蛋白纯化后纯度检测Fineness detection after purification of bait protein;M4:WB Marker;9:GST-CsBZIP40

A:感染溃疡病菌的叶片总蛋白GST pull-down结果The GST pull-down from total protein of leaves infected by Xcc;B:未感染溃疡病菌的叶片总蛋白GST pull-down结果The GST pull-down from total protein of leaves infected by LB medium

表1 抗病相关的CsBZIP40互作蛋白
2.5 CsBZIP40互作蛋白GO富集分析
对质谱得到的蛋白用OmicsBean在线软件从分子功能层面进行GO功能富集分析,证明这些蛋白的功能主要集中在分子功能。分子功能的前10个GO分别与结构分子活性(7个)、色素结合(4个)、蛋白质结合(20个)、核糖体结构成分(6个)、蛋白结构域特异性结合(6个)、硫氧还蛋白过氧化物酶活性(1个)、叶黄素结合(1个)、叶绿素结合(4个)、mRNA结合(4个)、Delta24甾醇还原酶活性(1个)有关或相关(图5-A)。在这些分子功能富集中,20个蛋白与蛋白结合有关,提示与CsBZIP40结合的蛋白主要参与了蛋白结合调控过程。从这53个蛋白的功能富集网络可以看出许多基因参与了几个不同的功能,比如Cs2g19680参与了蛋白结构域特异性结合、蛋白质结合、色素结合和叶绿素结合等多个功能(图5-B)。
2.6 CsBZIP40互作蛋白的KEGG分析
<0.05时,有3个可信度较高的富集通路,分别为淀粉和蔗糖代谢通路、光合作用天线蛋白通路和核糖体通路(图6-A)。这3个通路中淀粉和蔗糖代谢通路与光合作用天线蛋白通路属于代谢相关的通路,而核糖体通路则与遗传信息相关(图6-B)。有5个基因参与淀粉和蔗糖代谢通路、11个基因参与光合作用天线蛋白通路、6个基因参与核糖体通路,而且每个代谢通路中的几个蛋白之间也往往存在相互作用(图6-C)。KEGG结果表明CsBZIP40的互作蛋白可能在代谢、光合以及能量转换与利用方面发挥重要的作用。

A:CsBZIP40互作蛋白GO分子功能富集分析GO molecular functional enrichment analysis of CsBZIP40 interacting proteins;B:CsBZIP40互作蛋白GO分子功能蛋白互作分析GO molecular functional protein interaction analysis of CsBZIP40 interacting proteins
2.7 蛋白互作分析
用CsBZIP40的53个互作蛋白序列同模式植物拟南芥的蛋白互作数据库进行比对,挖掘与CsBZIP40同源的TGA9相互作用的蛋白(图7)。互作网络显示53个蛋白中与TGA9直接或间接结合的蛋白有44个已经得到数据支持,证明了本研究的可靠性。有9个蛋白在数据库中尚无数据支撑。在这44个蛋白的互作网络中有15个基因处于重要节点位置,它们与较多的蛋白存在相互作用,比如蛋白AT5G27850与其他6个蛋白存在相互作用;蛋白CR88与其他10个蛋白存在相互作用。这些节点蛋白在响应柑橘溃疡病菌侵染的过程中可能发挥着重要的作用,节点蛋白CR88是一个热休克蛋白,植物正常生长状态下组织中很少能检测到热休克蛋白的表达,而在胁迫下会有大量热休克蛋白表达,因此热休克蛋白在植物抵抗外界胁迫中具有重要意义[23]。同时与之互作的蛋白MYB[24]、NPR1[22]均与植物抵抗生物胁迫密切相关。CR88蛋白与多个广谱抗性蛋白互作,在柑橘体内协同发挥作用,共同抵抗溃疡病菌对机体的侵染。

A:CsBZIP40互作蛋白KEGG信号通路分析KEGG signaling pathway analysis of CsBZIP40 interacting proteins;B:可信信号通路基因数量统计 Gene quantity statistics of trusted signaling pathway;C:信号通路蛋白互作分析interaction analysis of signaling pathway protein
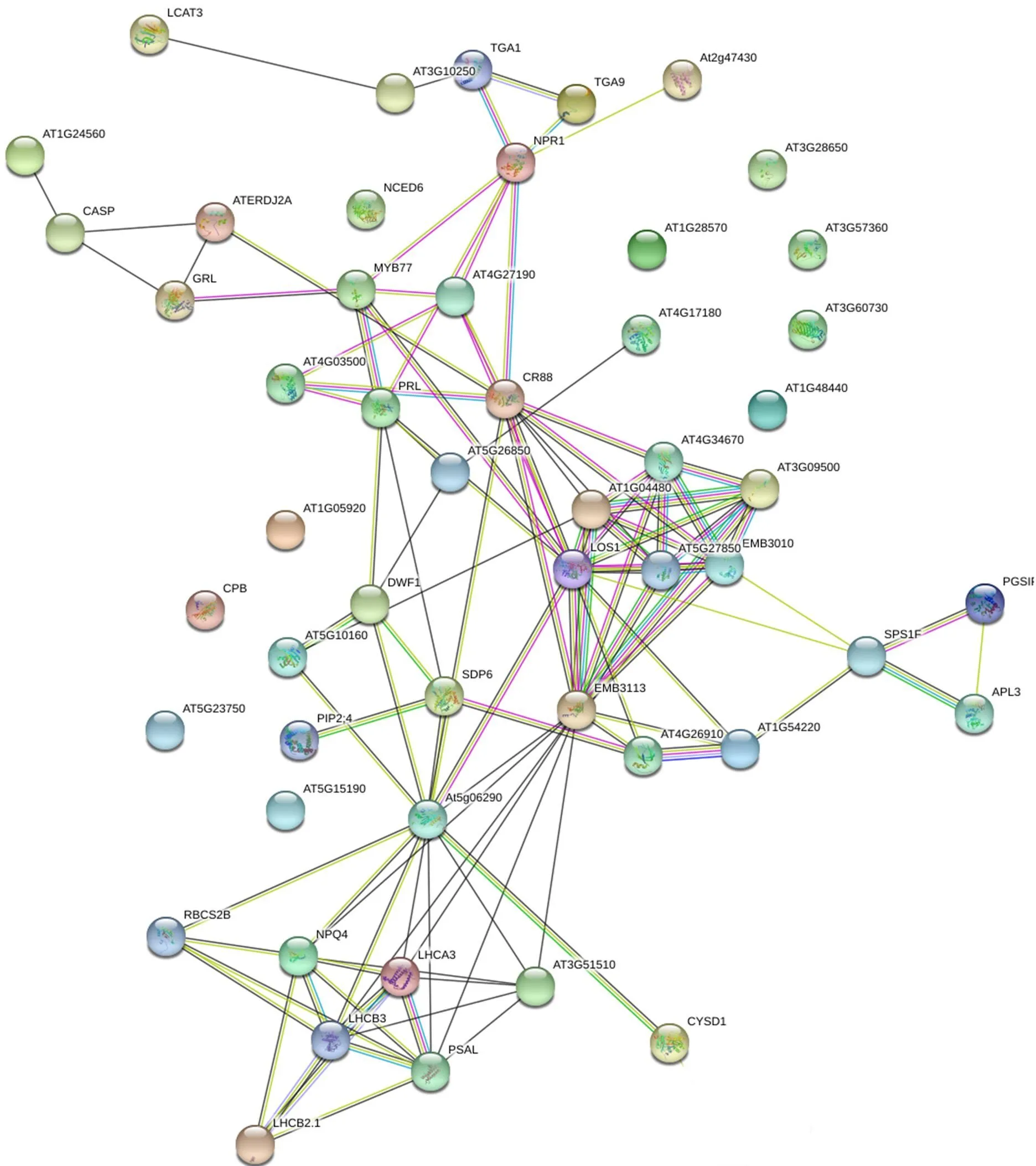
节点代表溃疡病菌侵染过程中CsBZIP40的结合蛋白,圆圈中的图案为预测的蛋白三级结构,空白表示三级结构未知。不同颜色的连线表示不同数据来源The circle in the figure is the binding protein of CsBZIP40. The pattern in the circle is the predicted protein tertiary structure, and the blank indicates that the tertiary structure is unknown. Line segments indicate that there is a clear link between the two proteins that has been proven or reported
3 讨论
植物在漫长的进化过程中逐渐形成了一系列复杂而有效的识别和保护机制来抵抗病原菌的侵染[23],主要包括植物抗病基因介导的侵染部位细胞程序性死亡、超敏反应与系统获得抗性等[25-27]。拟南芥中BZIP(TGA)转录因子在免疫反应网络中处于重要的位置,在前人的研究中发现,BZIP转录因子上游受到NPR(non-expressor of PR gene)基因的调控,NPR基因在植物的系统获得性抗性(systemic acquired resistance,SAR)响应中起关键的调节作用[28],NPR蛋白与TGA蛋白互作调控下游基因的表达[29]。CsBZIP40是柑橘中一个重要转录因子[30],前期对CsBZIP40的功能研究与分析发现该转录因子与柑橘溃疡病抗性明显相关,柑橘基因组中转录因子CsBZIP40与拟南芥中TGA9高度同源,均属于在病菌防御方面发挥作用的D亚家族[31]。CsBZIP40作为下游基因的调控因子[32-35],对植物的转录调控发挥着重要的作用。本研究中,对过表达柑橘植株的抗溃疡病评价结果表明过表达能显著提高柑橘对溃疡病的抗性,但机理尚不明确。本文从蛋白质层面入手,利用GST pull-down技术获取与CsBZIP40蛋白直接作用的蛋白,筛选出柑橘溃疡病菌侵染过程中的结合蛋白,对解析CsBZIP40的调控机理具有重要意义。
对溃疡病菌侵染过程中特异表达的53个蛋白结合相关的数据库检索、生物信息学预测、比对和功能分析,结果表明与数据库中得到的蛋白调控网络中部分重合,证明了该研究的准确性,同时丰富了数据库。GO注释显示,这53个蛋白的功能主要归类为能量代谢、光合作用以及植物抗逆相关蛋白。其中Cs1g02310、Cs3g05280、Cs3g23950、Cs6g13880、Cs7g12130、orange1.1t04973可能与柑橘抗病抗逆性密切相关。转录因子会通过上调或下调下游相关基因的表达来实现对某一过程的调控[36],CsBZIP40转录因子如何实现的这个调控尚不明确,直接调控还是间接调控也不明晰。在这个过程中,一些与转录调控相关的蛋白可能发挥关键作用。本研究结果显示,溃疡病菌侵染过程中特异表达的某些蛋白可能在柑橘抵抗溃疡病菌的过程中发挥着重要的作用,比如Cs3g05280在感染溃疡病中特异结合,此蛋白在其他物种中的同源基因几乎都参与抗病反应,在植物抗逆过程中起着重要的作用;Cs1g02310与拟南芥中TGA1高度同源,NPR1和TGA1是植物体内获得系统抗性的关键氧化还原调控因子[37];Cs6g13880是编码Peroxiredoxin-2酶的基因,过氧化物酶是一类清除生物体内活性氧的重要的酶,与提高植物抗逆性密切相关[38];活性氧在植物局部和整体防御反应中发挥着重要的作用[39]。因此,这两个基因(Cs1g02310、Cs6g13880)在提高转基因植株溃疡病抗性中可能发挥着重要的作用。还有部分基因能够提高柑橘对恶劣环境的耐受性,比如Cs3g05280与同源性较高,过表达能够提高拟南芥对渗透胁迫的耐受性[30];Cs7g12130编码热休克蛋白,热休克蛋白是植物逆境条件下产生的应激蛋白,通过分子伴侣保护机制保护逆境中的细胞,从而提高植物对逆境的忍耐力[40];Cs7g15030与油菜素甾类生物合成相关,油菜素甾类能诱导H2O2的积累,增强植物抗氧化性[41]。这些蛋白在柑橘抵抗溃疡病菌时,能够增强柑橘本身的防御功能,延缓发病时间,减轻发病症状,从而表现出过表达转基因植株对溃疡病的抗性。
4 结论
BZIP40属于病原菌抗性相关的转录因子,过表达转基因晚锦橙表现出对溃疡病的抗性。GST pull-down联合LC-MS/MS筛选出53个在感染溃疡病菌过程中与CsBZIP40互作的蛋白,这些蛋白包括转录调控蛋白、植物抗病性蛋白、细胞壁合成调控蛋白、过氧化物酶、细胞程序性死亡调控蛋白等,参与不同的分子功能和代谢通路,在响应柑橘溃疡病菌的侵染过程中与CsBZIP40协同发挥作用。
[1] 姚廷山, 周彦, 周常勇. 柑橘溃疡病分化及其研究进展. 园艺学报, 2015, 42(9): 1699-1706.
YAO T S, ZHOU Y, ZHOU C Y. Research development of the differentiation and control of citrus bacterial canker disease., 2015, 42(9): 1699-1706. (in chinese)
[2] BEHLAU F, CANTEROS B I, MINSAVAGE G V, JONES J B, GRAHAM J H. Molecular characterization of copper resistance genes fromsubsp.andsubsp.., 2011, 77(12): 4089-4096.
[3] 贾瑞瑞, 周鹏飞, 白晓晶, 陈善春, 许兰珍, 彭爱红, 雷天刚, 姚利晓, 陈敏, 何永睿, 李强. 柑橘响应溃疡病菌转录因子CsBZIP40的克隆及功能分析. 中国农业科学, 2017, 50(13): 2488-2497.
JIA R R, ZHOU P F, BAI X J, CHEN S C, XU L Z, PENG A H, LEI T G, YAO L X, CHEN M, HE Y R, LI Q. Gene cloning and expression analysis of canker-related transcription factor CsBZIP40 in citrus., 2017, 50(13): 2488-2497. (in chinese)
[4] 刘武, 戴良英. 植物抗逆相关ERF转录因子研究综述.中国农学通报, 2007, 23(4): 78-81.
LIU W, DAI L Y. ERF transcription factors related to plant stress-tolerance., 2007, 23(4): 78-81. (in chinese)
[5] LEHTI-SHIU M, PANCHY N,WANG P P, UYGUN S, SHIU S H. Diversity, expansion, and evolutionary novelty of plant DNA-binding transcription factor families., 2017, 1860(1): 3-20.
[6] MOLINA L, KAHMANN R. Angene involved in H2O2detoxification is required for virulence., 2007, 19(7): 2293-2309.
[7] LIN C H, YANG S L, CHUNG K R. The YAP1 homolog-mediated oxidative stress tolerance is crucial for pathogenicity of the necrotrophic fungusin citrus., 2009, 22(8): 942-952.
[8] LIAO Y, ZOU H F, WEI W, HAO Y J, TIAN A G, HUANG J, LIU Y F, ZHANG J S, CHEN S Y. Soybean,andgenes function as negative regulator of ABA signaling and confer salt and freezing tolerance in transgenic., 2008, 228(2): 225-240.
[9] Amorim L L B, da Fonseca Dos Santos R, Neto J P B, Guida-Santos M, Crovella S, Benko-Iseppon A M. Transcription factors involved in plant resistance to pathogens., 2017, 18(4): 335-351.
[10] LI X L, FAN S H, HU W, LIU G Y, WEI Y X, HE C Z, SHI H T. Two cassava basic leucine zipper (bZIP) transcription factors (MebZIP3 and MebZIP5) confer disease resistance against cassava bacterial blight., 2017, 8: Article 2110.
[11] FITZGERALD H A, CANLAS P E, CHERN M S, RONALD P C. Alteration of TGA factor activity in rice results in enhanced tolerance topv.., 2005, 43: 335-347.
[12] WANG H, ZENG X. Analysing protein-protein interactions using a GST-fusion protein to pull down the interacting target from the cell lysate., 2000, 5(1): 26-30.
[13] REN L, CHANG E, MAKKY K, HAAS A L, KABOORD B, QORONFLEH M W. Glutathione-transferase pull-down assays using dehydrated immobilized glutathione resin., 2003, 322(2): 164-169.
[14] Akiyama T, PILLAI M A, SENTOKU N. Cloning, characterization and expression of, a rice endo-1,3--glucanase gene regulated developmentally in flowers and hormonally in germinating seeds., 2004, 220(1): 129-139.
[15] 赵文, 王静, 李伟滔, 王静, 李晓冰, 朱立煌, 陈学伟. 应用GST pull-down技术筛选水稻抗稻瘟病蛋白PID3互作蛋白的研究. 植物病理学报, 2015, 45(5): 476-485.
ZHAO W, WANG J, LI W T, WANG J, LI X B, ZHU L H, CHEN X W. Screening of rice proteins interacting with the rice blast resistance protein PID3 by GST pull-down., 2015, 45(5): 476-485. (in chinese)
[16] 林生, 陈婷, 周明明, 陈观水, 林文雄. 果蔗SoSGT1与侵染下果蔗叶片蛋白的互作研究. 热带亚热带植物学报, 2015, 23(3): 252-261.
LIN S, CHEN T, ZHOU M M, CHEN G S, LIN W X. Studies on interaction between SoSGT1 and proteins in leaves of chewing cane infected by., 2015, 23(3): 252-261. (in chinese)
[17] CHEN M, HE Y R, XU L Z, PENG A H, LEI T G, YAO L X, LI Q, ZHOU P F, BAI X J, DUAN M J, JIANG X Y, JIA R R, ZOU X P, CHEN S C. Cloning and expression analysis of citrus genesandresponding topv.infection., 2016, 2(4): 193-202.
[18] COX J, MANN M. MaxQuant enables high peptide identification rates, individualized p.p.b.-range mass accuracies and proteome-wide protein quantification., 2008, 26(12): 1367-1372.
[19] KANEHISA M, SATO Y, FURUMICHI M, MORISHIMA K, TANNBE M. New approach for understanding genome variations in KEGG., 2018, 47(Database issue): D590-D595.
[20] SZKLARCZYK D, MORRIS J H, COOK H, KUHN M, WYDER S, SIMONOVIC M, SANTOS A, DONCHEVA N T, ROTH A, BORK P, JENSEN L J, MERING C. The STRING database in 2017: quality- controlled protein-protein association networks, made broadly accessible., 2017, 45(Database issue): D362-D368.
[21] XU Q, CHEN L L, RUAN X A, CHEN D J, ZHU A D, CHEN C L, BERTRAND D, JIAO W B, HAO B H, LYON M P, CHEN J J, GAO S, XING F, LAN H, CAHNG J W, GE X H, LEI Y, HU Q, MIAO YIN, WANG L, XIAO S X, BISWAS M K, ZENG W F, GUO F, CAO H B, YANG X M, XU X W, CEHNG Y J, ZHANG J, ROOSE M L, NAGARAJAN N, DENG X X, Ruan y. The draft genome of sweet orange ()., 2013, 45(1): 59-66.
[22] LINDERMAYR C, SELL S, MULLER B, LEISTER D, DURNER J. Redox regulation of the NPR1-TGA1 system ofby nitric oxide., 2010, 22(8): 2894-2907.
[23] SAFDAR W, MAJEED H, ALI B, HAVEED I. Molecular evolution and diversity of small heat shock proteins genes in plants., 2012, 44(special issue): 211-218.
[24] RAFFAELE S, RIVAS S, ROBY D. An essential role for salicylic acid in AtMYB30-mediated control of the hypersensitive cell death program in., 2006, 580(14): 3498-3504.
[25] Naseem M, Kaltdorf M, Dandekar T. The nexus between growth and defense signaling: auxin and cytokinin modulate plant immune response pathways., 2015, 66(16): 4885-4896.
[26] FEYS B J, PARKER J E. Interplay of signaling pathways in plant disease resistance., 2000, 16(10): 449-455.
[27] DANGL J L, JONES J D. Plant pathogens and integrated defense responses to infection., 2001, 411(6839): 826-833.
[28] MEUR G, BUDATHA M, CUPTA A D, PRAKASH S, KIRTI P B. Differential induction of NPR1 during defense responses in., 2006, 68(4): 128-137.
[29] MOU Z L, FAN W H, DONG X N. Inducers of plant systemic acquired resistance regulate NPR1 function through redox changes., 2003, 113(7): 935-944.
[30] DESPRES C, DELONG C, GLAZE S, LIU E W, FOBERT P R. TheNPR1/NIM1 protein enhances the DNA binding activity of a subgroup of the TGA family of bZIP transcription factors., 2000, 12(2): 279-290.
[31] JAKOBY M, WEISSHAAR B, DROGE-Laser W, Vicente- Carbajosa J, TIEDEMANN J, Kroj T, Parcy F. BZIP transcription factors in., 2002, 7(3): 106-111.
[32] BARAH P, WINGE P, KUSNIERCZYK A, TRAN D H, BONES A M. Molecular signatures inin response to insect attack and bacterial infection., 2013, 8(3): e58987.
[33] PERSAK H, PITZSCHKE A. Tight interconnection and multi-level control ofMYB44 in MAPK cascade signaling., 2013, 8(2): e57547.
[34] NIJHAWAN A, JAIN M, TYAGI A K, KHURANA J P. Genomic survey and gene expression analysis of the basic leucine zipper transcription factor family in rice., 2008, 146(2): 333-350.
[35] LIU J Y, CHEN N N, CHEN F, CAI B, SANTO S, TORNIELLI G B, PEZZOTTI M, CHENG Z M. Genome-wide analysis and expression profile of the bZIP transcription factor gene family in grapevine ()., 2014, 15: 281.
[36] CHEN X H, BARNABY J, SREEDHARAN A, HUANG X, OrboviC V, Grosser J W, Wang N, dong x, song w y. Over-expression of the citrus geneconfers resistance to bacterial canker disease., 2013, 84: 115-122.
[37] ORGEUR M, MARTENS M, LEONTE G, NASSARI S, BONNIN M A, BORNO S T, TIMMERMANN B, HECHT J, DUPREZ D, STRICKER S. Genome-wide strategies identify downstream target genes of chick connective tissue-associated transcription factors., 2018, 145: dev.161208.
[38] WOOD Z A, POOLE L B, KARPLUS P A. Peroxiredoxin evolution and the regulation of hydrogen peroxide signaling., 2003, 300(5619): 650-653.
[39] DELLEDONNE M, XIA Y J, DIXON R A, LAMB C. Nitric oxide functions as a signal in plant disease resistance., 1998, 394(6693): 585-588.
[40] Al-Whaibi M H. Plant heat-shock proteins: A mini review., 2011, 23(2): 139-150.
[41] ZHANG A, ZHANG J, YE N H, CAO J, TAN M, ZAHNG J, JIANG M. ZmMPK5 is required for the NADPH oxidase-mediated self- propagation of apoplastic H2O2in brassinosteroid-induced antioxidant defence in leaves of maize., 2010, 61(15): 4399-4411.
Screening of Interacting Proteins of Anti-Canker transcription Factor CsBZIP40 in Citrus by GST pull-down combined with LC-MS/MS
DOU WanFu, QI JingJing, HU AnHua, CHEN ShanChun, PENG AiHong, XU LanZhen, LEI TianGang, YAO LiXiao, HE YongRui, LI Qiang
(Citrus Research Institute, Southwest University/Chinese Academy of Agricultural Sciences, Chongqing 400712)
CsBZIP40 is a citrus canker-related transcription factor. The objective of this study is to screen the interacting proteins of CsBZIP40 in response tosubsp.() infection, and to analyze the interaction network of CsBZIP40, so as to provide a theoretical basis for molecular breeding of citrus canker resistance.The GST pull-down strategy was used to screen the interacting proteins of CsBZIP40 in the infection process of. Firstly, the vector of GST-CsBZIP40 was constructed and induced by IPTG (isopropyl-D-thiogalactoside). The fusion protein of GST-CsBZIP40 was purified for the next GST pull-down. Then GST-CsBZIP40 was fixed on the GST-beads and incubated with total proteins extracted fromover-expression plants infected byor LB medium as control. The protein complex bound to GST-CsBZIP40 bait protein was eluted and collected, and then verified by SDS-PAGE gel electrophoresis. The interacting proteins of CsBZIP40 were detected by LC-MS/MS and then annotated based on the genomic database of. The GO, KEGG pathways and the interaction network of the interacting proteins were also analyzed.The phenotype of transgenic plants over-expressionwas normal, and there was no significant difference between the transgenic plants and the control plants. The lesion area on the over-expression plant was significantly smaller compared to that on the wild-type (WT) (45%) and the disease index ofover-expression plant was significantly lower than that of WT (54%). The total proteins were successfully extracted fromover-expression plant infected byor LB medium, and the GST-CsBZIP40 was expressed and purified for the GST pull-down. GST-CsBZIP40 bait protein was used to catch the protein from the total proteins of-infected and uninfected citrus, then the protein was detected by LC-MS/MS.After comparison, annotation and screening, there are 53 interacting proteins specifically binding to GST-BZIP40 in the process ofinfection. These proteins are involved in many molecular functions and pathways. Among the 53 proteins, 6 proteins (Cs1g02310, Cs3g05280, Cs3g23950, Cs6g13880, Cs7g12130, orange1.1t04973) may be closely related to the plant disease resistance, 44 of the 53 proteins have been proven to interact directly or indirectly with CsBZIP40 in the database.In the infection of, 53 proteins interacted with CsBZIP40 were detected. According to the annotation, 6 proteins are closely related to plant disease resistance. These proteins may play an important role in improving the stress resistance of citrus under biological stress.
; citrus bacteria canker;subsp.(); BZIP; GST pull-down; interacting protein
10.3864/j.issn.0578-1752.2019.13.005
2019-03-12;
2019-04-03
国家重点研发计划(2018YFD1000306,2018YFD0201503)、中央高校基本科研业务费(SWU115025)、国家现代农业产业技术体系建设资金(CARS-26)、广西科技重大专项(桂科AA18118046-6)、重庆市社会事业与民生体系保障科技创新专项(cstc2016shms-ztzx80001,cstc2017shms-xdny80051)
窦万福,E-mail:douwanfu@foxmail.com。
李强,E-mail:liqiang@cric.cn。通信作者何永睿,E-mail:heyongrui@cric.cn
(责任编辑 岳梅)

