HPLC-PDA法测定恩诺沙星注射液中非法添加乙酰甲喹和水杨酸
薄永恒,李淑焕,李有志∗,冯 涛,徐红玮,张 琦
(1.山东省兽药质量检验所/山东省畜产品质量安全监测与风险评估重点实验室,济南250022;2.山东省农业工程学院食品科学与工程学院,济南250100)
恩诺沙星注射液收载于《中国兽药典》2015 版第一部[1],为广谱杀菌药,对大肠杆菌、沙门氏菌等都有杀菌效用,主要治疗由此病菌引起的消化系统、呼吸系统疾病。乙酰甲喹商品名称为痢菌净[2],兽医临床主要用于禽巴氏杆菌病、雏鸡白痢等。水杨酸属于非甾体抗炎药,常用于缓解家畜的发烧、感冒时的体温升高及关节疼痛等症状[3]。当前,某些不法兽药生产企业为了扩大恩诺沙星药物的疗效,而隐蔽乙酰甲喹和水杨酸的使用,在恩诺沙星注射液中添加乙酰甲喹和水杨酸的现象时有发生,造成乙酰甲喹和水杨酸的混乱使用,且不能执行其休药期,最终造成动物性食品中残留乙酰甲喹和水杨酸的严重后果。目前,关于乙酰甲喹和水杨酸的含量检测方法的报道较多,主要包括紫外可见分光光度法、液相色谱法、液相色谱-串联质谱法等。由于兽药制剂之间的检测方法差距较大,检测量上不在同一个级别,而且药物成分之间存在相互干扰[4],因此,急需开发一种同时检测恩诺沙星、乙酰甲喹和水杨酸的的方法,用以检测恩诺沙星注射液中乙酰甲喹和水杨酸的存在。为利于地市县等兽药检验部门开展兽药非法添加的检验工作,本研究将建立科学、有效、简单的恩诺沙星注射液中非法添加乙酰甲喹和水杨酸的检测技术,以有效杜绝非法添加的问题。
1 材 料
1.1 仪器 Waters 2695e 高效液相色谱仪,配二极管阵列检测器,美国Waters 公司;XS-205 电子天平,瑞士Mettler Toledo 公司。
1.2 试剂与材料 甲醇、乙腈为色谱纯,Merck KGaA 公司,其余试剂均为分析纯;实验用水为milli-Q超纯水。乙酰甲喹对照品(中国兽医药品监察所,批号:H0401204,含量:99.6%);恩诺沙星(中国兽医药品监察所,批号:H0081505,含量:99.5%);水杨酸(中国食品药品检定研究院,批号:130451-201203,含量:84.2%)。
2 方 法
2.1 色谱条件 色谱柱:Waters XBridge C18 色谱柱,(4.6 mm×250 mm,5 μm);流动相:0.025 moL/L磷酸溶液∶乙腈=85 ∶15(V∶V);流速1.0 mL/min;进样量:10 μL;柱温:25 ℃;二极管阵列检测器参考条件:定性采集波长范围200~400 nm;定量波长232 nm。
2.2 溶液的制备
2.2.1 供试品溶液 量取恩诺沙星注射液0.5 mL,置50 mL 容量瓶中,加甲醇稀释至刻度,摇匀,精密量取5 mL 置50 mL 容量瓶中,用流动相稀释至刻度,摇匀,即得。
2.2.2 对照品溶液 称乙酰甲喹、水杨酸对照品50 mg(准确至0.01 mg),置50 mL 容量瓶中,加甲醇稀释至刻度,摇匀,作为对照品储备液,精密量取1 mL 置100 mL 容量瓶中,用流动相稀释至刻度,摇匀,作为对照品工作液。
2.2.3 系统适应性溶液 分别精密量取乙酰甲喹、水杨酸对照品储备液100 μL 和200 μL,置10 mL量瓶中,用流动相稀释并定容至刻度,即得。
2.2.4 阴性添加溶液 分别精密量取乙酰甲喹、水杨酸对照品储备液适量,置10 mL 量瓶中,用阴性无添加的恩诺沙星注射液的供试品溶液稀释并定容至刻度。
2.3 方法学考察
2.3.1 系统适用性试验 乙酰甲喹、水杨酸在试验条件下完全分离,分离度均大于1.5,各化合物的色谱峰理论塔板数均大于5000,方法专属性良好。系统适应性溶液色谱图(图1)及相应对照品光谱图(图2)。
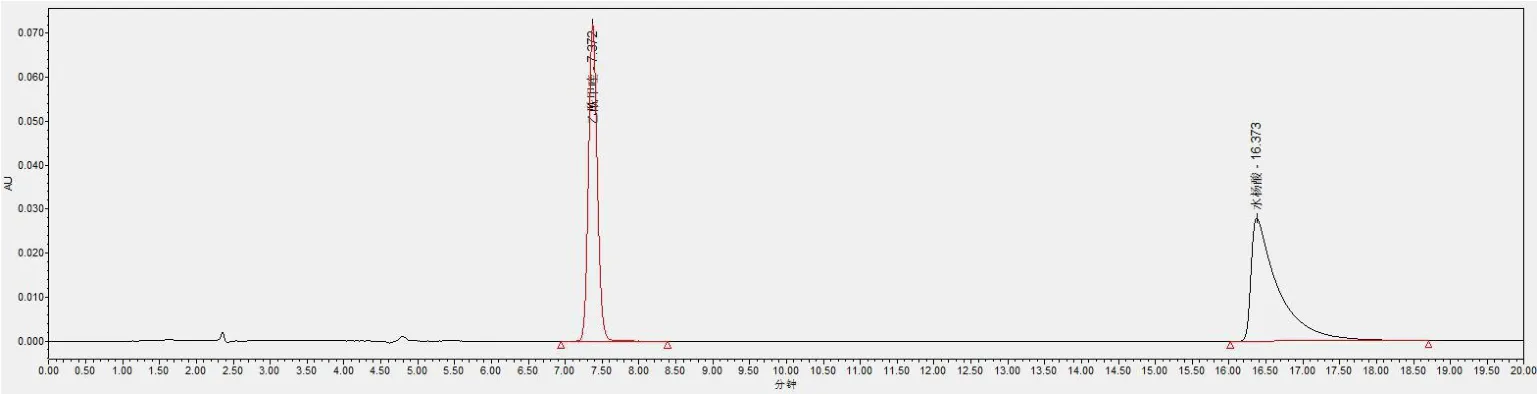
图1 水杨酸(浓度20μg/mL)、乙酰甲喹(浓度10μg/mL)色谱图Fig 1 Chromatogram of salicylic acid (20μg/mL) and acetoquine (10μg/mL)

图2 乙酰甲喹、水杨酸光谱图Fig 2 Spectrum of acetoquine and salicylic acid
2.3.2 线性范围 精密称乙酰甲喹、水杨酸对照品50 mg(准确至0.01 mg),置50 mL 容量瓶中,加甲醇稀释至刻度,摇匀,备用。用流动相分别配制水杨酸、乙酰甲喹的混合标准溶液5 种,浓度分别为50、20 μg/mL、20、10 μg/mL、10、5 μg/mL、2、1 μg/mL、1、0.5 μg/mL。从低浓度到高浓度一次注入液相色谱仪测定,以峰面积为纵坐标,相应浓度为横坐标,绘制标准曲线,水杨酸、乙酰甲喹标准工作曲线回归方程分别为:y=35628.467x-4908.954、y=58342.897x+2297.349,相关系数R2分别为1.000、1.000。结果表明在线性范围内,水杨酸、乙酰甲喹浓度与峰面积呈现良好的线性关系。
2.3.3 峰纯度检查 对阴性空白添加样品的光谱图中两个目标化合物进行峰纯度检查,结果见图4~图5和表1。结果显示,阴性空白在232 nm处有吸收值,但与两个目标化合物有较大分离,分离度大于1.5,达到很好的分离,如图3,且各色谱峰的纯度角度均小于纯度阈值,表明此色谱条件下,两个目标化合物的出峰位置无其他干扰峰,为单一物质,方法可行。

图3 水杨酸(浓度20 μg/mL)、乙酰甲喹(浓度10 μg/mL)的阴性添加溶液色谱图Fig 3 Chromatogram of salicylic acid (20 μg/mL) and acetoquine (10 μg/mL) in negative addition solution

图4 阴性空白添加水杨酸的纯度图Fig 4 Purity diagram of the addition of salicylic acid to the negative blank

图5 阴性空白添加乙酰甲喹的纯度图Fig 5 Purity map of acetaminoquin added to negative blank
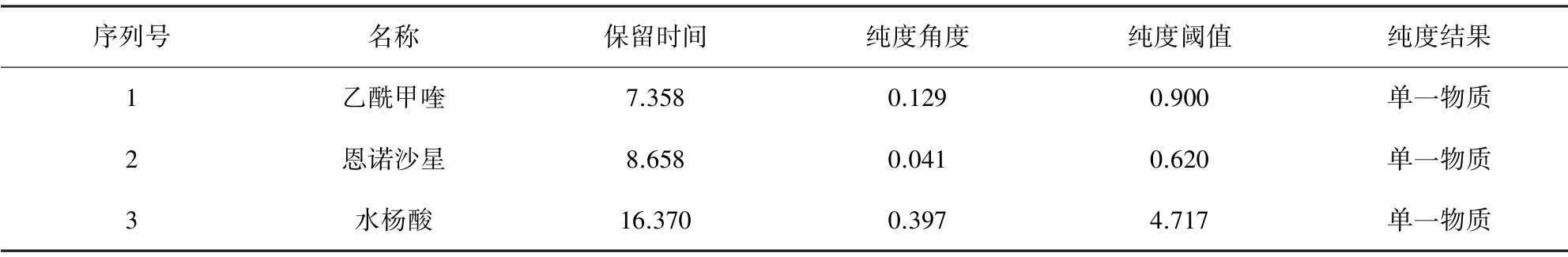
表1 峰纯度检查结果表Tab 1 Peak Purity Check Results Table
2.3.4 灵敏度试验 在阴性样品中添加乙酰甲喹、水杨酸标准溶液,获得0.5 μg/mL 和0.25 μg/mL 的添加乙酰甲喹终浓度样品和1 μg/mL 和0.5 μg/mL的添加水杨酸终浓度样品,进行检测,以光谱图失真的最大浓度作为方法的检出限[5]。水杨酸在0.5 μg/mL的添加终浓度下,光谱图已失真,如图6,因此,水杨酸的最低检出限浓度为1 μg/mL,在恩诺沙星注射液中的检出限为0.5 mg/mL;乙酰甲喹在0.25 μg/mL 的添加终浓度下,光谱图已失真,如图7,因此,乙酰甲喹的最低检出限浓度为0.5 μg/mL,在恩诺沙星注射液中的检出限为0.25 mg/mL。

图6 水杨酸的检出限光谱图(0.5mg/mL)Fig 6 Spectral map of salicylic acid detection limit (0.5mg/mL)
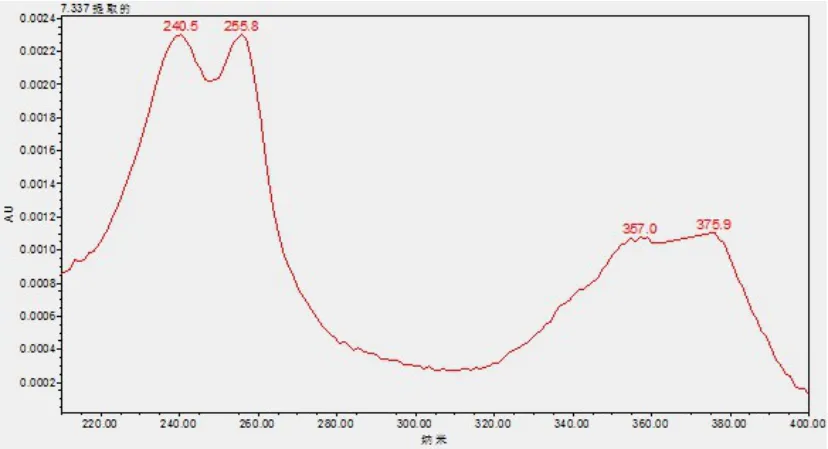
图7 乙酰甲喹的检出限光谱图(0.25mg/mL)Fig 7 Spectral map of detection limit of acetoquine (0.25mg/mL)
2.3.5 准确度和精密度试验 取制得的阴性空白溶液,分别加入适量的1 mg/mL 的水杨酸和乙酰甲喹标准溶液适量,制成高添加浓度样品(水杨酸20 μg/mL,乙酰甲喹10 μg/mL),中添加浓度样品(水杨酸10 μg/mL,乙酰甲喹5 μg/mL),低添加浓度样品(水杨酸2 μg/mL,乙酰甲喹1μg/mL)。每个浓度三份平行样品。计算回收率以及相对标准偏差。结果显示水杨酸平均回收率为99.51%;乙酰甲喹平均回收率为99.62%;相对标准偏差RSD在0.07%~3.44%之间,结果见表2~表3。
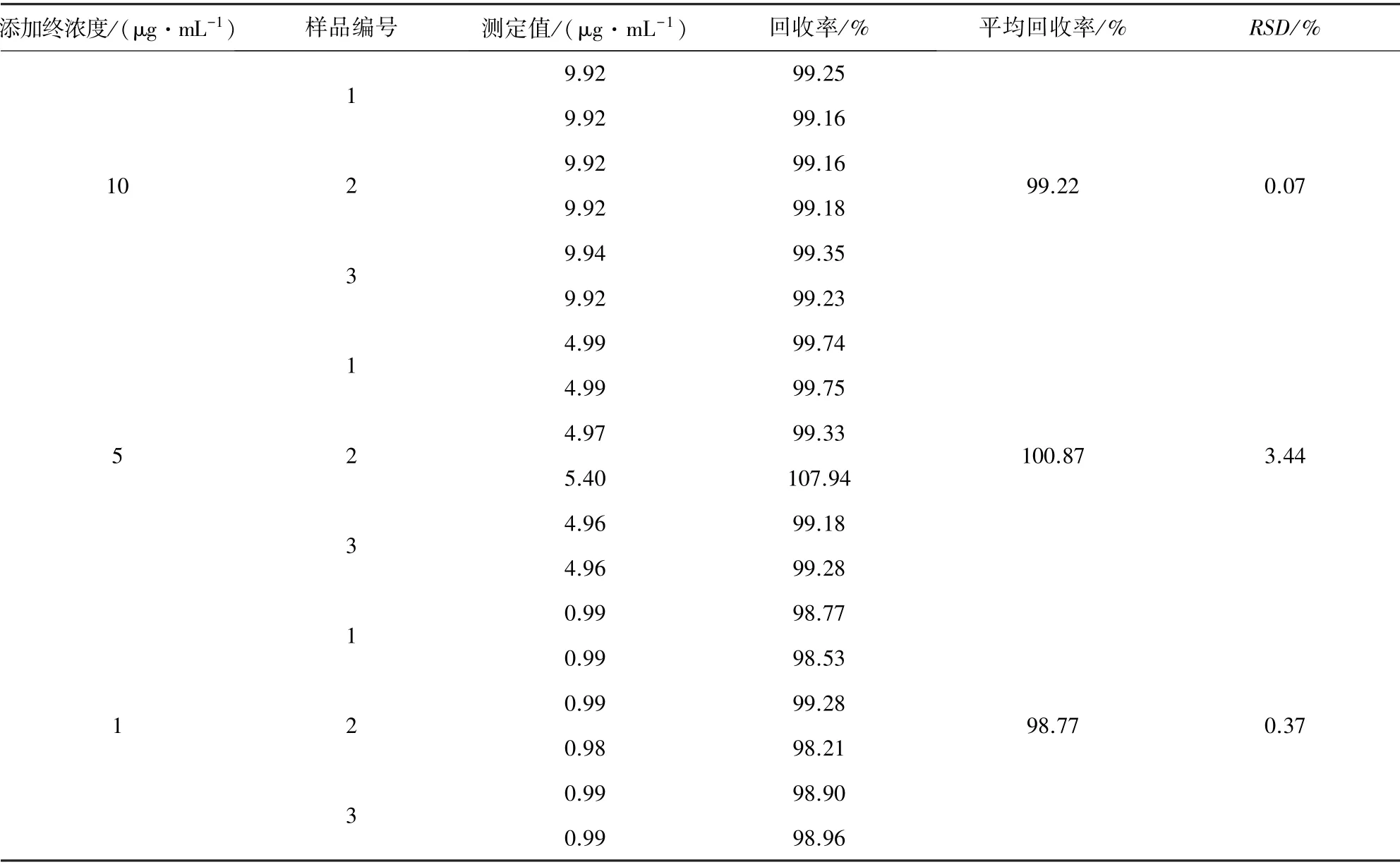
表2 恩诺沙星注射液中乙酰甲喹添加回收率实验结果Tab 2 Experimental results of recovery of acetoquine in enrofloxacin injection
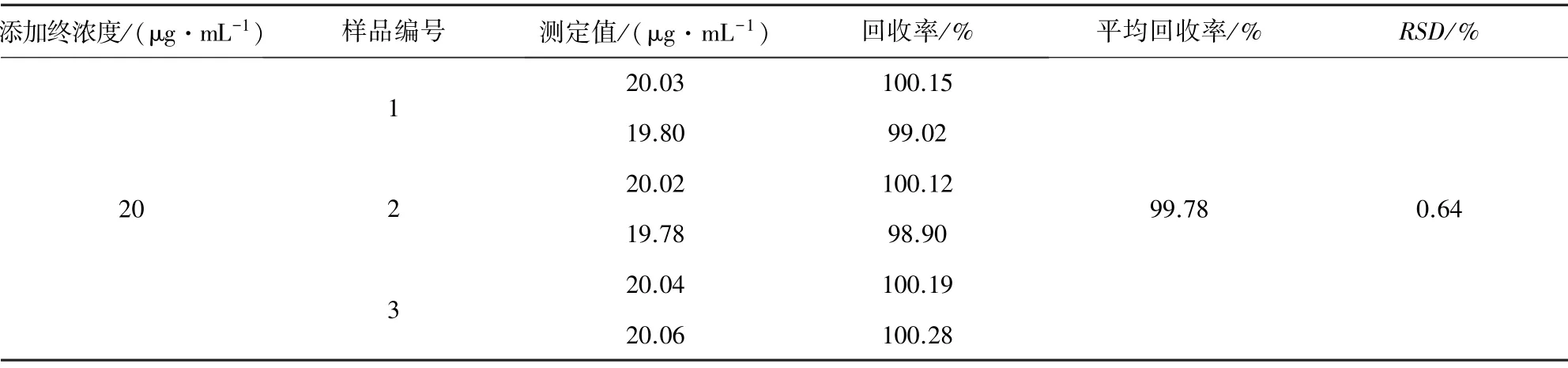
表3 恩诺沙星注射液中水杨酸添加回收率实验结果Tab 3 Experimental results of salicylic acid addition recovery rate in enrofloxacin injection
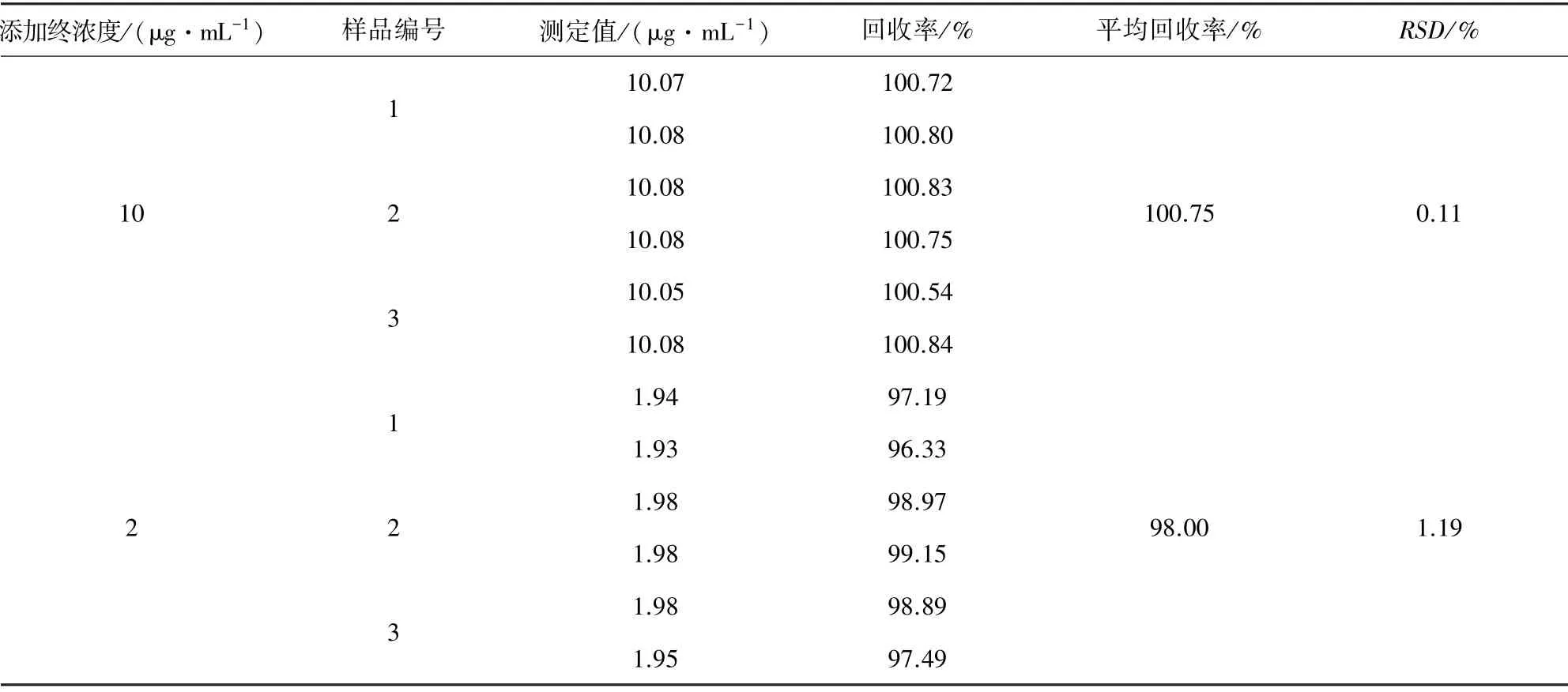
续表
2.3.6 稳定性试验 取同一阴性添加溶液,分别在0、2、4、8、12、24 h 进样10 μL,记录色谱峰面积,乙酰甲喹、水杨酸峰面积的RSD均小于0.4%。结果表明供试品溶液在室温下放置24 h 稳定。
2.3.7 耐用性 从柱温及色谱柱两个方面考察方法的耐用性。改变柱温为20、25、30、40 ℃,出峰顺序无变化,保留时间稍有变化。使用不同品牌、不同型号的色谱柱,例如,Thermp HypersiL GoLd(4.6×250 mm,5 μm);Waters XBridge C18(4.6×150 mm,5 μm);Waters XBridge C18(3.5×150 mm,5μm)等,结果3 种成份仍能很好的分离且出峰时间理想。最佳实验条件的选择中流速的变化对3 种成份的影响也不大,本方法的耐用性良好。
3 讨论与结论
3.1 流动相选择 根据《中国兽药典》2015 版第一部恩诺沙星注射液的含量测定方法,设定了流动相0.025 moL/L 磷酸溶液∶乙腈的比例,分别为83 ∶17,85 ∶15,90 ∶10,结果显示在流动相0.025 moL/L 磷酸溶液∶乙腈体积比为85 ∶15 时,恩诺沙星、乙酰甲喹、水杨酸的分离度符合分离的要求,因此,选择0.025 moL/L 磷酸溶液∶乙腈(85 ∶15)为流动相。
3.2 吸光度选择 由于在乙酰甲喹最大吸收值时,水杨酸的的吸收度较低,在水杨酸的最大吸收值232 nm 作为定量波长时,乙酰甲喹也有较大吸收,以便获得最准确的吸收值,因此,选择232 nm作为方法的吸收波长。
3.3 光谱图的处理 作为定性的最主要图谱,对阴性空白添加样品的光谱图中两个目标化合物进行峰纯度检查,当纯度角度小于纯度阈值时,判定为此出峰物质为单一物质,同时与标品光谱图比对出峰时间一致时,判定为此物质为对应出峰时间的标准物质添加,以此为添加物定性标准。
本方法采用二极管阵列检测器进行检测,实现了恩诺沙星注射液中添加乙酰甲喹、水杨酸的定性定量检测。同时可以通过峰纯度检查锁定非法添加物,通过保留时间与对照品进行对比,实现了恩诺沙星注射液中非法添加物的高效、快速、准确识别,成功建立了恩诺沙星注射液中添加乙酰甲喹、水杨酸的测定——高效液相色谱法。本方法乙酰甲喹检出限为0.25 mg/mL、水杨酸检出限为0.5 mg/mL。

