培美曲塞或多西他赛联合奈达铂二线治疗晚期非小细胞肺癌的临床观察Δ
杜 芳,刘 冰,王德林,曹玉娟,马丽萍
(北京大学首钢医院肿瘤内科,北京 100144)
肺癌的发病率和死亡率均居我国恶性肿瘤的第1位。其中,非小细胞肺癌(non-small cell lung cancer,NSCLC)患者约占肺癌患者数的85%~90%[1]。大多数NSCLC患者确诊时即为晚期,失去了手术治疗的机会[2]。我国NSCLC患者中表皮生长因子受体(epidermal growth factor receptor,EGFR)的突变率仅约25%,大部分患者仍需首选全身化疗;且一线化疗后,大部分患者在6个月内会出现疾病进展,其中约50%的患者可以进行二线治疗[3]。目前,美国食品药品监督管理局推荐的二线治疗NSCLC的药物包括多西他赛、培美曲塞及表皮生长因子受体酪氨酸激酶抑制剂(epidermal growth factor receptor-tyrosine kinase inhibitors,EGFR-TKI)[4-8]。有研究结果表明,二线治疗NSCLC的单药化疗有效率仅为10%,联合用药组患者的缓解率高于单药组[9]。随着保护性及支持性治疗的合理应用,晚期肺癌患者的ECOG评分较以往有所提高,且骨髓抑制得到明显控制,耐受双药联合化疗的患者越来越多。因此,本研究比较了培美曲塞或多西他赛联合奈达铂二线治疗晚期非小细胞肺癌的临床疗效和安全性。
1 资料与方法
1.1 资料来源
选取2011年10月至2015年4月北京大学首钢医院肿瘤内科收治的58例NSCLC患者进行开放性观察研究。纳入标准:年龄18~75岁;经二级甲等及以上医院临床病理细胞学及影像学检查,诊断为NSCLC;TNM分期为ⅢB—Ⅳ期;肺部有可测量病灶;ECOG评分≤2分;为二线治疗且既往未使用过培美曲塞、奈达铂及多西他赛进行全身化疗;预计生存期>3个月。排除标准:肺癌脑转移者;严重肝、肾及心脑血管疾病者;自身免疫系统疾病者;造血功能异常者;哺乳期或妊娠期女性;伴有精神障碍者;经研究者判断不能完成本研究者。根据就诊顺序, 依次将患者分为培美曲塞与奈达铂联合化疗组(A组)、多西他赛与奈达铂联合化疗组(B组),每组29例。两组患者基线资料的差异无统计学意义(P>0.05),具有可比性,见表1。
1.2 方法
(1)A组患者给予培美曲塞二钠注射液(规格:500 mg/支)500 mg/m2,静脉滴注,第1日;注射用奈达铂(规格:10 mg/支),第1、2日,总剂量为80 mg/m2。使用培美曲塞前给予叶酸、维生素B12预防骨髓抑制,化疗前及化疗期间常规给予地塞米松预防过敏反应。(2)B组患者给予多西他赛注射液(规格:20 mg/支)75 mg/m2,静脉滴注,第1日;注射用奈达铂(规格、用法与用量同A组)。使用多西他赛前及使用过程中常规给予地塞米松预防过敏反应。两组患者化疗期间均给予止吐和保护肝功能等对症治疗;均以21~28 d为1个化疗周期,均接受2~6个周期的化疗,总疗程≤6个月。
1.3 观察指标
(1)依照RECIST1.0标准[3],临床有效性指标包括客观缓解率(objective remission rate,ORR)、疾病控制率(disease control rate,DCR)、中位生存期(median survival time,MST)和无进展生存期(progression-free survival,PFS)。MST的定义为从化疗首日至半数生存的时间;PFS的定义为从化疗首日至肿瘤进展止的时间。(2)以用药期间的不良反应作为本研究的安全性指标,详细记录不良反应的名称、发生时间和严重程度等。其中不良反应判定标准依照美国国立癌症研究所5.0版《常见不良反应评价标准》进行评估,分为Ⅰ—Ⅴ级共5个级别,严重的不良反应为Ⅲ—Ⅴ级。
1.4 疗效评定标准
根据RECIST 1.0标准[3]评定临床疗效。完全缓解(complete remission,CR):所有靶病灶消失;部分缓解(partial remission,PR):靶病灶直径之和比基线水平减少至少30%;疾病稳定(stable disease,SD):介于PR与PD之间;疾病进展(progressive disease,PD):靶病灶直径之和比基线水平增加至少20%或新发病灶直径之和绝对值增加至5 mm。ORR=(CR病例数+PR病例数)/总病例数×100%;DCR=(CR病例数+PR病例数+SD病例数)/总病例数×100%。
1.5 统计学方法
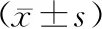
2 结果
2.1 两组患者临床疗效比较
两组患者全部完成治疗和随访,均未见CR病例;A组患者的ORR、DCR较B组略有优势,但两组的差异无统计学意义(P>0.05),见表2。

表2 两组患者临床疗效比较[例(%)]Tab 2 Comparison on clinical efficacy between two groups[cases(%)]
2.2 两组患者的MST、PFS比较
A组、B组患者的MST分别为7.8、8.7个月,PFS分别为4.0、3.3个月;A组患者的MST比B组短0.9个月,PFS比B组长0.7个月,但两组间比较,差异均无统计学意义(P>0.05),见表3—4。

表3 两组患者的MST比较Tab 3 Comparison of median survival time between two groups

表4 两组患者的PFS比较Tab 4 Comparison of progression free survival between two groups

表5 两组患者不良反应发生情况比较[例(%)]Tab 5 Comparison of incidences of adverse drug reactions between two groups[cases(%)]
2.3 两组患者不良反应发生情况比较
A组中发生Ⅲ—Ⅴ度不良反应的患者共13例,B组为18例,但不良反应均在可控制范围内,经对症治疗后好转,无1例患者因不良反应而停止化疗。两组患者各不良反应发生率的差异均无统计学意义(P>0.05),见表5。
3 讨论
近年来,我国肺癌的发病率和死亡率呈逐年升高趋势,其中NSCLC患者占绝大多数,严重威胁人们的生命安全。NSCLC患者确诊时大多失去了手术机会,治疗以全身化疗、靶向治疗或局部治疗为主。大部分NSCLC患者一线治疗失败后,可以继续接受二线治疗。研究结果表明,合理的二线治疗可以有效改善患者的生活质量并提高其生存率。多种化疗药,如多西紫杉醇、依立替康、拓扑替康、培美曲塞、吉非替尼、紫杉醇、吉西他滨和长春瑞滨等,可用于NSCLC的二线治疗[10]。研究结果发现,一线治疗中双药联合化疗优于单药化疗,而二线治疗中双药联合治疗是否优于单药治疗尚需要进一步临床验证[9]。本研究结果提示,NSCLC的二线治疗中,培美曲塞或多西他赛联合奈达铂的双药联合方案的疗效略高于文献报道的培美曲塞或多西他赛单药化疗的疗效,且不良反应可耐受。
培美曲塞为多靶点叶酸拮抗剂,多西他赛为M期周期特异性细胞毒药物;奈达铂为广谱抗肿瘤药,对部分耐受顺铂的细胞株有抑制作用。徐瑞华等[11]的研究结果表明,奈达铂对晚期NSCLC有一定疗效,用于对顺铂或卡铂耐药的NSCLC患者仍有一定的有效率。奈达铂与其他铂类药物间的交义耐药性并不完全。因此,本研究选用培美曲塞联合奈达铂和多西他赛联合奈达铂两个治疗方案,并观察上述两种方案用于NSCLC的有效性和安全性。
本研究结果显示,两组患者ORR、DCR、MST及PFS的差异均无统计学意义(P>0.05)。陆彼灵等[12]采用培美曲塞联合奈达铂二线治疗42例晚期NSCLC患者,结果显示,ORR为19.0%(8例),DCR为61.9%(26例),中位疾病进展时间(time-to-progression,TTP)为3.6个月,MST为8.2个月,与本研究结果相近。郑积华等[13]采用培美曲塞与多西他赛分别二线治疗晚期NSCLC,结果显示,单药培美曲塞组、多西他赛组患者的DCR分别为46.3%、33.3%,低于本研究结果。赵玲娣等[14]针对多西他赛与培美曲塞分别用于晚期NSCLC二线治疗的临床研究结果显示,二线化疗的ORR约10%,TTP仅3个月,也明显低于本研究结果。结合以上研究,提示培美曲塞或多西他赛联合奈达铂双药化疗方案在NSCLC二线治疗中可能比培美曲塞或多西他赛单药化疗更有优势。
全身化疗导致的不良反应是化疗所面临的主要问题之一。本研究观察期间,两组患者的不良反应发生率相近,主要为血液毒性和胃肠道反应等。付娜等[15]报道,单药培美曲塞、多西他赛组患者白细胞减少症发生率分别为42.6%、80.0%,贫血发生率分别为17.0%、60.0%,血小板减少症发生率分别为17.0%、54.0%,恶心呕吐发生率分别为29.8%、64.0%,肝功能异常发生率分别为2.1%、38.0%。本研究结果与上述文献报道比较,骨髓抑制、肝肾功能异常明显增多,但不影响后续治疗;胃肠道反应有所减轻,考虑与止吐药的广泛应用有关。本研究未观察到其他严重不良反应,提示双药联合化疗的不良反应可耐受,适合NSCLC的二线全身化疗。
此外,按体表面积计算,培美曲塞联合奈达铂组患者平均花费 5 736元/(人·28 d),多西他赛联合奈达铂组患者平均花费4 055元/(人·28 d),提示多西他赛联合奈达铂方案更具有经济优势。
综上所述,对晚期NSCLC二线化疗药的选择,应综合考虑药物的疗效、安全性及费用等因素。培美曲塞或多西他赛联合奈达铂方案可提高晚期NSCLC的ORR、DCR、MST和PFS;且不良反应可耐受,适合晚期NSCLC二线化疗。临床治疗中,要根据患者的具体情况,权衡各方案的利弊,选出不良反应小、患者能耐受的方案,使患者获得最大收益。因本研究为开放性观察设计,且研究样本量较少,在患者选择、评估等多方面均存在偏差;没有对病理类型、一线治疗方案等进行更深入的分析,且引用的文献质量有差别,故本研究的结论可能存在偏差。在以后的工作中,还需进一步积累“标准化”患者的数量,以便得出相对准确的结论。

