刺五加提取液对小鼠学习记忆障碍和淀粉样前体蛋白酶解通路影响及作用机制
朱雯菲 付朝旭 代霖 许妍姬
(延边大学医学院预防医学教研室,吉林 延吉 133000)
老年性痴呆又称阿尔茨海默病(AD),一种呈进行性发展的神经退行性疾病。患者认知功能逐渐恶化且发展不可逆转。病因迄今未明,并且仍未找到能够有效遏制或治疗AD且毒副作用较小的药物。AD的神经病理学特征是β-淀粉样蛋白(Aβ)斑块在细胞外沉积,即老年斑(SP)及高度磷酸化的tau蛋白构成的神经纤维缠结(NFTs)〔1〕。Aβ和淀粉样前体蛋白(APP)-β-分泌酶C-末端片段(CTFs)可以引起糖原合成酶激酶(GSK)-3β的过度兴奋和tau磷酸化水平升高〔2〕,而GSK-3β是AD病理作用中的重要调控基因,GSK-3β在Ser-9位磷酸化时,其活性被抑制,可促进神经元存活,提高细胞结构稳定性。SP的主要核心成分APP经过β、γ-分泌酶酶解产生Aβ,但经过α-分泌酶通过非淀粉样途径代谢却会产生可溶性片段 sAPPα,sAPPα具有保护和营养神经作用,能竞争性减少 Aβ 产生,从而延缓 AD 发展〔3〕。APP酶解异常是AD病理机制的重要环节,β、γ-分泌酶活性增高且α-分泌酶活性减低,可使Aβ和APP-CTFs产生过量,是AD病理开始的最根本基础。中草药因其多途径、多靶点的综合调治作用在AD治疗中受到越来越多的关注,有研究表明,刺五加对神经变性疾病如老年性痴呆或帕金森病有保护作用〔4〕。本实验检测各种酶的相关基因如α-分泌酶整合素-金属蛋白酶(ADAM)10(α-)、β-分泌酶(BACE)1、γ-分泌酶(PS)1蛋白表达水平,探讨刺五加对衰老模型小鼠学习记忆能力及APP酶解通路的影响。
1 材料与方法
1.1实验动物 2月龄昆明种雄性小鼠70只,体重16~20 g,由延边大学动物科学实验中心提供。随机分为正常对照、衰老模型、衰老+刺五加低剂量、衰老+刺五加中剂量、衰老+刺五加高剂量、刺五加高剂量、衰老+维生素E组7组,每组10只,在其适应条件下饲养5 d后开始建AD模型。
1.2药品与试剂 刺五加药材由中国北京同仁堂有限责任公司提供。0.9%生理盐水、D-半乳糖(Solarbio LIFE SCIENCES);维生素E购于聊城澳键生物技术有限公司(批准文号:国食健字G20150980);鼠α-、β-、γ-分泌酶、鼠Aβ1~42、鼠sAPPα酶联免疫吸附实验试剂盒均购于上海酶联生物科技;磷酸化(Phospho)-GSK-3β(Ser9)抗体、抗微管蛋白、GSK-3β抗体、辣根过氧化物酶标记山羊抗小鼠IgG(H+L)、二喹啉甲酸(BCA)蛋白浓度测定试剂盒、辣根过氧化物酶标记山羊抗兔IgG(H+L)、十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)试剂均购于碧云天生物技术,抗ADAM10抗体、抗BACE1抗体、抗膜蛋白1抗体购于英国abcam公司。
1.3实验仪器 脱式摇床(金坛市科技仪器)、数显恒温水浴锅(金坛市科析仪器,HH-6)、TG-328B 型分析天平(上海天平仪器厂)、移液器(芬兰,Biohit)、SMART V3.0行为学视频追踪系统(美国 Hayward 公司) 、酶标仪(南京华东电子)、超声波细胞破碎机(上海乔跃电子)、制冰机(日本Sanyo)、电泳仪(碧云天生物技术)、微量振荡器(无锡县金城仪器厂,型号 WZS-2A)、小动物避暗穿梭测试仪(北京众实迪创,型号YLS-17B)、小动物跳台记录仪(北京众实迪创,型号YLS 3TB)、Morris 水迷宫(上海欣软)、恒温CO2培养箱(THERMO 3111型)、高速冷冻离心机(法国 Thermo Electron,型号 CR3i)、干式恒温器(江苏海门市其林贝尔仪器制造,GL-150B)。
1.4刺五加提取液配制步骤 取0.5 kg刺五加,于水中浸泡1 h后加入1.5 kg水。煮沸1 h后再次加入1.5 kg水,共重复提取3次,最终将提取液合并,浓缩至500 ml,而后加水配制为25%(250 g/L)、50%(500 g/L)、75%(750 g/L)的刺五加溶液〔5〕。
1.5衰老模型建立 实验动物依照体重0.1 ml/10 g的剂量原则给药,建模所用D-半乳糖浓度为20 mg/ml,维生素E(40 mg/kg)各组均每日上午十时颈部注射,正常对照组颈部皮下注射0.9%生理盐水间隔8 h后灌胃等体积的一蒸水;衰老模型组皮下注射D-半乳糖间隔8 h灌胃等体积一蒸水;衰老+刺五加低、中、高剂量组皮下注射D-半乳糖间隔8 h灌胃等体积25%、50%、75%刺五加提取液;刺五加高剂量组颈部皮下注射0.9%生理盐水间隔8 h灌胃等体积75%刺五加提取液;衰老+维生素E组皮下注射D-半乳糖间隔灌胃等体积维生素E。连续染毒55 d,实验总时长60 d。每日记录实验动物的状态、体重、摄食与饮水量。
1.6Morris水迷宫测试 实验第53天时进行Morris水迷宫定位航行实验训练。于每日2点对实验动物进行训练,水温控制在(20±2)℃,水迷宫池面平均分为4个象限,每天将小鼠头朝向池壁,分别从第一、二、三、四象限的入水点放入水池。假设实验动物在训练过程中60 s内找到平台,并在指定位置处停留时间长达5 s,则为实验动物找到平台,而后让其在该位置停留10 s,增加记忆;若没有在60 s内找到平台,需要引导实验动物找到台子并使其在台子上停留10 s。重复上述实验,进行6 d的实验训练,于第7天进行空间探索实验,实验时将平台去除,将实验动物从平台的对侧象限放入,记录穿台数目并且记录寻找时间(逃避潜伏期)及活动轨迹〔6〕。
1.7避暗实验 58 d时训练,将实验动物放置在避暗仪中,让其适应环境,3 min后打开明暗室之间的隔板,开启避暗仪,训练5 min,每日训练1次,连续2 d后进行测试,记录潜伏期及5 min内错误次数。
1.8跳台实验 58 d时训练,将实验动物放入跳台箱内,让其适应环境,在3 min后底部通电,实验动物受到电击,跳至平台上躲避伤害性刺激,多次训练后小鼠会形成记忆继而不跳下台子,药物因素(脑损伤)的改变会增加或者削弱这种记忆保留时间。24 h后重新测试,记录各组第一次从平台跳下所需的时间(跳台潜伏期)和5 min内错误次数,若动物在观察期内未跳下平台,错误次数计为0,跳台潜伏期计为观察时间。
1.9脑组织中 α、β、γ-分泌酶、sAPPα、Aβ1~42含量检测 处死小鼠后于冰上取脑,天平称重后按9(ml):1(g)比例稀释,剪碎后用超声粉碎机粉碎,所有操作在冰上进行。样本处理后,上清液采用 ELISA 法检测,按照说明书严格操作。
1.10脑组织中ADAM10、BACE1、PS1、GSK-3β、Phospho-GSK-3β(Ser9)蛋白表达水平检测 采用蛋白印迹法,杀鼠后取出的脑组织经过剪碎、超声粉碎、离心后取上清,严格按照BCA 蛋白浓度测定试剂盒说明书操作得到蛋白浓度。之后进行电泳实验,配制SDS-PAGE 凝胶,待凝固后,注入浓缩胶,插入梳子。按比例稀释蛋白样品后将其置于100℃恒温器中,加热 3~5 min,使之充分变性,取出后放在冰上冷却,降温后用小离心机离心,之后加样。电泳仪电泳分离蛋白,电压70 V进行30 min后转为90 V直至样本转移到达底部,将仪器转换为200 mA电流使印迹转移至聚偏氟乙烯(PVDF)膜,洗涤液洗去残留的转膜液,封闭液封闭 2 h,一抗摇床1.5 h,再 4℃孵育过夜,次日回收一抗,洗涤后加入二抗,室温摇床孵育1 h,回收二抗,再次洗涤后用超敏电化学发光(ECL)试剂盒显影,曝光取影。以β-tubulin作为内参,计算蛋白表达情况。
1.11统计学方法 采用SPSS16.0软件进行用单因素方差分析和t检验。
2 结 果
2.1小鼠Morris水迷宫实验结果
2.1.1定位航行实验结果 衰老模型组潜伏期实验第1~6天较正常对照组明显延长,刺五加高剂量组潜伏期从第一天开始以缓慢下降趋势缩短,作用效果逐渐加强,第6天效果最为显著(P<0.05)。和衰老模型组相比,衰老+刺五加提取液中、高剂量组潜伏期显著缩短(P<0.05)。衰老+维生素E组和衰老+刺五加高剂量组效果相似,对学习记忆能力有一定巩固和提高作用。见表1。
表1 各组观察各时间点定位航行实验逃避潜伏期
与正常对照组比较:1)P<0.05;与衰老模型组比较:2)P<0.05;与前一天比较:3)P<0.05;下表同
2.1.2空间探索实验结果 刺五加高剂量组目标象限停留时间最长,穿台次数高于其他组别,衰老模型组目标象限停留时间,穿台次数都是最低的,空间记忆障碍明显(P<0.05)。各组游泳速度未见明显差异(P>0.05)。见表2。正常对照组具有很强的空间学习能力,而刺五加高剂量组不仅学习能力强,且具有更强的目的性,游泳轨迹多集中于目标象限,活动位置极其靠近平台。衰老模型组学习记忆能力极差,游动轨迹漫无目的毫无规律,衰老+刺五加低、中、高剂量组学习能力逐渐好转,游动轨迹有向目标象限探索的趋势,且对平台位置的记忆越来越清晰,游动轨迹有很强的目的性。见图1。
2.2避暗和跳台实验 与正常对照组比较,衰老模型组潜伏期明显缩短,错误次数显著增加(P<0.05);和衰老模型组相比,衰老+刺五加中、高剂量组潜伏期明显增长(P<0.05),衰老+刺五加高剂量组错误次数明显减少(P<0.05)。见表2。
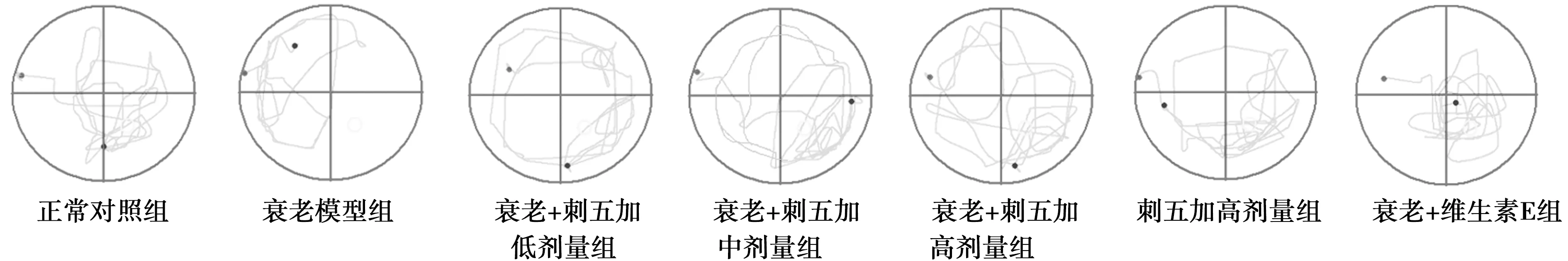
图1 各组空间探索实验活动轨迹
组别空间探索实验目标象限停留时间(s)穿越平台次数(次)游泳速度(mm/s)避暗实验潜伏期(s) 错误次数(次)跳台实验潜伏期(s)错误次数(次)正常对照组12.26±4.235.80±1.98297±30.56156.6±18.443.1±1.19 214.2±34.06 4.9±1.96衰老模型组7.92±2.651)2.10±1.161)274±41.6577.8±37.561) 5.6±2.501)45.7±21.371) 11.5±3.371)衰老+刺五加低剂量组8.25±2.153.20±1.85265±53.6191.9±17.50 4.5±2.22 64.7±40.759.7±4.00衰老+刺五加中剂量组10.04±4.592)3.90±1.432)270±33.47128.5±17.672)3.7±2.16140.1±31.712) 8.4±3.23衰老+刺五加高剂量组11.35±3.252)5.00±1.292)268±50.12138.4±27.942)2.1±0.872)188.5±25.492) 7.11±2.892)刺五加高剂量组16.76±4.871)7.10±1.341)302±85.36182.6±28.721)2.00±1.151) 245.7±32.853.60±1.241)衰老+维生素E组12.24±2.642)4.30±1.942)287±29.65137.6±38.102)3.00±2.002)122.4±33.702) 7.80±2.142)
2.3脑组织α,β,γ-分泌酶活性及sAPPα,Aβ1-42含量 与正常对照组比较,衰老模型组α-分泌酶、sAPPα含量明显降低(P<0.05),β、γ-分泌酶、Aβ1~42含量明显增高(P<0.05);刺五加高剂量组α-分泌酶含量明显增高(P<0.05),β、γ-分泌酶和Aβ1~42含量明显降低(P<0.05);与衰老模型组相比,衰老+刺五加处理组、衰老+维生素E组的α-分泌酶、sAPP含量显著增高(P<0.05),β、γ-分泌酶、Aβ1~42含量明显降低(P<0.05),且作用效果随着刺五加提取液浓度的升高而增强;维生素E的作用效果和刺五加提取液比较相对较弱。见表3。

表3 各组脑组织α,β,γ-分泌酶活性、sAPPα、Aβ1~42含量比较
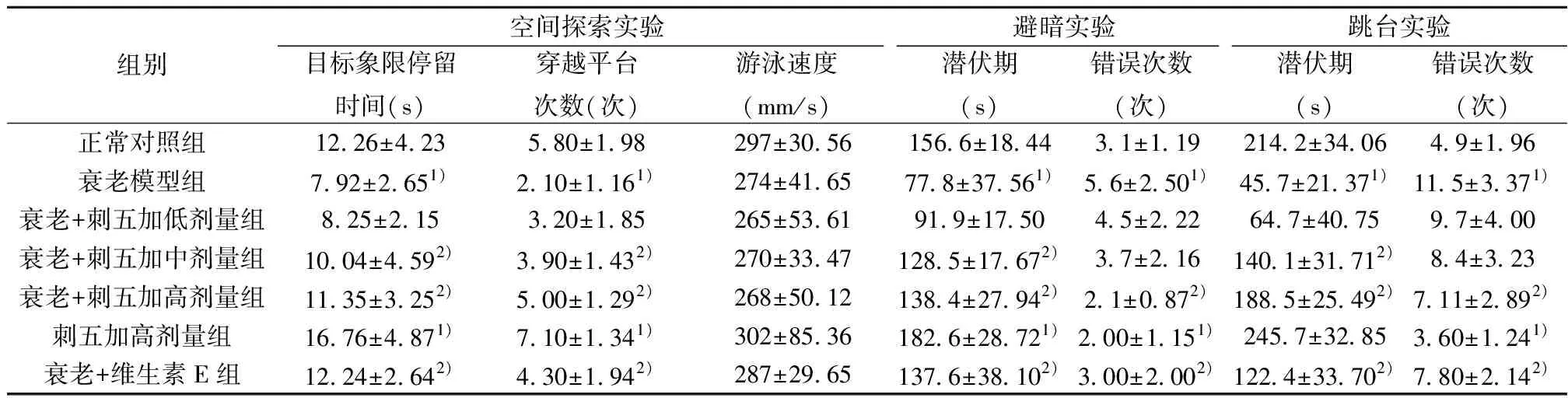
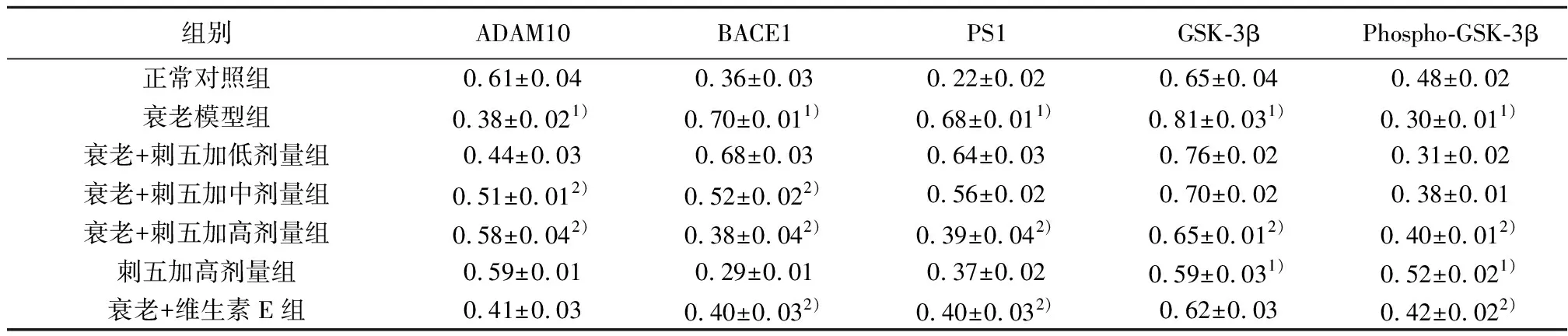
2.4各组脑组织ADAM10、BACE1、PS1、GSK-3β、Phospho-GSK-3β(Ser9)蛋白表达的影响 与正常对照组相比,衰老组 BACE1、PS1蛋白表达水平明显增强(P<0.05),ADAM10表达水平减弱,GSK-3β总蛋白明显上调,而抑制GSK-3β活性的 Ser9 位点磷酸化水平显著下调;与衰老模型组比较,刺五加低、中、高剂量组BACE1、 PS1、GSK-3β、Phospho-GSK-3β(Ser9)蛋白表达水平均显著缓解(P<0.05),ADAM10表达水平显著上调(P<0.05)。其中,高浓度剂量组效果更好。见图2和表4。
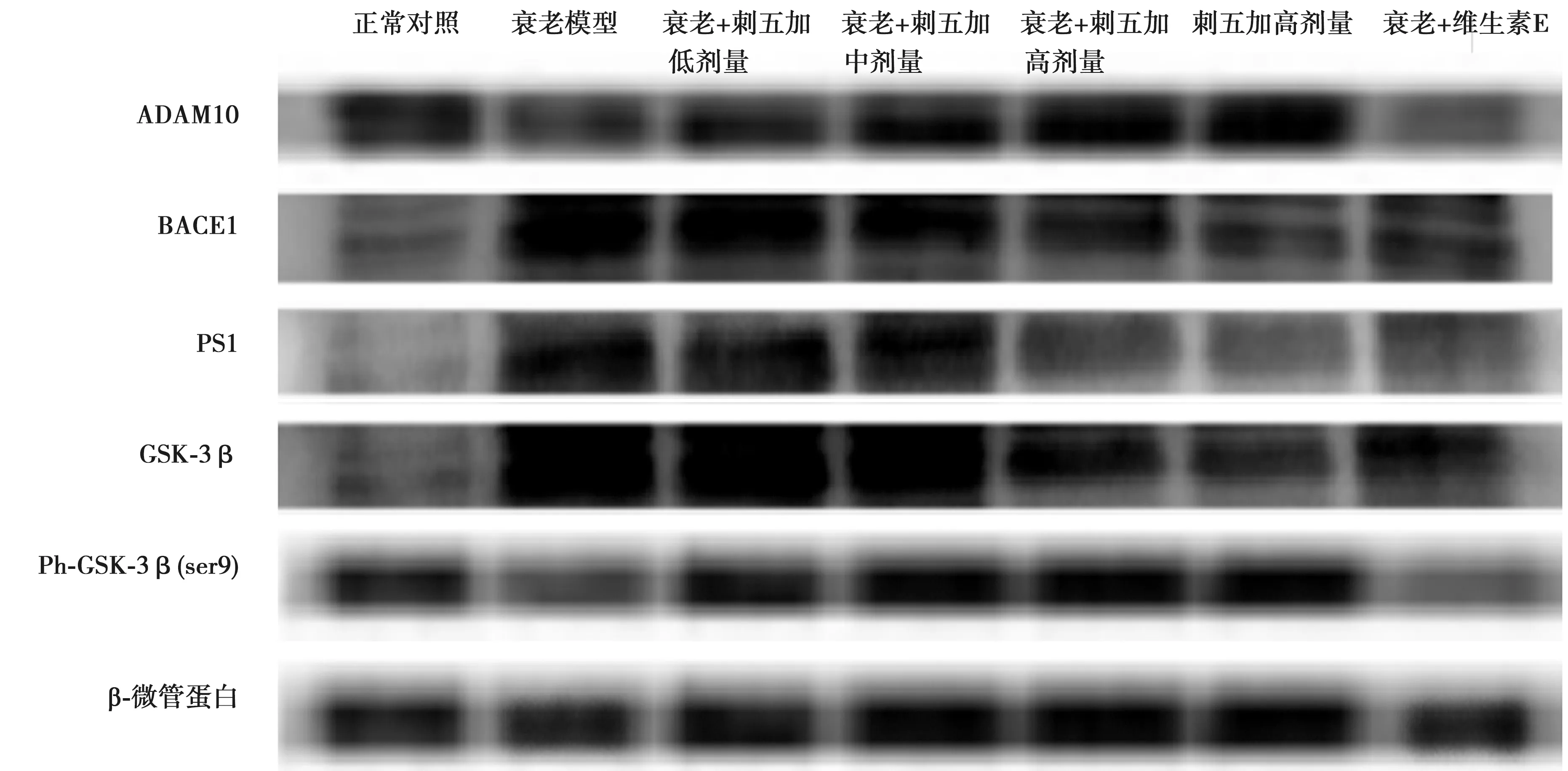
图2 各组ADAM10、BACE1、PS1、GSK-3β、Phospho-GSK-3β(Ser9)蛋白表达
组别 ADAM10BACE1PS1 GSK-3βPhospho-GSK-3β正常对照组0.61±0.040.36±0.030.22±0.020.65±0.040.48±0.02衰老模型组0.38±0.021)0.70±0.011)0.68±0.011)0.81±0.031)0.30±0.011)衰老+刺五加低剂量组 0.44±0.030.68±0.030.64±0.030.76±0.020.31±0.02衰老+刺五加中剂量组 0.51±0.012)0.52±0.022)0.56±0.020.70±0.020.38±0.01衰老+刺五加高剂量组0.58±0.042)0.38±0.042)0.39±0.042)0.65±0.012)0.40±0.012)刺五加高剂量组0.59±0.010.29±0.010.37±0.020.59±0.031)0.52±0.021)衰老+维生素E组0.41±0.030.40±0.032)0.40±0.032)0.62±0.030.42±0.022)
3 讨 论
APP酶解异常是AD病理机制的重要环节,Aβ大量累积最终导致AD的形成。应用D-半乳糖建立的衰老模型是AD的预防和治疗研究中一个极有价值的动物模型,D-半乳糖是体内一种还原糖,未代谢完全的半乳糖及其代谢物会堆积于脑组织,阻碍细胞的正常生物功能,造成细胞内氧自由基(ROS)升高、细胞脆性增加、损伤,最终使脑功能退化,认知损伤、Aβ沉积〔7,8〕。这种出现在生化和组织病理学方面的表现与在AD患者中观察到的神经退行性变化类似。因此,应用D-半乳糖建立的衰老模型已被广泛应用于研究AD的机制和药物作用评估。本研究使用D-半乳糖建立衰老模型基于Aβ假设模拟AD病理、生化和行为变化,是一个可靠的研究模型。
中草药因其多靶点、多环节、多途径的综合调控作用在疾病的预防和治疗中越来越受到关注,从中草药中寻找能够天然增加α-分泌酶活性的激活剂及 β、γ-分泌酶的抑制剂对预防AD至关重要。刺五加含有超氧化物歧化酶,有抗氧化、抗自由基的功能,也有增强免疫力的作用〔9〕,其含有的多种活性成分对中枢神经系统也具有重要的影响〔10〕。本实验提示刺五加提取液具有增加小鼠学习记忆保留时间,缓解衰老小鼠记忆障碍的功效。有研究表明,维生素E可通过抗氧化作用保护神经元,提高空间记忆能力〔11〕。
本研究显示,刺五加提取液可以抑制β、γ-分泌酶活性,促进α-分泌酶表达,进而减少Aβ1~42的产生,增加具有保护作用的sAPP生成。研究表明,硒、锌可以通过抑制β、γ-分泌酶的活性,激活α-分泌酶进而遏制过多的 APP 水解为 Aβ1~42〔12〕。本研究结果在病理机制上与其保持一致,刺五加提取液可干预APP酶解机制,对AD起预防和保护作用。
ADAM10为Aβ裂解过程中的组成α-分泌酶,在减少Aβ的生成中起关键作用。研究表明,无论是在体内还是体外,它在减轻AD的病理损害方面都发挥了有益作用,ADAM10不仅降低了Aβ的生成,还可能通过潜在的机制影响AD的病理学,包括抑制tau蛋白磷酸化,维持正常的突触功能,促进海马神经元网络的稳态〔13〕。 BACE1是产生Aβ的限速酶,抑制BACE1的酶活性可减少Aβ产生〔14〕。有研究表明,GSK-3β活化可抑制促神经元存活的转录因子,反之,其失活可促进神经元存活,提高细胞结构的稳定性。PS1是γ-分泌酶切割的作用位点〔15〕。很多研究均已报道GSK-3β与Aβ沉积有关,也可引起tau蛋白磷酸化水平升高〔16〕,因此,GSK-3β在AD病理作用中发挥重要作用。本实验提示刺五加提取液有抑制β、γ-分泌酶活性,增强α-分泌酶活性的作用。经刺五加提取液处理后,GSK-3β和其在Ser9位点的磷酸化水平较衰老组有所改善,提示刺五加可能具有调控 GSK-3β表达水平的功效,从而实现预防AD的目的。
体内和体外实验证明刺五加提取液对衰老模型小鼠的学习记忆障碍和脑组织中各种酶的活性变化有较好的保护作用,刺五加的保护作用机制可能是其抗氧化作用。综上,刺五加提取液对AD有一定的保护和治疗作用,其作用机制可能是通过调节APP酶解通路,减少Aβ的产生和沉积,改善衰老小鼠的学习记忆障碍,其更深层次的分子生物学机制有待研究。

