阿米福汀对局部晚期非小细胞肺癌患者肺功能及免疫功能的影响
阎保强
(河南省焦作市人民医院放疗科,河南 焦作 454002)
肺癌早期无典型征象与症状,确诊难度大,多数患者在确诊时已发展至局部晚期或晚期,失去最佳手术治疗机会,需采取放射治疗及化疗,且以根治性放射治疗为主,但随着根治性放疗的开展,患者所需放射性剂量增加,治疗带来的毒副反应随之加重[1]。为减少放射治疗带来的毒副反应,临床常在放射治疗前后联合其他药物治疗,阿米福汀目前已被美国食品药监局批准在放疗前后使用[2],以减轻放疗导致的毒副反应,但该药用于局部晚期非小细胞肺癌放疗后是否能增加放疗安全性,是否会对放疗效果产生影响,尚无定论,本研究将阿米福汀用于局部晚期非小细胞肺癌放疗前治疗,旨在观察药物对放疗近期疗效的影响,并分析药物对患者肺功能及免疫功能的影响,以指导临床。
1 资料与方法
1.1 纳入与排除标准
选择2017年1月—2019年1月我院收治的60例局部晚期非小细胞肺癌患者,全部患者均符合如下标准:纳入标准:①经细胞学或病理检查证实为晚期局部非小细胞肺癌;②接受胸部CT检查提示肿块均属于可评价病灶;③既往未接受其他放射治疗;④肝肾功能检查均符合放射治疗要求;⑤无远处转移灶;⑥肿瘤分期为Ⅱb~Ⅲb期。排除标准:①对研究所用药物有禁忌者;②意识不清或有语言沟通障碍,无法很好的配合治疗者。本研究获得我院医学伦理委员会批准同意。患者及家属对本研究内容知情并签署知情同意书。
1.2 一般资料
根据随机数字表法将患者分为对照组与治疗组,各30例。对照组男17例,女13例;年龄41~75岁,平均年龄(56.77±4.47)岁;疾病确诊时间2~10个月,平均确诊时间(4.57±2.34)个月;病理类型:10例鳞癌,13例腺癌,其他7例;临床分期:Ⅱb期4例,Ⅲa期10例,Ⅲb期16例。治疗组男18例,女12例;年龄40~75岁,平均年龄(57.02±4.51)岁;疾病确诊时间2~9个月,平均确诊时间(4.49±2.29)个月;病理类型:11例鳞癌,13例腺癌,其他6例;临床分期:Ⅱb期5例,Ⅲa期10例,Ⅲb期15例。两组一般资料比较,差异无统计学意义(P>0.05),具有可比性。
1.3 方法
对照组单纯接受放射治疗,治疗组在放射治疗基础上联合使用阿米福汀(注射用氨磷汀,美罗药业股份有限公司,国药准字:H20010403)。
1.3.1 放疗 Precise直线加速器由瑞典ELEKTA公司提供,使用3D-CRT方案,即三维适形放疗方案与Precise Plan计划系统,输出能量:6 MV,剂量:2.0 Gy/次,频率:1次/d,5次/周。癌总量:DT60~66 Gy,需6周完成;癌总量:DT54~60 Gy,需5.5周完成。
1.3.2 阿米福汀给予治疗组200~300 mg/m²阿米福汀,溶于0.9%氯化钠注射液50 mL内,在放疗前15 min静滴,15 min内滴完。使用阿米福汀前,为减少药物导致的恶心呕吐等情况发生,可给予患者5~10 mg地塞米松[远大医药(中国)有限公司,国药准字:H42021943] 或5-HT3受体拮抗剂。
1.4 近期疗效评价标准
参照WHO实体肿瘤近期疗效评价标准[3]:完全缓解(CR):全部可测量病灶完全消失且持续至少4周;部分缓解(PR):病灶较治疗前缩小≥30%且持续至少4周;疾病稳定(SD):病灶较治疗前缩小不足30%或增加不足20%;疾病进展(PD):病灶较治疗前增加>20%或有新的病灶出现。
客观有效率=(CR+PR)/总例数×100%。
1.5 观察指标
①肺功能:分别于治疗前、治疗结束时,使用肺功能仪(日产AS-600型)检测并比较两组患者肺功能,包括用力肺活量(FVC)、第一秒用力呼气容积(FEV1);②免疫功能:分别于治疗前、治疗结束时,抽取患者空腹外周静脉血3 mL,处理后使用血细胞分析仪检测其T细胞亚群,包括CD3+、CD4+、CD8+、CD4+/CD8+。③不良反应:参照WHO《抗癌药物急性及亚急性毒性反应分度标准》[4]:放射性肺炎、放射性食管炎、血液学不良反应等。
1.6 统计学方法
2 结果
2.1 疗效
治疗结束时,治疗组CR、PR、SD、PD分别为6例、11例、8例、5例,客观有效率为56.67%(17/30),对照组CR、PR、SD、PD分别为6例、10例、8例、6例,客观有效率为53.33%(16/30)。组间客观有效率比较,差异无统计学意义(χ2=0.067,P=0.795)。
2.2 不良反应
治疗组放射性肺炎、放射性食管炎、血液学不良反应发生率分别为23.33%(7/30)、20.00%(6/30)、30.00%(9/30),均低于对照组的 63.33%(19/30)、70.00%(21/30)、66.67%(20/30),差异有统计学意义(χ2=9.774、15.152、8.076,P均< 0.05)。
2.3 肺功能
治疗结束时,治疗组FVC、FEV1水平与治疗前比较,差异无统计学意义(P>0.05),但均高于对照组,差异有统计学意义(P<0.05)。见表1。
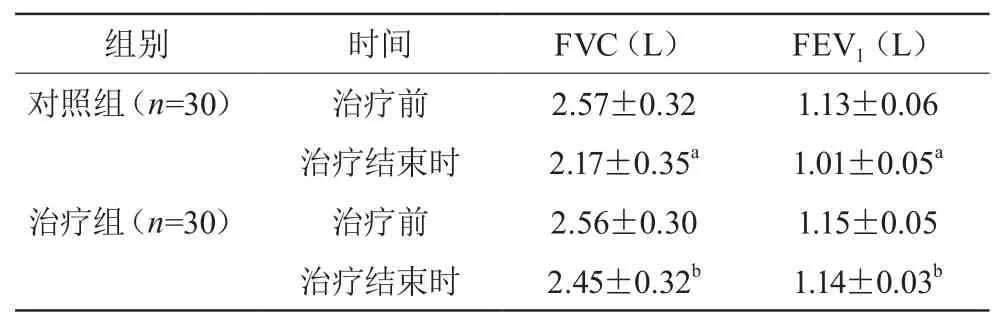
表1 两组治疗前后肺功能比较
2.4 免疫功能
治疗结束时,治疗组CD3+、CD4+、CD4+/CD8+水平均高于对照组,CD8+水平低于对照组,差异有统计学意义(P<0.05)。见表2。
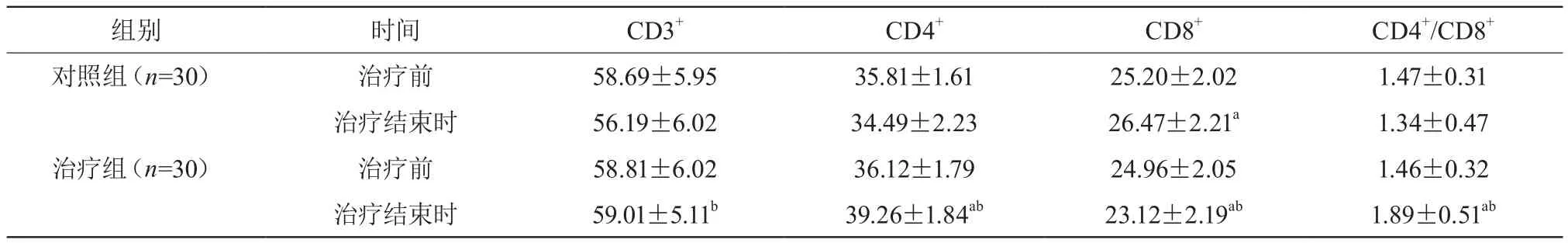
表2 两组治疗前后免疫功能比较
3 讨论
目前,为减少放疗带来的毒副反应,保护患者免疫机制不受影响,临床上提出两个主要手段,一是改良放疗技术,尽可能减少正常组织接受放射剂量,诸如现下流行的三维适形调强放疗;二是寻找安全有效的放疗保护药物,这类药物能减少放疗毒副作用,但不会对放疗效果产生影响[5]。
阿米福汀是目前广泛用于放疗细胞保护类药物,一开始作为预防核辐射保护剂使用,后被用于卵巢癌与非小细胞肺癌患者化疗及放疗中[6]。本研究结果显示,治疗组客观有效率与对照组比较差异无统计学意义,治疗期间治疗组放射性肺炎等毒副反应发生率均低于对照组,表明阿米福汀用于局部晚期非小细胞肺癌放疗并不会影响放疗效果,且在一定程度上可降低放疗的毒副反应,提高放疗安全性。此外,本研究结果显示,治疗组治疗期间肺功能指标变化程度小,且免疫功能指标均优于对照组,提示阿米福汀的使用不仅不会影响患者肺功能,还利于提高患者免疫功能,增强机体防御能力,提高放疗效果。究其原因为,阿米福汀是公认的放疗细胞保护剂,属于半胱氨酸化合物,能结合组织细胞膜表面碱性磷酸酶,发生磷酸化反应,生成活性代谢产物与WR-1065,WR-1065的游离硫醇不仅能直接结合铂类及烷化剂,还可清除自由基,进一步氧化生成与精胺及多胺类似的对称性二硫化物,松解DNA超螺旋结构;此外,WR-1065还可直接结合活化因子蛋白1、P53、转录因子核因子KB,增强调节性DNA列靶标与蛋白结合,激活下游基因,从而降低放疗毒副反应,在保护正常细胞的同时,增强机体防御能力[7-8]。
综上所述,晚期局部非小细胞肺癌患者放疗期间使用阿米福汀,利于减少因放疗带来的毒副反应,可提高患者免疫功能,且不会影响放疗效果及肺功能,安全可靠,值得推广应用。

