CT引导下经皮穿刺置管引流治疗60例细菌性肝脓肿的临床分析
彭建,郭鑫,赵子军,周彤
(1.仪陇县中医医院普通外科;2.仪陇县人民医院普通外科,3.仪陇县人民医院放射科;4.川北医学院胃肠外科,四川 南充 637000)
细菌性肝脓肿是肝胆外科常见的感染性疾病,如不及时有效治疗,患者的死亡率可高达 6%~14%[1]。抗感染并尽早行脓肿切开引流是有效治疗细菌性肝脓肿的关键。近年来,随着新材料、新技术的应用及微创手术治疗观念的普及,经皮穿刺置管持续引流成为治疗细菌性肝脓肿的首选术式[2]。本研究拟通过对60例细菌性肝脓肿患者临床资料的回顾,分析CT-PDLA治疗细菌性肝脓肿的疗效及安全性。
1 资料与方法
1.1 一般资料
收集2010年1月至2018年5月仪陇县人民医院普外科收治的60例细菌性肝脓肿患者的临床资料,其中男性37例(61.6%),女性23例(39.4%),平均年龄为(60.1±20.5)岁;入院时临床表现为发热56例(93.3%),寒战19例(31.6%),右上腹部疼痛46例(76.7%),感染性休克3例(5%);腹部超声检查提示肝脏脓肿31例(51.7%),腹部CT平扫检查提示肝脏脓肿45例(75.0%),其余15例经增强CT检查确诊为肝脏脓肿;合并糖尿病28例(46.7%),合并胆道感染18例(30.0%);肝右叶脓肿45例(75.0%),肝左叶脓肿9例(15.0%),居左右两叶者6例(10%);脓肿直径均≥5 cm(图1)。
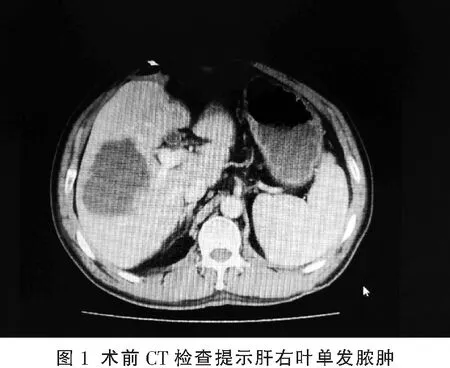
1.2 方法
1.2.1 手术方法 患者取平卧位或左侧卧位经CT定位扫描后,常规消毒、铺巾,用2%利多卡因对穿刺点皮肤作局部浸润麻醉,在CT引导下用COOK8.5 Fr穿刺引流套件行肝内脓肿穿刺,待穿刺针尖端位置准确置入脓腔(图2)后拨出针芯及支撑管,抽出少量(浅)黄绿色脓液,调整引流管远端位置并使其成攀。固定引流管,无菌包扎伤口,外接引流袋。穿刺抽出脓性液体送微生物室作细菌培养及药敏试验,以利于术后抗菌药物选择。
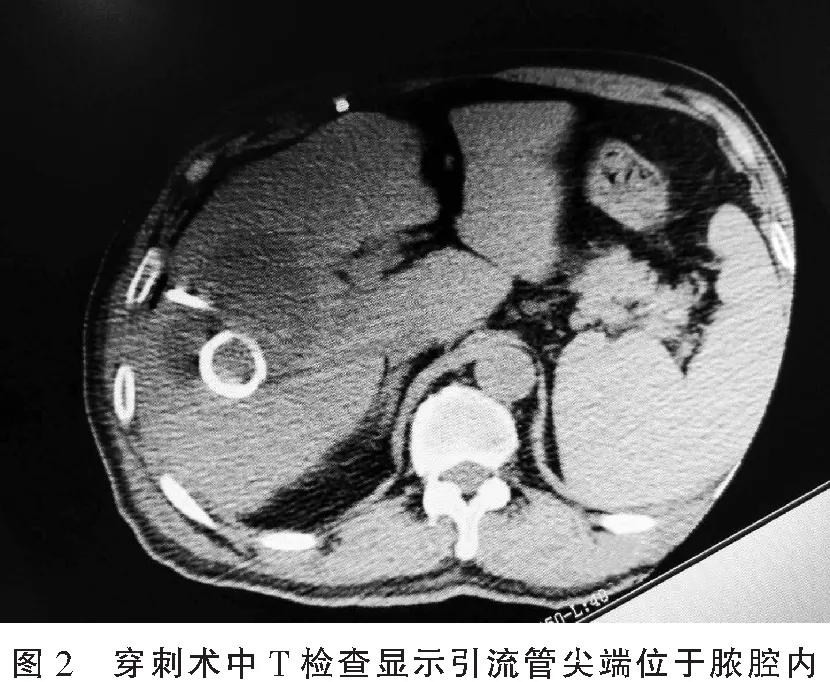
1.2.2 CT引导下肝脓肿穿刺定位要求 (1)选择通过部分肝脏组织的较短路径;(2)穿刺中避免损伤膈肌及肝内血管等组织器官,预防气胸及出血等并发症;(3)放置的脓肿引流导管位置需平、短、直、低,以利于通畅引流。
1.2.3 穿刺后治疗措施 (1)先用广谱抗生素联合抗厌氧菌抗生素联合治疗,待细菌培养及药敏试验结果明确后,再选用敏感有效的抗生素治疗;(2)加强营养支持治疗:补充足量维生素、蛋白质、热量;(3)对于引流不畅者,反复生理盐水冲洗脓腔;(4)对于穿刺后多发小脓腔,给予保守治疗。
1.2.4 拔管标准(1)复查血常规,白细胞及其中性粒细胞值正常;(2)停用抗生素后体温连续3 d或以上正常;(3)脓腔引流量每日<5 mL;(4)超声或者CT检查提示未见明显脓液(图3)。
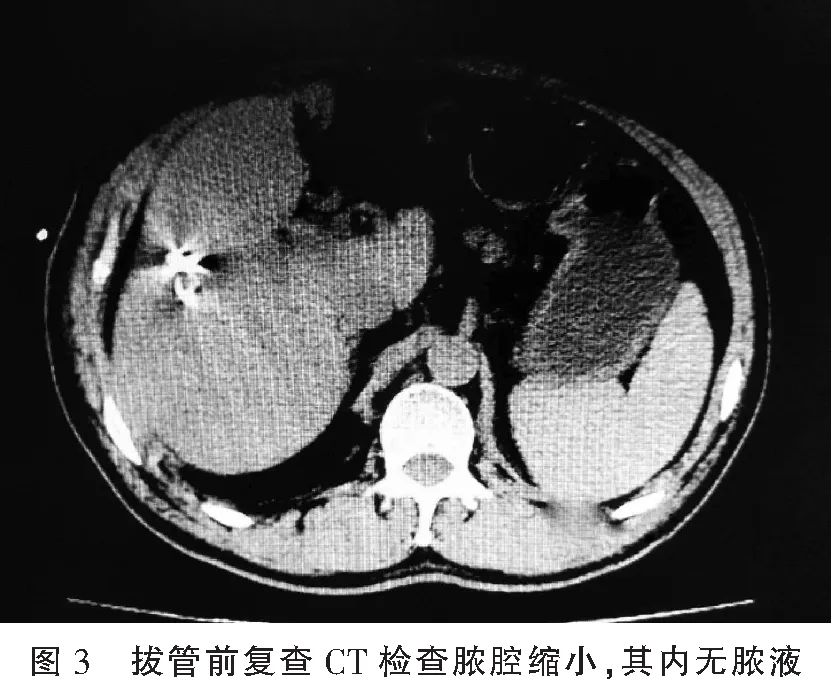
2 结果
60例细菌性肝脓肿患者均在CT引导下行经皮穿刺置管持续引流手术治疗,治愈57例(95.0%)。其余3例(5.0%)患者再行开腹脓肿切开引流术。其中,2例患者脓液粘稠,引流不畅,重新穿刺更换较粗直径引流管并给予生理盐水反复冲洗仍不能充分引流,观察治疗3 d后患者继续发热;另外1例为临近第二肝门的多发脓肿,穿刺引流较大脓肿后,患者仍发热。3例患者开腹手术后均痊愈。57例CT-PDLA患者平均住院时间(15.4±6.8)d,平均带管引流时间(25.6±11.3)d,术后无出血、胆瘘、气胸等严重并发症。
3 讨论
3.1 细菌性肝脓肿的病因及诊断
细菌性肝脓肿典型的临床表现:(右)上腹部疼痛,畏寒发热,体温可升高达40 ℃,伴有肝区叩击痛,血常规检查白细胞及中性粒细胞显著升高。再结合肝脏超声或者上腹部CT等影像学检查,细菌性肝脓肿诊断并不困难[3-4]。若患者同时合并糖尿病、胆道感染等疾病史或者有肝脏动脉化疗栓塞手术史[5],则更有助于细菌性肝脓肿的诊断。本组资料中,腹部CT平扫阳性诊断率(75.0%)明显高于超声检查(51.7%)。对于位置较深、脓肿较小、液化不明显者,则需增强CT检查才有助于肝脓肿的确诊。
3.2 PDLA治疗肝脓肿的优势
相较于开腹脓肿切开引流、腹腔镜下肝脓肿切开引流及肝部分(段)切除术,CT-PDLA治疗肝脓肿对机体创伤小、恢复快、住院时间短、费用低、切口感染率低、患者痛苦小等优势[6-7]。此外,CT-PDLA治疗肝脓肿还可反复多次穿刺。
3.3 PDLA治疗肝脓肿的手术时机
(1) 诊断确切的肝脓肿患者,单发病灶或多发脓腔相通病灶,脓腔直径>5 cm 以上,影像学提示脓腔液化良好,血象虽趋于下降,仍维持低烧者,应考虑尽快实施CT-PDLA,以避免因病情迁延导致的肝肾功损害、肺部感染等并发症的发生。穿刺引流使用的“猪尾管”应采用内径较粗的,有利于通畅引流。(2) 诊断确切的肝脓肿患者,其脓腔直径>5 cm单灶或多灶相通、血象及体温顽固性增高难以控制、全身消耗较大者,即使采用及时的全身营养支持,也会因肝肾功受损严重,对开放性手术的耐受性变差,如实施开腹肝脓肿切开引流术(incision and drainage for liver abscess,IDLA),则有导致患者肝肾功能衰竭,甚至全身衰竭的风险。因此,及时实施CT-PDLA,控制体温和血象,既可降低细菌性肝脓肿患者病情加重导致的死亡风险,也可避免IDLA带来的附加风险[8]。
3.4 细菌性肝脓肿病原菌分析
通过对60例患者血液及脓液病原菌培养分析发现,血液细菌培养率极低(5%),而脓液细菌培养率则明显较升高[9],达到43.3%。感染细菌以肺炎克雷伯菌为主(28.%),也有大肠埃希菌、金黄色葡萄球菌等,表明肺炎克雷伯菌已成为细菌性肝脓肿的优势菌[10-14]。
根据药敏结果显示,肺炎克雷伯菌对针对革兰式阴性菌的头孢菌素类、半合成青霉素类及喹诺酮类药物敏感,而大肠埃希菌则多耐药。
3.5 开腹肝脓肿切开引流手术适应症
60例患者中,有3例患者CT-PDLA治疗后,再行开腹脓肿切开引流,主要原因为: 2例患者脓液粘稠,引流不畅,重新穿刺更换较粗直径引流管并给予生理盐水反复冲洗仍不能充分引流,观察治疗3 d后患者继续发热;另外1例为临近第二肝门的多发脓肿,穿刺引流较大脓肿后,患者仍持续发热。因此,凡有下列情况者,宜作开腹脓腔引流手术[4,15]:(1)经置管穿刺引流术后仍持续发热,CT检查引流不畅者;(2)肝脓肿已破溃或有破溃危险,流入腹腔导致非手术难以控制的腹膜炎者;(3)脓肿位置较深,临近第一、二肝门,穿刺风险较大者;(4)肝脏多发脓肿,穿刺引流难以治愈者。
3.6 腹腔镜下肝脓肿切开引流手术适应症
相对于传统开腹手术,腹腔镜肝脓肿切开引流手术具有机体创伤小、切口感染率低、术后恢复快等优点[16]。其尤其适合位置表浅不易穿刺的单发性肝脓肿[17],如膈下脓肿。但随着腔内超声的广泛应用,腹腔镜下肝脓肿切开手术适应症逐渐放宽,为临床治疗肝脏脓肿提供更多选择。
3.7 肝部分(段)切除术治疗肝脓肿的手术适应症
肝部分(段)切除术治疗肝脓肿的手术适应症[18]:(1)慢性厚壁脓肿[19];(2)肝内胆管结石或胆管狭窄导致的胆源性肝脓肿;(3)液化不完全的局限性肝脓肿;(4)肝癌继发肝脓肿。肝部分(段)切除能完整切除脓肿,且可消除肝脓肿的诱发因素,是治疗的有效方法之一。但因其手术创伤大,手术时间长,加之肝脓肿患者一般情况差,难以耐受手术,故需慎重选择。
综上,随着影像学技术迅猛发展,利用影像学来进行辅助治疗已经成为常规的医疗手段,CT-PDLA因其有效性、安全性成为治疗细菌性肝脓肿首选术式,但其并非唯一选择。对于不适合作CT-PDLA患者,应根据病情,及时选择开腹或腹腔镜下肝脓肿切开引流术或肝部分(段)切除术,以免贻误病情。

