新型二维高效液相色谱测定人血清伏立康唑浓度方法的建立与应用*
王新茗,张仲林,袁明勇
1.成都医学院 药学院(成都 610500);2.成都医学院第一附属医院 药学部(成都 610500)
伏立康唑是三唑类的抗真菌药物,是氟康唑衍生物,具有抗菌谱广,抗菌效力强等特点,是治疗侵袭性念珠菌、曲霉菌的主要药物[1-2]。但伏立康唑受遗传代谢影响,个体间药动学参数差异较大,利福平、卡马西平、西咪替丁、他克莫司等许多药物会影响伏立康唑血药浓度[3],可能发生药物不良反应,且伏立康唑具有非线性药代动力学特征[4],因此对伏立康唑进行治疗药物监测(therapeutic drug monitoring,TDM)十分重要[5]。目前伏立康唑血药浓度检测方法多为高效液相色谱法和质谱法[6-7],质谱法具有极佳的检测灵敏度,但成本高,难以推广。传统高效液相色谱法具有一定经济性,但存在前处理复杂,色谱柱易被血清内源性物质损坏等问题。二维高效液相色谱通过技术及设备的改进,简化样品前处理过程,更为有效地解决复杂体系样品的分析问题,适用于高通量检测,被广泛应用于复杂样品及血药浓度分析[8]。本研究旨在建立快速、简便、准确的新型全自动二维高效液相色谱测定伏立康唑血药浓度的方法。
1 材料与方法
1.1 仪器
二维高效液相色谱(2D-HPLC)由FLC-2420全自动二维液相色谱耦合仪(湖南德米特仪器有限公司)和LC-20AT色谱模块(日本岛津)构成;SPD-10A检测器(日本岛津);TDZ4-WS 台式低速离心机(湖南湘仪实验仪器开发有限公司);XW-80A旋涡混合器(上海驰唐电子有限公司);Mini-15K微型高速离心机(杭州奥盛仪器有限公司);PWC124电子分析天平(英国艾德姆公司)。
1.2 药品与试剂
伏立康唑对照品(上海源叶生物科技有限公司,批号:J27M6F1,供含量测定用,含量98%);醋酸铵、三乙胺、三氟乙酸、高氯酸、磷酸铵均为分析纯;乙腈、甲醇均为色谱纯;空白马血清(Gibco)、空白血清和患者血清由成都医学院第一附属医院临床科室提供。
1.3 方法
1.3.1 色谱条件 第一维色谱系统(LC1)为岛津LC-20AT,第二维色谱系统(LC2)的色谱泵为岛津LC-20AT四元低压色谱泵。第一维色谱柱(LC1 column)为ASTON SC2柱(4.6 mm×25 mm,5 μm);流动相为V20 mmol/L磷酸铵∶V乙腈∶V甲醇=3∶1∶1,磷酸调pH=5.4),流速∶1.2 mL/min。第二维色谱柱(LC2 column)为SHIMADZU C18柱(4.6 mm×150 mm,5 μm);流动相为10 mmol/L醋酸铵(三乙胺调pH7.0)∶10mmol/L醋酸铵(三氟乙酸调pH3.0)∶甲醇∶乙腈=30∶10∶10∶50(V∶V∶V∶V),流速为1.0 mL/min,中间柱(Middle column)为ASTON SH柱(3 mm×10 mm,5 μm),辅助流动相为纯水。检测波长256 nm,运行时间9 min,温度:40 ℃,进样量:200 μL。检测流程:色谱耦合仪通过设置的时间程序,自动将色谱状态分为富集净化、捕获、转移和分析。富集净化:一维色谱柱对进样样品进行萃取和富集;捕获:目标物即将通过一维色谱柱时,中间柱开始截取与目标物有关的部分(中心切割技术);转移:中间柱将目标物转移至二维色谱柱;分析:二维色谱柱继续对样品分析,中间柱和萃取柱在LC1在线清洗(图1)。
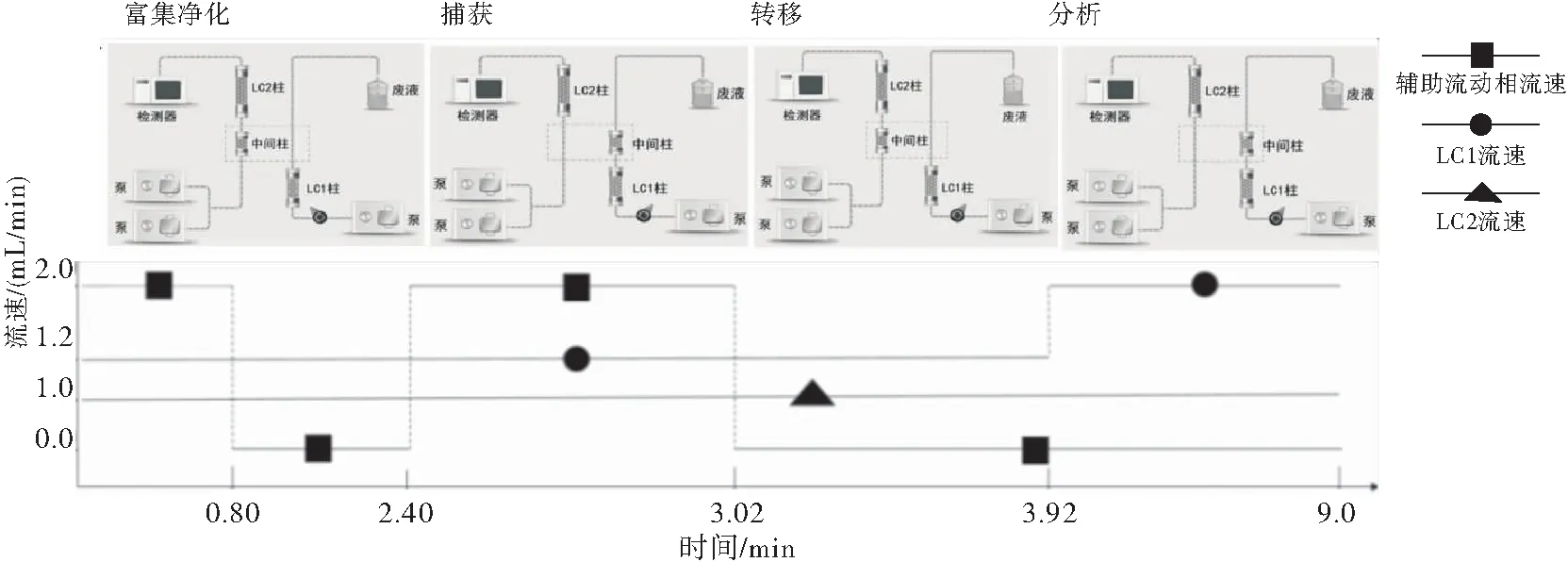
图1 FLC-2420分析过程及程序设置
1.3.2 对照品溶液的配制 精密称取伏立康唑对照品14.1 mg,用25%甲醇定容至10 mL,制得1.41 mg/mL对照品母液,取上述母液2 mL用25%甲醇再次稀释至10 mL得对照品溶液(282 μg/mL),置-20 ℃冰箱保存备用。
1.3.3 血清样品预处理 血液样品3 000 r/min离心5 min,离心半径12.3 cm,精密量取待测血清样品300 μL至1.5 mL的EP管,加入10%高氯酸900 μL,涡旋振荡30 s后,14 500 r/min,离心8 min,离心半径6 cm,取上清液1 000 μL至进样瓶,加入5.0 mol/L磷酸铵100 μL调节pH,涡旋振荡15 s,进样200 μL,以外标法定量分析。
2 结果
2.1 专属性考察
取空白马血清、对照品加空白马血清、空白人血清、患者血清,按“1.3.3”项下方法前处理后,按“1.3.1”项色谱条件进行分析,空白马血清、空白人血清在目标峰处无干扰,伏立康唑与杂质分离较好,保留时间为8.1 min。空白血清色谱图中此处未发现干扰,血清内源性物质及其他杂质已完全分离不影响样品的含量测定(图2)。
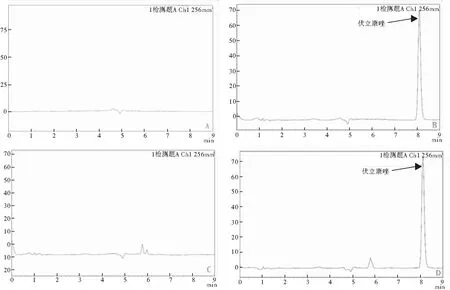
图2 伏立康唑高效液相色谱图 注:A:空白马血清;B:对照品+空白马血清;C:空白人血清;D:患者血清
2.2 基质效应
取空白人血清和空白马血清按“1.3.3”项下方法预处理后,加入适量母液配置成对应浓度样本(0.28、0.70、2.82、16.92 μg/mL),按“1.3.1”项下方法测得的峰面积与同浓度标准品的峰面积相比,计算基质效应,马血清与人血清基质效应符合要求,两者无明显差异(表1)。
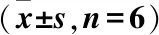
表1 基质效应考察结果
2.3 线性
用空白马血清将伏立康唑对照溶液稀释成系列浓度溶液(0.28、0.70、1.41、2.82、5.64、11.28、22.56 μg/mL),构成标准曲线的7个点,按“1.3.3”项下方法处理,“1.3.1”项下色谱条件分析,以伏立康唑的峰面积比值(Y)对伏立康唑浓度(X)进行线性回归,结果伏立康唑在0.28~22.56 μg/mL与峰面积呈良好的线性关系,其回归方程为Y=104 251X+8 279.72(r=0.999 9)。最低定量限为0.28 μg/mL(S/N>10,RSD<10%),检测限为0.04 μg/mL(S/N=3)完全满足临床伏立康唑血药浓度检测要求。
2.4 回收率与精密度
用空白马血清将伏立康唑对照品溶液稀释成高、中、低及定量下限(16.92、2.82、0.70、0.28 μg/mL)4个浓度的质控溶液,按“1.3.3”项方法处理样品,“1.3.1”项下色谱条件进样,每个浓度每日平行测定5份样品,连续测定3日,将测得的伏立康唑峰面积代入标准曲线方程,计算伏立康唑的精密度和方法回收率;将预处理后质控样品测得峰面积与同浓度标准品的峰面积相比,得提取回收率。本方法的日内、日间RSD均<9%,方法回收率99.01%~104.62%(RSD<9%),提取回收率>85%(RSD<8%),符合生物样品分析要求(表2)。
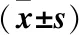
表2 血清中伏立康唑精密度(RSD)、方法回收率
2.5 转移稳定性试验
二维高效液相色谱将目标物从LC1转移至LC2的准确性和稳定性由转移回收率和转移精密度来表示,将282 μg/mL对照品母液在“1.3.1”项下的色谱条件进行检测,进样体积5 μL,得到的峰面积与在LC2模式下单独通过分析柱所得的峰面积进行比较,设置6组平行,计算转移回收率为98.31%,RSD为1.25%。表明二维高效液相色谱转移回收率高且稳定。
2.6 稳定性试验
取高、中、低及定量下限4个浓度的伏立康唑质控溶液各5份,在室温放置24 h,冷冻10 d及反复冻融3次取出复温,按“1.3.3”项操作处理后,按“1.3.1”项色谱条件测定,伏立康唑RSD均<9%,表明室温放置24 h、冷冻10 d及反复冻融3次对伏立康唑测定结果无影响,满足临床血药浓度监测。取“2.2”项高、中、低及定量下限4个浓度的伏立康唑质控溶液各5份,按“2.3”项操作处理后,室温放置24 h,RSD均<9%表明样品经处理后室温放置24 h对检测无影响(表3)。
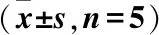
表3 稳定性试验
2.7 临床应用
案例1:患者刘某,男性,53岁,痰培养出白假丝酵母菌,使用伏立康唑胶囊(四川美大康华药业有限公司),首日400 mg po q12 h,序贯200 mg po q12 h,3 d后送检伏立康唑血药谷浓度,检测值为0.415 μg/mL,低于治疗浓度(1 μg/mL),请临床药师会诊,是否增加伏立康唑的剂量?临床药师会诊时发现患者有肺结核,正在使用利福喷丁,考虑伏立康唑血药浓度过低的原因可能是利福喷丁与伏立康唑的相互作用所导致,建议停用伏立康唑,更换成棘白菌素类的抗真菌药物。临床予以采纳,患者后续感染控制,好转出院。
案例2:患者杨某,女性,89岁,痰培养出克柔假丝酵母菌,使用伏立康唑(辉瑞),首日负荷剂量330 mg ivgtt q12 h,序贯200 mg ivgtt q12 h,用药第10 d出现精神、食欲、睡眠差,予以完善相关检查和对症处理后症状仍持续,请多学科会诊,临床药师会诊时发现患者合并使用奥美拉唑,奥美拉唑对CYP2C19具有抑制作用,可能升高伏立康唑血药浓度,导致神经系统不良反应,建议检测伏立康唑血药浓度。经检测该患者的伏立康唑血药谷浓度为17.78 μg/mL,远超过治疗参考谷浓度上限(5.0 μg/mL),建议暂停使用伏立康唑。患者停药后精神症状逐渐好转,未再进行抗真菌治疗,原发疾病治疗好转后出院。
该方法具有检测快速,操作简便,结果准确的特点,确定的线性范围能满足伏立康唑血药浓度监测需要,可以作为临床分析人血清中伏立康唑血药浓度的方法。
3 讨论
TDM起源于上个世纪八十年代,是临床药学一个重要分支学科[9]。TDM对提高药物治疗效果和预防不良反应的发生具有重要意义,是目前新形势下提升药学服务能力和开展个体化药物治疗的一项重要举措。
目前检测伏立康唑血药浓度的方法多为高效液相色谱法及质谱法[10-11],两种方法对样品纯净度要求高,而血液样本成分复杂,通常需要经过复杂的前处理才能进行检测,增加操作负担和误差。传统高效液相色谱法使用紫外检测器,检测灵敏度有时不能满足需要,需对样品进行氮吹、复溶等操作对样品进行富集[12],增加操作步骤及误差,也降低了报告的及时性;质谱法检测灵敏度能满足临床检测需求,但质谱仪价格昂贵,检测成本高,不适用于临床应用。
本研究建立的新型二维高效液相色谱测定伏立康唑血药浓度方法,利用全自动二维色谱高效的自动化在线样品处理能力,样品无需复杂的前处理,沉淀蛋白后直接进样,富集和净化均由二维色谱自动化完成,9 min即可完成萃取、转移及分析,能为临床快速出具检测结果。
传统高效液相色谱法多采用内标法进行定量,以消除样品前处理的误差。本方法由于样品进入分析柱前已净化,杂质干扰小,高度自动化也使人工操作误差降低,使用外标法就能进行精准定量,避免添加内标物的繁琐操作,也使临床批量样本检测时的可操作性更强。
二维高效液相色谱的一维流路和二维流路分别负责样品的萃取和分析,辅助流动相(水)受时间程序控制,在萃取和转移初期增加一维流路的极性,可将待测物富集于色谱中避免流失。故增加进样量不会影响峰型,且灵敏度会提高,使用紫外检测器就能满足检测需要,检测成本较质谱法和免疫法低,利于临床开展使用;样品进入分析阶段后,中间柱与萃取柱立即启动清洗程序,完成样品的检测后,色谱柱已清洗完成,可立即检测下一样品,保证本系统连续分析时的可靠性,缩短等待时间。
综上所述,该方法检测成本低、自动化程度高、检测快速、灵敏度及准确性好,可以满足临床报告及时性、准确性和测定范围等要求,可以作为伏立康唑TDM的有效方法。