皮质基底节变性1例报告
姜季委, 王一岚, 张 健, 王晓婷, 梁怡凡, 商秀丽
皮质基底节变性(corticobasal degeneration,CBD)是一组罕见的、隐匿起病慢性进展的神经系统变性疾病,发病率仅约4.9~7.3/10万[1]。CBD临床表现复杂多样且随病情进展不断变化,文献报道多为不对称的运动异常、局限性肌张力障碍、特征性肌阵挛、异己手、失用症、皮质感觉缺失以及痴呆等,但这些临床表现亦可出现在帕金森病(Parkinson’s diease,PD)或其他非典型帕金森综合征中[2]。与其他神经变性疾病相似,CBD的诊断仍以病理学为“金标准”,但研究表明仅有25%~56%临床诊断的患者可获得病理活组织检查印证[3,4]。由此可知,CBD因十分罕见,临床表现与其他帕金森综合征重叠,病理活检不易获取等多因素使其临床诊断具有重大挑战。我们查阅国内近些年关于CBD的文献发现,报道寥寥无几且就该病目前的临床诊断标准、新型辅助检查的把握仍不十分透彻[5,6]。因此,我们报道1例我院诊治的符合临床诊断标准的CBD患者,复习国外近年来相关文献,总结该病相对特异的临床表现和辅助检查选择,以提高临床对CBD的认识,减少漏诊与误诊。
1 临床资料
患者,男性,74岁,右利手,以“右侧肢体笨拙、僵硬5 y,进行性加重伴反应迟钝2 m”为主诉于2019年7月就诊于中国医科大学附属第一医院神经内科。患者5 y前无明显诱因出现右侧肢体笨拙、僵硬,走路不稳、前倾、明显缓慢,摔倒两次,伴右上肢运动性震颤,常发生于穿衣、用汤匙时,面部表情少,于当地医院诊断“帕金森病”,给予多巴丝肼125 mg每日3次口服,上述症状进行性加重,家属述其右上肢不愿活动,2 y前出现口齿不清、说话费力,紧张或有障碍物时出现双下肢特征性肌阵挛,数秒后好转,2 m前家属发现患者反应迟钝,记忆力明显下降,询问今年年份患者回复1999年,伴失眠、易激惹。患者病来无意识不清,无抽搐发作,无饮水呛咳及吞咽困难,无幻觉,无视物不清及视物成双,精神状态尚可,饮食可,偶有尿便失禁,近期体重未见明显下降。既往史:高血压10 y,平素血压控制在130/80 mmHg左右,否认糖尿病和冠心病病史;否认滥用药物史及毒物接触史;否认家族类似疾病史。神经查体:意识清楚,反应迟钝,构音障碍,声音低;双侧瞳孔等大正圆,D≈3.0mm,光反应灵敏,双眼水平运动充分,垂直运动欠充分(垂直注视麻痹),无眼震;面部表情减少,双侧额纹及鼻唇沟对称,伸舌居中;四肢肌力Ⅴ级,肌张力增高,右侧为甚,右侧齿轮样强直;不能按医嘱执行右手摸左耳(观念运动性失用),双下肢遇障碍物时剧烈抖动,约5~10 s可自行停止(刺激敏感性肌阵挛)(视频);BCR(L:,R:),TCR(L:,R:),PSR(L:,R:),ASR(L:,R:),Babinski征(L:-,R:-),掌-颌-唇反射阳性,痛温觉、振动觉、位置觉等未见明显异常,两点间辨别觉及图形觉减退,指鼻、轮替试验未见明显异常。
实验室检验未见明显异常。简易智力状况量表(mini-mental state examination,MMSE) 22分(时间定向1分,延迟记忆0分,语言0分),蒙特利尔认知评估(montreal cognitive assessment,MoCA):16分(视空间执行功能1分,延迟记忆0分,时间定向0分)。头部T1加权成像示:左侧额、顶、颞叶皮质较右侧明显萎缩(见图1)。头部MRI+DWI示:左侧额叶(额下回)、顶叶脑外间隙明显增宽,双侧颞叶萎缩,左侧为重(见图2)。脑血流灌注断层显像示:左侧额叶(下回为著)、颞叶、基底节区较右侧血流灌注量明显降低(见图3)。临床诊断:CBD,高血压2级(高危)。嘱患者3个月后神经内科门诊复诊。
2 讨 论
1968年,Rebeiz等人报道了3例以明显运动障碍、缓慢而笨拙的随意运动和姿势异常为特征表现且不同于既往报道的任何一种帕金森综合征的病例,首次明确地描述了CBD这一概念[7]。研究表明,CBD的诊断以病理学为“金标准”,其特征性病理改变为神经元和胶质细胞中高磷酸化的4-重复序列tau蛋白广泛沉积,并在星形细胞远端异常聚集形成星形细胞斑[8,9]。由于临床工作中病理活检较难实现,故而人们将病理学组织检查确证的诊断称为CBD,而未经过病理学活检印证仅临床诊断的称为皮质基底节综合征(Corticobasal Syndrome,CBS)[10]。2013年,Armstrong等人提出了新的CBD诊断标准,将其分为可能的CBD和很可能的CBD两类,强调CBD的临床症状与体征在诊断该病中的重要地位[11]。同时,目前国外研究显示降tau蛋白疗法已进入临床试验阶段,可能对CBD治疗有效[12,13]。因此,临床早期、准确识别CBD对减轻患者疾病负担,改善预后具有重大意义。
近年来,随着对CBD的不断认识与探索,研究发现CBD不仅仅局限于CBS一种临床表现,还包括额叶行为空间综合征,非流利性/语法缺失性原发性进行性失语以及进行性核上性麻痹综合征,共4种临床表型[14]。CBD的临床表现以运动症状与高级皮质病变相关症状的不同组合为特点。运动相关症状主要表现为非对称的耐左旋多巴的帕金森综合征,肌张力障碍和局限性特征性肌阵挛[15]。患者多以一侧肢体笨拙为初始症状,随后可伴有强直或震颤,区别于PD的静止性震颤,CBD的震颤可以是静止性、姿势性、运动性甚至无特殊定义的[2,15]。另一个值得注意的运动障碍表现即是肌阵挛,既往报道称约55%~93%的CBS可出现特征性肌阵挛[16],与皮质肌阵挛特点相似,CBD的肌阵挛多为活动诱发、刺激敏感,以局限性、小幅度、高频率和短暂性为特点,较常发生在上肢和面部[17]。然而,研究显示经典的神经生理学技术均未发现明确的皮质脊髓束参与CBD肌阵挛的证据,相反,皮质下运动系统、增强的长环反射通路的变性可能参与其中[18,19]。本例患者即以一侧肢体笨拙、运动缓慢起病,左旋多巴治疗无效,伴运动性震颤与刺激诱发的双下肢局限性特征性肌阵挛,与上述文献报道一致。
高级皮质病变主要表现为失用症、肢体异己征、皮质感觉缺失、认识障碍、行为改变以及失语等[20]。失用症是CBD的核心症状,最常见于观念运动性失用,偶有口颊失用和肢体运动失用的报道[21]。肢体异己征最常见于上肢(即异己手),表现为复杂的无意识的干扰正常工作肢体或感觉肢体是外来的,有自己的意志,但目前有关导致异己手的原因尚不十分清楚,有报道认为与顶叶、中央后回、原发性感觉皮质后部以及第三感觉皮质病变导致自我属性功能紊乱有关[21,22]。失语在CBD患者中亦可见报道,多为原发性进行性失语、进行性失语、进行性非流利性失语,随着疾病的进展可能完全失去语言功能[10]。有研究发现这种失语可能与右侧肢体运动障碍累及大脑左侧半球有关[23]。此外,研究表明超过半数CBD患者起病时即存在认知障碍,70%患者在病程中出现,多为明显的近期记忆受损,执行、语言和视觉空间域记忆受累,而情景记忆相对保留[24];行为异常,如淡漠、人格变化、易怒、临床抑郁状态亦可见报道;这是临床常与阿尔茨海默病混淆的重要原因[25]。
本患发病年龄>50岁,隐匿起病,缓慢进展,症状持续5 y,否认遗传史和类似疾病家族史;临床表现为非对称的耐左旋多巴的肢体强直和运动迟缓、刺激敏感性肌阵挛、观念运动性失用、皮质感觉缺失(图形觉与两点间辨别觉)、伴认知障碍与抑郁状态,与Armstrong等人提出的很可能的CBD诊断标准一致[11]。虽然上述诊断标准拓展了人们对CBD临床表型的认识,目前应用较为广泛,但Alexander等人后期通过对该诊断标准的印证发现其并未明显增加CBD诊断的特异性[26]。因此,有效的生化指标以及神经影像学特异性的探索对于早期识别该病十分必要。
既往研究表明,CBD疾病早期头部CT或MRI通常无明显异常;随着病情进展可有不对称(受累肢体对侧)的额、顶叶皮质以及基底节区萎缩,伴或不伴同侧侧脑室扩张[27]。
其他帕金森综合征,如进行性核上性麻痹常表现为中脑和被盖区萎缩伴第三脑室扩张,轴位观上丘水平中脑前后径缩小(“米老鼠征”),上部中脑扁平或凹陷,而脑桥相对保留(“企鹅征”);而AD多为双侧对称的颞叶、海马萎缩[28]。众所周知,核医学成像技术利用不同放射性标记配体来量化脑内区域代谢、血流灌注、受体或转运体的淀粉样蛋白沉积在神经系统变性疾病应用较为广泛,目前以单光子发射计算机断层扫描(single-photon emission computed tomography,SPECT)和18氟脱氧葡萄糖代谢正电子发射断层扫描(18furodeoxyglucose positron emission tomography,18F-FDG-PET)最常见[29]。上个世纪末,PET和SPECT诊断CBS的主要证据为额顶叶、基底节区与丘脑血流灌注与葡萄糖代谢的不对称减低[30];而近几年,研究发现CBD患者双侧额顶叶皮质,皮质下结构尤以尾状核、壳核为甚均可出现低代谢和低灌注,但临床受累肢体对侧脑区更为显著[31,32]。
目前,新型的核医学成像技术应用在CBD的诊断亦可见部分报道,如利用特异的SPECT(多巴胺转运体成像或D2受体成像)探究CBD患者尾状核和壳核多巴胺功能的不对称下降及高度变异性,疾病早期突触前黑质纹状体功能可保留,而疾病晚期多巴胺转运体活性降低,纹状体D2受体结合数目不对称性减少,这也解释了为什么多巴胺治疗对CBD患者的运动症状无明显效果[33,34];11CN-甲基哌啶-4-基乙酸显像PET提示CBS患者在旁中央区、额叶、顶叶和枕叶皮质胆碱能传递活性改变[35];18F-AV-1451和18F-THK5351显像PET发现受累肢体对侧脑区维持高tau结合率[36,37]。然而,尽管各种新型核医学成像技术在辅助CBD诊断的报道层出不穷,但其实用性均缺乏大型的临床研究证实,相比而言经典的18F-FDG-PET虽可见较多报道,但其成本效益分析、用于临床诊断CBD的价值仍缺乏研究证据支持[29,38]。因此,考虑目前国内外对诊断CBD核医学影像技术的研究进展,我国医疗国情以及神经影像在诊断CBD的辅助价值,我们仅对该患者完善头部MRI+DWI,脑血流灌注成像评估脑功能,检查提示受累肢体对侧(左侧)额顶叶、颞叶明显萎缩,额叶、颞叶上部以及基底节区脑血流灌注明显低于右侧,其病变与临床症状和体症呼应,与既往文献报道一致。
综上,与其他非典型帕金森综合征不同,CBD多以不对称的高级皮质受累和基底节区病变为主要表现,神经影像学多提示受累肢体对侧皮质(额、顶叶多见)和基底节区明显萎缩、血流灌注与葡萄糖代谢减低。虽然CBD的诊断仍以病理学为“金标准”,但加强对其临床表型的认识,早期准确识别该病对于减轻患者疾病负担、改善预后具有重要意义。未来期待开展更多关于CBD特异性生物学标志物及核医学成像实用性的研究。

A:矢状位示额、顶叶处脑沟池裂明显增宽;B:冠状位示双侧额叶萎缩,左侧较右侧尤以额下回蛛网膜裂隙明显增宽;C:冠状位示左侧额、顶叶蛛网膜裂隙较右侧明显增宽,提示左侧额、顶、颞皮质明显萎缩
图1 头部磁共振T1加权成像

A~E:双侧额、颞叶脑沟池裂明显增宽,左侧明显重于右侧;F~J:左侧额叶(额下回明显)、顶叶脑外间隙明显增宽,提示左侧额、颞、顶叶皮质明显萎缩;D、E、I、J:头部DWI与ADC图示未见弥散受限信号
图2 头部磁共振平扫+弥散加权成像
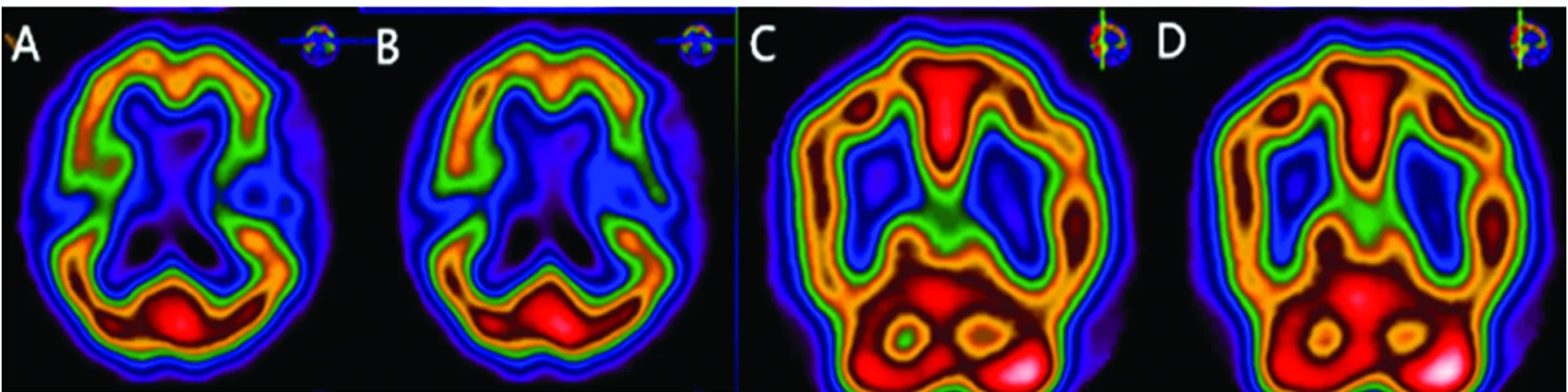
A,B:平均脑血流量:右半脑 34.4 ml/100 g·min,左半脑 30.0 ml/100 g·min;局部脑血流量:右额叶49.96 ml/100 g·min,左额叶36.76 ml/100 g·min,右颞叶56.89 ml/100 g·min,左颞叶47.75 ml/100 g·min;C,D:右基底节:65.29 ml/100 g·min,左基底节56.19 ml/100 g·min;提示左侧额叶(下回为著)、颞叶、基底节区较右侧血流灌注量明显降低
图3 脑血流灌注断层显像

