白藜芦醇与呋咱氮氧化物偶联物的合成及抗肿瘤活性研究
戴 一,曹殿洁
1安徽新华学院药学院,合肥 230088;2中国科学技术大学化学系,合肥 230036
白藜芦醇为一多羟基茋类化合物,存在于多种植物中如葡萄、花生及中药虎杖等[1]。白藜芦醇具有多种药理活性如心脏保护[2]、神经保护[3,4]及抗抑郁作用[5]等。近年来,白藜芦醇作为抗癌成分引起了广泛地关注。白藜芦醇通过作用多靶点如P53、Bax/Bcl-2、Caspase-9、、PARP、Cyclins、cdks、MAPK、 PI3K/AKT、JAK、NF-κB、AP-1、MMP-2、VEGF等抑制肿瘤细胞增殖、诱导细胞凋亡及阻滞肿瘤转移等[6,7]。一氧化氮(NO)是一气体信使分子,生物活性多样[8],高剂量NO(微摩尔浓度)可以抑制肿瘤生长[9]及逆转肿瘤的多药耐药性[10].鉴于NO为活泼性气体且不易操作,因此NO的使用多为一些能在体内产生NO的化合物即NO供体,呋咱氮氧化物即是一类NO供体,且对酸碱比较稳定,在体内巯基化合物的作用下释放出NO。多药联合是抗肿瘤的有效方法[11]。本实验设计合成了白藜芦醇与呋咱氮氧化物偶联物,并进一步采用MTT法评价了设计化合物的抗肿瘤活性,为白藜芦醇与NO供体的一体化研究开发提供参考。
1 材料与方法
1.1 仪器与试剂
BruckerACF-300型核磁共振仪(美国布鲁克科技有限公司),API3000质谱仪(美国PE公司),bio-rad mode 680酶标仪(美国伯乐生命医学产品有限公司),白藜芦醇(纯度大约98%)即化合物1,购与大连美仑生物技术有限公司。DEME培养基购于hyclone公司,胎牛血清FBS购于lonsera公司,MTT 购置于碧云天公司,其他试剂均为分析纯。
1.2 受试细胞株
人肝癌HepG2细胞、人乳腺癌MCF-7细胞及人肺癌A549细胞来自于ATCC(美国)。
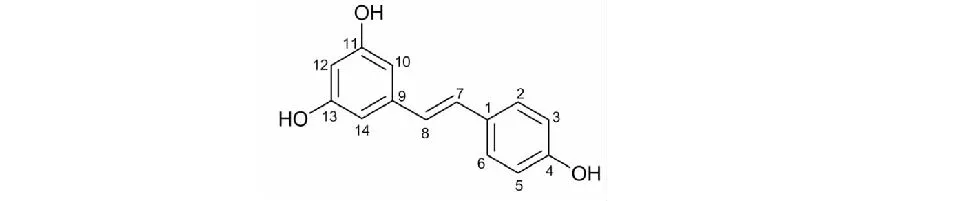
图1 白藜芦醇(化合物1) 结构Fig.1 The structure of resveratrol(compound 1)
1.3 结构修饰路线
以肉桂醇为底物,首先合成呋咱氮氧化物2,再与丁二酸酐反应引入羧基制得化合物3,化合物3在EDCI,DMAP条件下与白藜芦醇酚羟基成酯制备出白藜芦醇与呋咱氮氧化物偶联物(化合物4),见图2。产物经NMR、MS确认结构。
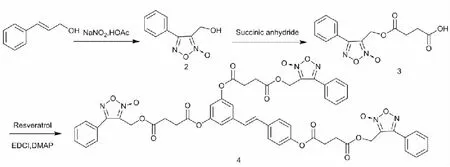
图2 白藜芦醇呋咱氮氧化物偶联物合成路线图Fig.2 The synthesis of conjugente of resveratrol and furoxans.
1.4 化学合成
1.4.1 化合物2的合成[12]
取肉桂醇(5.37 g,40 mmol)溶于8 mL冰乙酸中,往其中滴加120 mmol NaNO2饱和水溶液10 mL,温度不超过70 ℃,滴加完毕,室温继续搅拌1 h,加水100 mL,用乙醚萃取3次,乙醚层合并,用饱和食盐水洗涤3次,无水硫酸钠干燥,过滤,硅胶柱层析,以石油醚-乙酸乙酯(4∶1)洗脱,得浅黄色固体产物,收率为67%。
1.4.2 化合物3的合成
取化合物2(384 mg,2 mmol)溶于20 mL二氯甲烷中,加丁二酸酐(300 mg,3 mmol),DMAP(22.9 mg,0.2 mmol),室温反应,TLC跟踪,反应完毕,稀盐酸洗涤,冰水洗涤,无水硫酸钠干燥,过滤,浓缩至干,得灰白色固体,收率为86%。
1.4.3 化合物4的合成
取白藜芦醇(228 mg,1 mmol),化合物3(1.168 g,4 mmol),EDCI(1.712 g,9 mmol),DMAP(741 mg,6 mmol)溶于20mL丙酮中,室温搅拌反应,TLC跟踪,反应完毕,减压旋蒸除去溶剂,以乙酸乙酯溶解,分别以稀盐酸、饱和碳酸氢钠溶液及饱和食盐水洗涤,无水硫酸钠干燥,TLC分析(展开剂为石油醚∶乙酸乙酯=1∶1,主斑点Rf=0.3),过滤,粗产物过硅胶柱,以石油醚∶乙酸乙酯=2∶1洗脱,得白色固体,收率为64%。
1.5 白藜芦醇与呋咱氮氧化物偶联物体外NO释放[13]
1.5.1 NO 标准曲线绘制
取96孔板,各孔中分别加入稀释好的不同浓度NaNO2标准溶液(250、125、62.5、31.25、15.63、7.81、3.91 μM) 50 μL,复孔3个,再分别加入Griess试剂(含1.0%磺胺、5.0%磷酸、0.1% N-1-萘乙二胺盐酸盐水溶液)孵育10 min后于540 nm测定吸光度,绘制标准曲线,计算回归方程。
1.5.2 白藜芦醇与呋咱氮氧化物偶联物体外NO释放
化合物2、3、4分别溶于PBS(50 mM,pH7.4)/DMSO (1∶1)混合溶液均制成500 μM浓度,加入L-半胱氨酸 (5 mM) 溶液后于37 °C 避光孵育24 h。取样点样品按照1.5.1法置96孔板后加入Griess试剂(含1.0%磺胺、5.0%磷酸、0.1% N-1-萘乙二胺盐酸盐水溶液)孵育10 min后于540 nm测定吸光度,计算24 h NO的释放浓度。
1.6 白藜芦醇与呋咱氮氧化物偶联物抗肿瘤活性研究
取对数生长期细胞培养于96孔板中,每孔加培养基100 μL(约含3 000个细胞),于37 ℃,5% CO2的全湿条件下培养,培养12 h后给不同浓度的待测化合物,平行3个孔,阴性对照组加给药组等体积的培养基,以DEME 培养基作为空白对照组,给药后继续培养48 h,弃去培养液,每孔加5 mg/mL的MTT溶液20 uL,继续孵育4 h,弃去上清液,每孔加入DMSO 150 uL,震荡10 min,酶标仪570 nm测定吸光度OD值,计算抑制率及IC50值。
抑制率(%)=[1-(A实验组-A空白组)/(A对照组-A空白组)]×100%
2 结果与分析
2.1 化合物表征
化合物2浅黄色固体,TLC分析Rf约0.6(展开剂为石油醚∶乙酸乙酯=2∶1);1H NMR (300 MHz,Chloroform-d) δ 7.91~7.79 (m,2H),7.66~7.50 (m,3H),4.77 (s,2H),2.64 (brs,1H),与文献一致[11]。
化合物3为白色固体,TLC分析Rf约0.2(展开剂为石油醚∶乙酸乙酯=2∶1);1H NMR (300 MHz,Chloroform-d) δ 7.79~7.66 (m,2H),7.67~7.47 (m,3H),5.19 (s,2H),2.77~2.60 (m,4H),与化合物2比较分析,结构正确。
化合物4白色固体,TLC分析Rf约0.3(展开剂为石油醚∶乙酸乙酯=1∶1);mp.119~121 ℃;UV (MeOH)λmax (logε) 231 (4.06),274 (3.78),299 (3.80),311 (3.79) nm;IR (KBr)νmax3010,2821,1751,1684,1523,1495,1397,1335,1187,1050,913,868,790,659 cm-1;1H NMR (300 MHz,Acetone-d6) δ 7.97-7.87 (6H,m,Ph-H(6),7.79~7.60 (11H,m,Ph-H(9,H-2,6),7.46~7.17 (6H,m,H-3,5,8,10,12,14),6.93 (1H,d,H-7),5.38 (6H,s,O-CH2-),3.08~2.95 (6H,m,-CH2-CH2-),2.94~2.83 (6H,m,-CH2-CH2-);13C NMR (100 MHz,Acetone-d6) δ 171.4 (CO),170.4 (CO),157.3 (C=N-O),151.6 (C-11,13),150.8 (C-4),139.7 (C-9),134.6 (C-1),131.3 (Ph-C) ,129.7 (C-2,6),129.4(Ph-C) ,127.8 (Ph-C),127.7(C-7),127.0 (C-8),126.3 (Ph-C) ,122.0(C-3,5),117.0 (C-10,14) ,114.6(C-12),111.7(C=N=O),54.5(-CH2-O),28.8(-CH2-CH2-),28.6(-CH2-CH2-);m/z (ESI-MS) 1 068.9[M+H2O]+,1 073.7[M+Na]+,综合分析为预期化合物4。
2.2 白藜芦醇与呋咱氮氧化物偶联物体外NO释放
2.2.1 NO 标准曲线绘制
采用Griess法测定不同浓度NaNO2标准溶液吸光度,绘制标准曲线,计算回归方程为y=0.004 3x+0.046 5,r=0.999 5。表明NaNO2在250~3.91 μM浓度范围内线性关系良好。
2.2.2 白藜芦醇与呋咱氮氧化物偶联物体外NO释放
考察白藜芦醇偶联物4及中间体化合物2、3的NO的释放情况,结果见图3,在过量半胱氨酸存在下,24 h内化合物4释放较高浓度的NO,达到70.7 μM,为化合物3释放的近3倍,为其抗癌活性的发挥奠定了基础。
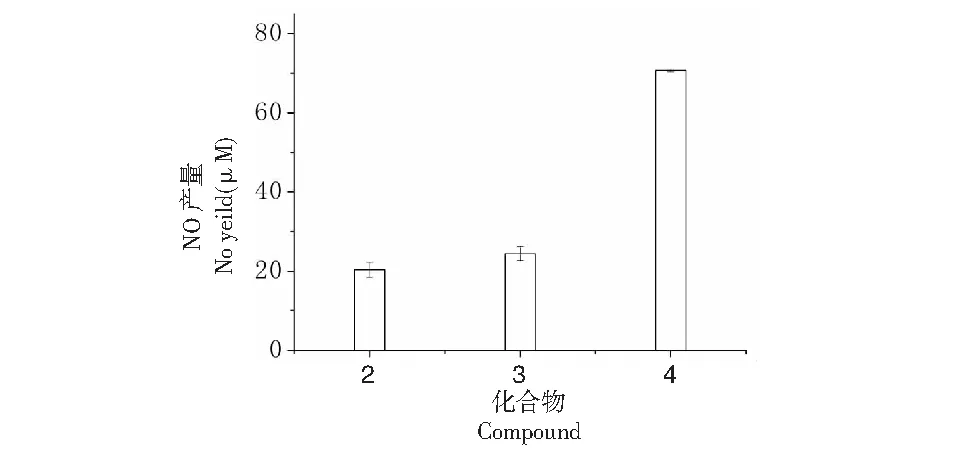
图3 白藜芦醇呋咱氮氧化物偶联物及相关中间体的NO释放研究Fig.3 The releasing of NO of conjugate of resveratrol and furoxans and related intermediates
2.3 白藜芦醇与呋咱氮氧化物偶联物抗肿瘤活性研究
对化合物1、3和4及由化合物1和3按1∶3摩尔比组成的混合物进行MTT抗癌活性实验,结果如图4所示。对A549细胞、HepG2细胞及MCF-7细胞,化合物4均表现出较强的肿瘤抑制活性,IC50值分别为21.65、10.44和41.40 μM,相比于母体化合物1(对同样细胞IC50值分别为67.48、133.15和95.01 μM)、化合物1+3混合物(对同样细胞IC50值分别为43.94、100.93和57.74 μM)及化合物3(对同样细胞IC50值大于400 μM)活性显著提高,可见,白藜芦醇与呋咱氮氧化物进行偶联,具有较强的协同效果。因此白藜芦醇进行NO供体化修饰是发现先导化合物的一条有效途径。

图4 白藜芦醇呋咱氮氧化物偶联物及相关化合物MTT实验结果Fig.4 The results of MTT for conjugate of resveratrol and furoxans and related compounds
3 结论
白藜芦醇为一多功能植物成分,尤其是在抗癌活性领域研究较为活跃;NO为一重要的气体信使分子,与肿瘤的发生发展密不可分,而高浓度NO可以抑制肿瘤的生长,本实验通过把白藜芦醇与NO供体呋咱氮氧化物进行共价结合制备了化合物4,该偶联物对三种肿瘤细胞A549、HepG2及MCF-7均表现出较强肿瘤抑制活性,IC50值分别为21.65、10.44和41.40 μM,相比于母体化合物肿瘤抑制活性有了明显的提高,为白藜芦醇的NO供体化开发提供了参考。

