酸酯碱成分结合指纹图谱优选盐黄柏炮制工艺
程中琴,刘小妹,施崇精,王姗姗,盛 蓉,袁强华,宋 英
1成都中医药大学药学院,成都 610075;2成都中医药大学附属医院,成都 610072
黄柏来源于芸香科植物黄皮树PhellodendronchinenseSchneid.的干燥树皮。习称“川黄柏”[1]。始载于《神农本草经》,列为上品。[2]该药味苦、性寒,归肾、膀胱经。具有清热燥湿,泻火除蒸,解毒疗疮之效。用于湿热泻痢、黄疸、带下、热淋、脚气、骨蒸劳热、盗汗、遗精、疮疡肿毒、湿疹瘙痒等病的治疗,为临床常用药[3]。传统理论认为生黄柏性味苦寒,清热燥湿、泻火解毒作用强,但苦寒过甚,应用不当易伤脾胃;盐炙后可缓和苦寒之性,不易伤脾胃,并借盐引药入肾之功而增强滋阴泻相火之力[4]。根据2015年版《中国药典》的附录ⅡD盐水炙法中对盐制黄柏规定:“取净药材,加盐水拌匀,闷透,置锅内,以文火加热,炒至规定的程度时,取出,放凉。每100 kg净药材用食盐2 kg。”[1]但对黄柏的盐制工艺如炮制温度和时间、炒药量并未做明确规定。本文以指纹图谱全面反映药材的化学成分,以盐黄柏中三大类主要成分(生物碱和酸类、酯类)为指标,定性定量的分析不同炮制工艺,以期为进一步规范黄柏盐炙工艺,确保良好的临床效果。通过探讨影响黄柏盐炙工艺的几个因素,为制定黄柏盐制的合理炮制工艺标准提供科学依据。
1 仪器与试药
1.1 仪器
1260-Ⅱ型HPLC仪,包括四元泵、DAD检测器、在线脱气装置、Openl AB工作站(Agilent公司,美国);BP211D型十万分之一电子分析天平(Mettler-Toledo公司,瑞士);AS20500BD 型超声清洁仪(天津奥特赛恩斯仪器有限公司);CXP-500A 型高速多功能粉碎机(上海市晟喜制药机械有限公司);MS-5型炒货机(迈斯机械)。
1.2 试药
对照品盐酸小檗碱(批号:15401-69-1,纯度98.0%),盐酸小檗红碱(批号633-65-8,纯度为 98%),巴马汀(批号10605-02-4,纯度98.0%),木兰花碱(批号:2141-9-5,纯度98.0%),黄柏内酯(批号:1180-71-78,纯度99.03%),异绿原酸B(批号:1453461-3,纯度98.97%),3.5-O-二咖啡酰奎宁酸(批号:89919-62-0,纯度99.25%),均购自成都植标化纯生物技术有限公司;盐酸黄柏碱(批号:111895-201504,纯度94.9%),盐酸药根碱(批号:110733-201609,纯度89.5%),均购自中国食品药品检定研究院。生黄柏(批号:170721),由四川省中药饮片有限责任公司提供,经成都中医药大学附属医院盛蓉主任药师鉴定为芸香科植物黄皮树的干燥树皮。乙腈、甲醇(天地公司,美国,色谱纯),水为纯化水(怡宝水),未加碘精制盐(厂家:中盐榆林有限公司;批号:201707041S)其余试剂为分析纯。
2 分析方法与结果
2.1 含量测定方法
2.1.1 对照品溶液的制备
精密称取盐酸小檗碱、木兰花碱、盐酸小檗红碱、黄柏碱、巴马汀、药根碱、3.5-O-二咖啡酰奎酸、异绿原酸B、黄柏内酯25.46、10.88、7.51、9.66、10.10、11.09、8.55、6.43、9.25 mg,分别置 10 mL 量瓶中,用甲醇溶解并稀释至刻度,摇匀,即得各对照品储备液。精密移取各生物碱对照品储备液1 mL,置 10 mL 量瓶中,用甲醇稀释至刻度。得到盐酸小檗碱、木兰花碱、盐酸小檗红碱、黄柏碱、巴马汀、药根碱质量浓度分别为249.5、106.6、73.6、91.7、99.0、99.1 μg/mL 的混合对照品溶液。置4℃的冰箱中保存备用。
2.1.2 HLPC色谱条件
色谱柱:Inertsil ODS-3 5 μm 4.6×250 mm;流相:乙腈A-0.1%磷酸B(15∶85、PH=2.10),进行梯度洗脱(见表1);柱温:30 ℃;流速:1.0 ml/min,进样量:5 μL;检测波长:327 nm。

表1 梯度洗脱表

图1 不同炮制温度下盐黄柏三类主要成分HPLC指纹图谱Fig.1 HPLC fingerprint of three main components of Phellodendron chinensis under different processing temperatures注:S1 120 ℃;S2 140 ℃;S3 160 ℃;S4 180 ℃;S5 200 ℃;1 异绿原酸B;2 3.5-O-二咖啡酰奎酸;3黄柏内酯;4黄柏碱;5木兰花碱;6药根碱;7巴马汀;8盐酸小檗红碱;9盐酸小檗碱。Note:S1 120 ℃;S2 140 ℃;S3 160 ℃;S4 180 ℃;S5 200 ℃;1 Isochlorogenic acid B; 2 3.5-Isochlorogenic acid;3 obakulactone;4 Phellodendrine;5 magnoflorine;6 jateorhizine;7 palmatine;8 berberubine;9 berberine.
2.1.3 供试品溶液得制备
精密称取盐黄柏药材粉末(过三号筛)1.0 g,置100 mL锥形瓶中,精密加入25 mL盐酸:甲醇(1∶100)混合溶液,称定重量,超声处理1 h,冷却后加入盐酸:甲醇(1∶100)混合溶液,补足失去的重量,静置,取上清液过0.45 μm滤膜,即得供试品溶液。
2.2 单因素炮制工艺考察
2.2.1 炮制温度考察
称取100 g黄柏饮片10份,按每 100 g 药材加入2 g未加碘精制盐的比例,分别加入40 mL水将2 g盐溶解,用喷壶均匀喷洒在药材表面,并置密闭容器中闷润60 min,分别120、140、160、180、200 ℃炮制15 min,粉碎,按2.1.3进行含量测定。记录峰面积,计算含量,结果见表2、图1。
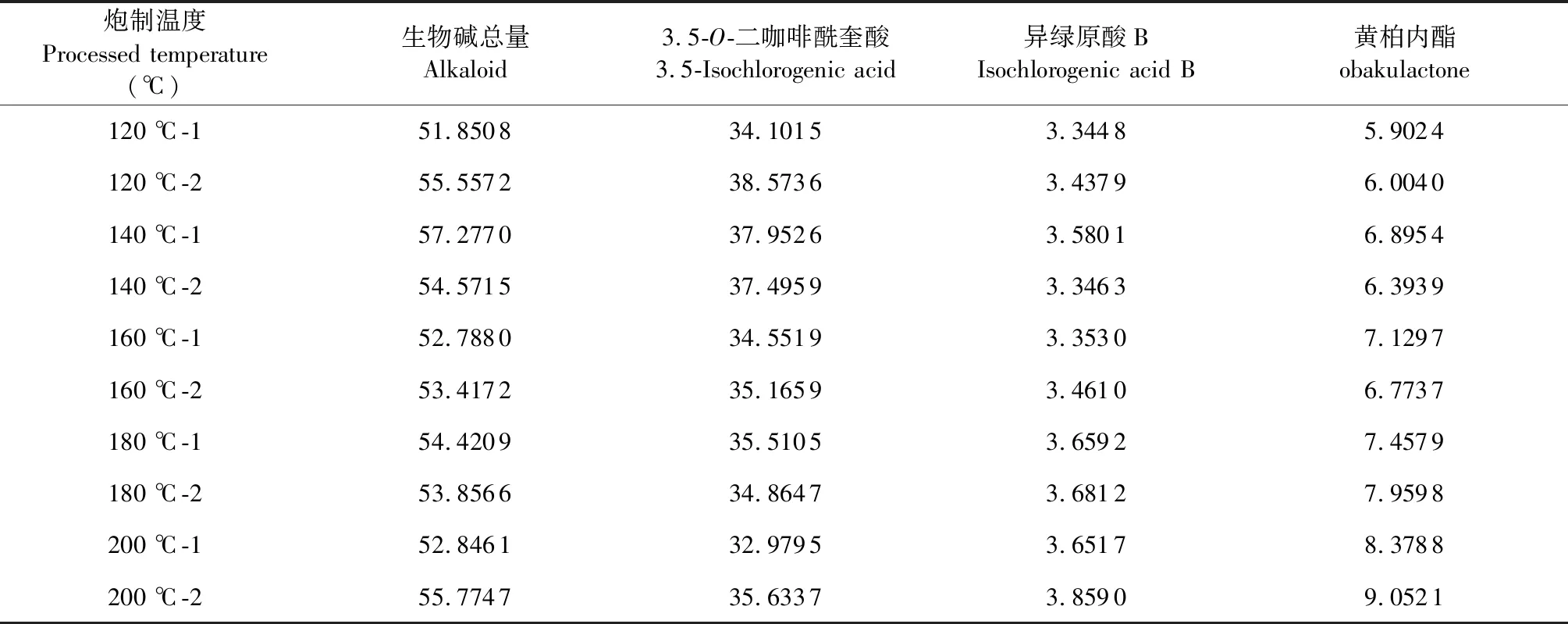
表2 炮制温度对盐黄柏指标成分含量影响(mg/g)
实验过程发现,炮制温度对盐黄柏得炮制有一定影响,特别是盐酸小檗红碱的含量,随着温度得升高,盐酸小檗红碱含量增加,以及内酯成分亦有所提高,并且温度过低,盐黄柏不易炒干,但温度过高容易炒焦,故综合考虑,最终确定盐黄柏炮制温度范围为120~180 ℃。
2.2.2 炮制时间考察
称取100 g黄柏饮片10份,按每100 g 药材加入2 g盐的比例,分别加入40 mL水将2 g盐溶解,用喷壶均匀喷洒在药材表面,并置密闭容器中闷润90 min,在150 ℃炮制10、15、20、25、30 min,粉碎,按2.1.3进行含量测定。记录峰面积,计算含量,结果见表3、图2。
结论:盐黄柏炮制时间不同,生物碱总量变化较小,但个别成分得含量变化较大,炮制温度不同,炮制时间亦有相应调整,但为节约生产成本,应将其炒药时间控制在30 min以内,并且时间过长,会使黄柏饮片炒焦,此外,时间太短,盐黄柏未炒干,会影响黄柏的储存,综上所述,本实验最终确定时间范围为15~25 min。
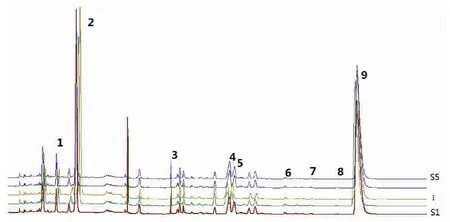
图2 不同炮制时间下盐黄柏三类主要成分HPLC指纹图谱Fig.2 HPLC fingerprint of three main components of Phellodendron chinensis under different processing time注:S1 10 min;S2 15 min;S3 20 min;S4 25 min;S5 30 min;1 异绿原酸B;2 3.5-O-二咖啡酰奎酸;3黄柏内酯;4黄柏碱;5木兰花碱;6药根碱;7巴马汀;8盐酸小檗红碱;9盐酸小檗碱。Note:S1 10 min;S2 15 min;S3 20 min;S4 25 min;S5 30 min;1 Isochlorogenic acid B; 2 3.5-Isochlorogenic acid;3 obakulactone;4 Phellodendrine;5 magnoflorine;6 jateorhizine;7 palmatine;8 berberubine;9 berberine.

炮制时间Processed temperature(min)生物碱总量Alkaloid3.5-O-二咖啡酰奎酸 3.5-Isochlorogenic acid异绿原酸BIsochlorogenic acid B黄柏内酯Obakulactone水分Water(%)10 min-160.819537.38651.47048.152925.36 10 min-253.592834.31061.43727.605525.7515 min-157.390936.97321.44438.062418.74
续表3(Continued Tab.3)

炮制时间Processed temperature(min)生物碱总量Alkaloid3.5-O-二咖啡酰奎酸 3.5-Isochlorogenic acid异绿原酸BIsochlorogenic acid B黄柏内酯Obakulactone水分Water(%)15 min-254.974735.01811.33857.824018.7620 min-157.272536.23131.49188.035912.2020 min-254.094535.25151.35627.595212.9825 min-154.951238.01611.34537.416310.4425 min-258.079639.07761.43548.028910.4230 min-152.659234.05341.34158.12837.2730 min-253.738634.32421.38267.52607.31
2.2.3 炒药量考察
分别取生黄柏饮片50、100、150、200、250、300 g饮片各2份,分别按每100 g药材加入40 mL水(含2 g盐)的比例,浸润60 min,150℃炮制15 min,粉碎,按2.1.3进行含量测定。记录峰面积,计算含量。结果见表4、图3。
实验结果表明,炒药量对各类成分影响较小,炒药量对炮制品的影响主要与所配置机器容量得总体积相关,调查多个药厂,根据多名炒药师傅多年炮制经验,炒药量一般不多于炒药机总容量1/4,本实验所用炒药机所容纳黄柏饮片总量约为1 200 g,炒药量太少容易炒焦甚至炒碳,影响饮片质量,炒药量过多容易造成饮片翻炒不均匀,部分饮片未炒干,影响饮片的储存,最终确定正交炒药范围为100 g~300 g。

图3 不同炒药量下盐黄柏三类主要成分HPLC指纹图谱Fig.3 HPLC fingerprint of three main components of Phellodendron chinensis under different processing amount注:S1 50g;S2 100g;S3 150g;S4 200g;S5 250g;1 异绿原酸B;2 3.5-O-二咖啡酰奎酸;3黄柏内酯;4黄柏碱;5木兰花碱;6药根碱;7巴马汀;8盐酸小檗红碱;9盐酸小檗碱。Note:S1 50g;S2 100g;S3 150g;S4 200g;S5 250g;1 Isochlorogenic acid B; 2 3.5-Isochlorogenic acid;3 obakulactone;4 Phellodendrine;5 magnoflorine;6 jateorhizine;7 palmatine;8 berberubine;9 berberine.

炒药量Processed amount(g)生物碱总量Alkaloid3.5-O-二咖啡酰奎酸 3.5-Isochlorogenic acid异绿原酸BIsochlorogenic acid B黄柏内酯Obakulactone50g-142.730829.90811.04534.586750g-241.741829.71231.45874.7394100g-144.844432.67351.09655.0910100g-243.376531.89351.00995.2639150g-142.966328.43001.00095.0139150g-242.082029.50220.96905.2438200g-141.596927.24290.99115.3217200g-242.239629.10611.05065.0719250g-139.982127.39800.80985.4976250g-245.685228.75171.06336.1125
2.3 AHP法确定各指标成分权重
根据各成分药效作用以及各成分含量多少,将指标成分含量作为权重予以量化,即将4个指标成分分成4个层次,并确定各指标得优先顺序:生物碱总量>3.5-二咖啡酰奎酸>黄柏内酯>异绿原酸B。以此构成成对比较的优先矩阵,并获得各指标的相对评分,指标成对比较的判断优先矩阵见表5。
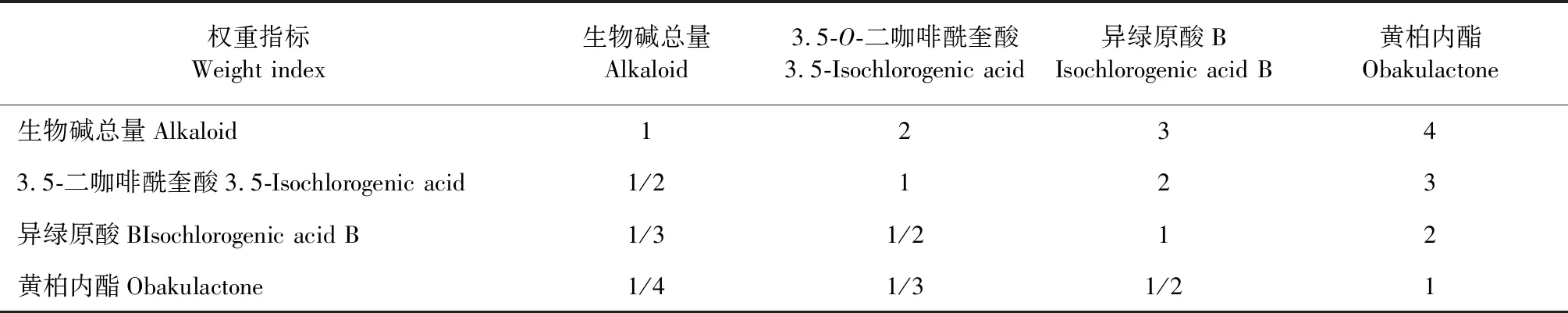
表5 指标成对比较的判断优先矩阵
根据表5评分结果,AHP法计算生物碱总量、3.5-二咖啡酰奎酸、黄柏内酯、异绿原酸B各项指标权重系数分别为0.466 8、0.277 6、0.160 3、0.095 3,一致性比例因子CR=0.007 3<0.1,即指标优先比较判断矩阵具有一致性,权重系数有效。
2.4 正交设计优选炮制工艺
根据单因素实验,优选炒制温度、炒制时间、炒药量三个因素三水平优选炮制工艺。根据因素和水平数,选择L9(34)正交表。因素、水平设定和实验安排见下表。
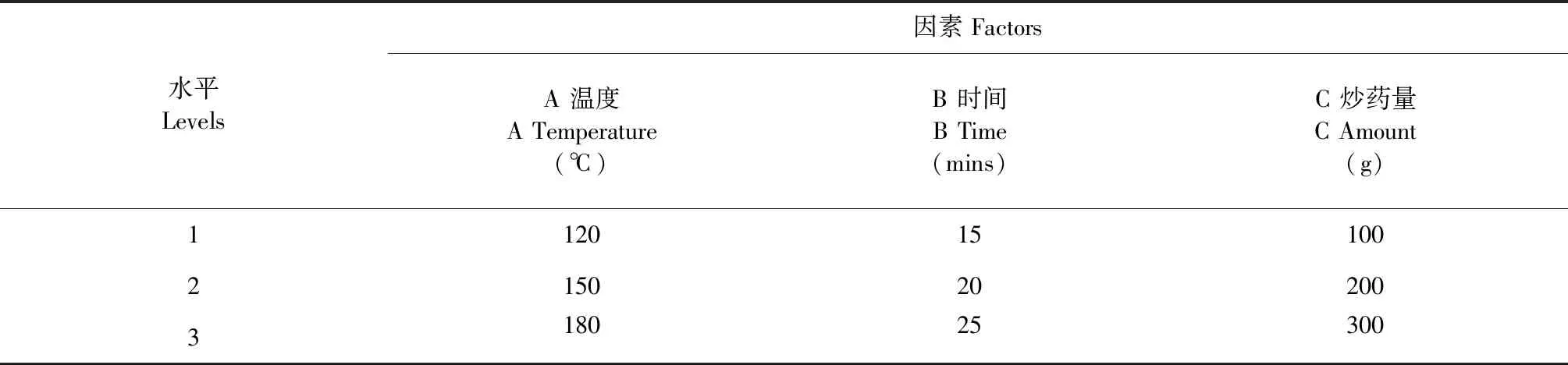
表6 正交因素水平表
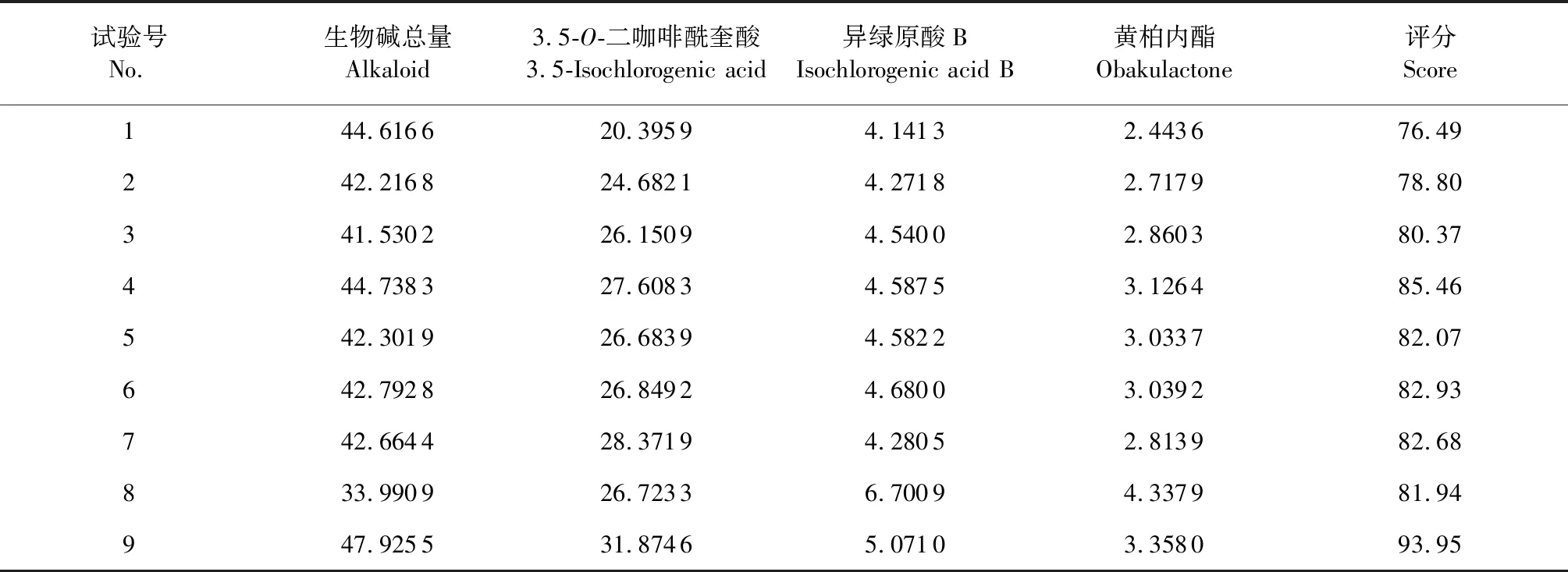
表7 正交实验安排与结果
2.5 提取工艺的确定
采用AHP法得到的权重系数对实验结果进行综合评分,利用SPSS 19.0对正交结果进行分析,直观分析结果见表8,方差分析结果见表9。
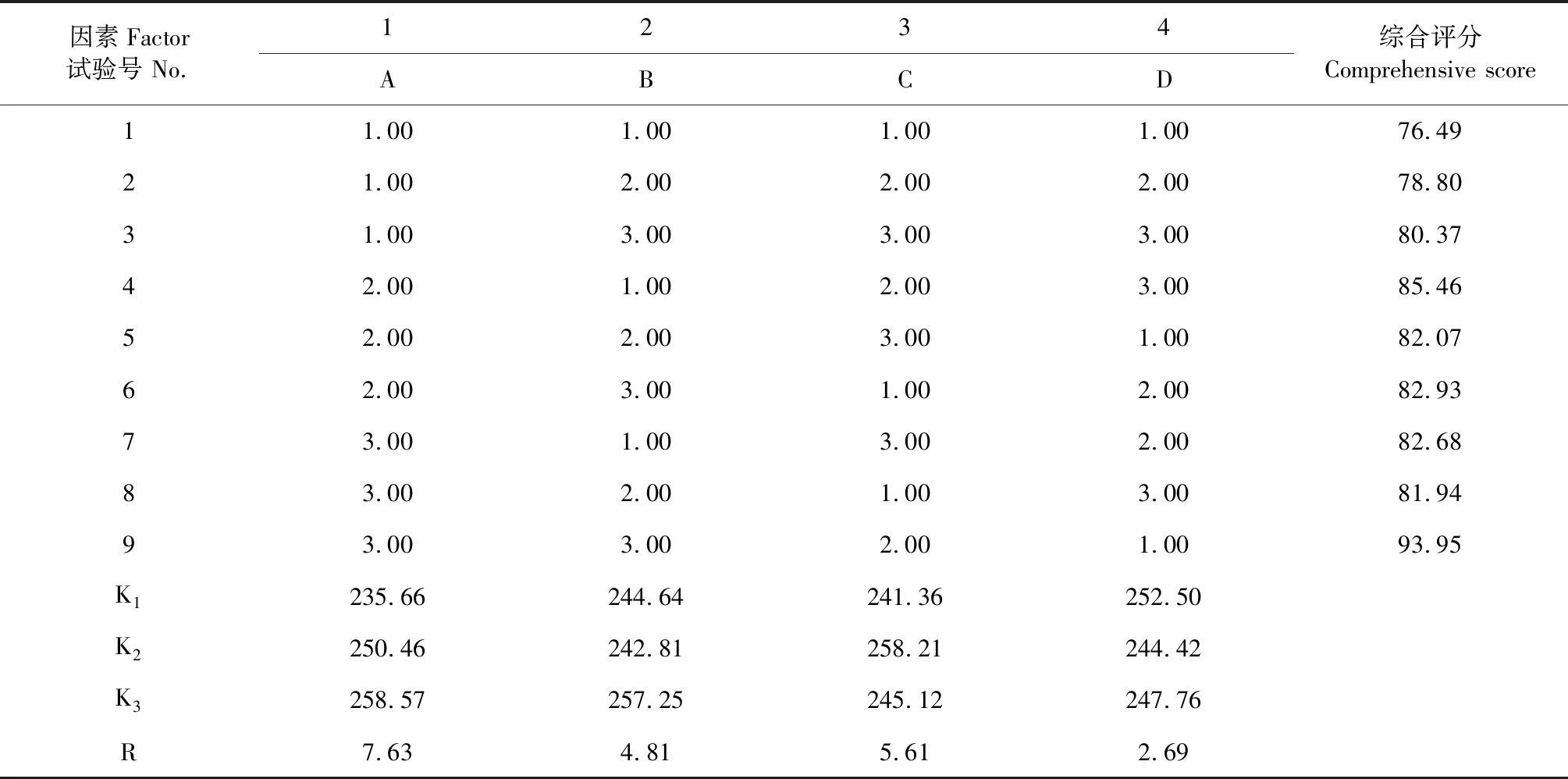
表8 正交试验综合评分结果
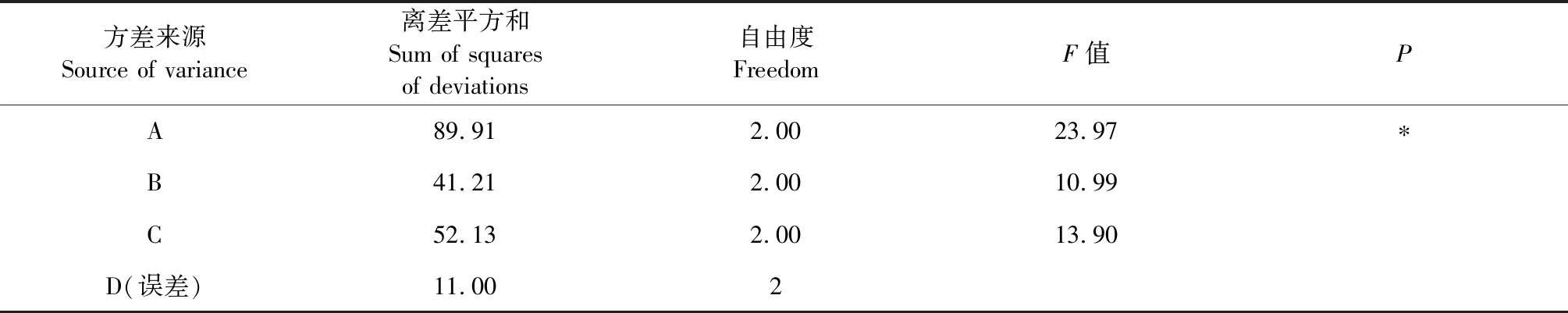
表9 方差分析
注:F0.05(2,2)=99.0。
Note:F0.05(2,2)=99.0.
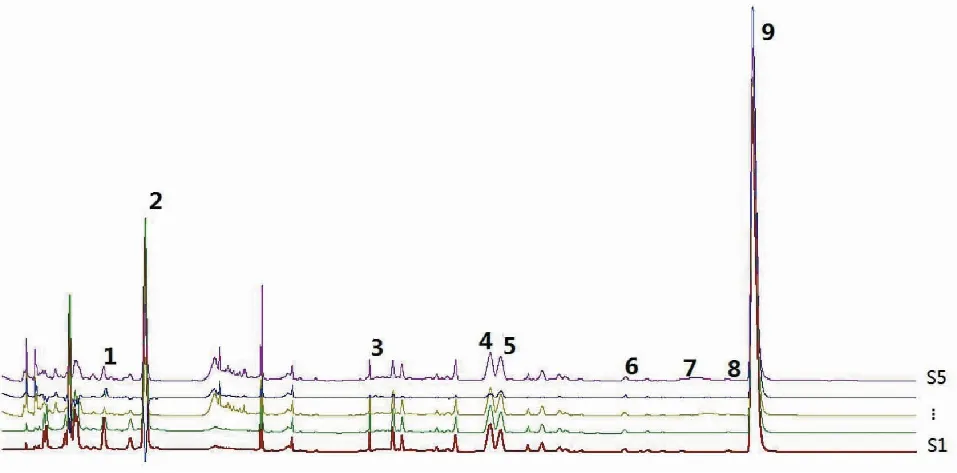
图4 正交实验HLPC指纹图谱Fig.4 HLPC fingerprint of orthogonal design
正交实验结果表明,不同的炮制工艺对盐黄柏个别成分影响较大,直观分析表明,影响炮制工艺的主次为:A>C>B,A因素对综合评分具有显著影响,得最佳工艺为A3B3C2,但由于B因素和C因素对实验结果影响不显著,考虑工业化大生产,为节约成本,同时保证饮片炒干,最终确定炮制工艺为:A3B2C3,即180 ℃,炒20 min,加入容器体积1/4饮片量。
2.6 正交验证试验
称取300g黄柏饮片(三份),分别加入80 mL盐水(含4 g盐),闷润90 min,放入预热至180 ℃炒药机翻炒20 min,粉碎,过筛,按“2.1项”进行含测。实验结果表明,RSD<5%,该工艺稳定、可行,可运用于盐黄柏炮制工艺生产。
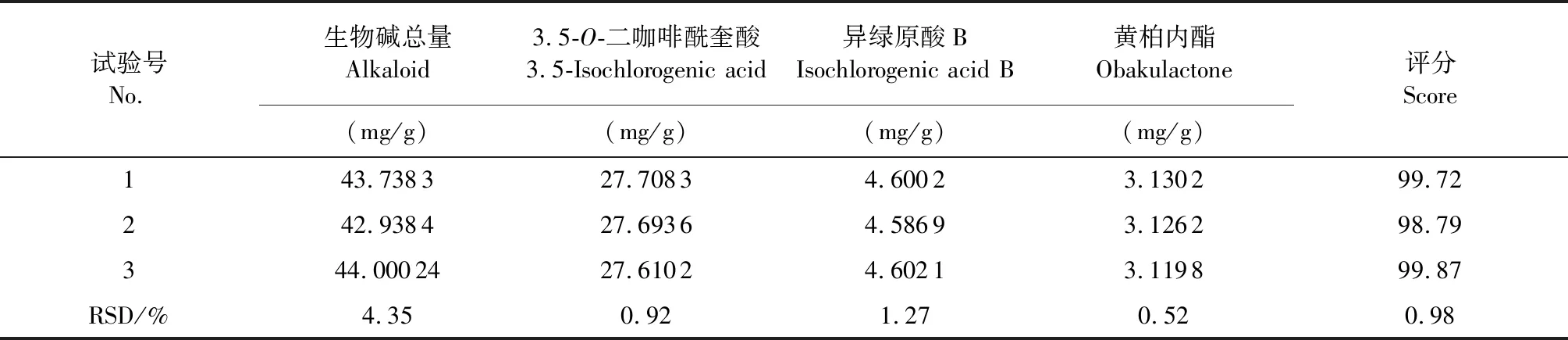
表10 验证结果
3 讨论
3.1 指纹图谱分析
试验发现盐黄柏不同炮制品均存在这9个共有峰,但各成分含量有一定差异。不同炮制品中生物碱总量变化较小,主要变化成分为盐酸小檗红碱及黄柏内酯。盐酸小檗红碱可能是由于加热使某些成分发生了转变,研究发现黄柏炮制后,小檗红碱含量增加是由盐酸小檗碱转化而来。但不同炮制温度对化学成分的转化有所不同,研究发现,加碘盐和非加碘盐黄柏内酯含量相差较大,其主要原因可能是碘使其溶出率的变化所致。黄柏生熟药效有异,生品性寒而沉;盐炙后缓和苦燥之性,不伤脾胃,引药下行入肾,增强资肾阴、泻肾火的作用。通过指纹图谱比较,发现黄柏炮制前后存在化学成分的变化,这可能是导致其药效发生变化的原因。[4]
3.2 盐黄柏饮片质量评价
实验结果表明,不同盐黄柏炮制品各类成分含量不呈正比趋势增长,故以单一成分来评价药材质量的优劣是不全面的,需多成分,多指标进行综合考虑。本实验通过三类有效成分的精确定量测定,为盐黄柏药材质量的控制和评价提供更好技术参考[5-7],并结合指纹图谱,定性定量得反映盐黄柏质量,为本课题接下来进一步盐黄柏的炮制工艺参数研究奠定基础。
3.3 炮制工艺的确定
本实验初期采用单因素实验,确定各影响因素的范围,[8]筛选出对盐黄柏质量影响较大的炮制影响因素,并采用正交设计进一步优选,实验结果采用多成分、多方面评价,[9]使筛选工艺更具科学性、可行性,所筛选的工艺对盐黄柏炮制稳定、可行,适用于实际生产中进一步验证,同时该试验为阐释黄柏的炮制机理提供了一定的参考依据,所建立的方法也可用于盐黄柏的质量控制。

