葛根芩连汤对吡格列酮在大鼠体内药动学行为的影响
陈 阳, 崔 波, 张艺竹, 安 叡, 邵建华
(上海中医药大学,上海201203)
中西药联合应用后,可导致不同药物之间发生相互作用,主要体现在理化性质、药动学、药效学3个方面[1-4]。其中,药动学相互作用可发生在体内吸收、分布、代谢、排泄过程中的某一个或多个环节,直接影响药物疗效,甚至产生毒副作用[5-7],故研究联合用药后的药动学变化对指导临床合理用药具有重要意义。
葛根芩连汤是中医治疗泄泻、痢疾的经典方剂,现代医家也将其应用于糖尿病及其并发症的治疗,取得了良好的疗效,可减轻2型糖尿病患者对胰岛素的抵抗,促进胰腺B细胞功能上的恢复,并具有抗氧化活性[8-9], 方中葛根素[10-11]、 黄芩苷[12-13]、 小檗碱[14-16]对该疾病发生发展具有延缓和治疗作用。
吡格列酮为噻唑烷二酮类口服降糖药,可用于治疗2型糖尿病,但临床研究表明[17]服用该药物后会有胃溃疡复发的风险,并伴有低血糖、水肿、肝功能异常、腹胀腹泻等不良反应。葛根芩连汤与吡格列酮联合应用时,在发挥降低血糖作用的同时又可调理胃肠道症状,能降低或延缓后者不良反应的发生,避免糖尿病患者要逐渐增加药量才能达到治疗目的的弊端,具有一定临床意义。课题组前期研究表明,葛根芩连汤及其主要药效成分在大鼠肝微粒体中能抑制吡格列酮的代谢;本实验将考察葛根芩连汤对吡格列酮在大鼠体内药动学行为的影响,以期为临床合理用药提供参考依据。
1 材料
1.1 仪器 UPLC XR超高效液相色谱/TSQ三重四级杆串联质谱仪 (日本 Shimadzu公司/美国Thermo Fisher公司);VX-200漩涡混悬器 (美国Labnet公司);BT125D电子天平 (德国Sartoris公司);DC12H水浴氮吹仪 (上海安谱科学仪器有限公司);5424R冷冻离心机、Research plus移液枪(德国Eppendorf公司)。
1.2 试药 盐酸吡格列酮片 (批号170801-153B,15 mg/片),由日本武田药品工业株式会社生产。葛根 (批号170316)、黄芩 (批号170708)、黄连(批号170727)均购于上海康桥中药饮片有限公司,炙甘草 (批号170306)购于上海金桥养和堂药店,经上海虹桥饮片厂陈燕军药师鉴定为正品,均符合2015年版 《中国药典》规定。吡格列酮(批号100634-200401)、罗格列酮 (批号100673-200401)均购于中国食品药品检定研究院。甲醇(德国Merck公司)、甲酸 (德国CNW公司)均为色谱纯;乙酸乙酯、乙酸铵均为分析纯,羧甲基纤维素钠为化学纯,均购于国药集团化学试剂有限公司;水为双蒸水。
1.3 动物 清洁级SD大鼠,雄性,体质量(200±20)g,由上海中医药大学实验动物中心提供,合格证号SCXK (沪)2014-0008。
2 方法与结果
2.1 LC-MS/MS条件
2.1.1 色谱条件 Agilent Poroshell 120 EC-C18色谱柱 (4.6 mm×50 mm,2.7 μm), 预柱月旭 XBC18色谱柱 (3 μm); 流动相 5 mmol/L 乙酸铵 (含0.1%甲酸) (A) -甲醇 (B),梯度洗脱 (0 min,70%B; 2 min, 95%B; 2.1 min, 70%B; 4 min,70%B);体积流量0.3 mL/min;柱温30℃;进样量 5 μL。
2.1.2 质谱条件 电喷雾电离 (ESI)源,正离子模式检测,扫描方式多反应检测 (MRM);毛细管温度280℃;雾化温度300℃;鞘气30 psi(1 psi=6.895 kPa);辅助气8 psi;碰撞气氩气;正离子源喷射电压3 000 V;m/z 357.4→134.2(吡格列酮),m/z 358.1→135.2(罗格列酮,内标)。
2.2 溶液制备
2.2.1 对照品溶液 精密称取吡格列酮对照品适量,甲醇溶解定容,制成201 μg/mL溶液,即得,4℃下保存备用。
2.2.2 内标溶液 精密称取罗格列酮对照品适量,甲醇溶解定容,制成200 μg/mL贮备液,精密吸取适量,甲醇稀释至2 μg/mL,即得,4℃下保存备用。
2.2.3 葛根芩连汤 按处方比例 (葛根 ∶黄芩 ∶黄连 ∶炙甘草=16∶9∶9∶5)加8倍量水,葛根先煎20 min,其他药材共煎30 min,煎煮2次后滤过,合并滤液,浓缩成每1 mL含1.4 g生药的药液,即得,-20℃下保存备用。
2.2.4 给药溶液 将盐酸吡格列酮片研磨至粉末,精密称取适量置于小烧杯中,加入0.5%羧甲基纤维素钠配制成混悬液 (含药量0.3 mg/mL),超声15 min,即得,使用前摇匀。
2.3 给药
2.3.1 单次给药 12只大鼠随机分成葛根芩连汤+吡格列酮组和吡格列酮组,每组6只,给药前禁食 12 h,自由饮水,以 14 g/kg葛根芩连汤、3 mg/kg吡格列酮灌胃 (给药体积 10 mL/kg), 其中葛根芩连汤+吡格列酮组以葛根芩连汤与吡格列酮相继灌胃,间隔30 min;吡格列酮组用生理盐水代替葛根芩连汤 (给药体积10 mL/kg),其余步骤同葛根芩连汤+吡格列酮组。分别于给药前及给药后0.083、 0.25、 0.5、 1、 1.5、 2、 2.5、 3、 5、 8、12、24、32 h眼眶后静脉丛取血200 μL,肝素抗凝,冷冻离心 (8 000 r/min、4℃)8 min,取上层血浆,-80℃冰箱中冷冻保存备用。
2.3.2 多次给药 12只大鼠随机分成葛根芩连汤+吡格列酮组和吡格列酮组,每组6只,给药前禁食 12 h,自由饮水,以 14 g/kg葛根芩连汤、3 mg/kg吡格列酮灌胃 (给药体积 10 mL/kg), 其中葛根芩连汤+吡格列酮组每天早晨灌胃葛根芩连汤1次,吡格列酮组每天早晨灌胃生理盐水1次(给药体积10 mL/kg),连续7 d,第8天给药前禁食12 h,自由饮水,葛根芩连汤+吡格列酮组以葛根芩连汤与吡格列酮相继灌胃,间隔30 min,吡格列酮组以生理盐水与吡格列酮相继灌胃,间隔30 min。分别于给药前及给药后 0.083、0.25、0.5、 1、 1.5、 2、 2.5、 3、 5、 8、 12、 24、 32 h 眼眶后静脉丛取血 200 μL,肝素抗凝,冷冻离心8 min(8 000 r/min、 4℃), 取上层血浆, -80℃冰箱中冷冻保存备用。
2.4 血浆处理 取肝素抗凝后的血浆50 μL,加入 10 μL 罗格列酮 (2 μg/mL, 内标)、 1 mL 乙酸乙酯,涡旋混匀1 min, 冷冻离心 (12 000 r/min、4℃)8 min,吸取上清液 500 μL,氮气吹干,200 μL流动相复溶, 冷冻离心 (13 500 r/min、4℃)10 min,取上清液进样分析。
2.5 方法学考察
2.5.1 专属性考察 取空白血浆、空白血浆+吡格列酮、灌胃给药2.5 h后血浆,在 “2.1”项条件下进样分析,结果见图1。由图可知,色谱峰峰形理想,与血浆中的内源性成分达到很好的基线分离,空白无干扰,方法专属性良好。

图1 吡格列酮MRM色谱图Fig.1 MRM chromatograms of pioglitazone
2.5.2 线性关系考察 取空白血浆50 μL,加入吡格列酮 10 μL, 配制成 1.05、 2.10、 5.25、 10.05、21.0、 52.5、 105、 210、 525、 1 050 ng/mL, 按“2.4”项下方法处理,在 “2.1”项条件下进样分析。以对照品质量浓度 (X)对对照品与内标峰面积之比 (Y)进行回归,得到方程为Y=0.019 2+0.006 74X (r=0.999 5), 在 1.05~1 050 ng/mL范围内线性关系良好,定量限 (S/N>10)为1.05 ng/mL。
2.5.3 精密度、准确度试验 取空白血浆50 μL,按 “2.5.2” 项下方法制成5.25、210、1 050 ng/mL质控样品各5份,连续测定3 d,测得吡格列酮批内、批间精密度RSD均小于15%,准确度86.6%~109.1%,均符合生物样品分析要求。
2.5.4 回收率、基质效应试验 取空白血浆,精密加入适量对照品溶液,配制成 5.25、210、1 050 ng/mL, 按 “2.4” 项下方法处理, 平行 5份,在 “2.1”项条件下进样分析,得峰面积A1;取相同体积空白血浆,按 “2.4”项下方法处理,平行5份,取上清液,加入对照品溶液,使其质量浓度与A1一致,在 “2.1”项条件下进样分析,得峰面积A2;流动相稀释对照品溶液至与A1一致,平行5份,在 “2.1”项条件下进样分析,得峰面积 A3, 计算提取回收率 (A1/A3)、 基质效应(A2/A3)。结果,吡格列酮提取回收率为89.93%~94.06%,RSD<15%;基质效应为 85%~115%,RSD<15%,符合相关要求,无明显内源性物质干扰。
2.5.5 稳定性试验 取低、中、高质量浓度质控样品各5份,分别考察含吡格列酮的血浆,按“2.4”项下方法处理,立即在 “2.1”项条件下进样分析;4℃下保存4 h后按 “2.4”项下方法处理,上清液放置24 h及-80℃下反复冻融3次、冷冻放置2周的稳定性。结果,血浆在上述条件下的RSD均小于15%,表明该方法稳定性良好。
2.5.6 稀释效应 配制8.04 ng/mL对照品溶液,血浆稀释10倍,测定稀释样品中吡格列酮质量浓度。结果,吡格列酮准确度、精密度RSD分别为8.3%、5.9%,表明稀释不影响血浆中吡格列酮的质量浓度。
2.6 药动学研究
2.6.1 单次给药 取 “2.3.1”项下血浆,按“2.4”项下方法处理,计算吡格列酮血药浓度,绘制血药浓度-时间曲线,结果见图2,再通过DAS 2.0软件计算药动学参数,结果见表1。由此可知,与吡格列酮组比较,葛根芩连汤-吡格列酮组可显著降低 Cmax, 显著延长 Tmax、 MRT0~t(P<0.05)。
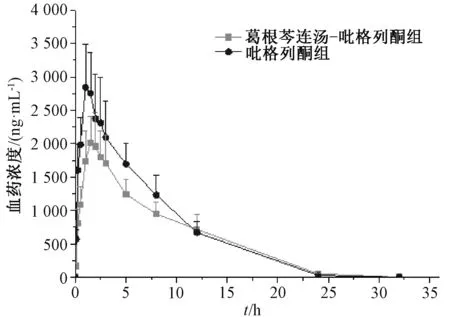
图2 吡格列酮血药浓度-时间曲线 (单次给药)Fig.2 Plasma concentration-time curves for pioglitazone(single administration)
表1 吡格列酮药动学参数 (单次给药) (±s, n=6)Tab.1 Pharmacokinetic parameters for pioglitazone(single administration) (±s, n=6)

表1 吡格列酮药动学参数 (单次给药) (±s, n=6)Tab.1 Pharmacokinetic parameters for pioglitazone(single administration) (±s, n=6)
注:与吡格列酮组比较,∗P<0.05
参数 单位 吡格列酮组 葛根芩连汤-吡格列酮组AUC0~t μg·L-1·h 23 085.02 ±3 490.70 18 972.22 ±3 495.61 AUC0~∞ μg·L-1·h 23 742.91 ±3 727.37 19 287.09 ±3 596.27 MRT0~t h 5.24 ±0.45 6.00 ±0.59∗Cmax μg·L-1 2 993.22 ±483.77 2 040.49 ±436.33∗Tmax h 1.20±0.27 1.70±0.27∗t1/2 h 2.58 ±0.42 2.40 ±0.65 CLz/F L·(kg·h)-1 0.13 ±0.02 0.16 ±0.03
2.6.2 多次给药 取 “2.3.2”项下血浆,按“2.4”项下方法处理,计算吡格列酮血药浓度,绘制血药浓度-时间曲线,结果见图3,再通过DAS 2.0软件计算药动学参数,结果见表2。由此可知,与吡格列酮组比较,葛根芩连汤-吡格列酮组可极显著提高 AUC,极显著降低 CLZ/F(P<0.01), 同时显著提高 MRT0~t、 Cmax, 显著延长Tmax(P<0.05)。

图3 吡格列酮血药浓度-时间曲线 (多次给药)Fig.3 Plasma concentration-time curves for pioglitazone(multiple administration)
表2 吡格列酮药动学参数 (多次给药) (±s, n=6)Tab.2 Pharmacokinetic parameters for pioglitazone(multiple administration) (±s, n=6)

表2 吡格列酮药动学参数 (多次给药) (±s, n=6)Tab.2 Pharmacokinetic parameters for pioglitazone(multiple administration) (±s, n=6)
注:与吡格列酮组比较,∗P<0.05,∗∗P<0.01
参数 单位 吡格列酮组 葛根芩连汤-吡格列酮组AUC0~ t μg·L-1·h 17 839.13 ±3 117.00 34 286.18 ±5 809.71∗∗AUC0~∞ μg·L-1·h 17 853.55 ±3 116.31 34 369.24 ±5 784.80∗∗MRT0~t h 6.21 ±0.32 6.94 ±0.37∗Cmax μg·L-1 2 821.59 ±662.42 4 342.44 ±685.17∗Tmax h 1.33±0.26 1.67±0.26∗t1/2 h 4.07 ±1.81 4.10 ±0.38 CLz/F L·(kg·h)-1 0.17 ±0.03 0.09 ±0.02∗∗
3 讨论
3.1 血浆样品前处理方法确定 生物样品前处理是色谱分析中必不可少的步骤,方法主要有液液提取、蛋白沉淀、固相萃取等,可改善分析结果的准确度和精密度,延长色谱柱寿命,排除基质干扰,富集被测组分[18],故有效的前处理方法和HPLCMS联用技术已成为药动学研究中的有力工具。本实验采用液液萃取法,考察了酸、中、碱性条件下乙酸乙酯、二氯甲烷作为萃取剂时的萃取条件,发现以中性乙酸乙酯为萃取剂时萃取完全,杂质干扰小。
3.2 色谱条件确定 吡格列酮结构中含有氮杂环,在反相C18色谱柱上的拖尾现象比较严重。为了改善峰形,本实验考察了甲醇-水、甲醇-水 (含0.1%甲酸)、甲醇-1 mmol/L乙酸铵 (含0.1%甲酸)、甲醇-5 mmol/L乙酸铵 (含0.1%甲酸)等流动相,发现甲醇-5 mmol/L乙酸铵 (含0.1%甲酸)洗脱时峰形对称性良好,分离度高。
3.3 内标确定 本实验考察了卡马西平、柚皮苷、吡格列酮的同系物罗格列酮,发现罗格列酮在质谱响应、色谱行为上都与吡格列酮接近,而且能与后者完全分离。
3.4 药动学分析 多次给药后,葛根芩连汤-吡格列酮组 AUC0~t、Cmax分别较吡格列酮组升高了1.92、 1.54倍, MRT0~t显著增加, CLz/F 极显著下降;与单次给药比较,AUC0~t、Cmax分别升高了1.81、 2.13 倍, MRT0~t显著增加, t1/2显著延长,CLz/F显著下降。由此可知,葛根芩连汤多次给药能提高吡格列酮体内暴露量,推测可能是由于所含药效成分 (如小檗碱等)不断与肝脏中的CYP1A2、 CYP2C11、 CYP3A1/2酶发生作用, 导致其活性受到抑制,从而抑制吡格列酮肝代谢及消除,而单次给药不能明显提高该药物在大鼠体内的生物利用度。

