生物制剂治疗银屑病药物选择
李祥,张小艳,张理涛
(1.天津市中医药研究院附属医院,天津 300120;2.天津医科大学,天津 300070)
银屑病是一种常见的免疫相关的慢性复发性炎症性皮肤病。该疾病是一种全球性疾病,影响着全世界约2%~3%的人口[1]。银屑病病情顽固,难以治愈,对患者的身心健康影响较大。目前发现的参与银屑病发病的T细胞亚群主要有CD4+Th1细胞、Th17细胞和Th22细胞。这些T细胞亚群及其分泌的一系列细胞因子,形成异常的炎性环境,从而促进银屑病的发生发展。近年来的研究发现白细胞介素(IL)-23/Th17/IL-17轴是银屑病发病机制中的关键环节。IL-23主要作用于Th17细胞,维持其活化与增殖。活化的 Th17 分泌 IL-17、IL-17F、IL-22、肿瘤坏死因子(TNF)-α等,募集中性粒细胞并且促进角质形成细胞的增殖,导致银屑病的发生发展[2-3]。目前针对上述银屑病免疫发病环节出现了许多靶向生物制剂。
生物制剂种类丰富,包括单克隆抗体、细胞因子、融合蛋白、RNA、反义寡核苷酸和激酶抑制剂。银屑病中最常用的种类包括单克隆抗体和融合蛋白。有许多生物制剂已被美国食品药品监督管理局(FDA)批准用于治疗中重度银屑病,根据其作用机制分类如下:①抑制T细胞活化制剂:阿法西普(Alefacept)、依法利珠单抗(Efalizumab);②TNF-α拮抗剂:英夫利昔单抗(Infliximab)、阿达木单抗(Adalimumab)、依那西普(Etanercept)、赛妥珠单抗(Certolizumab Pegol);③IL-12/IL23 P40亚单位拮抗剂:乌司奴单抗(Ustekinumab);④IL-17抑制剂:苏金单抗(Secukinumab)、Ixekizumab、Brodalumab;⑤IL-23 抑制剂:Tildrakizumab、Guselkumab。目前,已上市或已取得明确疗效数据的生物制剂见表1。除了这些生物制剂之外,目前还有更多的生物制剂正在开发中。来自临床试验和随访评估的数据表明,每种类型的生物疗法在功效、安全性、不良反应和其他特征方面彼此不同。本文对这些靶向生物制剂在银屑病治疗中的药物选择进行探讨。
1 T细胞活化阻断剂
1.1 阿法西普(Alefacept) Alefacept是FDA批准用于治疗银屑病的首个生物制剂[4]。Alefacept是人类白细胞功能相关抗原(LAF)-3与CD2结合的细胞外部分与人免疫球蛋白IgG重链的绞链区和稳定区(CH2和CH3)部分融合而成的二聚体蛋白。其与活化的T细胞表面的CD2分子结合,从而阻断抗原呈递细胞(APC)对T细胞的共刺激。此外,其选择性地靶向记忆效应T细胞,从而二者都起到抑制T细胞活化和消耗记忆性T细胞的作用[5]。随着越来越多的生物制剂出现,Alefacept在银屑病治疗中的地位越来越低。2013年一项关于银屑病生物制剂成本效益的研究显示,与阿达木单抗、依那西普、Infiiximab和Ustekinumab相比,Alefacept是成本效益最低的生物制剂[6]。2011年Alefacept退出市场。
1.2 依法利珠单抗(Efalizumab) Efalizumab与Alefacept同年获FDA批准。该药是一种人源化单克隆IgG1抗体,针对LFA-1的CD11a亚基,可阻断LFA-1与细胞间黏附分子(ICAM)-1之间的相互作用,与Alefacept相似,当与APC接触时会干扰T细胞的共刺激。在上市后阶段,安全问题变得明显。依法珠单抗长期治疗与罕见但危及生命的疾病进展性多灶性白质脑病(PCL)的发生之间的关系已建立[7]。因此,依法利珠单抗在2009年退出市场。
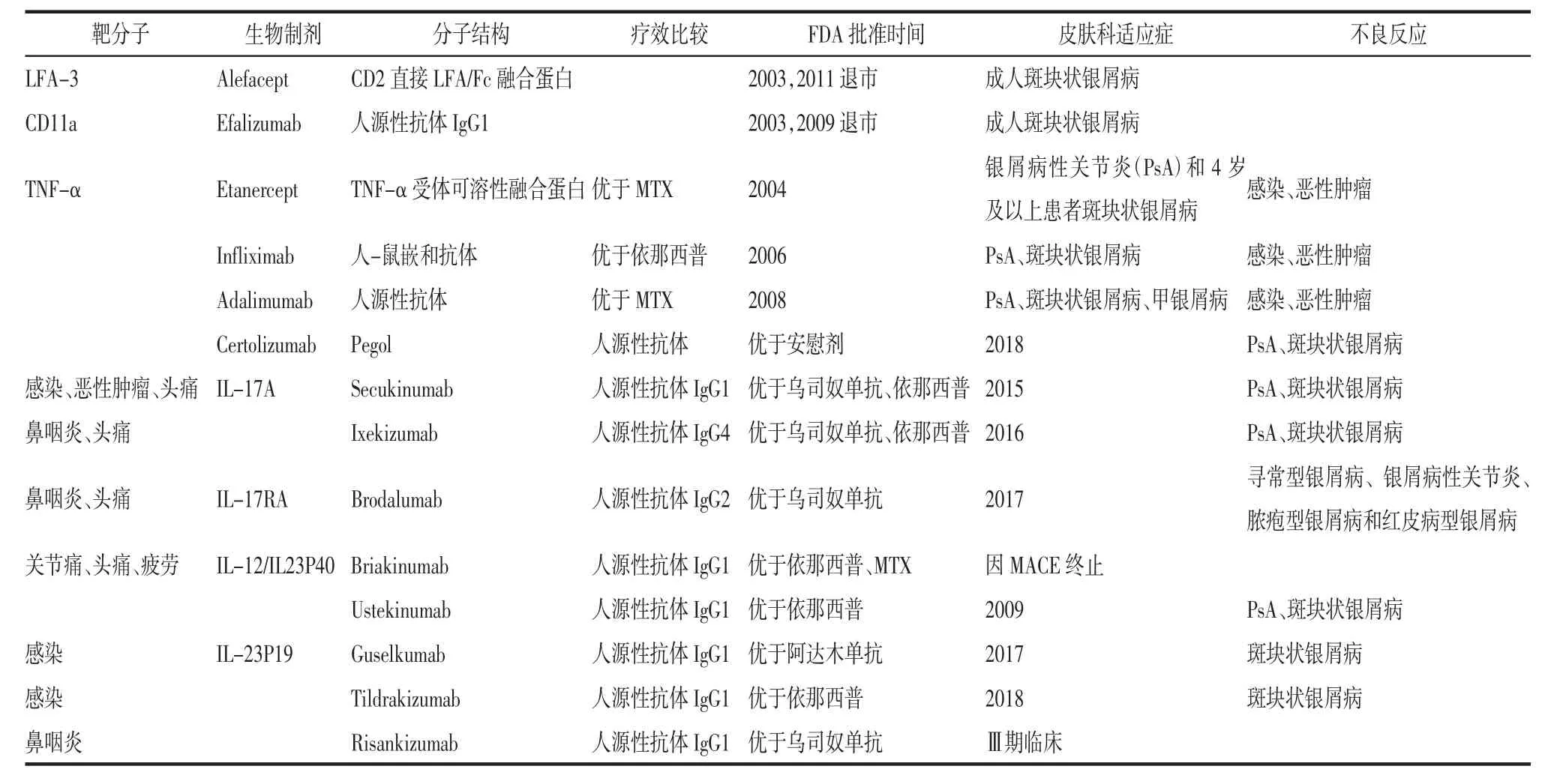
表1 已上市或已取得明确疗效数据的生物制剂
2 TNF-α拮抗剂
2.1 依那西普(Etanercept) Etanercept是一种TNF受体融合蛋白,其主要作用机制是通过与血液中的TNF竞争性结合,阻断TNF和细胞表面的TNF受体结合,从而降低其活性达到减轻炎症反应的目的。2002年,依那西普被批准用于治疗银屑病关节炎。直到2004年5月,FDA才批准该药用于治疗成人斑块状银屑病。最近其批准用于4~17岁儿童慢性斑块型银屑病,使其成为第一个批准用于该人群的生物治疗。根据试验数据,依那西普有严重感染和恶性肿瘤风险。此外,一些报道指出TNF抑制剂与心力衰竭的新发或恶化有关[8]。因此,医生应该谨慎使用这种药物在心力衰竭人群。依那西普的推荐剂量为50 mg/次,2次/周,连续3个月,随后50 mg/周维持注射。
2.2 阿达木单抗(Adalimumab) 阿达木单抗是抗TNF-α的全人源化IgG1单克隆抗体,可特异性地与游离型及膜结合型的TNF-α结合,阻断TNF-α的生物活性。2005年获FDA批准用于治疗PsA,2008年1月,根据相关研究的结果,阿达木单抗被批准用于治疗中重度斑块型银屑病成人患者[9]。近来阿达木单抗获得批准用于指甲型银屑病。同样其有恶性肿瘤、感染和心力衰竭新发或恶化的风险。推荐给药剂量为初始负荷剂量80 mg,然后每隔1周注射40 mg。
2.3 英夫利昔单抗(Infliximab) Infiiximab是一种人鼠嵌合的单克隆抗体,其作用方式与阿达木单抗相同。其在2005年被批准用于治疗银屑病关节炎,在2006年被批准用于治疗慢性斑块型银屑病。Infiiximab是作为输液而不是注射给药的。Infiiximab的推荐剂量开始于第0周、第2周和第6周5 mg/kg静脉注射诱导,随后每8周5 mg/kg维持治疗。
2.4 赛妥珠单抗(Certolizumab pegol) Certolizumab pegol是一种聚乙二醇化(PEG)的人源化IgG1单抗Fab片段,被批准用于克罗恩病、类风湿性关节炎、银屑病关节炎和强直性脊柱炎。PEG部分延长了循环中分子的寿命。2018年5月,该药获得FDA批准,用于治疗成人中度至重度斑块型银屑病。与其他生物制剂不同,Certolizumab pegol已被发现不能通过母乳转移,并且胎盘转移极少或没有。因此,这种药物可能成为治疗需要全身用药的妊娠和哺乳期妇女银屑病的靶向治疗。目前批准用于斑块状银屑病的剂量为每隔1周400 mg(2次,200 mg/次)。对于体质量<90 kg的患者,可以考虑降低初始和第2周和第4周400 mg诱导期的剂量,然后每隔1周注射200 mg维持量。
3 IL-12/IL-23p40拮抗剂
乌司奴单抗(Ustekinumab) Ustekinumab是一种靶向IL-23和IL-12的双重抑制剂。其是结合IL-23和IL-12共同的p40亚基的抗体,抑制IL-23和IL-12的生物活性。可阻断幼稚T淋巴细胞向Th1及Th17分化。Ustekinumab于2009年9月获FDA批准用于成人银屑病的治疗。根据相关试验的结果,该药2013年被FDA批准用于治疗银屑病关节炎。最近该药被批准用于12岁及以上患有斑块型银屑病的青少年。Ustekinumab的使用剂量是基于质量的,≤100 kg的患者在随后的第0周、第4周和每12周应接受45 mg注射;>100 kg的患者应在同一时间段内接受90 mg注射。
4 IL-17A及其受体拮抗药
4.1 苏金单抗(Secukinumab) Secukinumab是一种高选择性的IL-17A全人源化单克隆IgG1k抗体。选择性中和参与银屑病进展的细胞因子IL-17A,减轻炎症反应的作用。FDA于2015年1月批准该药,使其成为市场上首个用于治疗成人银屑病的抗IL-17抗体。此外,该药被批准用于银屑病关节炎和严重头皮银屑病[10]。在炎症性肠病患者中应避免使用苏金单抗,其他IL-17拮抗药也应避免。药物的推荐剂量包括诱导阶段300 mg剂量,1次/周,持续4周,随后从第8周开始每个月300 mg的维持阶段。
4.2 Ixekizumab Ixekizumab是一种人源性抗IL-17A的单克隆IgG4抗体,可选择性地结合并中和IL-17A。Ixekizumab于2016年3月获批用于斑块型银屑病成人患者的治疗。2017该药也被批准用于银屑病关节炎。IL-17参与调节胃肠道,因此伴有炎性肠病的患者必须谨慎使用。该药物的推荐剂量包括160 mg负荷剂量,诱导期每2周80 mg,持续3个月,维持期每个月80 mg。
4.3 Brodalumab Brodalumab是一种人源性抗IL-17A受体的IgG2单克隆抗体,能结合并阻断通过IL-17A受体的信号,有效缓解中重度斑块状银屑病。基于相关研究,其在2017年2月被FDA批准用于成人慢性斑块型银屑病[11]。使用这种药物前应注意确定任何以前或目前的自杀行为。Brodalumab增加自杀意念或行为风险。目前给药剂量为210 mg/次,1 次/周,共 3 周,然后每 2 周 210 mg。
5 IL-23抑制剂
5.1 Guselkumab Guselkumab是一种人源性IgG1单克隆抗体,通过结合IL-23的p19亚单位发挥作用。其是市场上首个选择性IL-23抑制剂,2017年7月获FDA批准用于成人银屑病。第0周、第4周推荐给药剂量为100 mg,随后每8周给药1次。
5.2 Tildrakizumab Tildrakizumab是一种针对IL-23的p19亚单位的IgG1人源化抗体。该药于2018年3月获得FDA批准用于治疗成人中度至重度斑块型银屑病。Tildrakizumab的给药是在第0周和第4周诱导注射后每12周1次,这12周的给药方案使得Tildrakizumab和Ustekinumab对有依从性问题的患者特别有益。近期的随机对照试验被用来证明Tildrakizumab在银屑病中的有效性[12]。
5.3 Risankizumab Risankizumab能够特异性抑制IL-23p19亚基。该药物目前在临床试验中,数据表明,该药物在治疗中重度银屑病中具有显著疗效,且优于乌司奴单抗[13]。
随着生物制剂的引入,中重度银屑病的治疗取得了重大进展。尤其是最近批准的IL-17和IL-23靶向生物制剂被证明是高效的,在短期临床试验中有良好的安全性。但是只有临床研究和上市后监测的长期结果才能决定新疗法在多大程度上取得成功。目前我国批准的银屑病生物制剂有益赛普、英夫利西单抗、阿达木单抗、乌司奴单抗,IL-17A单抗(Secukinumab)已完成注册临床试验,使用这些生物制剂应权衡利弊。近年来随着生物类似物及双靶标抗体的研究,将为不同的患者提供新的解决方案。相信随着银屑病发病机制更深入的揭示,将会研制出更高效和更安全的靶向制剂用于银屑病的治疗。

