海洋动物蛋白药物及其研究进展
潘 南,刘智禹
(1.福建省水产研究所,福建省海洋生物增养殖与高值化利用重点实验室,福建 厦门 361013; 2.福建省海洋生物资源开发利用协同创新中心,福建 厦门 361013)
新药研究开发核心之一是将基础化学、生物分子和疾病联系起来,完成高通量筛选、合成优化、药理、毒理等临床前试验,主要由政府提供资金的科研院校、研究机构完成;其二是临床研究、注册上市和售后监督等,耗资大、耗时长、参与人数多,一般由制药企业和委托研究机构(Contract research organization,CRO)完成。市场竞争的加剧促使制药企业加快产品管线的更新换代,因此制药产业界从本质上对药效突出、技术前沿、开发前景好的基础科研项目趋之若鹜。海洋动物经历数百万年的进化微调而演化出极高的靶向亲和效力和稳定性的代谢产物[1],这使得它们成为制药业药品开发管线的灵感源泉之一。本文对海洋动物蛋白药物及其研究现状进行了梳理,总结了海兔毒素、芋螺毒素、海鞘毒素、海绵活性多肽、海葵活性多肽及其结构类似物、衍生物的来源、结构、药理、分子靶标、临床试验研究现状和发展瓶颈。
1 海兔毒素及其衍生物
1.1 海兔毒素Dolastatins
Pettit课题组于1987年首次报道了印度洋无壳软体动物截尾海兔(Dolabellaauricularia)消化腺毒素dolastatins的分离、鉴定[2]。Dolastatins是一种线性五肽,包含dolavaline(Dov)、valine(Val)、dolaisoleuine(Dil)、dolaproine(Dap)和dolaphemine(Doe)五个子单元[3]。其中dolastatin 10和dolastatin 15在体外实验中表现出极强的抑制细胞增殖、抗肿瘤活性,其通过与β微管蛋白结合,迫使细胞分裂停滞,进而凋亡。由于天然存在的dolastatins含量非常低,Pettit和合作者被迫开发了全新的化学合成方法,以便获得足够的材料进行基本的细胞生物学研究,在此基础上进一步合成出一系列dolastatin衍生物auristatin PE(又称Soblidotin;TZT-1027;YHI-501)、tasidotin(又称Synthadotin;BSF 223651;ILX 651;LU 223651;SYN-D)和Cemadotin(又称LU-103793;NSC D 669356)。然而由于药物细胞毒性和/或缺乏功效,海兔毒素dolastatin 10、15衍生物均没有进行超过临床二期的研究(表1)[4]。
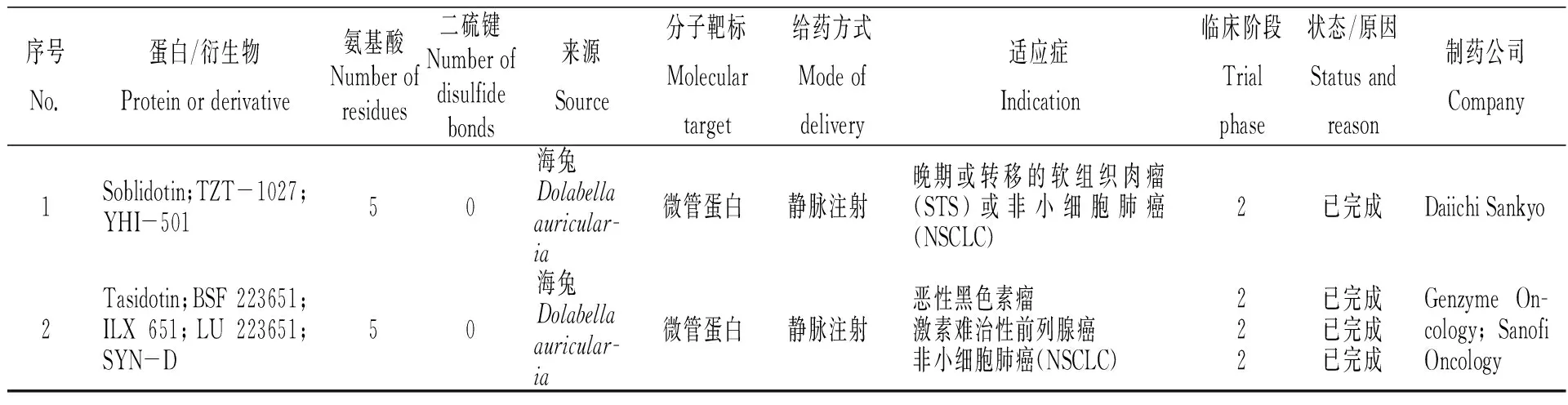
表1 经药品监督管理机构审批进入临床的海兔毒素dolastatin 10、15衍生物[4]
1.2 海兔毒素衍生物Auristatins
为了提高作用效力,Pettit课题组对dolastatin 10的C 端或N 端进行修饰,合成了auristatins 系列药物(auristatin E、auristatin PHE 、auristatin PYE、auristatin-2-AQ、auristatin-6-AQ)[5],增强了药物水溶性的同时仍然保持了显著体外抗肿瘤效力(10~100 pM,取决于所用的细胞株系)。然而体内试验结果仍然不尽理想。
1.3 经批准上市的auristatins 抗体-药物偶合物(Adcetris®)
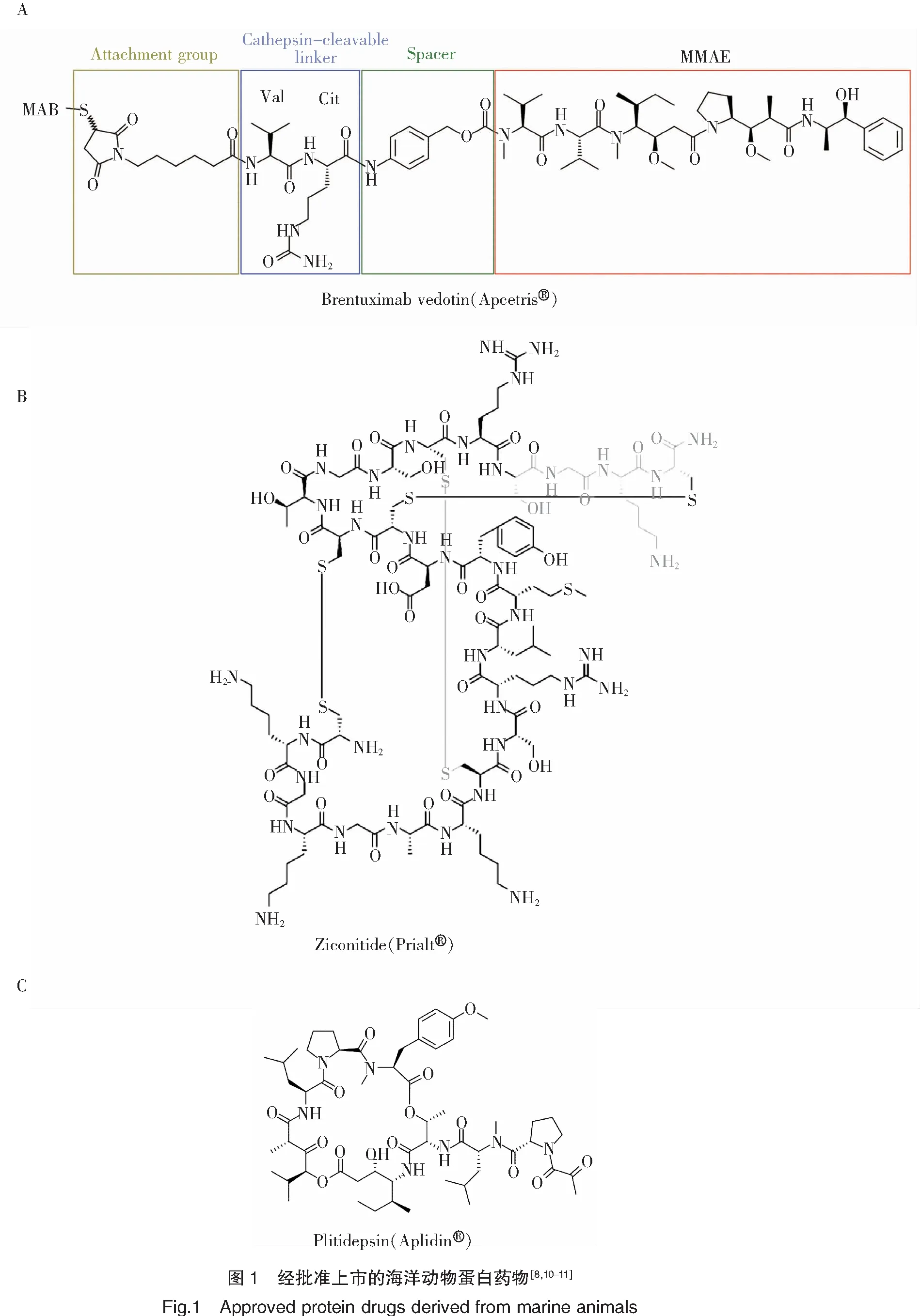
美国西雅图遗传学公司(Seattle Genetics)于2003年首次发表了其在auristatins 抗体-药物偶合物的研究进展,其在单甲基auristatin E(MMAE)的N端通过对氨基苄氧羰基(PABC)间隔体键合缬氨酸-瓜氨酸(vc)连接体以偶合cAC10(CD30 抗体),形成特异性肿瘤靶向抗体-药物偶合物Brentuximab vedotin(又称cAC10-vcMMAE;SGN-35)(表2)[6]。通过cAC10 靶向识别肿瘤细胞膜上的CD30蛋白, Brentuximab vedotin与 CD30蛋白结合后经细胞网格蛋白的调节被内吞入细胞,在溶酶体中被蛋白酶水解释放出MMAE,进一步抑制微管蛋白聚合,使细胞停留在G2-M期,促使细胞凋亡[7]。经历一系列临床研究,美国食品药品管理局(FDA)于2011年、欧洲医药管理局(EMA)于2012年批准Brentuximab vedotin以商品名Adcetris®(图1-A)上市,用于治疗CD30表达的霍奇金淋巴瘤和系统性间变性大细胞淋巴瘤[8]。美国西雅图遗传学公司与日本武田公司(Millenium,Takeda)合作,该药物于2014年在日本获得卫生、劳动和福利部(MHLW)批准上市[9]。
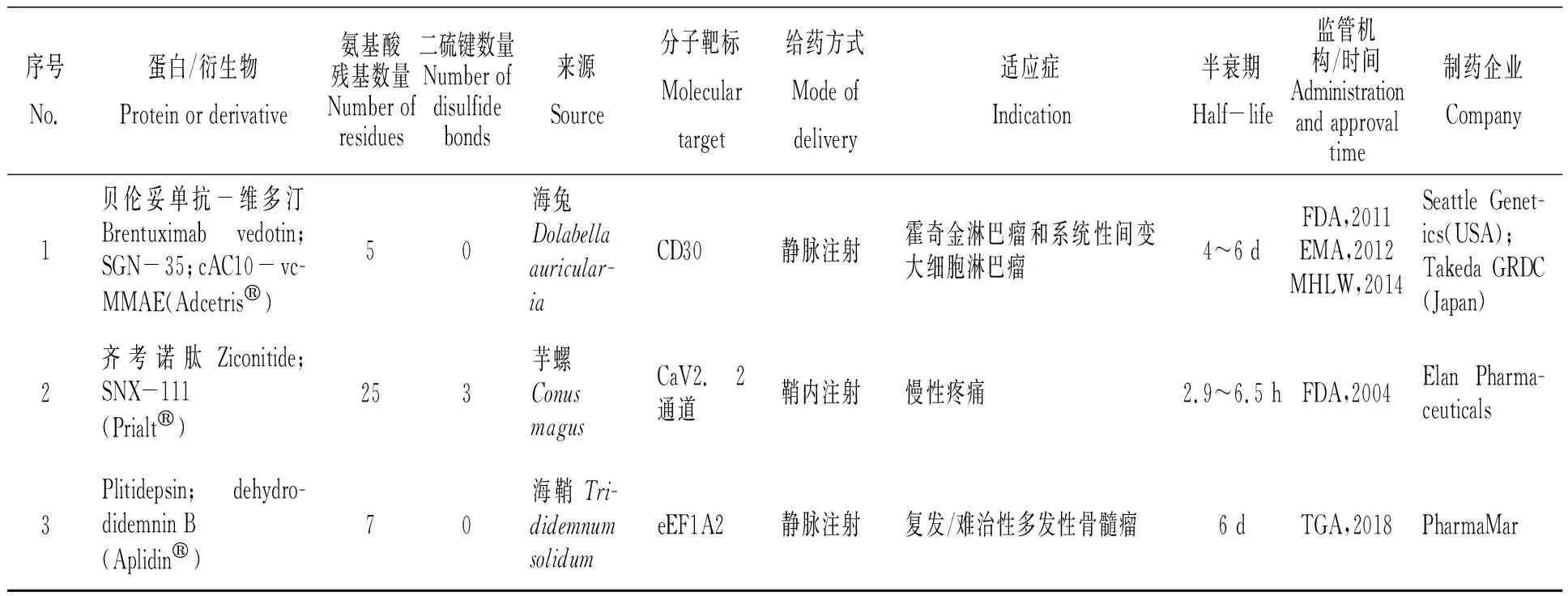
表2 经药品监督管理机构批准上市的海洋动物蛋白药物[6,8-11]
1.4 经审批进入临床试验的auristatins抗体-药物偶合物
随着肿瘤细胞靶点单克隆抗体研究和连接体技术的高速发展,为寻求更好的临床试验结果,高效、高活性的海洋动物细胞毒性蛋白受到单克隆抗体药物研究者的青睐。以海兔毒素dolastatin 10为母体化合物合成的auristatins系列被广泛应用于抗体-药物偶合物临床试验中。表3总结了目前经审批进入临床试验的auristatins抗体-药物偶合物,但必须指出的是,这份表格不是“完整的”,原因一是表格内容采用已公开的科学研究报道(论文、专利)[12-34]和公共数据库(NIH ClinicalTrial.gov数据库、NIH PubChem公共化学数据库、Adis Insight Springer数据库)资料[35-37],临床试验药物的靶点、连接体技术、细胞毒性药物的公开与否由投资者、合作者决定,因而无法掌握临床试验药物的全部细节;原因二是与临床试验现状不一定相符,药物效力、患者招募、投资决策等风险因素时刻影响临床试验阶段的变化,企业不一定及时将产品管线临床研究的信息更新。从目前整理的信息来看,共有32种auristatins抗体-药物偶合物经药品监督管理机构审批进入临床/临床前试验阶段,其中:2种auristatins抗体-药物偶合物进入临床三期阶段;11种auristatins抗体-药物偶合物进入临床二期阶段;19种auristatins抗体-药物偶合物进入临床一期阶段。
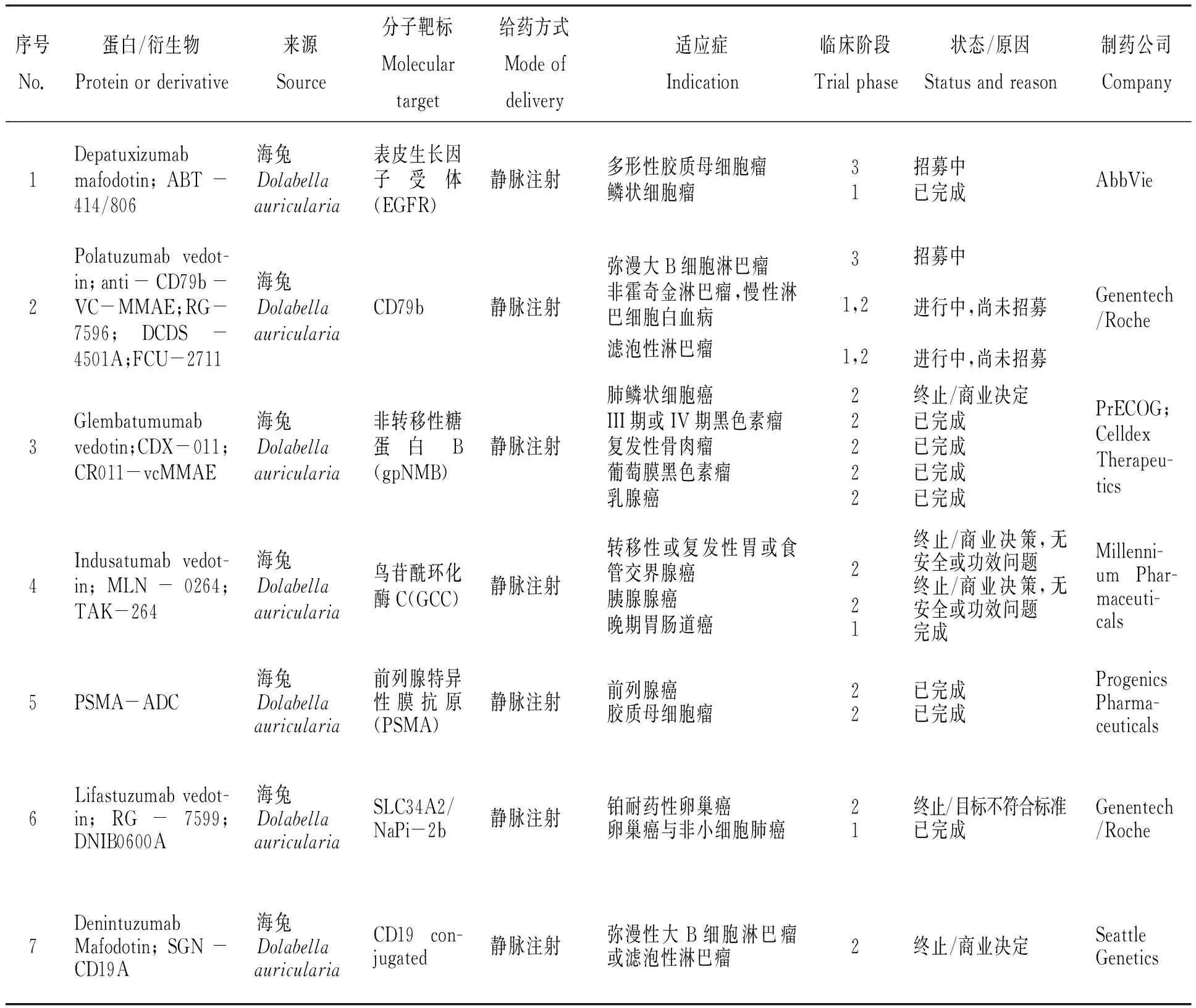
表3 经药品监督管理机构审批进入临床研究的auristatins抗体-药物偶合物[12-37]
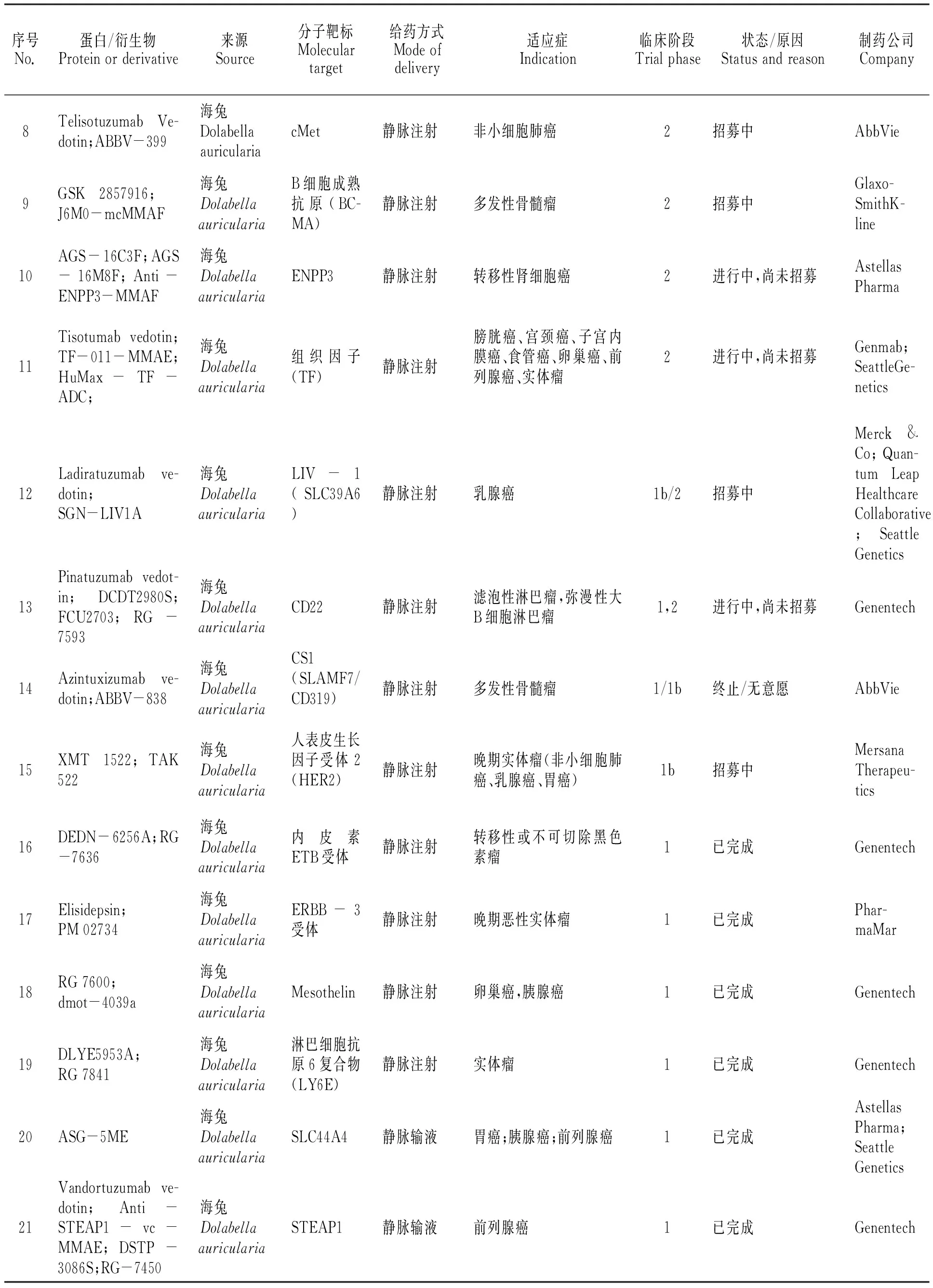
续表3
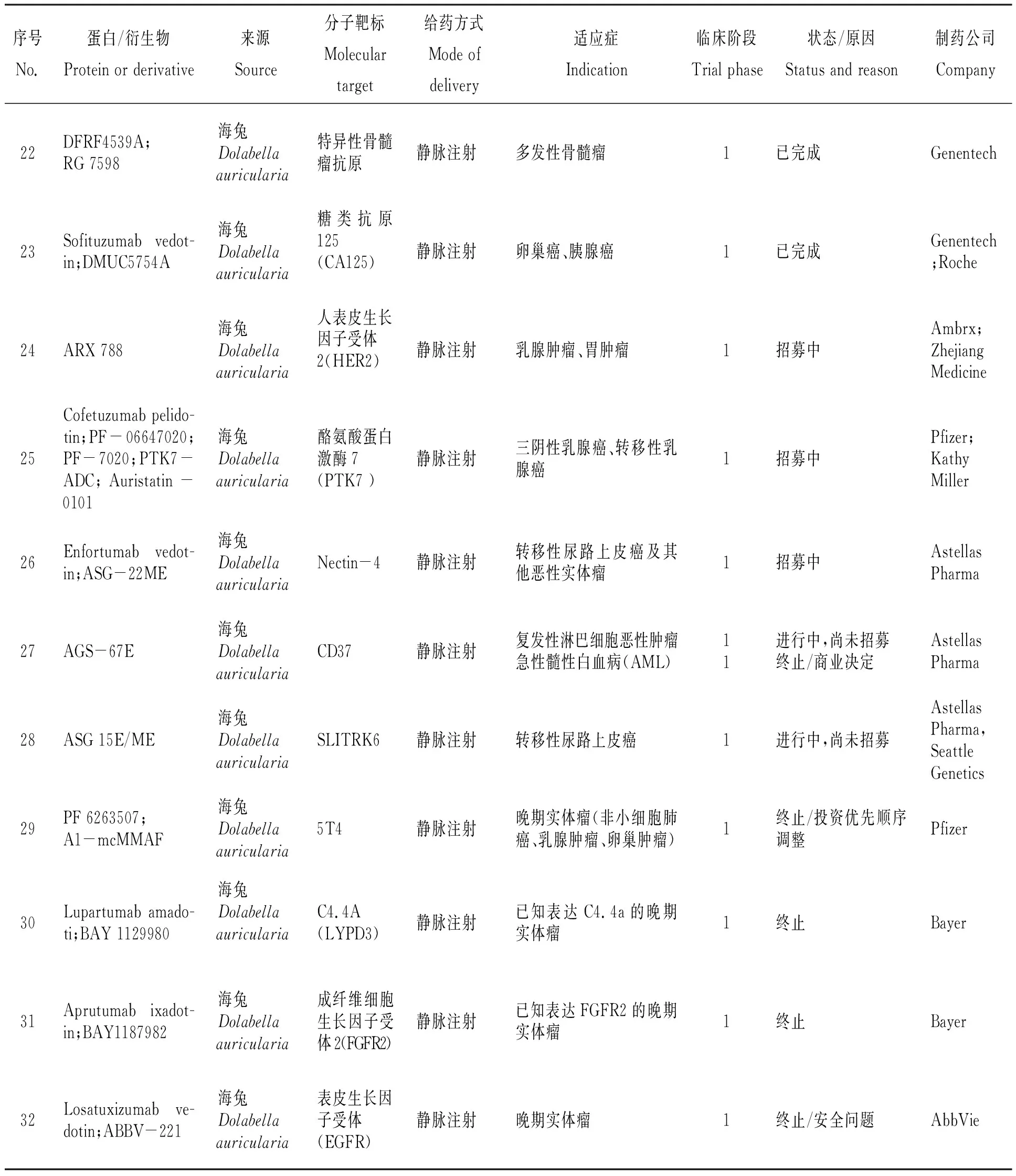
续表3
2 芋螺毒素及其衍生物
Cruz课题组于1985年首次报道了食鱼性地纹芋螺(Conusgeographus)毒液多肽conotoxins(CTxs)的分离、鉴定[38]。Conotoxins是一类富含二硫键的神经肽(10 - 30个氨基酸残基),根据与不同脊椎动物神经递质/激肽受体和离子通道的特异性靶向亲和能力,其分类为α-、δ-、κ-、μ-、ω-[39]。引人注意的是conotoxins通过翻译后修饰(PTM),如C-端酰胺化、N-端焦谷氨酸化和关键氨基酸残基的L到D异构化,以及广泛的半胱氨酸交联支撑,天然形成稳定的分子结构以对抗极端环境和蛋白酶水解。稳定、效力和靶向性等特质吸引了制药企业和资本推动conotoxins从研发向临床应用转化。
2.1 经批准上市的芋螺毒素Ziconitide(Prialt®)
Ziconitide(又称SNX-111)是由美国Elan公司研发的太平洋幻芋螺毒液多肽ω-MVIIA 的化学合成体,其与中枢神经系统N型电压敏感性钙离子通道高度亲和,无需第二信使或G蛋白,故不会引起药物依赖或成瘾。经历一系列临床研究,美国食品药品管理局(FDA)于2004年批准了Ziconitide以商品名Prialt®(图1-B)上市,用于治疗慢性疼痛(表2)[10]。尽管Prialt®具有3个二硫键稳定结构,但由于中枢神经受体的特殊性,其采用了鞘内注射的药物输送方式以增强中枢神经系统靶向效力。然而与肠外或口服给药相比,鞘内注射具有内在风险[40],这使得Prialt®在患者接受度和市场渗透率方面受到了极大的限制。与同功效药物对比,辉瑞公司口服活性镇痛/抗癫痫药物Neurontin®在2003年达到27亿美元的销售高峰[41],而Prialt®在2009财政年度的最终用户销售额仅为2 000万美元,Azur Pharma在2010年仅以1 460万美元收购了Prialt®欧洲版权[1],Prialt®在营销方面不尽理想。
2.2 经批准进入临床/临床前试验的芋螺毒素
由于conotoxins种类丰富,在中枢、外周神经系统中靶向位点众多,且不易被蛋白酶水解,天然结构具有较强的药物开发潜质,制药界在临床/临床前研究中对其日益关注。表4总结了目前经审批进入临床/临床前试验的芋螺毒素,靶向位点包括去甲肾上腺素转运蛋白、GABAB a和 nAChR、神经降压素受体、NMDA受体、CaV2.2通道、Shaker类型KV 通道,适用领域包括术后疼痛、神经病理性疼痛、难治性癫痫、心肌梗塞[1,35-37,42-45]。然而由于药物缺乏功效、投资决策变更或撤资等因素影响,芋螺毒素均没有进行超过临床二期的研究。由此可见,与其他类型药物相比,目前海洋动物蛋白药物在中枢神经系统靶向开发成功率较低。
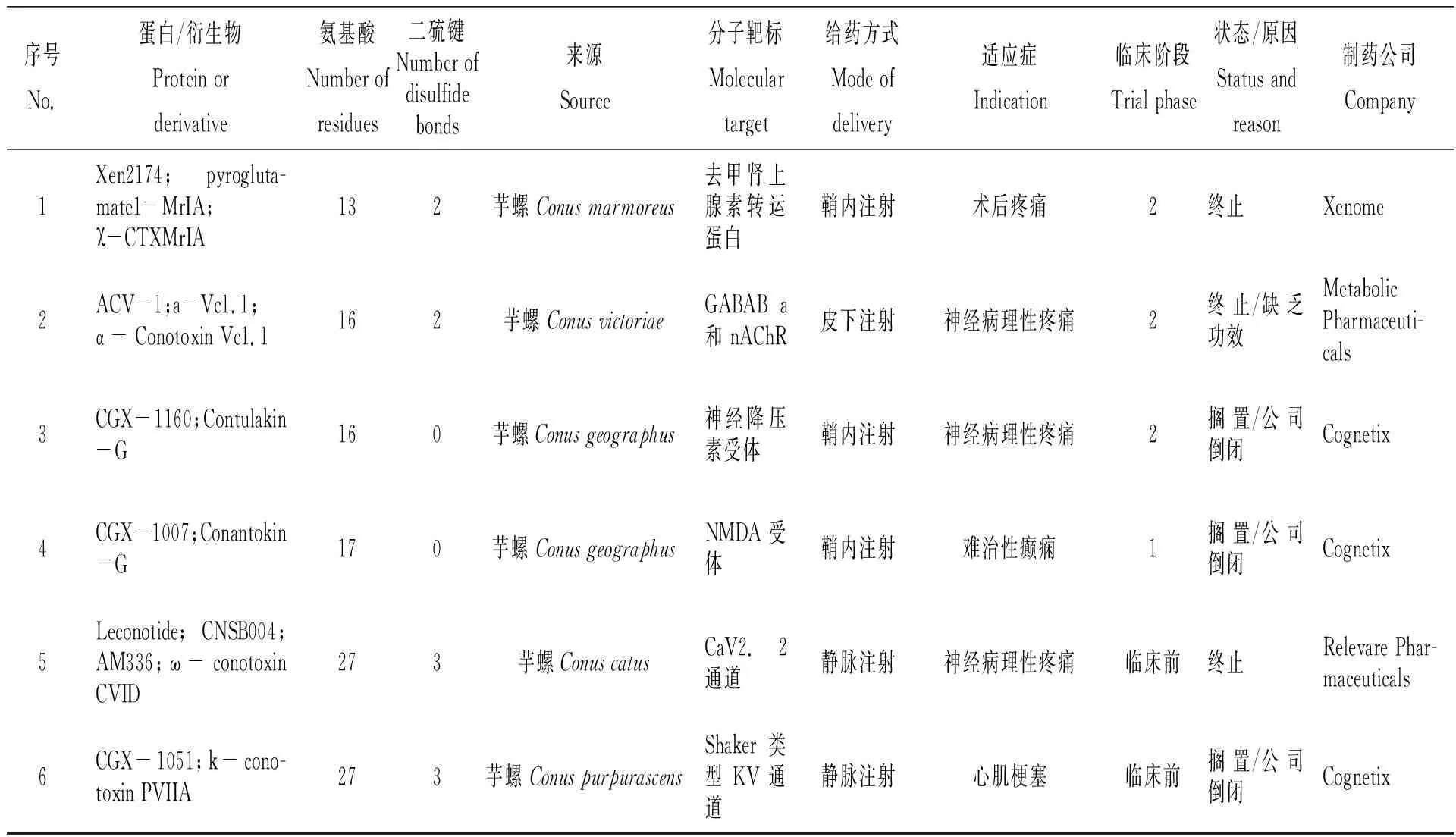
表4 经药品监督管理机构审批进入临床/临床前研究的芋螺毒素[1,35-37,42-45]
3 海鞘毒素及其衍生物
Rinehart课题组于1981年报道了加勒比海海鞘(Trididemnumsolidum)提取物didemnins的分离、鉴定[46]。Didemnins是一类环形缩肽,具有较高的抗肿瘤活性,其中didemnin B的功能活性最强,通过特异性结合真核翻译延长因子1A(eEF1A),启动细胞凋亡,致使肿瘤细胞程序性死亡,成为美国第一个进入临床试验的海洋抗肿瘤天然产物[47]。Didemnin B(表5)已完成了针对复发性或难治性间变性星形细胞瘤或多形性胶质母细胞瘤的二期临床试验。不幸的是,该化合物由于患者中高发生率的过敏反应而显示出高毒性,试验已终止[48]。Didemnin同系物脱氢 didemnin B(又称Plitidepsin)(表2、5)目前已完成了针对复发/难治性多发性骨髓瘤的临床三期试验[49],并向医药监管机构申请了上市许可。澳大利亚药品管理局(TGA)于2018年12月批准了plitidepsin以商品名Aplidin®(图1-C)上市,其将联合地塞米松用于对其他疗法治疗失败或有抵抗的复发性或难治性多发性骨髓瘤患者的治疗[11]。
4 海绵活性多肽
Kashman课题组于1994年报道了南非海绵(Hemiasterellaminor)提取物中细胞毒性多肽hemiasterlin的分离、鉴定[50]。Hemiasterlin是一种三肽化合物,其通过与微管蛋白结合,使微管解聚,影响纺锤体形成,诱导有丝分裂停滞,促进细胞凋亡。为了提高作用效力,课题组合成了一系列衍生物,其中以Taltobulin(又称HTI-286)和E 7974细胞毒性比天然产物hemiasterlin更佳,继而进入临床试验阶段。然而HTI-286因商业决策改变,不在制药企业管线中体现而终止开发,E 7974则完成临床一期试验(表5)[9]。
5 海葵活性多肽
Karlsson课题组于1995年报道了加勒比海葵(Stichodactylahelianthus)毒液神经肽Stichodactyla toxin(ShK)的分离、鉴定[51]。ShK由35个氨基酸残基组成,特异性作用于电压门控Kv1.3钾离子通道。2015—2017年,ShK类似物ShK-186(又称Dalazatide)成为美国第一个进入临床试验的自身免疫疾病Kv1.3阻断制剂,目前已完成临床一期试验(表5)[35-37]。Lazdunski课题组于2004年报道了海葵(Anthopleuraelegantissima)毒液神经肽APETx2的分离、鉴定[52]。APETx2是42个氨基酸、包含3个二硫键的神经多肽,特异性抑制感觉神经元中的酸敏感通道ASIC3。目前已进入临床前试验,适用于治疗炎性疼痛(表5)[53]。
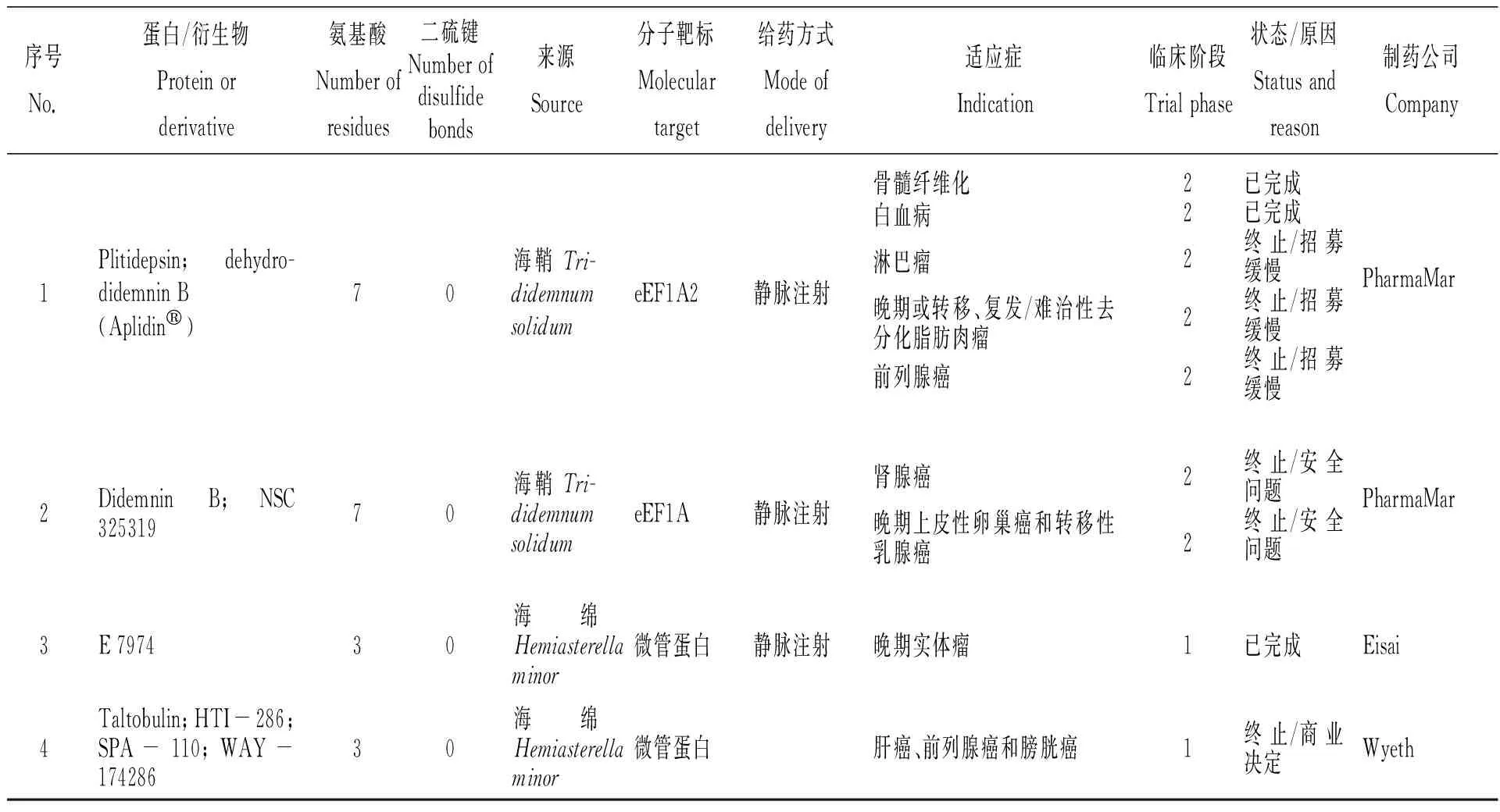
表5 经药品监督管理机构审批进入临床/临床前研究的海鞘毒素、海绵活性多肽、海葵活性多肽[9,35~37,48-49,53]
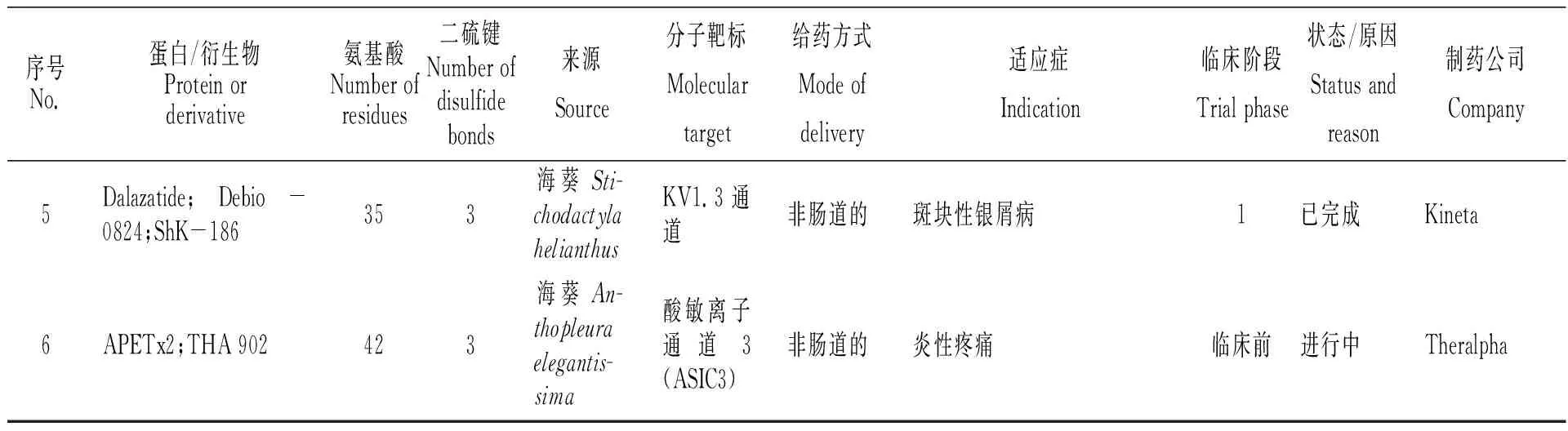
续表5
6 结语与展望
本文对海洋动物来源蛋白药物的最新研究进展进行了梳理。从功效领域来看,海洋动物蛋白主要归类为细胞毒性蛋白、神经毒素蛋白和离子通道抑制剂。从药物开发领域来看,海洋动物细胞毒性蛋白主要应用于抗癌和免疫药物开发,市场转化率好且呈现蓬勃发展的态势;海洋动物神经毒素蛋白和离子通道抑制剂主要应用于治疗慢性疼痛药物开发,由于药物代谢进入中枢神经系统的成功率仅为1%,故海洋动物神经毒素蛋白和离子通道抑制剂针对中枢神经系统靶标开发的衍生药物成功率较低。从市场应用进展来看,目前共有3种海洋动物蛋白药物(商品名Prialt®、Adcetris®和Aplidin®)获得药品监督管理机构批准成功上市,分别用于治疗慢性疼痛、霍奇金淋巴瘤、系统性间变大细胞淋巴瘤和复发性或难治性多发性骨髓瘤。从药物临床进展最高阶段来看,目前共有32种auristatins抗体-药物偶合物、6种芋螺毒素、2种海鞘毒素、2种海绵活性多肽、2种海葵活性多肽经药品监督管理机构审批进入临床/临床前试验阶段。其中2种auristatins抗体-药物偶合物进入临床三期阶段,具有较好的药品商业转化预期和前景;11种auristatins抗体-药物偶合物、3种芋螺毒素、2种海鞘毒素进入临床二期阶段;19种auristatins抗体-药物偶合物、1种芋螺毒素、2种海绵活性多肽、1种海葵活性多肽进入临床一期阶段;2种芋螺毒素、1种海葵活性多肽经药品监督管理机构审批进入临床前试验阶段。
纵观天然产物的药物发展历程,从20世纪70、80年代美国癌症研究中心(NCI)和美国农业部(USDA)启动轰轰烈烈的陆源、海源天然药物筛选项目,到90年代制药企业纷纷终止天然产物项目,再到本世纪初高通量筛选和组合化学以及近十年来发展迅猛的细胞毒性药物-单克隆抗体联合药物,海洋动物蛋白药物完整经历了技术更新、资金和时间的考验,在恶性肿瘤、慢性疼痛等疾病治疗以及神经系统离子通道特异性诊断方面取得了实实在在的成果。据此,相信在未来,随着质谱、核磁共振波谱、转录组学技术的发展,将有越来越多海洋动物来源的活性蛋白被发现;随着单克隆肿瘤抗体靶向技术和突破血脑屏障缓释技术水平的提升,海洋动物蛋白药物的效能与给药方式的瓶颈将得以突破。我们期待更多的药物从自然海洋走向医护救治。

