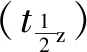LC-MS/MS测定大鼠血浆中烟花苷浓度及其药代动力学和生物利用度△
贾田芊,田曼,翟思成,任丽,孙静*
1.陕西科技大学 镐京学院,陕西 咸阳 712046;2.陕西中医药大学,陕西 咸阳 712046
黄花油点草来源于百合科Liliaceae植物黄花油点草Tricyrtismaculate的干燥全草,具有安神除烦、活血消肿之功效,用药历史悠久,疗效突出,是跌打损伤重要品种之一。该药材蕴藏量较大,主要分布在陕西、四川、贵州等地海拔2300~2800米的山坡上。该植物是陕西重要的道地药材,广泛分布在秦岭地区。近年来,黄花油点草引起了研究者广泛关注。现代研究结果表明,黄花油点草中黄酮类[1-4]成分在小鼠微循环、鼠血栓、急性脑梗阻具有很强的药效。烟花苷[5-7](结构如图1,nicotiflorin)是黄花油点草主要成分之一,是一种连接有芸香糖的黄酮醇苷类水溶性化合物,存在于多种植物当中,现代药理研究表明[8-10]其具有抗氧化、抗菌、抗病毒、抗炎镇痛及神经保护等多种生物活性,并有较强的活血作用。
由于药用植物属于当地的传统品种,基础研究较少,目前未有关于烟花苷体内过程的报道。本实验参考文献[11-14]并不断探索,以柚皮苷为内标,建立了烟花苷的血浆药物浓度LC-MS/MS测定方法并测定了烟花苷在大鼠体内的药代动力学和生物利用度,为进一步提高烟花苷生物利用度及其临床联合治疗提供了科学依据。
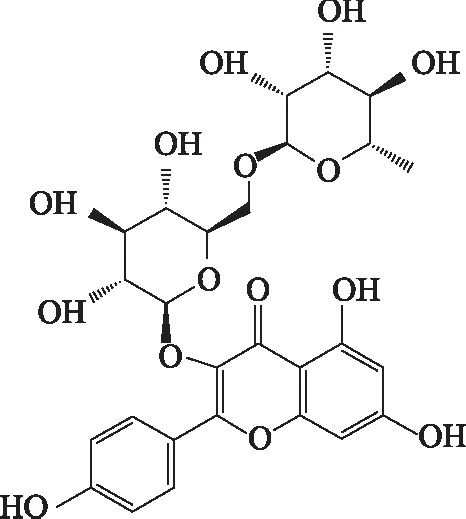
图1 烟花苷结构图
1 材料
1.1 仪器
岛津Nexera XR LC-20AD高效液相色谱仪(日本SHIMADZU),AB SCIEX QTRAP4500型质谱仪(美国AB SCIEX公司),KH-400KDE高功率数控超声波清洗器(昆明市超声仪器有限公司),MS205DU十万分之一电子天平(北京赛多利斯仪器系统有限公司),EYELA MG-2200氮吹仪(上海赛默生物科技发展有限公司),Allegra64R冷冻离心机(美国贝克曼库尔特有限公司),SK-2涡旋振荡器(上海奥然科贸有限公司)。
1.2 试剂与动物
烟花苷(批号:100080-201610,纯度:91.9%)、柚皮苷(批号:K21F3C1,纯度:98%)均来自上海源叶生物有限公司。甲醇、乙腈为色谱纯(天津医药化学技术有限公司),磷酸为分析纯(南通天昊化工有限公司),水为娃哈哈纯净水。
雄性SD大鼠,SPF级,体质量(200±20) g,[成都达硕实验动物有限公司,合格证号:SCXK(川)2015-030]。
2 方法与结果
2.1 色谱条件
Hypersil GOLD C18(100 mm×2.1 mm,1.9 μm,5 μL);流动相为乙腈(B)-0.1%磷酸(A);梯度为0~10 min,15%~25%B,10~12 min,25%~15%B;柱温 40 ℃;体积流量0.3 mL min-1;进样量 5 μL。
2.2 质谱条件
离子源采用电喷雾电离(ESI)源,检测方式:正离子检测。采用多反应监测(MRM)方式进行扫描;离子化电压(IonSpray Voltage):-4500 V,气帘气(CUR):241.325 kPa,离子源温度(TEM):550 ℃,喷撞气(CAD):Medium,喷雾器(Ion Source Gas 1):344.75 kPa,辅助加热(Ion Source Gas 2):344.75 kPa。烟花苷和内标的离子对及质谱见表1。

表1 烟花苷及内标质谱条件
2.3 对照品溶液的制备
精密称定烟花苷、柚皮苷适量,用甲醇溶解并配制成质量浓度为1 mg mL-1烟花苷和1 mg mL-1柚皮苷储备液,于4 ℃冰箱中保存待用,临用时稀释配制。
2.4 灌胃和尾静脉方式给药
大鼠适应性饲养一周,实验前禁食不禁水12 h,实验每组平行6只大鼠,一组先将烟花苷溶于1%的吐温80中,后用0.5%羧甲基纤维素钠进行稀释灌胃(50 mg kg-1),给药后5、10、20、40、50、60、70、90、120、180、240、480、720、1440 min进行眼眶采血0.5 mL,置肝素抗凝离心管中,摇匀后离心,取上清液-20 ℃保存,采血过程中灌胃补充0.9%氯化钠溶液;另一组将烟花苷溶于1%的吐温80中,后用0.5%羧甲基纤维素钠进行稀释尾静脉注射(5 mg kg-1),给药后5、10、15、20、25、30、45、60、90、120、180、240、300、360、720、1440 min进行眼眶采血0.5 mL,置肝素抗凝离心管中,摇匀后离心,取上清液-20 ℃保存,采血过程中灌胃补充0.9%氯化钠溶液。
2.5 血浆样品处理
吸取上清液200 μL,加入20 μL内标柚皮苷溶液(0.203 μg mL-1),加500 μL甲醇,涡旋振荡1 min,12 000 r min-1离心10 min,取上清液,氮气吹干,150 μL甲醇复溶,过0.22 μm滤膜,进样。
2.6 专属性考察
取空白血浆、烟花苷对照品溶液、内标溶液以及大鼠给药后血浆样品适量,按2.5项方法处理后,在2.1项色谱条件测定,结果表明动物体内内源性物质不影响烟花苷的测定,见图2。
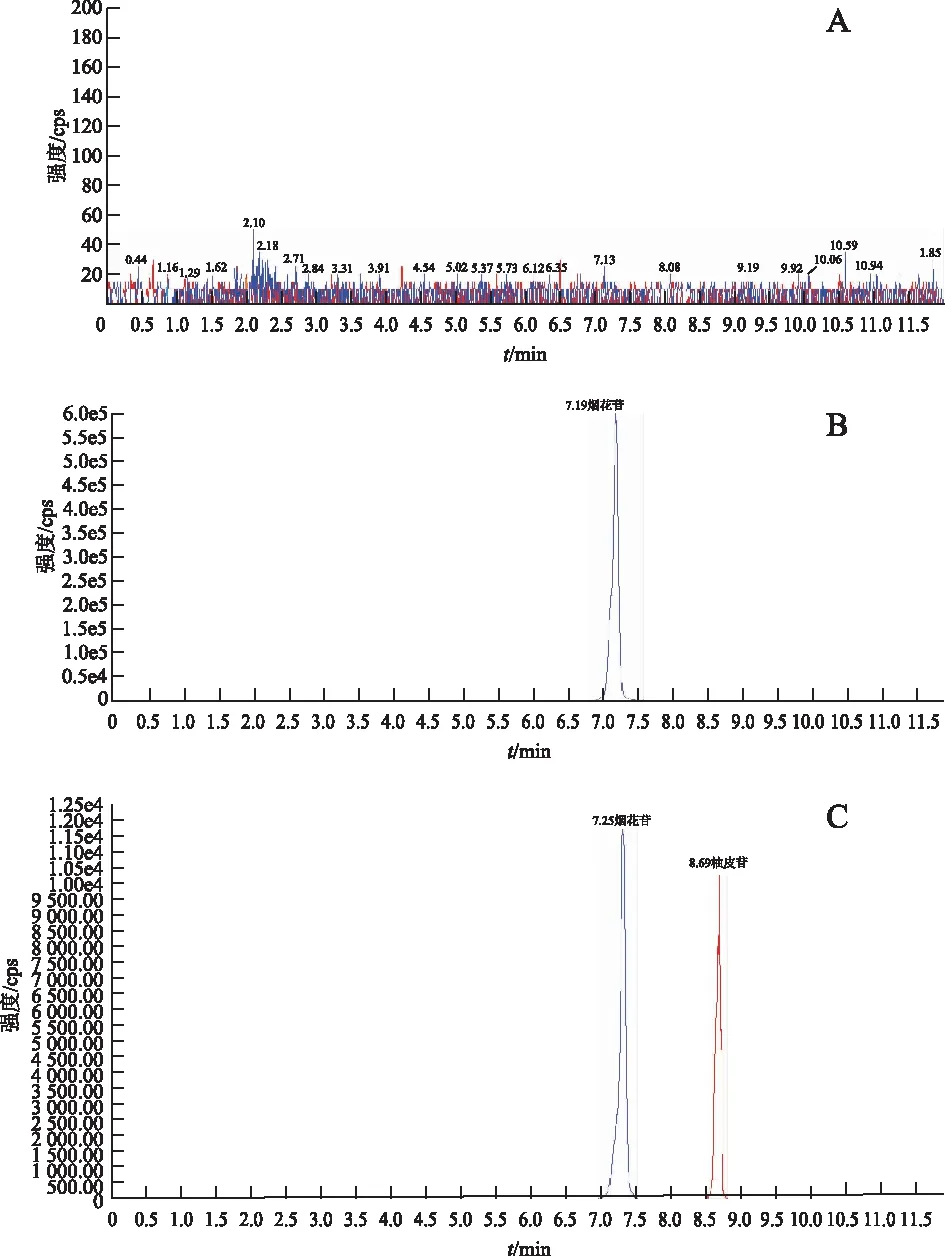
注:A.空白血浆;B.含对照品的空白血浆;C.灌胃给药后2 h血浆。图2 烟花苷及内标MRM离子色谱图
2.7 线性关系
取烟花苷储备液适量,用甲醇稀释成系列质量浓度的对照品溶液。取0.5、1、5、10、50、100、200、500、1000、2000、5000、8000 ng mL-1烟花苷溶液各200 μL,氮气吹干,加200 μL血浆涡旋2 min,按2.3项方法处理后,在2.1项色谱条件下进样测定相应峰面积。以样品血药浓度平方分之一(1/X2)为横坐标,样品峰面积与内标峰面积之比(Y)为纵坐标进行线性回归,得烟花苷回归方程Y=0.003X+0.02,(r>0.99),烟花苷在0.5~8000 ng mL-1线性关系良好,按《中华人民共和国药典》相应方法求出最低检测限(LLOD)的S/N≥3,定量下限(LLOQ)的S/N≥10,并于一天内检测6次,3 d检测3批,计算所得RSD均小于15%,烟花苷的LLOD为0.5 ng mL-1,LLOQ为4 ng mL-1。
2.8 精密度与准确度
精密吸取烟花苷的对照品溶液,加入空白血浆制成质量浓度为1、50、500、5000 ng mL-1的烟花苷质控样品,按2.5项方法处理。不同质控样品各5份,连续5 d测定血浆日内、日间精密度,见表2。
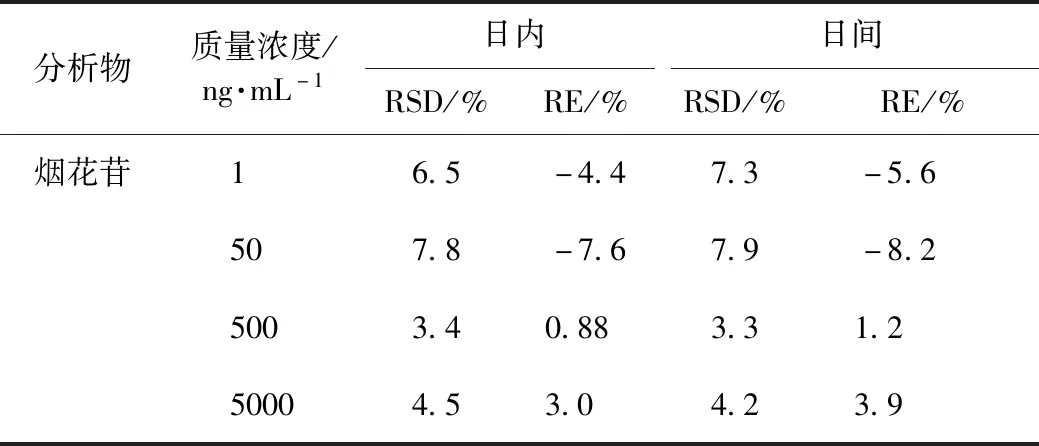
表2 血浆中烟花苷的精密度与准确度(n=5)
2.9 基质效应与提取回收率
1)精密吸取烟花苷对照品溶液及内标溶液制成1、50、500、5000 ng mL-1的质控样品,按2.1条件下测定并记录烟花苷及内标的峰面积A、B,平行测定5次。2)分别取6只不同来源的大鼠空白血浆各200 μL,按照2.5方法处理,向获得的大鼠血浆样品中加入烟花苷和内标溶液,制备成浓度为 1、50、500、5000 ng mL-1的QC样品,取5 μL进行LC-MS/MS分析,获得色谱图峰面积分别为A1、B1。3)分别取1、50、500、5000 ng mL-1的QC样品各200 μL,氮气吹干,加含内标的大鼠空白血浆各200 μL,涡旋混匀按照2.5方法处理,获得色谱图峰面积分别为A2、B2。按照2015版《中华人民共和国药典》指导原则计算归一化后的基质效应和提取回收率。结果见表3。
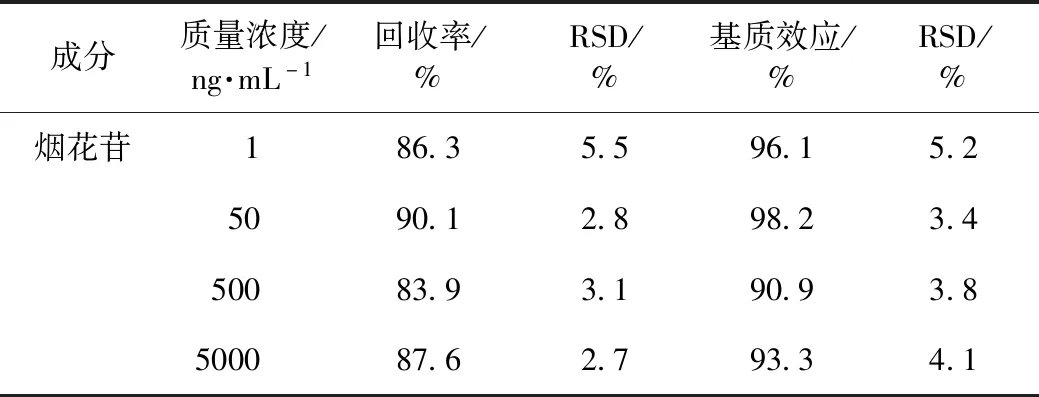
表3 烟花苷的基质效应和提取回收率(n=6)
2.10 稳定性
精密吸取烟花苷的对照品溶液,加入空白血浆制成1、50、500、5000 ng mL-1的烟花苷质控样品,按2.5项方法处理,平行制样5份,分别置于20 ℃ 12 h,-80 ℃ 30 d,-20 ℃下反复冻融3次(每次间隔24 h),4 ℃ 24 h,见表4。
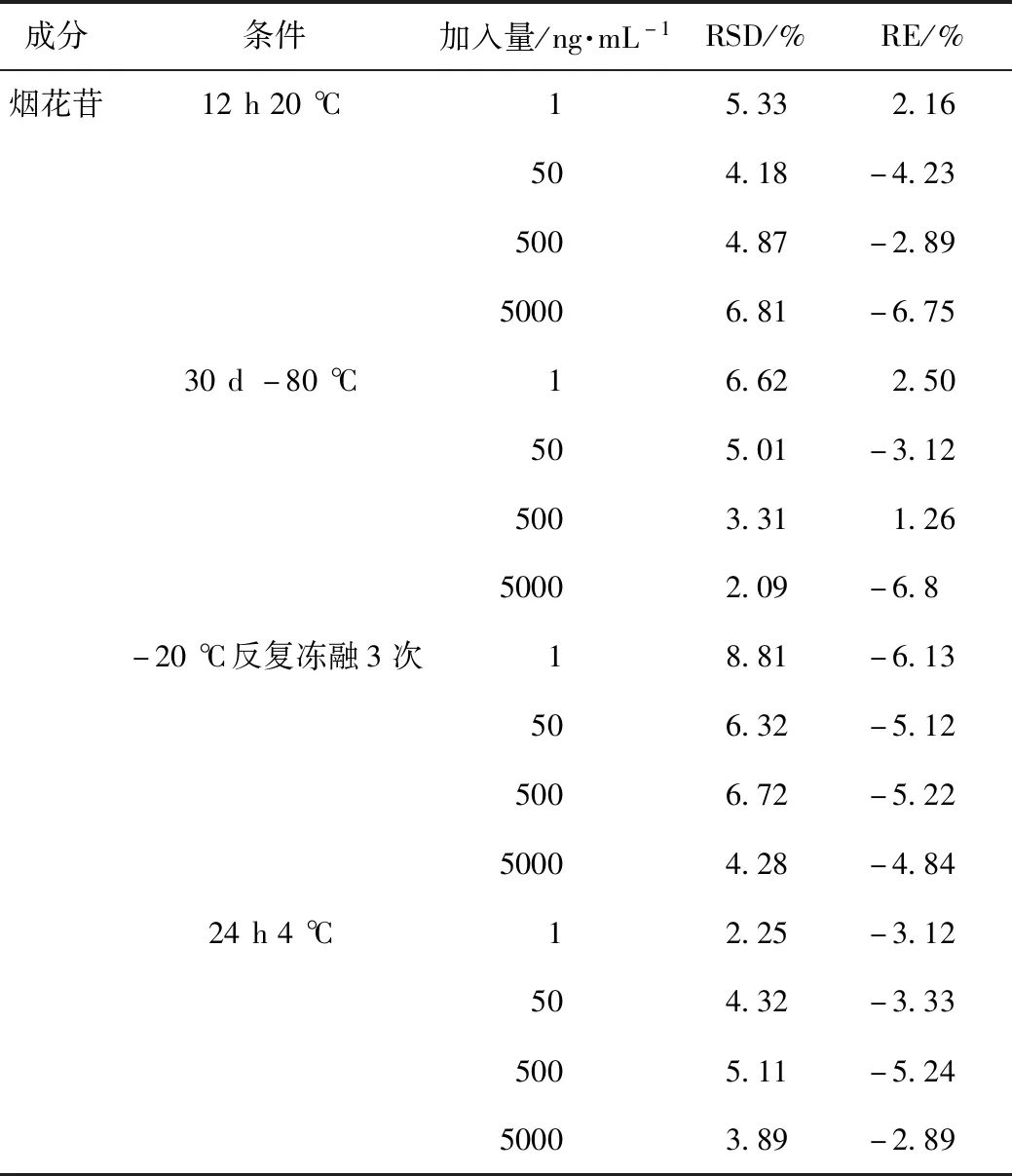
表4 血浆中烟花苷在不同储存条件下的稳定性(n=5)
2.11 烟花苷的血浆药动学
烟花苷灌胃给药和尾静脉注射给药后,所得数据经DAS药代动力学软件处理,采用药代动力学程序进行非房室模型拟合。药代动力学参数结果见表5,血药浓度-时间曲线见图3,根据公式(1),计算烟花苷的口服生物利用度为1.7%。
口服生物利用度F=[(AUC口服×静注的给药剂量)/(AUC静注×口服的给药剂量)]×100%
(1)
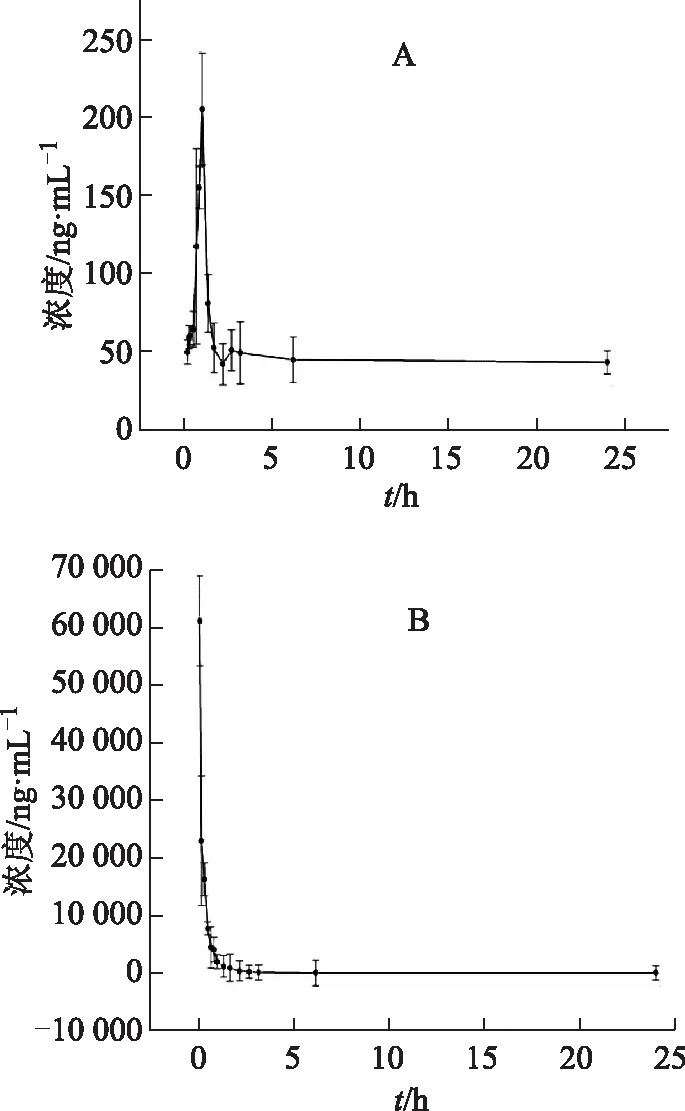
注:A.灌胃给药;B.静脉注射给药。图3 烟花苷在大鼠血浆中的血药浓度-时间曲线(n=6)
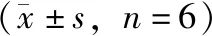
表5 烟花苷的药代动力学参数
注:—表示没有tmax值。
3 讨论
本研究建立了一种简便、灵敏的LC-MS/MS方法,用于研究烟花苷的药代动力学及生物利用度。结果表明,烟花苷的色谱总运行时间为12 min,LLOQ为0.5 ng mL-1,该方法快速、灵敏,可满足更广泛的检测要求。
血浆处理方法选择时,依照简单、方便的原则选择甲醇、10%的三氯乙酸、乙腈对血浆进行一步沉淀处理,10%的三氯乙酸处理所得色谱图中烟花苷回收率较低,故不选;乙腈处理所得色谱图中出现非检测成分的较大吸收峰,影响所选成分的检测,故不选;甲醇处理所得色谱图中烟花苷回收率良好,故选择甲醇对其进行沉淀蛋白。