肺结核空洞伴曲霉菌感染并咯血的外科治疗*
胡汶斌,张六伢,张康,韩晓亮,苏超,袁顺达,陈雪芳,刘祖平
[绍兴文理学院附属医院(绍兴市立医院) 1.胸外科;2.科教科;3.病理科,浙江 绍兴 312000]
肺结核空洞是肺组织干酪坏死液化后经支气管排出形成。空洞一旦形成,易并发曲霉菌等真菌感染,抗结核及抗真菌等内科治疗效果差,容易产生结核菌耐药,多伴有长期反复痰血或咯血,且有致命性大咯血风险,而手术能彻底清除病灶,是此类患者的最佳治疗手段。本院2013年1月-2016年12月收治施行外科手术治疗肺结核空洞伴曲霉菌感染并咯血25例患者,取得了良好的效果。现报道如下:
1 资料与方法
1.1 一般资料
本研究共25例。其中,男19例,女6例,年龄33~65岁,平均52岁。25例患者均有结核病史,病程1~8年余,均经过本院呼吸结核科正规抗结核治疗3个月以上,同时予抗真菌和止血等其他内科保守治疗2周以上,仍反复咯血及痰血,临床症状得不到改善要求手术而转入胸外科治疗。
1.2 术前症状及影像学资料
1.2.1 术前症状 咯血、痰中带血25例,其中大咯血5例;咳嗽、咳痰19例;不同程度的胸闷、胸痛8例;发热、盗汗5例。病灶分布:右上肺13例,右下肺2例,左上肺6例,左下肺1例,右上肺及右下肺跨两叶2例,其中1例伴右肺中叶毁损,左上肺及左下肺跨叶1例。
1.2.2 辅助检查 胸部CT表现:22例为典型的空洞性病变内结节状伴周围新月状或环状空气半月征,即“洞中球征”(图1),3例表现为附壁结节。痰或支气管镜肺泡灌洗液抗酸杆菌涂片及结核菌培养阳性12例,5例经内科抗结核治疗术前痰菌转阴,7例患者经结核菌培养确诊耐多药,痰找抗酸杆菌持续阳性;痰真菌培养曲霉菌2例;支气管镜检查未见明显异常6例,支气管黏膜局部红肿11例,支气管部分狭窄3例,2例见菜花样新生物,表面覆盖白色坏死组织,经肺泡灌洗液真菌涂片及培养发现曲霉菌3例;心电图检查频发室性早博2例。
1.3 治疗方法
全组均采用吸入与静脉复合麻醉,双腔气管插管,单肺通气。23例行胸腔镜辅助小切口治疗(图2),标准后外侧切口2例,其中右肺上叶切除13例,右肺下叶切除2例,左肺上叶切除6例,左肺下叶切除1例,左全肺切除1例,右肺上叶切除合并右肺下叶背段切除1例,右肺上中叶切除合并右肺下叶背段切除1例。
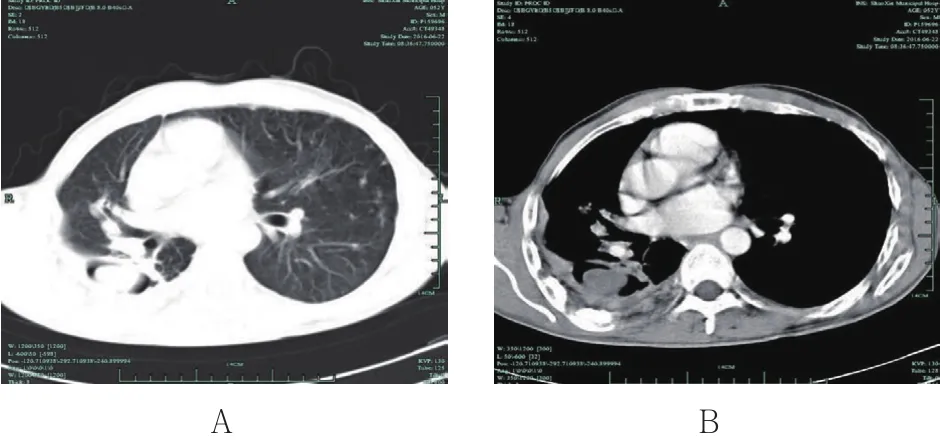
图1 CT下所示Fig.1 Images of CT
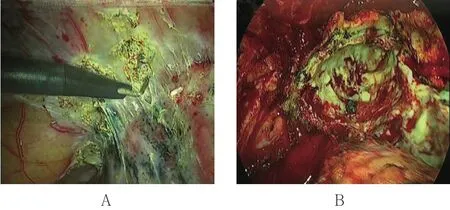
图2 胸腔镜下所示Fig.2 Images of thoracoscopy
2 结果
2.1 术中情况及放置胸管时间
手术时间120~330 min,平均160 min,术中出血200~2 000 ml,平均350 ml,术后放置胸管时间3~21 d,平均7 d。
2.2 病理学检查
空洞壁内纤维组织、淋巴组织增生伴曲霉菌球形成(图3),内均见大量真菌体,假菌丝相互交叉融合成菌团,呈淡紫蓝色,粗细基本一致,如毛刷状,散在有许多小圆形孢子。局部见芽肿性炎及钙化(图4)。抗酸染色阳性14例,诊断结核空洞伴曲霉菌感染。
2.3 术后并发症
全组无并发支气管胸膜瘘及脓胸,围手术期死亡1例,为健肺肺部感染导致呼吸衰竭。局限性肺不张8例,心律失常7例,胸腔渗血1例,反复少量咯血1例,均采用相应治疗痊愈,复查胸部CT肺复张良好。见图5。
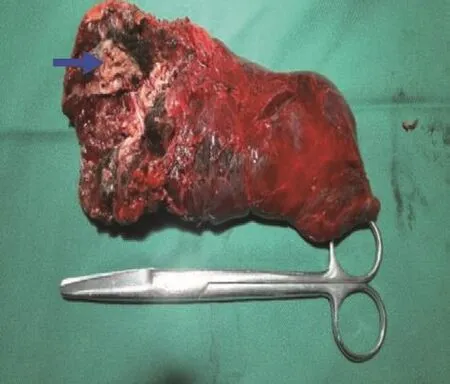
图3 手术标本Fig.3 Surgical specimens
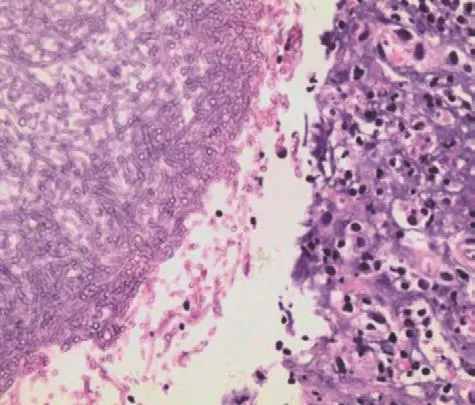
图4 显微镜下见大量真菌体 (HE×200)Fig.4 A large amount of fungi under the microscope (HE×200)
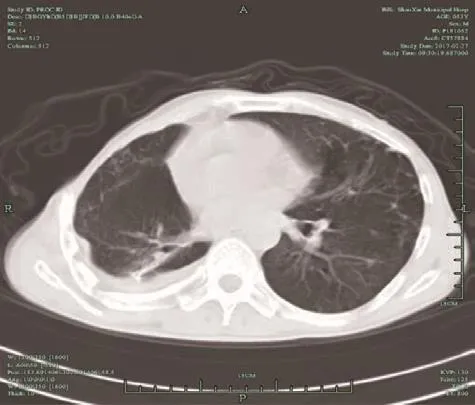
图5 CT下所示Fig.5 Image of CT
2.4 随访结果
采用门诊定期复诊的随访方式。失访2例,其余22例随访3~36个月,咯血、痰血消失,痰抗酸杆菌涂片均转阴,咳嗽、咳痰、胸闷和胸痛等症状明显缓解,生活质量提高,效果满意。
3 讨论
肺结核空洞一旦形成,抗结核药治疗效果差,在此基础上继发曲霉菌感染,抗真菌药物也很难渗透到曲霉菌病灶内。反复的抗结核、长期抗真菌治疗,易引起细菌耐药和肝功能损害等严重不良反应,而手术能够彻底清除病灶,是治愈的关键。但此类患者病程长,胸腔粘连致密,手术难度大、风险高,术后并发症多,临床处理棘手。
肺结核空洞伴曲霉菌球感染患者常反复咯血,且逐渐加重,部分患者会突然无征兆地出现致命性大咯血[1]。咯血原因主要考虑有以下几方面[2-3]:①曲霉菌球引起空洞壁及其周围肺组织的炎症反应,并且继发血管病变畸形而形成丰富的血管网,曲霉菌球在空洞内机械运动摩擦具有丰富血管网或血管瘤的洞壁,引起血管破裂出血;②曲霉菌产生的内毒素和溶蛋白酶致组织血管坏死溶解,导致出血;③炎性损伤的刺激引起空洞发生变化,导致出血;④在结核的基础上并发支气管扩张所致出血。本组25例均有不同程度的反复咯血,其中大咯血5例。
目前,对于肺结核合并肺曲霉菌感染并咯血的手术治疗仍有争议。一部分学者认为,此类患者胸腔粘连严重、手术难度大、术后并发症发生率和死亡率较高,且可能导致曲霉菌播散,故手术切除仅适用于严重咯血的患者[4-5]。但大部分学者认为,曲霉菌球一旦形成,抗真菌药物是无效的,且部分患者会突然出现无征兆的致命性大咯血,而手术治疗能够提供一个根治的机会[2]。笔者的观点是:在肺结核空洞基础上,一旦明确并存在曲霉菌感染,病变局限且能耐受手术的患者,均应首选手术治疗。对于手术时机的选择需把握以下几点[6-7]:①一般痰菌阳性患者,经过正规强化抗结核治疗2个月左右,痰菌转阴后可择期手术;②耐多药患者适当延长强化抗结核时间至3个月以上,病灶无变化,空洞仍然开放,痰菌仍持续阳性;③大咯血,急诊手术;④下叶空洞,厚壁或纤维坚壁空洞,经3个月抗结核治疗,空洞无明显缩小,仍反复痰血、咯血;⑤不能排除癌性空洞;⑥空洞破裂形成脓气胸。
本组23例采用胸腔镜辅助小切口下手术。笔者认为,在胸腔镜辅助小切口下手术,能充分地暴露手术视野,操作显得更安全,且创伤小,应作为首选手术方式。但对于胸腔胼胝样粘连者不可盲目追求微创。只要患者肺功能允许,应尽量选择行肺叶切除和肺段切除,对于表浅病灶可慎重选择肺楔形切除,切缘离病灶应>2 cm[8-9]。对于靠近锁骨下动脉及上腔静脉等大血管处致密粘连,可不追求完整切除,暂可残留部分病灶,甚至可先横断空洞,移除切下病肺后再作进一步处理,以免损伤血管大出血;肺门冻结,可采用心包内处理血管的方法以提高手术安全性[10]。
并发大咯血患者,出血部位明确且为单侧,血气分析提示能耐受肺段、肺叶切除,无心、肝和肾等重大脏器功能不全,应该果断采取手术。笔者认为,对于大咯血的救治需争分夺秒,尽快明确出血部位,可先单腔管插管麻醉,气管镜引导下吸出支气管内的积血,观察出血的支气管,快速断定出血肺叶,拔出单腔管后插入双腔管行急诊手术。分离粘连后,首先解剖结扎支气管动脉,优先闭合离断支气管,以减少术中继续出血。
术后无1例并发脓胸及支气管胸膜瘘。对于脓胸,笔者的具体防治措施是:①术前正规抗结核及抗真菌,并发肺部感染者同时联合抗感染治疗;②对于空洞致密粘连,术中横断空洞时使用纱布等隔离病灶,避免结核菌、曲霉菌进入胸腔引起结核及真菌播散;③术中常规游离叶间裂及术后早期负压吸引促进肺复张,避免大的残腔形成;④术后抗结核治疗半年,抗真菌治疗3个月。肺结核患者肺切除术后支气管胸膜瘘发生率约2.0%~6.0%。预防支气管胸膜瘘具体做法:①术前行支气管镜检查,排除支气管内膜结核;②术中处理支气管时,使用一次性切割缝合器加可吸收线缝扎加固,部分患者可考虑用肋间肌肉覆盖支气管残端;③处理支气管残端时,残端游离不宜过长,保证残端的血液供应。术后主要并发症是局限性肺不张,本组8例出现局限性肺不张,对于肺不张的处理可采取以下措施:①常规雾化吸入,湿化气道解除支气管痉挛,加强主动、有效的咳嗽咳痰,加强叩背,必要时行纤维支气管镜吸痰;②确切止痛;③水封瓶早期负压吸引;④高效抗生素,正规抗结核,有效抗真菌;⑤术后早期下床活动;⑥常规游离叶间裂、下肺韧带。心律失常多发生在老年患者,因心肺功能减退,再加上手术麻醉应激、术后疼痛刺激和电解质紊乱等易出现心律失常。本组术后发生心律失常7例,均为快速型房颤,通过心律平、胺碘酮抗心律失常及时处理后复律。术后胸腔渗血多,因胸腔粘连重、剥离创面大及术中止血不彻底等所致。1例患者术后第2天胸管引流暗红色血性液体达1 200 ml,应用血凝酶、血浆和纤维蛋白原后血止。1例患者术后3个月再次出现反复少量咯血,考虑对侧病灶所致,继续予以伏立康唑片口服抗真菌及止血等对症支持治疗后咯血渐止,密切随访,必要时再次评估,进行对侧手术切除病灶。术后常规服用伏立康唑片(0.2 g/12 h)抗曲霉菌治疗3个月。
综上所述,外科手术治疗肺结核空洞伴曲霉菌感染并咯血效果确切,安全可行,对于符合条件的患者应不失时机地手术治疗。

