非肌层浸润性膀胱癌复发与吡柔比星灌注不良反应的关系
刘华伟,杨 璐,魏 强
(1.四川省德阳市人民医院泌尿外科,四川德阳 618000;2.四川大学华西医院泌尿外科,四川成都 610041)
膀胱癌是泌尿系统最常见的恶性肿瘤之一,发病率居恶性肿瘤前十之列[1]。膀胱癌包括非肌层浸润性膀胱癌(non-muscle invasive bladder cancer,NMIBC)和肌层浸润性膀胱癌,约75%~85%新发膀胱癌为NMIBC[2],膀胱癌复发率高,严重影响患者生活质量与生存。而术后辅以膀胱灌注免疫治疗或者膀胱灌注化疗能明显降低复发率[3],故膀胱灌注治疗是NMIBC的重要辅助治疗手段,目前的研究多集中在不同灌注药物疗效和剂量等方面,大多数文献都报道了研究中所发现的灌注药物的不良反应,仅少数进行了不良反应种类、严重程度等方面的评价。临床工作中发现膀胱灌注化疗的患者对药物的不良反应程度不同,肿瘤复发情况及健康相关生活质量等也不尽相同。作为晚期转移性肾癌靶向治疗的一线药物索拉非尼、舒尼替尼有良好疗效的同时却有较严重的手足综合症等不良反应[4-5]。在膀胱灌注治疗中,被认为最有效、优于其它常用灌注药物的卡介苗也有着更大的不良反应[6]。因此,我们推测膀胱灌注药物的不良反应程度可能与患者对灌注药物的敏感性和耐受性有关,可能影响患者的肿瘤复发情况和健康相关生活质量等。本研究通过回顾性研究分析不同预后(肿瘤复发组和肿瘤未复发组)的非肌层浸润性膀胱患者的临床资料、灌注不良反应种类及程度,以探索肿瘤复发情况与膀胱灌注化疗不良反应程度的关系。
1 资料与方法
1.1病例资料纳入四川大学华西医院经尿道膀胱肿瘤切除术(transurethral resection of bladder tumor,TURBT)术后行膀胱吡柔比星灌注化疗的新发NMIBC患者80例。在术后1年内膀胱肿瘤复发的36例患者为肿瘤复发组(男性27例,女性9例),观察期间未见复发的44例患者纳入肿瘤未复发组(男性29例,女性15例),回顾性分析两组患者的临床资料。
1.2研究方法膀胱灌注使用一线灌注药物吡柔比星。纳入的80例NMIBC均行过经尿道膀胱肿瘤切除术并在术后辅以膀胱灌注化疗,均使用灌注一线药物吡柔比星按中华医学会泌尿外科指南方案实施[7]。将膀胱灌注化疗药物不良反应按照VAN DER等[8]报道的分类方法将不良反应分为局部泌尿系统不良反应和全身系统性不良反应,局部泌尿系统不良反应包括尿频、尿急、尿痛、血尿、脓尿、排尿困难等泌尿系统不良反应,全身系统性不良反应包括一般情况、骨骼肌肉系统、呼吸系统、皮肤、消化系统、眼睛、心血管系统等系统不良反应。按照国际上BASSI等[9]报道的分级方法将膀胱灌注化疗药物不良反应的严重程度分级如下(0级,无不良反应;1级,无需治疗的不良反应;2级,需治疗的不良反应;3级,需延迟灌注的不良反应;4级,需中断灌注的不良反应。)对比两组患者灌注化疗的药物剂量、灌注次数、不良反应(采用问卷方式收集患者尿频、尿急、尿痛、血尿、脓尿、排尿困难等局部不良反应及系统不良反应)、膀胱镜复查结果、膀胱肿瘤复发和进展等情况,返回的有效问卷纳入统计学分析。
1.3统计学方法采用SPSS 17.0版本软件进行统计学分析,符合正态分布的计量资料组间差异分析运用t检验进行处理;计数资料的组间差异分析运用卡方检验进行处理;等级资料的组间差异分析运用秩和检验进行处理,P<0.05为差异具有统计学意义。
2 结 果
本研究共纳入膀胱尿路上皮癌患者80例,其中男性患者56例(70.0%),女性患者24例(30.0%),最大年龄85岁,最小年龄27岁,肿瘤复发组36例,肿瘤未复发组44例,两组NMIBC患者的两组患者的人口学及肿瘤学特征基线一致 (表1)。
表1研究人群人口学及肿瘤学特征(例)
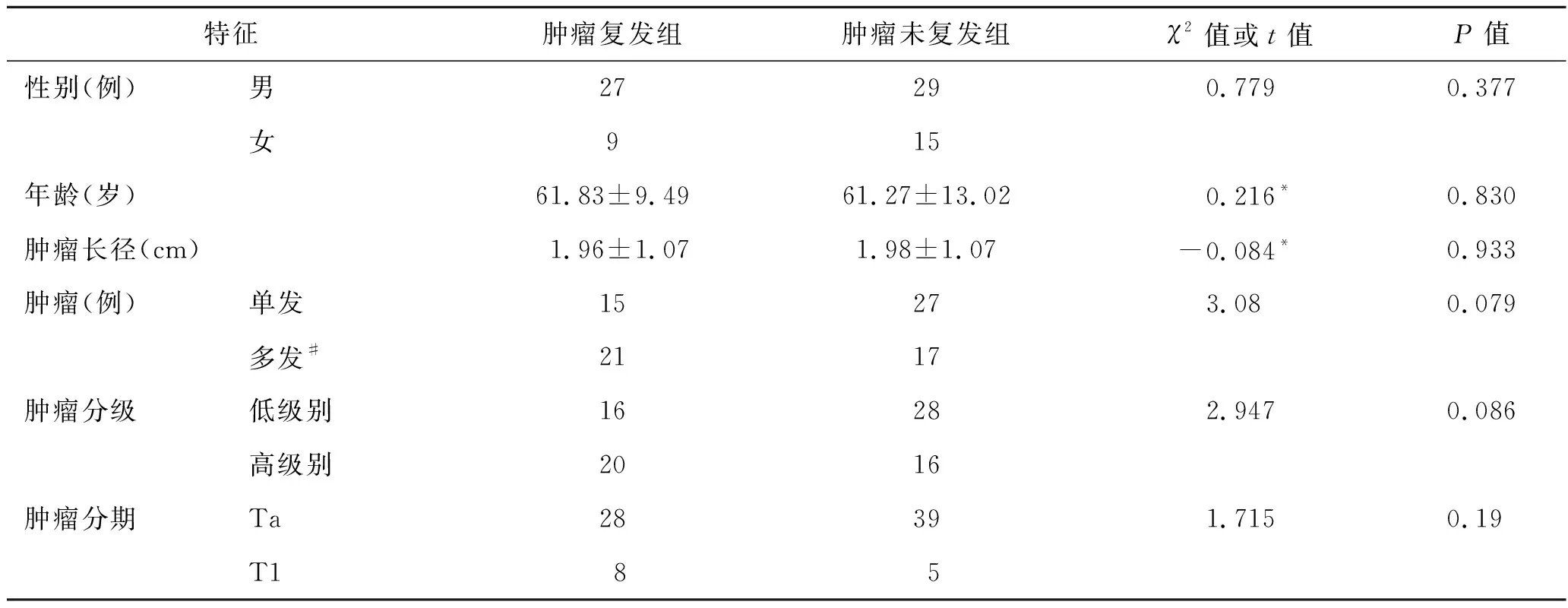
*:t值;#:肿瘤个数≥2个。
2.1泌尿系统不良反应80例患者不良反应中尿痛发生率60.0%、尿频52.5%、尿急50.0%,排尿困难、血尿、脓尿的发生率分别为15.0%、8.7%、5.0%。大部分泌尿系统不良反应程度为Ⅰ、Ⅱ级,自限性病程无需治疗,或者是给予抗胆碱药物等对症支持即可缓解,无需中断膀胱灌注化疗。仅有6例患者(7.5%)发生泌尿系统Ⅲ级药物不良反应,需要延迟膀胱灌注化疗(表2)。
2.2全身系统性不良反应在全身系统性不良反应中,发生率最高的是以乏力、精神欠佳、发热等为主要症状的一般情况不良反应,占23.7%,其次是肌肉骨骼疼痛,发生率为7.5%,恶心等消化系统不良反应发生率为5.0%,以瘙痒为主要症状的皮肤不良反应发生率为3.7%,以视力下降为主要症状的眼睛不良反应和以心悸为主要症状的心血管系统的不良反应发生率均为2.5%。全身系统性不良反应严重程度均为Ⅰ级药物不良反应,自限性病程无需治疗(表3)。
表2两组患者泌尿系统不良反应种类及程度(例)
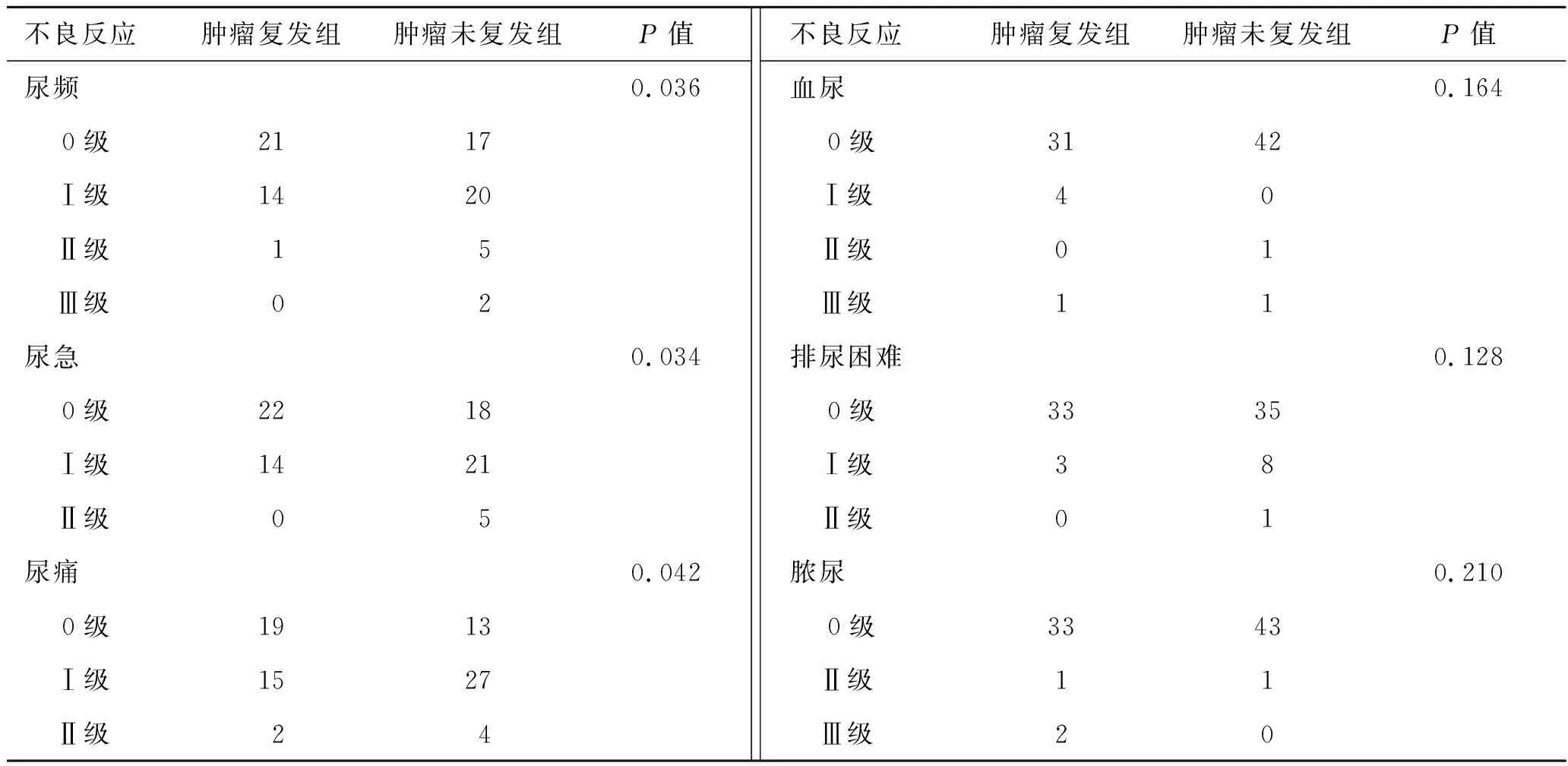
不良反应肿瘤复发组肿瘤未复发组P值尿频0.0360级 2117Ⅰ级 1420Ⅱ级 15Ⅲ级 02尿急0.0340级 2218Ⅰ级 1421Ⅱ级 05尿痛0.0420级 1913Ⅰ级 1527Ⅱ级 24不良反应肿瘤复发组肿瘤未复发组P值血尿0.164 0级3142 Ⅰ级40 Ⅱ级01 Ⅲ级11排尿困难0.128 0级3335 Ⅰ级38 Ⅱ级01脓尿0.210 0级3343 Ⅱ级11 Ⅲ级20
等级资料的组间差异分析运用秩和检验统计方法。
表3两组全身系统性不良反应种类及程度(例)
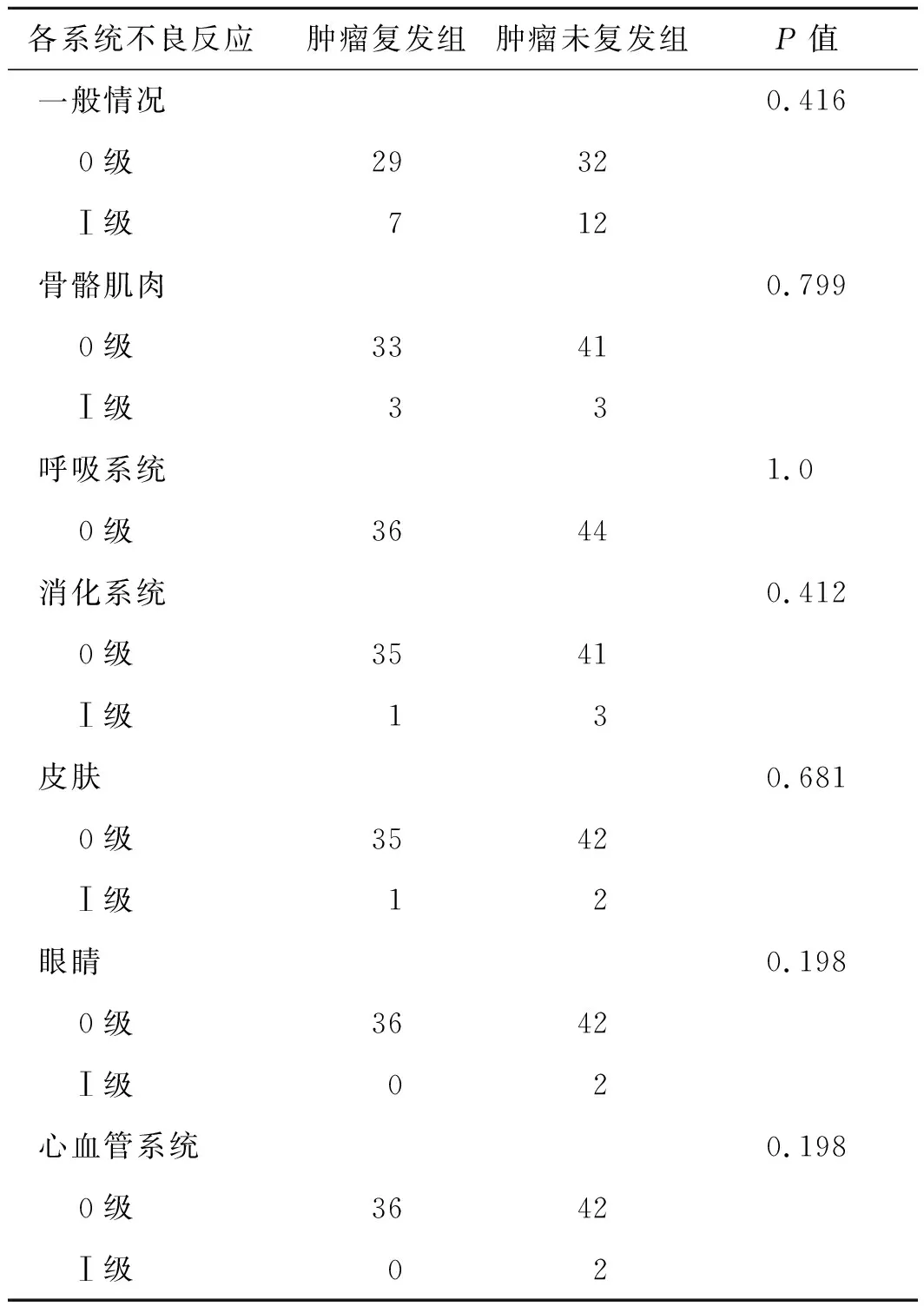
各系统不良反应肿瘤复发组肿瘤未复发组P值一般情况 0.416 0级 2932 Ⅰ级 712骨骼肌肉 0.799 0级 3341 Ⅰ级 33呼吸系统 1.0 0级 3644消化系统 0.412 0级 3541 Ⅰ级 13皮肤 0.681 0级 3542 Ⅰ级 12眼睛 0.198 0级 3642 Ⅰ级 02心血管系统 0.198 0级 3642 Ⅰ级 02
等级资料的组间差异分析运用秩和检验统计方法。
3 讨 论
NMIBC的复发和进展与肿瘤的大小、数目、分期、分级、肿瘤复发的时间和频率、是否伴原位癌等因素密切相关[10]。本研究中肿瘤复发组与未复发组的患者性别构成比、平均年龄、肿瘤的平均大小、肿瘤的单发和多发构成比、肿瘤分期和分级构成比差异无统计学意义;且两组患者均为新发膀胱癌患者、不伴原位癌,影响NMIBC患者预后的最主要的因素在两组患者之间相似,确保了两组患者的可比性。本研究中显示吡柔比星膀胱灌注化疗局部泌尿系统不良反应发生率较高(86.2%),且严重程度分别有Ⅰ、Ⅱ、Ⅲ级;全身系统性不良反应发生率相对较低(33.7%),且严重程度最高为Ⅰ级,自限性病程无需治疗。局部泌尿系统不良反应发生率最高的是尿频(52.5%)、尿急(50.0%)和尿痛(60.0%),排尿困难、血尿、脓尿的发生率分别为15.0%、8.7%、5.0%。而全身系统性不良反应发生率最高的就是以乏力、精神不佳、发热等为主要症状的一般情况不良反应,占23.7%,其他系统性不良反应发生率均较低;无Ⅳ级药物不良反应,也显示了吡柔比星作为NMIBC膀胱灌注化疗一线药物的安全性。国内外未见文献报道膀胱肿瘤复发和膀胱灌注化疗药物不良反应的关系,本研究将复发和未复发的膀胱癌患者做回顾性分析研究其膀胱吡柔比星灌注化疗期间不良反应的程度。本研究结果显示两组患者在灌注全身系统性不良反应方面差异无统计学意义,这可能与吡柔比星分子量较大,不容易被系统吸收进入血液[11],从而较少引起全身系统性不良反应有关。但是两组患者在发生率最高的尿路刺激症状(尿频、尿急、尿痛)方面表现出显著统计学差异,未复发的膀胱癌患者较复发的患者在膀胱灌注期间有更为严重的尿路刺激症状,而在血尿、排尿困难等其他泌尿系统不良反应症状方面差异无统计学意义。我们推测两组间不良反应程度差异的出现可能与膀胱组织间隙的大小有关,从而引起膀胱组织对灌注化疗药物吸收的浓度的差别而导致药物不良反应程度和疗效的差别,同时也有可能因未复发组患者行TURBT手术时切除的深度较深、切除范围更大而致灌注化疗期间更严重的尿路刺激症状和更好的疗效,但需要未来进一步的研究来证实。这样泌尿外科临床医生根据膀胱灌注不良反应的程度判断患者对灌注药物的敏感性和耐药性及预测患者的预后就成为可能,可以更好地选择或者更换合适的灌注药物以及管理灌注药物不良反应,将更大程度地降低膀胱肿瘤复发率和提高患者生活质量。
本研究中膀胱灌注化疗药物不良反应发生率最高的是尿痛(发生率60.0%)、尿频(发生率52.5%)和尿急(发生率50.0%);肿瘤未复发组局部泌尿系统不良反应严重程度显著高于肿瘤复发组的症状是尿频、尿痛、尿急为主的尿路刺激症状,而血尿、排尿困难、脓尿局部不良反应症状两组间差异无统计学意义(P>0.05)。两组间发生的以乏力、精神欠佳、发热为主要症状一般情况不良反应差异无统计学意义(P>0.05)。经尿道膀胱肿瘤切除术后1年内膀胱肿瘤未复发组较复发组的NMIBC患者在膀胱吡柔比星灌注化疗期间有更严重的尿频、尿痛、尿急症状(尿路刺激症状),而两组患者的其他局部泌尿系统不良反应(排尿困难、血尿、脓尿症状)和全身系统性不良反应程度相似。

