神经分子影像:阿尔茨海默病的动态神经病理
纪勇,艾林
作者单位
1100070 北京
首都医科大学附属北京天坛医院认知障碍中心,国家神经系统疾病临床医学研究中心
2首都医科大学附属北京天坛医院PET中心
神经退行性疾病多数是一个或多个折叠或错误折叠的病理性积累,与聚集的蛋白质相关。既往唯一确定诊断方法是尸检(神经病理)来确认这些异常蛋白质沉积或病理变化的存在。尸检或活检发现这种特征性病理改变是诊断疾病的必要条件。如果能在早期发现确诊,即在疾病的不可逆性改变之前可能会得到更好的干预治疗。因为脑组织反复活检是不现实的,所以无创或微创的特异性诊断技术被迫切需要。阿尔茨海默病(Alzheimer's disease,AD)是最常见的神经退行性疾病,是导致老年期痴呆的主要原因[1]。目前特异性诊断AD的生物学标志物有脑脊液的β-淀粉样蛋白(amyloid β-protein,Aβ)和tau蛋白的测定,另一个就是正电子发射断层扫描(position emission tomography,PET)确定脑内AD的特征性病理蛋白:Aβ(老年斑)和tau(神经纤维缠结)[2]。本文主要讨论Aβ和tau蛋白在脑内的病理性成像变化,通过可重复的评估患者脑内整体和局部的Aβ沉积和tau成像与临床结合的特点,阐明二者在AD的特异性早期诊断、发病机制与临床症状的关系、治疗靶点及治疗效果的评估。本文介绍典型和非典型AD的影像学特点。
AD细胞外Aβ沉积和细胞内tau神经纤维缠结是其两个主要神经病理学特征。很多研究表明Aβ积累是一个漫长的过程,可以在AD发病前20年开始沉积。Aβ-PET成像已被批准用于临床,应用于抗Aβ治疗的临床试验中患者的筛选和治疗结果评估。
随着神经分子影像学技术的进步,神经分子影像可以在活体确定AD的神经病理特征,可以说等同于神经病理诊断。AD的相关学术机构也顺应这种变化,不断地更新了AD相关的概念和诊断标准。近期美国国家衰老研究所(National Institute of Aging,NIA)和阿尔茨海默病协会(Alzheimer's Association,AA)发布了AD新的定义,即AD是脑内的淀粉样斑块和神经纤维缠结的病理积累[3]。美国AA最新发表的《2017年的阿尔茨海默病事实和概况》及时反映了这种进展与术语的变化,认为以往临床诊断的“阿尔茨海默病”,以后应该称为“阿尔茨海默痴呆”[4]。
AD的临床特征是进行性的记忆力减退和认知障碍并且影响患者的日常生活[5]。AD在临床诊断之前一般有3~6年的遗忘型轻度认知障碍(mild cognitive impairment,MCI)[6]。迄今为止,虽然仍然有争议,但几乎所有病理、遗传、生化细胞学证据都支持这样的观点:各种遗传、环境因素、机体的状态等导致Aβ产生增加和(或)清除减少,致其在大脑中的沉积是AD发病的核心机制[7]。
神经分子影像是当前核医学领域的前沿与热点,尤其是以PET为代表的核医学分子影像技术为药物的快速研发提供了一个崭新的、强有力的高技术平台。应用放射性示踪剂进行中枢神经系统的显像研究,可以阐明神经系统疾病的发生、发展机理,辅助选择、确立治疗方案,还可以为治疗药物的研制提供指导。
淀粉样蛋白成像技术第一次在活体内反映了β样淀粉蛋白的病理特征,与尸检检测Aβ的含量具有相同的力度和局限性[8]。淀粉样蛋白成像的示踪剂检测的是β折叠型的纤维状Aβ。虽然目前应用的示踪剂也能结合到β折叠形式的寡聚体,但寡聚体相对于不溶性Aβ纤维处于低浓度状态,在活体内很难单独显示。
淀粉样蛋白成像一般由专业医师通过临床和认知评估综合应用[9]。一般遵循以下标准:对持续性或进行性无法解释的认知障碍患者,年龄≤65岁的痴呆或进展性非典型痴呆或不明原因者。下列情况一般不做淀粉样蛋白PET成像检查:很可能的AD患者,典型的发病年龄,为确定痴呆严重程度;无症状患者或未确认的认知障碍患者;有痴呆家族史或存在APOE e4等位基因;用于非医疗目的,如诉讼纠纷或健康保险等。
1 氟化脱氧葡萄糖PET应用于阿尔茨海默病的成像基础
脑氟化脱氧葡萄糖(fluorodeoxyglucose,FDG)-PET作为脑代谢有效的生物标志物被广泛地应用,主要反映内在的突触活性。因为脑几乎完全依靠葡萄糖作为能量的来源,所以葡萄糖的类似物FDG用18F进行标记后通过PET来检测,能作为脑代谢很好的示踪剂。脑的能量主要是维持脑内静息时的活动,在皮层主要是保持谷氨酸能的突触信号传递。FDG-PET的吸收率与尸检证实的突触小泡蛋白-突触素水平明显相关。
典型的AD(typical AD,TAD)患者脑内主要葡萄糖代谢率减低部位为双侧颞顶叶或颞顶联合区、楔前叶、后扣带回,部分患者额叶外侧皮层代谢减低;尾状核为主要皮质下代谢减低的部位。轻度AD患者葡萄糖代谢率减低主要部位为颞顶联合区皮层、楔前叶、后扣带回、尾状核等,对称或不对称受累;中度AD患者较轻度AD患者以上代谢减低范围扩大及额叶外侧、前扣带回等部位。后皮质萎缩(posterior cortical atrophy,PCA)患者主要代谢减低部位为双侧颞顶枕联合区、楔前叶、后扣带回,多呈不对称分布。以执行功能障碍为主的额叶变异型AD(frontal variant Alzheimer's disease,FvAD)患者代谢减低主要位于双侧额叶内外侧皮层、双侧颞-顶叶联合皮层、后扣带回、楔前叶等。寡语性原发性进行性失语(logopenic primary progressive aphasia,LPA)轻度痴呆患者表现为左侧或右侧颞顶叶为主的代谢减低,部分出现同侧额叶外侧代谢减低,中度痴呆患者出现对侧颞顶联合区代谢减低(图1)。
2 淀粉样蛋白PET应用于阿尔茨海默病的成像基础
淀粉样蛋白成像技术在AD中最重要的突破是第一次在活体内反映了Aβ的病理[10]。淀粉样蛋白成像在诊断中的应用与尸检判断Aβ的含量具有相同的力度和局限性。淀粉样蛋白成像另一个重要问题是:到目前为止,淀粉样蛋白成像的示踪剂检测的都是β折叠型的纤维状Aβ[11]。典型的致密的、有核心的和神经丝样的淀粉样沉积斑块有大量的纤维状蛋白,蓬松的、无定型的斑块很少(尤其在小脑),而弥漫的斑块没有明确的定义,Aβ的量变异很大。由于有相似的排列,脑血管淀粉样变性有大量纤维状Aβ,是淀粉样示踪剂很好的结合底物[11]。寡聚体的Aβ毒性也越来越得到重视[12]。目前应用的示踪剂也能结合到达到一定量的β折叠形式的寡聚体(可能至少是三聚体或四聚体),但因为寡聚体相对不溶,Aβ纤维处于低浓度状态,在活体内很难显示。
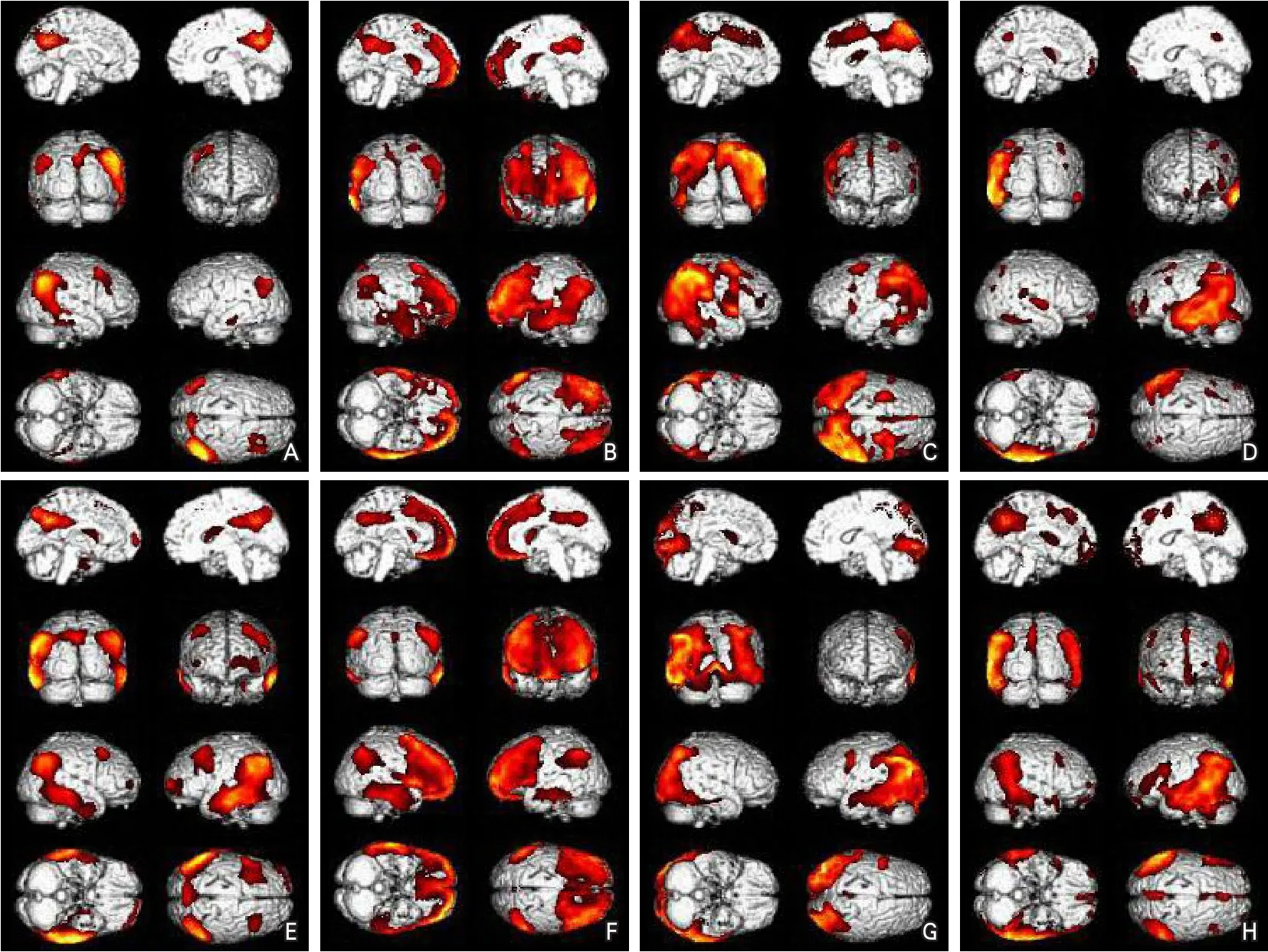
图1 不同亚型AD患者大脑葡萄糖代谢SPM图
既往的PET研究发现,约25%~35%临床上认知功能正常的老年人患有不同程度的Aβ阳性滞留,主要在后方扣带回、楔前叶和前额叶[13-14]。这些结果与验尸完全一致。研究还显示年龄≥75岁的非痴呆人群中约25%有Aβ沉积,也可能代表是临床前AD[15-17]。此外,(N-甲基-11C)2-[4'-(甲氨基)苯基]-6-羟基苯并噻唑,也称为匹茨堡化合物B(Pittsburgh compound B,PIB)高滞留率约每十年的增加率与非痴呆个体尸检的淀粉样沉积斑块增加率的速度相同[13]。早期或临床前期的特异性的Aβ检查,可以帮助AD的早期诊断和治疗。
视觉分析显示,对照组人群注射PIB 45 min后,皮质、皮质下核团、脑桥、小脑放射性活性基本上已清除。AD患者在相同的时间点,双侧对称或不对称的额叶、顶叶皮层、颞叶外侧、楔前叶、后扣带回、枕叶等部位PIB沉积阳性(图2)。基于体素水平自动化分析显示各组患者所有感兴趣区PIB标准化摄取值比值(standard uptake values ratio,SUVR)没有显著差异。
3 tau蛋白PET应用于阿尔茨海默病的成像基础
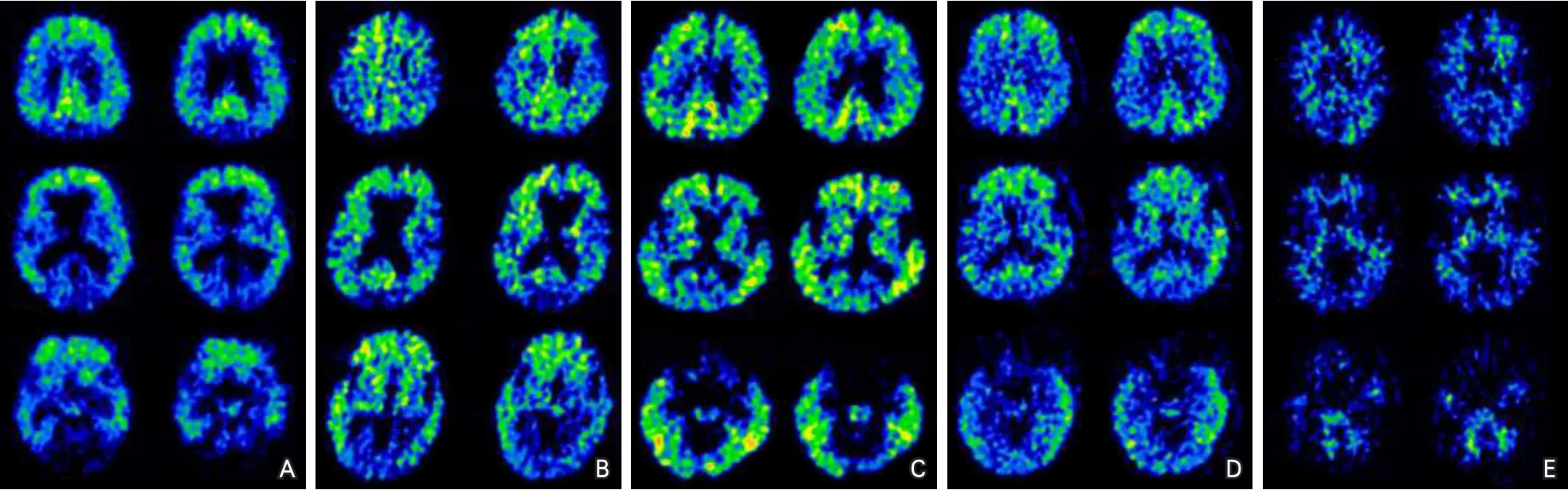
图2 不同亚型AD的PIB PET图像比较
神经纤维缠结是AD的主要病理改变,神经纤维缠结主要由高度磷酸化tau蛋白组成。高度磷酸化的tau蛋白在细胞内形成不溶性的双螺旋丝。尸检证实神经纤维缠结的负荷与痴呆和神经变性的严重程度相关,提示神经纤维缠结对神经变性有直接的影响。在活体内检测tau蛋白聚集将对研究AD的病理生理改变提供有用的信息。tau蛋白的标记较老年斑困难,因为tau蛋白位于细胞内,这就要求示踪剂必须能穿越血脑屏障和细胞膜;tau蛋白在脑内的含量较低且tau蛋白有多个同型异构体,与微管结合的结构域重复三次(3R)还是四次(4R)代表着选择性剪切的形式。目前认为tau蛋白的水平与神经细胞的死亡有关,即与AD的症状和疾病进展密切相关,希望其特异性标志物尽早应用于临床。
最近,一些PET的示踪剂已经用来检测人脑中的tau蛋白的病理变化(图3)[18]。这些示踪剂大多数都结合到tau蛋白质的β折叠结构,对tau蛋白的寡聚体不敏感。AD患者在近中线附近的颞叶,颞顶叶和后扣带皮质区域显示明显的示踪剂滞留,有时延伸至额叶。
AD具有共同的病理表现,老年斑的沉积和神经纤维缠结,但临床表现多样,除了典型的记忆障碍为主型,还包括其他亚型即AD的变异型,也就是不典型AD:后部皮质萎缩(posterior cortical atrophy,PCA),又称为视觉变异型AD(visual variant of AD),患者早期症状主要为视空间障碍、视觉失认、失用、方向感缺失、失写及失算。神经心理量表提示视空间结构、书写、计算力受累突出,患者视较大物体检查出现错误率更高,是“只见树木,不见森林”,有时也成为“大字不识”。LPA临床上以命名、找词和重复语言障碍为主。FVAD特点为在痴呆的早期额叶功能受损。
国际工作组(International Working Group,IWG)及美国NIA-AA推出的AD诊断标准能够更好地定义临床表型以及将生物标志物整合进诊断进程中,从而全面覆盖疾病各个时期(从无症状到最严重痴呆阶段)[3]。根据这个标准,我们根据结构影像和分子影像简单概述了典型AD和非典型AD的影像学诊断特点(图4~图7)。
随着影像技术的发展与成熟,神经分子影像已经成为AD早期诊断和鉴别诊断的重要且必要手段,是进一步揭示AD病理机制不可缺少的工具。

图3 显示tau标志物THK5351注射40~60 min后SUVR在PET-MRI图像的平均值[18]

图4 典型AD患者影像学特点

图5 非典型AD——FvAD患者影像学特点

图6 非典型AD——PCA患者影像学特点

图7 非典型AD——LPA患者影像学特点

