回归原点,阿尔茨海默病的概念与诊断的进步
纪勇,艾林
作者单位
1100070 北京
首都医科大学附属北京天坛医院认知障碍中心,国家神经系统疾病临床医学研究中心
2首都医科大学附属北京天坛医院神经影像中心
基于生物学标志物,目前用于研究目的,由(美国)国家衰老研究所(National Institute of Aging,NIA)和阿尔茨海默病协会(Alzheimer's Association,AA)近期发布了阿尔茨海默病(Alzheimer's disease,AD)的最新诊断框架(NIA-AA Research Framework),简称AT(N)诊断框架,即通过脑内的β淀粉样蛋白蓄积沉积和tau蛋白异常及形成的神经纤维缠结即可诊断AD[1]。AT(N)诊断框架中“A”表示由正电子发射断层扫描(position emission tomography,PET)上淀粉样蛋白显影或脑脊液(cerebrospinal fluid,CSF)β-淀粉样蛋白(amyloid β-protein,Aβ)42(Aβ42/Aβ40比率)测量的Aβ状态;“T”代表异常tau蛋白,PET tau显影(神经纤维缠结)或CSF磷酸化tau(phosphorylated tau,P-tau)(图1);“N”表示神经变性或神经元损伤的生物标志物,如CSF总tau(total tau,T-tau),氟化脱氧葡萄糖(fluorodeoxyglucose,FDG)-PET或通过磁共振成像(magnetic resonance imaging,MRI)测量的脑皮质萎缩。A(老年斑)和T(神经纤维缠结)作为AD病理学的特异性特征,二者的阳性标记可以确诊AD。由于N代表的萎缩不是疾病特异性的,多数的阳性N表示疾病的晚期或一定的疾病程度,所以N加以括号(表1)[2]。
在AT(N)诊断框架中,AD的诊断并不以疾病的临床表现(症状/体征)为基础,而是将AD的定义从综合征转变为生物学结构概念。2018年的AD诊断框架也可以使用(N)作为生物学标志物,与NIA-AA 2011的标准相比,2018年AD诊断框架的一个新颖之处在于,AD不再是三个不同的临床阶段,而是将其概念化为独立于认知状态的生物构建体,这使NIA-AA 2018符合国际工作组(International Working Group,IWG)的标准,并且是一项重大改进。另一个变化是2018年AD分类方案将tau标记(T)与神经元损伤标记(N)分开,这种分离意味着这些标记是不同的实体。
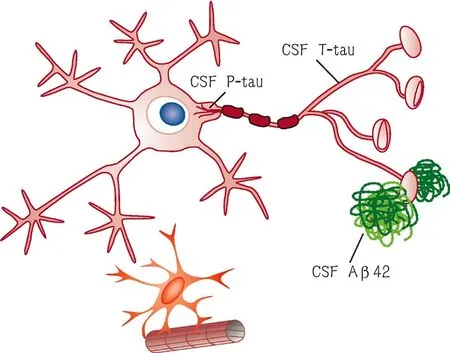
图1 阿尔茨海默病脑脊液病理变化
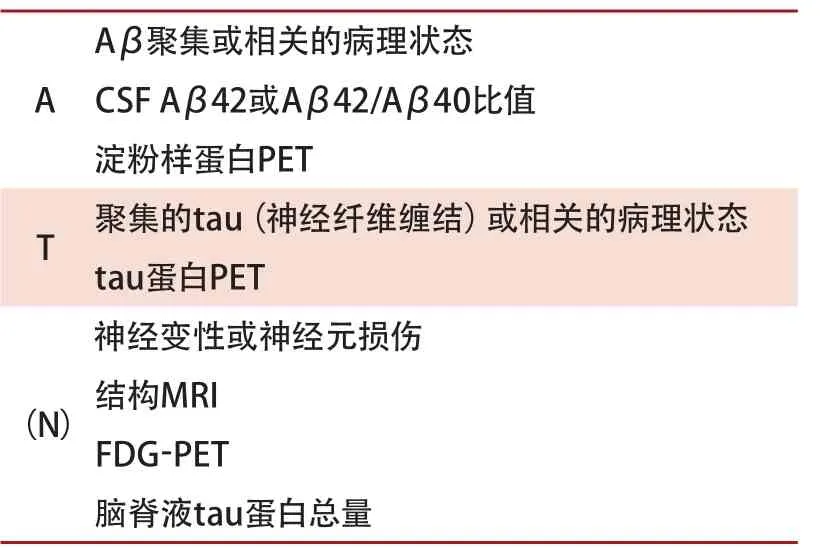
表1 AT(N)生物标志物分组
2018年AD诊断框架为:有A和T的证据则定义为阿尔茨海默病,在研究实践中即可诊断为AD;如果只有A的证据,没有T的证据则定义为阿尔茨海默病的病理改变,不能确诊为AD;以上二者并不是孤立的,是AD连续发展的不同时期而已;但如果没有A的证据则是非阿尔茨海默病(表2)。
新的NIA-AA 2018 AD诊断框架标志着如何看待这种疾病并向更好的诊断原则迈出了一大步。诊断基于病理的生物学标志物而不再是临床分期的框架,将有助于改善临床研究及药物试验。同时美国食品和药品管理局最近也做出了类似的建议决定,其中生物标志物在临床试验中的重要性已经更新[3]。新的AD诊断框架与早期的NIA-AA方案与IWG标准的基本一致,一个非常重要的变化是基于病理生物标志物代谢,识别并将AD定义为单一疾病,而不是三种不同的综合征。这是将阿尔茨海默病的诊断与任何临床症状区分开来的一步。根据新框架,疾病分期独立于基于生物标志物的诊断。该框架提出了两种用生物标志物确证的AD的分期方案(表3)。一种使用额外的神经变性生物标志物,另一种涉及症状。对于后者,该委员会提倡使用1~6数字量表,标志从认知无损到痴呆不同阶段。同时,该框架也指出,在医疗实践中如果没有生物标志物数据的情况下,可以保留对认知的综合分期,这保留了熟知的从无认知功能障碍、轻度认知功能障碍和痴呆的分类,但一般不能明确病因。
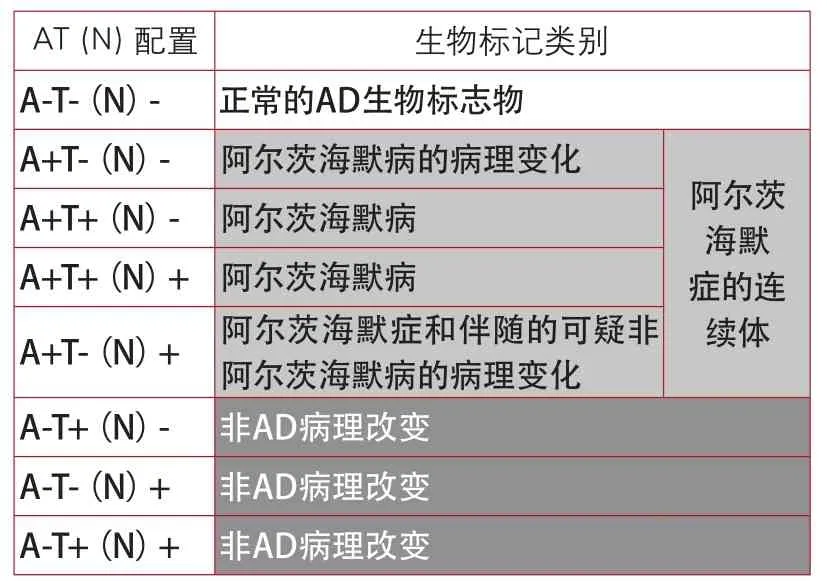
表2 AD生物标志物的概况和类别
AA最新发表的《2017年AD事实和概况》反映了这种进展与术语的变化[4]。也就是说,术语“阿尔茨海默病”是描述疾病的整个连续过程,而“阿尔茨海默痴呆”是描述连续性的痴呆阶段。过去报告使用“阿尔茨海默病”,现在的最新版本中使用“阿尔茨海默痴呆”。最明显的是患病率的描述,2017年以前报道:2016年美国有540万人患有阿尔茨海默病,而2018年报道:美国有550万人患有阿尔茨海默痴呆。唯一改变的是这个词的用语不同。
关于AT(N)系统,可能会有以下的问题:
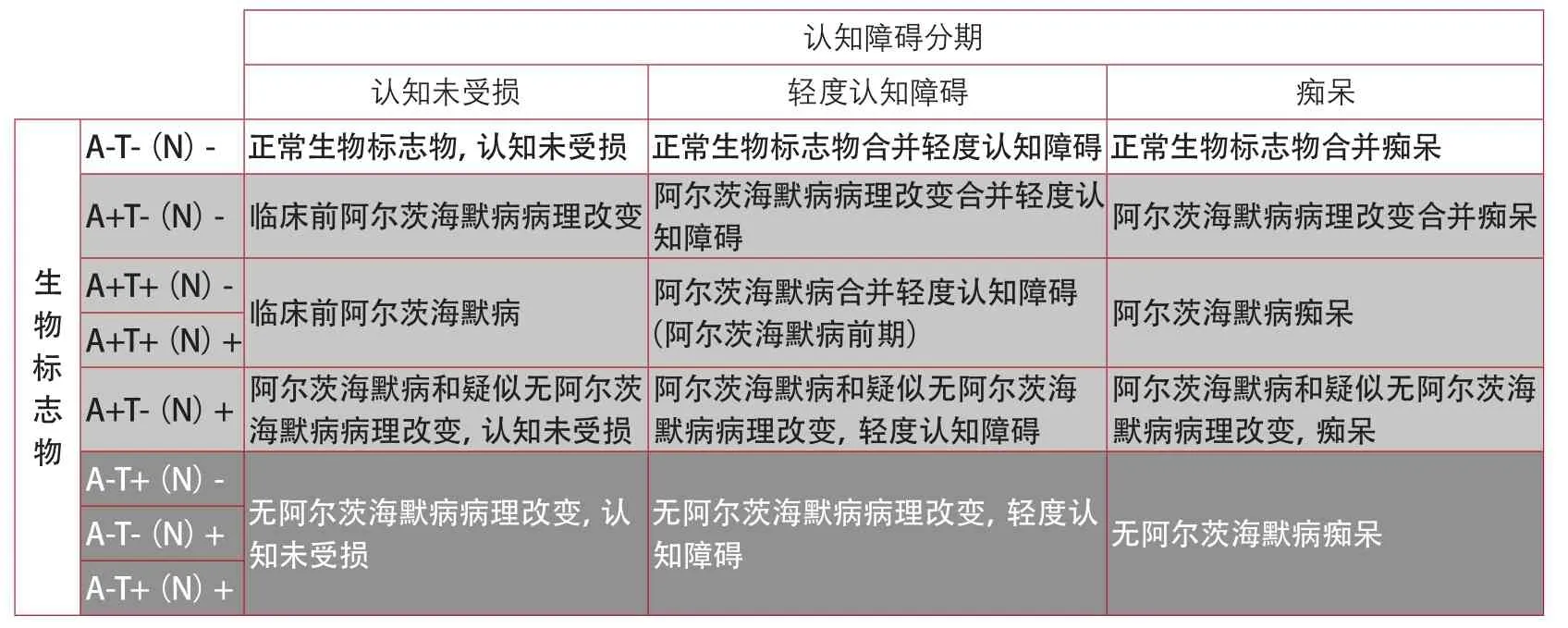
表3 基于AD生物标志物的认知障碍分期(AD分期)
(1)作为一个新的诊断框架,肯定有很多不成熟的地方,首先是现实的应用问题。发达国家可能试用容易些,但其他国家,比如在我国,留取脑脊液还很难普及,PET检查,特别是AD的分子影像学检查只有在为数不多的几个医疗单位常规开展,所以在短期内难以普及试用。
(2)这个框架是在Aβ蛋白级联瀑布学说不断被证实的基础上,结合生物学标志物和分子影像学的进步,适应研究和药物开发等需要制定的(尽管还有很多争议,将来也许会发现新的发病机制)[5]。目前Aβ+作为AD病理性诊断及AT(N)模型中的中心,是否有其他可能性?比如:疾病开始于Aβ-/tau+模式随着时间推移进入Aβ+/tau+?
(3)如果按此新的诊断标准,即从临床诊断分类转换到生物学框架,有可能很多路易体痴呆被归入AD,因为相当一部分的路易体痴呆(dementia with Lewy body,DLB)有Aβ改变和老年斑沉积,同时tau蛋白也有相应改变。DLB的主要病理所见是α-突触核蛋白为主的路易小体,其比较好的生物学标志物是通过单光子发射计算机断层成像(single photon emission computed tomography,SPECT)或PET显示的基底节中多巴胺转运蛋白摄取减少;异常(低摄取)123I-碘苄胍(meta iodo benzyl guanidine,MIBG)心肌显像和多导睡眠脑电图确认的快速动眼期(rapid eye movement,REM)睡眠行为障碍[6]。所以AT(N)分类系统怎样能够很好地区分类似的病例,还需要更明确,就是说在鉴别诊断上是否需要更多的标志物和其他信息作为补充?
(4)如何能够让潜在的患者在没有出现任何症状之前来做检查?
(5)一些学者担心tau生物标志物,特别是tau PET的有效性即生物标志物的假阳性问题,尤其是在T和N类别中,PET tau和CSF P-tau有时会给出不同的信息,N组中的不同标志物也是如此。
(6)另一方面,AT(N)系统应灵活加入正在开发的其他生物标志物,比如血浆Aβ可以作为A,血浆p181 tau作为T,神经丝或神经颗粒素作为N。未来可以添加新的类别,比如使用血管损伤标记、胶质炎症或其他过程、其他病理蛋白如核蛋白TAR DNA结合蛋白(transactive response DNA-binding protein of 43 ku,TDP-43)或α-突触核蛋白等。
(7)特异性生物学标志物将来也需要分级,从生物学标志物研究中分级更有助于明确诊断,比如分为正常、可能区间和明显异常等。
新的诊断框架,尽管还需要完善,但因为它的早期准确地反应临床病理,必将给今后的AD的临床诊疗与科研带来重大影响。

