神经内镜辅助下显微血管减压术的临床研究
向 晖,冷景兴,刘如恩
(江西省人民医院神经外科,南昌 330006)
随着血管压迫被广泛认识为颅神经疾病[单侧特发性面肌痉挛(HFS)、原发性三叉神经痛(PTN)、原发性舌咽神经痛(GN)等]的主要病因,显微血管减压术(microvascular decompression,MVD)已成为治疗颅神经疾病的首选方法。50多年来MVD取得了长足的进步。光学系统的完善和手术器械的改进使得颅神经疾病的治愈率逐步提高,并发症发生率大大下降。临床手术中如何寻找及充分暴露责任血管,并进行相应有效的MVD更是保证疗效的关键。近年来神经内镜技术不断发展,BROGGI等[1]对141例三叉神经痛(TN)手术患者进行总结,认为神经内镜是一种有用的MVD辅助方式。作者将本院260例颅神经疾病患者根据手术方式不同分为内镜组与显微镜组,评估其手术疗效,现报道如下。
1 资料与方法
1.1一般资料 选择2014年1月至2016年9月本院行MVD治疗的颅神经疾病患者260例,入选标准:单侧特发性HFS、PTN、原发性GN。排除标准:继发性HFS、面瘫后HFS、继发性TN(STN);不典型TN;既往接受过外科治疗的TN,包括射频消融、甘油灌注、球囊压迫、神经撕脱、神经阻滞、伽马刀;已有面部感觉减退的TN;继发性GN。根据手术方式不同分为内镜组和显微镜组,内镜组(n=138):男64例,女74例;年龄32~78岁,平均57.60岁;病程3个月至30年,平均3.67年;左侧75例,右侧63例;单侧特发性HFS 53例,PTN 83例,原发性GN 2例。显微镜组(n=122):男60例,女62例;年龄30~90岁,平均62.40岁;病程6个月至22年,平均4.08年;左侧61例,右侧61例;单侧特发性HFS 51例,PTN 70例,原发性GN 1例。两组患者入院前均经过药物、针灸等治疗3个月以上无明显效果。术前均行头部MRI扫描,桥小脑角区未见明显肿瘤。
1.2方法
1.2.1手术方法 患者取健侧卧位,均在全身麻醉下采用乙状窦后入路切口,以乳突根部为中心,行乳突后长约5 cm直切口,乙状窦后开圆形骨窗直径约2 cm,骨窗上缘暴露横窦和乙状窦边缘,十字切开硬脑膜。显微镜组:在显微镜下充分打开桥小脑角(CPA)池及蛛网膜下腔,逐步释放脑脊液待脑组织回缩后,探查手术区,发现责任血管并小心分离,再于责任血管与神经或脑干区(REZ)之间垫入涤纶隔离片(Teflon),后逐层关颅。CPA内镜组:在切开硬膜后用神经内镜沿小脑表面进入CPA区,开始进入时应选择0°镜,如遇到REZ区显露不充分时可以选用30°镜观察,发现责任血管并小心分离,再于责任血管与神经或REZ之间垫入Teflon,撤出神经内镜,移入显微镜观察,并对比术野显露的效果,后逐层关颅。
1.2.2评价指标 记录两组患者术后症状立即消失、术后1年症状消失、听力下降、面部感觉减退、共济失调、面瘫、颅内感染、颅内出血、脑脊液漏、口周疱疹、死亡等,参照文献[2]对两组患者疗效进行评估。
1.3统计学处理 采用SAS9.4软件进行统计学分析,计数资料以率表示,组间比较采用χ2检验;部分单元格计数太小(如听力下降、共济失调等)的采用Fisher精确检验,以P<0.05为差异有统计学意义。
2 结 果
2.1两组患者临床疗效及并发症比较 两组患者均未出现颅内感染、死亡、面瘫、脑内出血。两组患者临床效果及并发症比较,差异均无统计学意义(P>0.05),见表1。
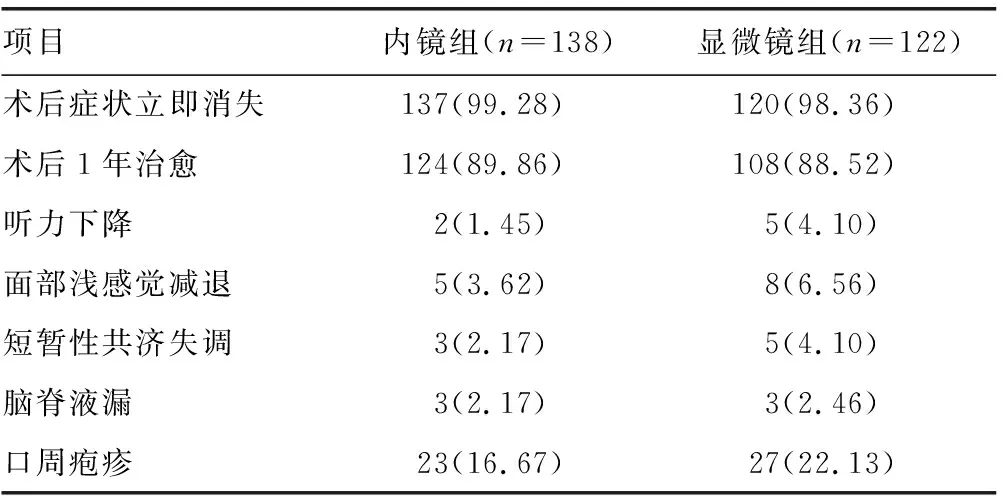
表1 两组患者临床疗效及并发症比较[n(%)]
2.2典型病例 患者,女,70岁,左侧面部疼痛4年,呈闪电样,疼痛部位由鼻翼、上唇向面颊部放射,洗脸、刷牙、咀嚼均可诱发。在神经内镜下手术治疗效果满意。手术治疗过程,见图1。
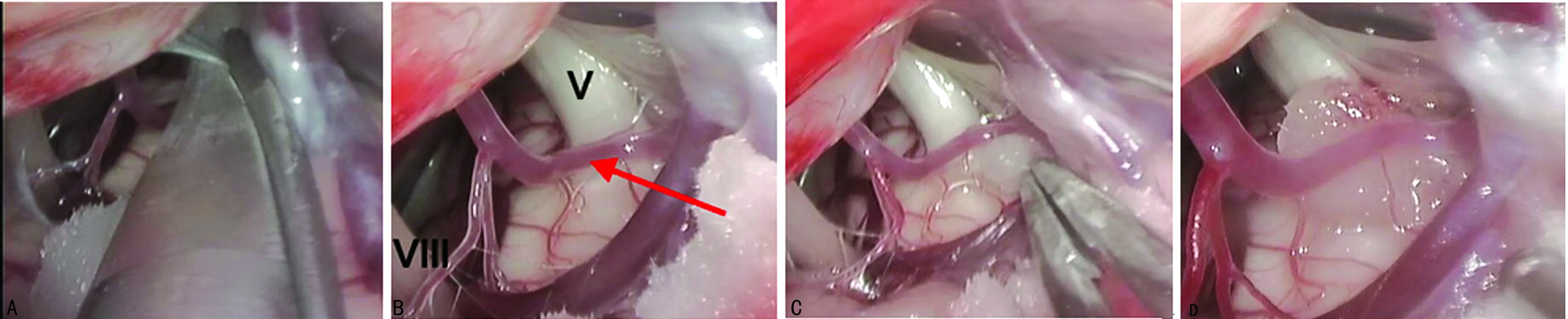
A:内镜下松解蛛网膜;B:内镜下探查见小脑前下动脉(红色箭头所示)压迫REZ区;C:内镜下减压;D:内镜下减压完成
3 讨 论
在颅神经疾病的诸多治疗方法中,MVD能达到最高的治愈率和最长时间的缓解率[3]。还有学者认为CPA区解剖结构复杂,在神经根出脑干2~3 mm处容易形成死角,神经根区域有时由于小脑遮挡,显露困难或不充分,造成责任血管遗漏,手术中需要反复牵拉小脑,导致脑、颅神经及血管损伤,致术中或术后并发症发生。部分手术失败和复发被认为与该区域责任血管遗漏或手术过程减压不充分有关[4-5]。有文献报道提示神经内镜能多角度观察手术区域,弥补手术显微镜不足,甚至优于手术显微镜[6]。一些文献报道了神经内镜下发现了显微镜下遗漏的责任血管[1,7-8]。近年来有研究认为在颅神经疾病的MVD治疗中神经内镜下的疗效明显优于显微镜下,并发症明显低于显微镜下[9-10],也有研究者认为神经内镜在该领域应该是发展趋势[11-12]。
本研究中两组患者的临床效果和并发症比较差异无统计学意义(P>0.05),可能与样本量较小有关。作者认为内镜下MVD有以下优点:(1)增加照明区域,增大显露范围(图1、2);(2)减轻对小脑及脑神经(主要是面听神经)的牵拉;(3)成角内镜可消除CPA区间隙内(主要是内听道嵴造成的显微外科)的解剖死角;(4)有利于分离粘连增厚的蛛网膜,减少对微血管的损伤;(5)有利于辨认责任血管与神经及REZ的关系;(6)有利于术中评判垫入Teflon棉后的减压效果。但同时应该认识到:神经内镜只是提供了一个更好的视野及视角,并不能改变CPA区的解剖结构。在手术中,即使内镜下可以看到责任血管,如果血管位于手术器械不容易到达的区域,仍然需要通过牵拉小脑及神经结构来达到分离减压的目的,因此,显微外科操作技术是提高手术疗效和减少并发症的关键,一个有经验的显微神经外科医生,在显微镜下可以准确判断责任血管的位置。神经内镜技术同样存在着不利因素:(1)内镜下为二维视野,深度判别觉较差;(2)需要手眼协调配合。而且内镜操作需两人三手同时操作,在CPA区狭小的空间内3个器械同时操作,对术者和助手的配合提出了更高的要求[13]。有研究说明手术时间的延长是并发症发生的常见原因[14],也有学者提出把显微镜和内镜结合,以避免遗漏责任血管,减少牵拉,减少并发症[15]。在研究中,内镜组手术时间长于显微镜组,原因是早期内镜下操作不太熟练,当手术操作熟练之后,两组手术时间无明显差异。
本研究结果表明,内镜组和显微镜组患者术后疼痛缓解率及颅内感染、口周疱疹比较,差异均无统计学意义(P>0.05)。显微镜组听力下降、面部浅感觉减退及共济失调比例约高于内镜组(P>0.05),其原因应与内镜组对小脑及神经牵拉较轻有关。术中对小脑的牵拉显微镜组强于内镜组,但并不能因此得出显微镜需要较大程度牵拉小脑的确定性的结论,因为术中对手术区暴露的难易程度同时受到后颅窝发育情况、脑干周围池大小、小脑半球萎缩程度、岩静脉位置等因素的影响。神经内镜下虽然能够在不严重牵拉小脑的情况下取得良好视角,但看到并非能做到,手术器械要达到操作区域仍需要对小脑进行牵拉,在有些情况下甚至无法完成血管神经减压。
综上所述,本研究认为神经内镜在MVD中的地位相对于显微镜并非有绝对优势。在经过良好训练的神经外科医生,通过显微镜与神经内镜,可达到相似的手术效果。在减少手术并发症方面,神经内镜在某些方面优于显微镜,但对术者与助手的配合有较高的要求。单纯神经内镜MVD不能获得更高的手术治愈率,但能减少对脑组织的牵拉,从而减少部分手术并发症。

