GC-MS/MS法测定饮用水中2种卤代酸残留量
胡松,陈卢涛,周婷婷,俞璐萍,黎斌,刘小羽,胡晋峰,朱萌萌,*
(1.绿城农科检测技术有限公司,浙江杭州310000;2.安徽农业大学茶与食品科技学院茶叶生物与利用国家重点实验室,安徽合肥230036)
国内采用氯气消毒是最主要的消毒方式[1],70年代以来,人们已经发现氯化消毒副产物(disinfection by-products,DBPs)与人类癌症的发生有密切的相关关系,且消毒副产物中卤乙酸含量约占DBPs的50%左右,而二氯乙酸(dichloracetic acid,DCAA)、三氯乙酸(trichloroacetic acid,TCAA)是饮用水加氯消毒的副产物卤乙酸之一,其具有不易挥发、沸点高、致癌风险大等特点,其中DCAA和TCAA的致癌风险分别是三卤甲烷的50倍和100倍,已被美国国家环境保护局(Environmental Protection Agency,EPA)定义为人类潜在的致癌物[2]。世界各国对饮用水中氯乙酸规定了相应浓度限值,我国GB 5749-2006《生活饮用水卫生标准》中规定DACC、TCAA的含量分别不得超过50、100 μg/L;美国饮用水水质标准中规定卤乙酸总量不得超过60 μg/L;日本规定了DCAA、TCAA的含量分别不得超过30、40 μg/L;澳大利亚规定了DCAA、TCAA的含量分别均不得超过100 μg/L[3]。
目前国内外卤乙酸的检测分析方法主要包括气相色谱法(gas chromatography-hydrogen flame ionization detector,GC-ECD)[4-5],气相色谱质谱法(gas chromatograph-mass spectrometer,GC-MS)[6-8],离子色谱法[9-11],高效液相色谱法[12],液相色谱-串联质谱法(high performance liquid chromatography-tandem mass spectrometry,HPLC-MS/MS)[1,13]等。由于卤乙酸具有较强的极性,采用气相法检测通常需要先进行衍生化反应;液相色谱及液相色谱串联质谱法可以无需经过衍生化过程,大大缩短分析时间,但其检出限较高,为0.1 mg/L~1.0 mg/L[14];离子色谱法具有操作简单,测定迅速等优点,但该方法灵敏度低[3]。近年来,许多研究人员在前处理方法上进行各种改进,优化,或采用固相微萃取方式对卤乙酸进行富集,但效果不太明显。刘天洁[4]采用硫酸-甲醇溶液结合GC-ECD对DACC、TCAA的前处理过程进行优化,最终衍生条件为60℃烘箱衍生90 min,缩短了反应时间。三甲基硅重氮甲烷(trimethylsilyl diazomethane,TMS-CHN2) 是重氮甲烷的安全性替代物,已广泛被应用于苯氧羧酸类除草剂、酚类化合物[15]的衍生化反应上。本文拟采用优化后的TMS-CHN2衍生化前处理方法结合气相色谱-串联质谱 (gas chromatography-tandem mass spectrometry,GC-MS/MS)方法,探讨两种衍生化试剂用于生活饮用水中二氯乙酸、三氯乙酸残留量分析的差异,旨在探究一种操作简单、快捷高效、检出限低的前处理及衍生化方法,用于饮用水中痕量二氯乙酸、三氯乙酸残留量的检测分析。
1 材料与方法
1.1 材料与试剂
二氯乙酸、三氯乙酸标准品:1 000 μg/mL,农业部环境保护科研监测所;三甲基硅重氮甲烷(TMSCHN2、纯度≥96.0%)、2.0 mol/L己烷溶液:上海麦克林生化科技有限公司;甲醇:色谱纯,美国J.T.Baker公司;浓硫酸:优级纯,国药集团化学试剂有限公司;甲基叔丁基醚:≥99.0%,梯希爱(上海)化成工业发展有限公司;碳酸氢钠、氯化铵、无水硫酸钠:上海安谱实验科技股份有限公司;试验所用水均为去离子水;微孔有机滤膜:0.22 μm;棕色带聚四氟乙烯衬垫的螺口塞采样瓶;娃哈哈纯净水、屈臣氏蒸馏水:市售。
1.2 仪器与设备
气相色谱-串联质谱仪:GC-2010 plus气相色谱仪配TQ8040质谱仪,DB-5MS色谱柱(30 m×0.25 mm×0.25 μm),日本 Shimadzu公司;MTN-5800 氮吹仪:天津奥特赛恩斯仪器有限公司;CHK-121台式精密酸度计:北京昌科仪自动化科技有限公司;ST-16R离心机:美国Thermo Fisher公司;BSA2202S电子天平:德国Sartorius公司;talboys数显型漩涡混合器:美国Henry Troemner公司;V-700型旋转蒸发仪:瑞士Buchi公司;KQ5200E超声波清洗器:昆山市超声仪器有限公司。
1.3 试验条件
1.3.1 色谱条件
进样口温度:200℃;载气:高纯氦气;碰撞气:高纯氩气,纯度≥99.999%;柱流量:1.2 mL/min;进样方式:不分流进样,1.0 min 后开阀;进样量:1 μL;定量方法:外标法;升温程序:40℃保持1 min,以9℃/min升至130℃,以40℃/min升至150℃,保持3 min;
1.3.2 质谱条件
色谱-质谱接口温度:200℃;电离方式:EI;电离能量:70 eV;离子源温度:230℃;检测器电压:0.99 kV(+0.4 kV);测定方式:多重反应监测模式(multiple reaction monitoring,MRM);定性、定量离子、碰撞能量等参数见表1。

表1 二氯乙酸、三氯乙酸质谱检测参数Table 1 The MS/MS parameters of dichloracetic acid and trichloroacetic acid
1.4 试验步骤
1.4.1 提取
采集到的水样,使用棕色的带聚四氟乙烯衬垫的螺口塞采样瓶于4℃冰箱中保存。量取25.00 mL水样于50 mL离心管中,加入2.0 mL浓硫酸(调节pH≤0.5),摇匀后,再加入10.0 g无水硫酸钠,涡旋1.0 min,加入5.0 mL甲基叔丁基醚,涡旋器振荡5.0 min,静置30 min待有机相和水相分层,移取有机相至10 mL具塞刻度管中,缓缓氮气吹至近干,待衍生。
1.4.2 衍生化
1)向上述提取液中加入硫酸-甲醇溶液(体积比,20∶80)2.0 mL,盖上瓶塞,在50℃水浴条件下反应2.0 h,取出具塞刻度管并冷却至室温,逐滴加入2.0 mL饱和碳酸氢钠溶液以中和pH,加入1.0 mL甲基叔丁醚,涡旋1.0 min,取有机相过0.22 μm滤膜并转移至样品小瓶,待净化[16]。
2)向上述提取液中加入衍生化试剂三甲基硅重氮甲烷(TMS-CHN2)40μL,盖上瓶塞,涡旋1.0min,在30℃水浴条件下反应20.0 min,加入1.00 mL甲基叔丁基醚提取衍生后产物,涡旋后离心取上清液,待净化。
1.4.3 净化
先用5.0 mL正己烷预淋洗Florisil固相萃取柱,将上述待净化液转移至小柱上,再用10.0 mL甲基叔丁基醚溶液进行洗脱,收集全部流出液,在常温条件下氮气流吹至近干,用正己烷溶解并定容至1.0 mL,供气相色谱-串联质谱检测。
1.4.4 标准溶液的配制
称取二氯乙酸、三氯乙酸1.00 mL,用甲基叔丁基醚定容至25.0 mL,得到40.0 mg/L标准储备溶液;用甲基叔丁基醚稀释为5.00 mg/L的标准工作溶液,于0℃~4℃保存。
2 结果与分析
2.1 气相色谱-质谱条件的优化
在电子轰击离子源(electron bombardment ion source,EI)检测模式下对二氯乙酸、三氯乙酸甲酯后产物进行一级质谱分析(Q3 Scan),在质谱图中选择质荷比较大,绝对强度较大的离子为前体离子;设定3eV~45 eV(每3 eV一个间隔)的碰撞能量,对选定的前体离子峰进行二级质谱分析(产物离子扫描),根据二级质谱图,选择离子强度最大的为定量离子,离子强度次之的为定性离子。图1为使用优化后的气相色谱质谱条件采集二氯乙酸(2.00 mg/L)、三氯乙酸(2.00 mg/L)标准溶液MRM质谱图。


图1 二氯乙酸、三氯乙酸MRM色谱图Fig.1 Chromatogram of dichloracetic acid and trichloroacetic acid in multiple reactions monitoring mode(MRM)
2.2 三甲基硅重氮甲烷(TMS-CHN2)衍生条件优化
二氯乙酸、三氯乙酸具有较高的沸点(>190℃)和一定的极性,在水中难挥发且强酸性和极性会引起在色谱柱上吸附,通常需要衍生化反应后再进行气相色谱质谱分析,本试验比较了两种衍生化试剂:硫酸-甲醇溶液和TMS-CHN2己烷溶液对二氯乙酸、三氯乙酸两种卤代酸衍生化反应的效率和适宜性。
2.2.1 TMS-CHN2添加量考察
在具塞玻璃离心管中分别加入5.0 mg/L的二氯乙酸、三氯乙酸两种标准储备液0.400 mL,添加衍生化试剂 TMS-CHN2己烷溶液体积分别为 20、40、60、80、100 μL,在室温条件下,氮气流缓缓吹干有机溶剂,按照1.4.2中第二种衍生化方法进行衍生,并将最终体积定容为1.0 mL上机分析。结果表明(见图2),随着TMS-CHN2添加量的增加,二氯乙酸、三氯乙酸衍生化产物响应逐渐提高,当添加量增加到40 μL时,衍生化产物响应最高。继续增加TMS-CHN2己烷溶液的添加量,衍生化产物的响应呈稳定趋势。综合考虑,为保证衍生化反应完全,同时可以有效降低试验成本,选择TMS-CHN2己烷溶液的添加体积为40 μL。

图2 TMS-CHN2添加量对衍生化效率的影响Fig.2 The effects of the additives of TMS-CHN2on the derivatization
2.2.2 衍生化时间的考察
在具塞玻璃离心管中分别加入5.0 mg/L的二氯乙酸、三氯乙酸两种标准储备液0.400 mL,添加优化后的衍生化试剂TMS-CHN2己烷溶液体积40 μL,在室温条件下,氮气流缓缓吹干有机溶剂,按照1.4.2中第二种衍生化方法进行衍生,分别设置衍生化时间为10.0、20.0、30.0、40.0、50.0 min,并将最终体积定容为 1.0 mL上机分析。结果表明(见图3),随着衍生化时间的延长,衍生后产物的响应逐渐增强;当衍生化时间为20.0 min时,衍生后产物响应最高;当继续延长衍生化时间,衍生化产物响应稍有降低。综合考虑,为保证衍生化产物响应,同时可以有效节约试验时间,选择TMS-CHN2己烷溶液衍生化时间为20.0 min。

图3 不同衍生时间对衍生化效率的影响Fig.3 The effect of different derivative time on derivative efficiency
2.2.3 衍生化时间的考察
在优化好的衍生试剂添加量(40 μL)及衍生时间(20.0 min)基础上,对衍生化温度进行考察。在具塞玻璃离心管中分别加入5.0 mg/L的二氯乙酸、三氯乙酸两种标准储备液0.400 mL,添加优化后的衍生化试剂TMS-CHN2己烷溶液体积40 μL,在室温条件下,氮气流缓缓吹干有机溶剂,按照1.4.2中第二种衍生化方法进行衍生,分别设置衍生化温度为20.0、30.0、40.0、50.0、60.0、70.0℃,并将最终体积定容为1.0 mL上机分析。结果表明(见图4),从20℃开始,随着水浴温度的提高,两种卤代酸的响应逐渐增强,在30℃时响应最强。水浴温度逐渐升高,两种卤代酸的响应快速降低,由于正己烷沸点较低,在40℃及以上温度时,可明显看到具塞刻度管上层有明显黄色气体,可能由于正己烷的挥发带动TMS-CHN2与样品接触较少,衍生化反应不完全导致,因此,选择TMS-CHN2己烷溶液的最佳衍生化温度为30℃。
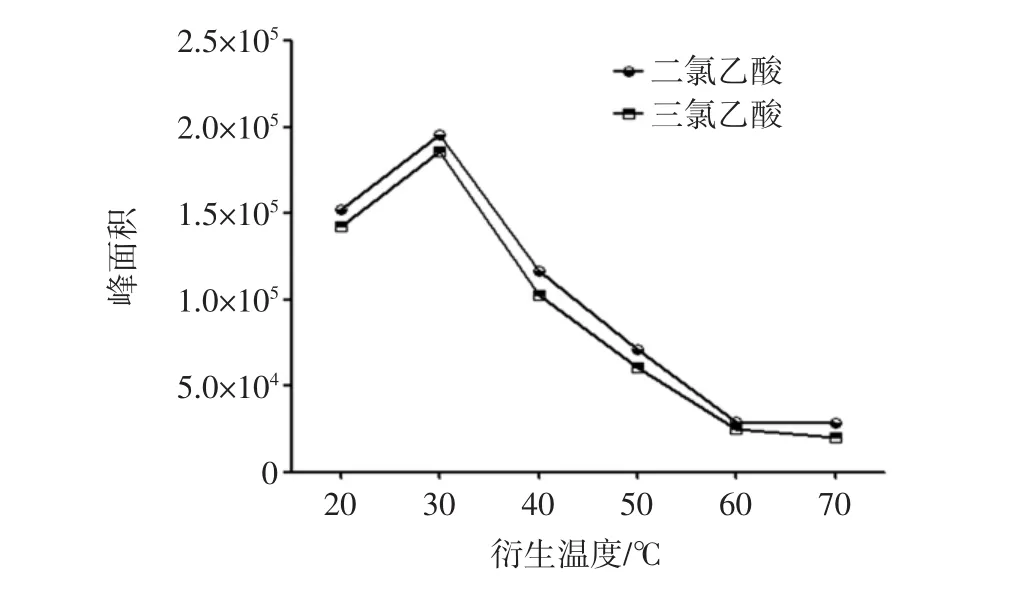
图4 不同衍生温度对衍生化效率的影响Fig.4 The effect of different derivative temperature on derivative efficiency
2.3 硫酸-甲醇溶液和TMS-CHN2两种衍生化试剂比较
参照GB/T 5750.10-2006《生活饮用水标准检验方法消毒副产物指标》及李志华等优化后的硫酸甲醇溶液衍生条件(即1.4.2),确定TMS-CHN2最佳添加量及衍生化时间的条件后,比较两种衍生化试剂在最佳添加量下对相同浓度的二氯乙酸、三氯乙酸衍生化效率。在具塞玻璃离心管中分别加入5.0 mg/L的二氯乙酸、三氯乙酸两种标准储备液0.400 mL,在室温条件下,氮气流缓缓吹干有机溶剂,分别按照1.4.2中1)和2)的衍生化方法进行衍生化反应。结果表明(见图5),在相同的仪器分析条件下,二氯乙酸经TMS-CHN2衍生后的响应是经硫酸-甲醇溶液衍生后响应的1.69倍,三氯乙酸经TMS-CHN2己烷溶液衍生后的响应是经硫酸-甲醇溶液衍生后响应的1.71倍。烷基化试剂主要由重氮甲烷、烷基卤、醇类等组成,其中重氮甲烷使用最广泛,且反应迅速、高效、无副产物,但其毒性大,不易保存,现经常被TMS-CHN2所代替,TMS-CHN2是重氮甲烷的安全性替代物,已广泛被应用于苯氧羧酸类除草剂、酚类化合物的衍生化反应上。两种衍生化试剂经比较可发现,TMS-CHN2己烷溶液在二氯乙酸、三氯乙酸的衍生化反应上,较常规硫酸-甲醇溶液衍生时间更短、衍生试剂量更少,衍生产物响应更高,操作也更为方便、简单,可以替代硫酸-甲醇溶液用于二氯乙酸、三氯乙酸的检测。

图5 两种衍生化试剂比较(n=3)Fig.5 The comparison of two derivatization reagents(n=3)
2.4 方法的线性范围、加标回收率、精密度和定量限
分别取5.0 mg/L二氯乙酸、三氯乙酸混合溶液25、50、100、200、500、1 000 μL 于 25 mL 容量瓶中,分别用纯净水定容至25.0 mL,配制后工作曲线的质量浓度分别为:5.0、10.0、20.0、40.0、100、200 μg/L。按 1.4 的方法进行萃取、衍生、分析,按优化色谱条件进样1 μL,以峰面积为纵坐标,标准样品的质量浓度为横坐标绘制标准曲线,其线性回归方程及相关系数见表2,以信噪比S/N≥3估算仪器的检出限(limit of determination,LOD),S/N≥10估算仪器的定量限(limit of quantitation,LOQ),结果见表 2。

表2 二氯乙酸、三氯乙酸化合物的线性方程、相关系数、检出限和定量限Table 2 Linear equations,correlation coefficient,limit of determination(LOD)and limit of quantitation(LOQ)of dichloracetic acid and trichloroacetic acid
分别量取自来水、娃哈哈纯净水、屈臣氏蒸馏水3个样品25.0 mL,分别添加0.02、0.04、0.1 mg/L不同水平的二氯乙酸、三氯乙酸标准溶液进行回收率试验,每个添加水平重复3次,加标回收结果见表3。
二氯乙酸、三氯乙酸的平均回收率范围为86.1%~96.5%,相对标准偏差小于5.2%,符合GB/T 27404-2008《实验室质量控制规范食品理化检测》附录F中对检测方法确认的要求。
3 结论
本试验第一次建立了三甲基硅重氮甲烷(TMSCHN2)结合气相色谱-串联质谱(GC-MS/MS)用于二氯乙酸、三氯乙酸衍生化反应的检测方法,比较了硫酸-甲醇溶液、三甲基硅重氮甲烷(TMS-CHN2)两种衍生化试剂用于二氯乙酸、三氯乙酸衍生化反应的优劣。两种试剂均可用于二氯乙酸、三氯乙酸的衍生化反应检测,TMS-CHN2己烷溶液在二氯乙酸、三氯乙酸的衍生化反应上,将衍生化反应时间从120 min缩短为20 min,较常规硫酸-甲醇溶液衍生时间更短、衍生试剂量更少,衍生产物响应更高,且添加回收试验结果精密度更高,操作也更为方便、简单。采用优化后的GC-MS/MS方法,在空白样品添加浓度为0.02、0.04、0.1 mg/L的范围内,二氯乙酸、三氯乙酸的平均回收率范围为86.1%~96.5%,相对标准偏差小于5.2%,符合GB/T 27404-2008附录F中对检测方法确认的要求。因此优化后的该方法检出限低、灵敏度高,适用于生活饮用水中二氯乙酸、三氯乙酸定量检测。
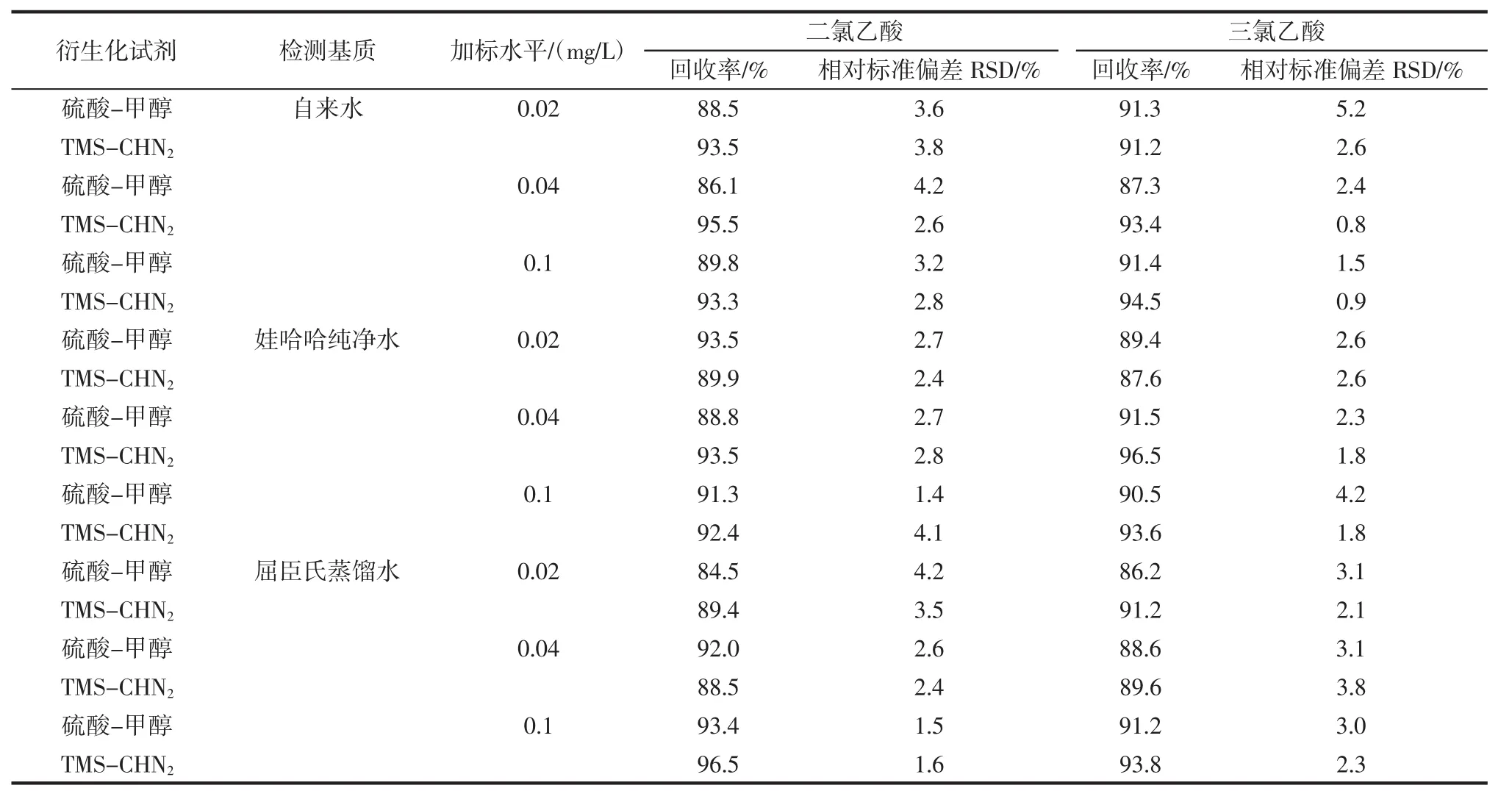
表3 二氯乙酸、三氯乙酸化合物的加标回收率及相对标准偏差(n=3)Table 3 Recoveries and RSD of dichloracetic acid and trichloroacetic acid in cabbage and citrus(n=3)

