复方氯霉素乳膏的处方筛选及质量标准研究*
喻 吉 ,林 彩 ,孙红武 ,2△,杨钦君
(1.中国人民解放军陆军军医大学第一附属医院药剂科,重庆 400038; 2.国家免疫制品工程技术研究中心·中国人民解放军陆军军医大学药学系微生物与生化药学教研室,重庆 400038)
氯霉素对革兰阳性菌、革兰阴性菌、厌氧菌等有效,尤其对引起痤疮的痤疮丙酸杆菌和金黄色葡萄球菌等具有显著抗菌作用[1]。甲硝唑对导致痤疮的厌氧菌及增生性的毛囊虫有明显杀灭作用[2]。本研究中以甲硝唑与氯霉素为主药,配以不同的乳膏基质,共获得7个处方,按乳膏质量标准[3-4]考察乳膏质量,获得最优处方,制备出复方氯霉素乳膏。由于复方氯霉素乳膏中,甲硝唑与氯霉素对临床疗效具有至关重要的作用,因此对其两种主药的含量测定对于其质量控制具有重要意义。目前,甲硝唑与氯霉素的含量测定方法有高效液相色谱(HPLC)法、双波长分光光度法、多波长系数法、比色法等,HPLC法具有重复性好、灵敏度高等优点[5-8]。本研究中拟建立同时测定复方氯霉素乳膏中甲硝唑与氯霉素含量的HPLC法。现报道如下。
1 仪器与试药
1.1 仪器
BME-1002型高剪切乳化机(上海威宇机电有限公司);KQ-600V型离心机(上海威尔机电制造有限公司);TE4101-L型电子天平(北京赛多利斯仪器有限公司);KQ-400KDE型高功率数控超声清洗器(昆明市超声仪器有限公司);DU650型紫外分光光度计(Beckman Coulter公司);Waters2487型高效液相色谱仪紫外检测器、Waters 510 Pump型高效液相色谱仪二元泵(美国Waters公司);Diamondsil C18色谱柱(150 mm ×4.6 mm,5μm,迪马科技有限公司);Mini-Q Plus 1.5 L/min型纯水机(美国Millipore公司)。
1.2 试药
甲硝唑(武汉武药制药有限公司,批号为150380);氯霉素(南京白敬宇制药有限公司,批号为CH150404);螺内酯(浙江郎华制药有限公司,批号为1501004);甘油(批号为 20150314),吐温 - 80(批号为 20140501),均由湖南尔康制药股份有限公司生产;HR-S乳化剂(丹东安康精细化工有限公司,批号为20150407213);白凡士林(南昌白云药业有限公司,批号为20150603);丙二醇(南京威尔化工有限公司,批号为20150503);单硬脂酸甘油酯(沈阳科瑞化工有限公司,批号为20140925);硬脂酸(湖州展望药业股份有限公司,批号为20141205);16-18醇(江苏东泰精细化工有限公司,批号为2014121204);Span-60(河南正通化工有限公司,批号为20150210);十二烷基硫酸钠(成都华邑药用辅料制造有限责任公司,批号为20140501);液体石蜡(吉林市吉化江城油脂化工有限责任公司,批号为150202);甲硝唑对照品(批号为100191-201507),氯霉素对照品(批号为130555-201203),均由中国食品药品检定研究院提供;甲醇(色谱纯,美国Burdick&Jackson公司);复方氯霉素乳膏(自制,批号分别为 160105-1,160105-2,160126 -1,160126 -2,160126 -3)。
2 方法与结果
2.1 处方设计与筛选
2.1.1 处方设计
按复方氯霉素乳膏基质成分配制比例及配制温度,筛选处方,设计出7个处方。详见表1。其中配置温度除处方3为60℃外,其余处方均为80℃。
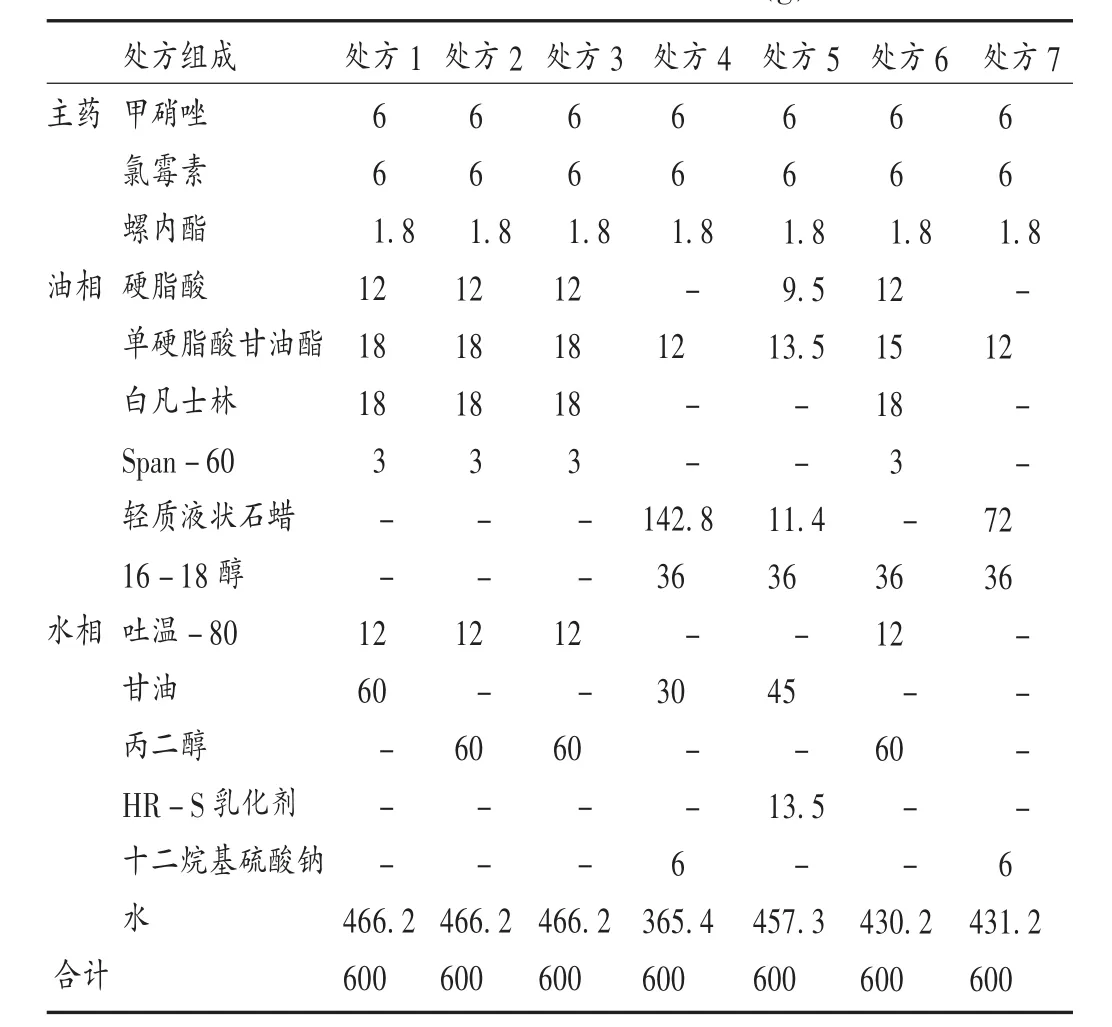
表1 复方氯霉素乳膏处方(g)
2.1.2 乳膏制备
处方1,2,6:油相,按处方量称取单硬脂酸甘油酯、硬脂酸、白凡士林、Span-60,混合加热,熔化,加入螺内酯使其溶解,溶液保持80℃。水相,按处方量称取水,加热至80℃后,加入甲硝唑与氯霉素,搅拌,使其完全溶解,然后加入甘油或丙二醇、吐温-80混匀。将80℃油相加至80℃的水相。
处方3:油相,按处方量称取单硬脂酸甘油酯、硬脂酸、白凡士林、Span-60,混合加热,熔化,加入螺内酯使其溶解,溶液保持60℃。水相,按处方量称取水,加热至60℃后,加入甲硝唑与氯霉素,搅拌,使其完全溶解,然后加入甘油或丙二醇、吐温-80混匀。将60℃油相加至60℃的水相。
处方4,7:油相,按处方量称取16-18醇、单硬脂酸甘油酯、轻质液状石蜡,混合加热,熔化,然后加入螺内酯使其溶解,溶液保持80℃。水相,按处方量称取水,加热至80℃后,加入甲硝唑与氯霉素,搅拌使其完全溶解,然后加入十二烷基硫酸钠、甘油后混匀。将80℃水相加至80℃的油相。
处方5:油相,按处方量称取单硬脂酸甘油酯、硬脂酸、16-18醇、轻质液状石蜡,混合加热,熔化,然后加入螺内酯使其溶解,溶液保持80℃。水相,按处方量称取水加热至80℃后,加入甲硝唑与氯霉素,搅拌,使其完全溶解,然后加入甘油、HR-S乳化剂后混匀。将80℃油相加至80℃的水相。
各处方油相水相相加时均随加随搅拌,搅匀后上机乳化25 min,冷却,分装。
2.1.3 质量评价与处方筛选结果
对复方氯霉素乳膏外观、黏稠度、粒度、4 000 r/min离心10 min后的稳定性、晶体析出时间进行考察,判定制备的复方氯霉素乳膏的质量。对制备的7个复方氯霉素乳膏处方的试验结果表明,处方5制备的乳膏最美观,手感最细腻,粒度最小,黏稠度适中,且最稳定。故处方5为最佳处方。
2.2 含量测定
2.2.1 检测波长确定
称取甲硝唑对照品与氯霉素对照品10 mg,精密称定,分别用甲醇溶解稀释,在200~400 nm波长范围内进行紫外扫描。结果甲硝唑、氯霉素最大吸收波长分别为273 mm和295 nm,综合考虑,选择280 nm为检测波长。
2.2.2 色谱条件
色谱柱:Diamondsil C18柱(150 mm×4.6 mm,5μm);流动相:甲醇 -水(35 ∶65);检测波长:280 nm;灵敏度:0.1AUFS;进样量:10μL;流速:1.0mL /min;柱温:30℃。
2.2.3 溶液制备
分别称取甲硝唑与氯霉素对照品各10.1 mg,用甲醇溶解并定容,制成质量浓度均为0.404 g/L的混合贮备液,配制成对照品溶液。称取含或不含甲硝唑与氯霉素的复方乳膏0.13 g,精密称定,加入甲醇溶解至25 mL容量瓶中,定容并混匀,超声处理10 min,4 000 r/min离心5 min,取上清液,配制供试品溶液、空白基质溶液。
2.2.4 方法学考察
系统适用性试验与专属性试验:取甲硝唑与氯霉素对照品溶液、供试品溶液、空白基质溶液,依法进样,色谱图见图1。可见,对照品溶液中甲硝唑的保留时间为2.244 min,氯霉素为9.510 min;供试品溶液的两主峰和甲硝唑、氯霉素对照品的色谱峰保留时间基本一致,且两主药的分离度好;同时空白基质溶液在上述保留时间处无明显色谱峰,表明其对检测无明显干扰。
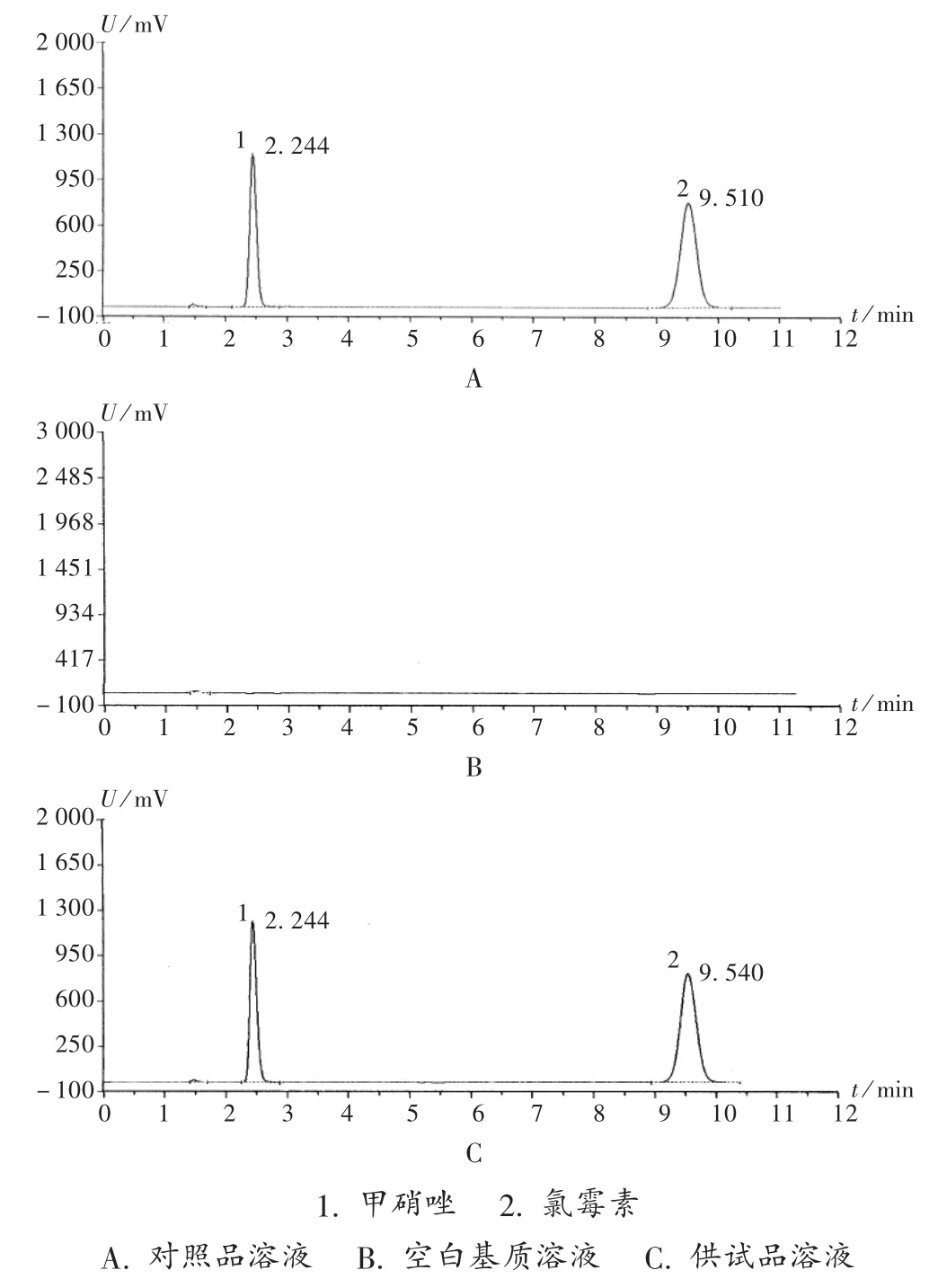
图1 高效液相色谱图
标准曲线绘制:分别吸取甲硝唑与氯霉素质量浓度均为0.404 g/L的混合贮备液,加甲醇制得两药质量浓度 均 为 40.40,44.44,48.48,52.52,56.56,60.60,64.64μg/mL的溶液。吸取上述溶液各10μL,注入高效液相色谱仪,每份溶液测定3次,计算峰面积,以质量浓度(X,μg/mL)为横坐标、峰面积(Y)为纵坐标绘制标准曲线,得回归方程,甲硝唑为 Y=224.49 X-219.4,r=0.999 9(n=7);氯 霉 素 为 Y=375.5 X-853.11,r=0.999 8(n=7)。结果表明,两药质量浓度在 40.40~64.64μg/mL范围内与峰面积线性关系均良好。
精密度试验:分别量取质量浓度为40.40,52.52,64.64μg/mL的甲硝唑与氯霉素溶液10μL,连续进样3次,注入高效液相色谱仪,记录峰面积,计算日内精密度。取等量相同溶液,分别于0,24,48 h时注入高效液相色谱仪,记录峰面积,计算日间精密度。结果见表2。

表2 精密度试验结果(n=3)
检测限与定量限确定:将已知质量浓度样品测出的信号与空白样品测出的信号进行比较,计算能被检测出的最低质量浓度与能被定量的质量浓度。以信噪比为3∶1时相应的质量浓度为检测限,以信噪比为10∶1时相应的质量浓度为定量限,结果甲硝唑的检测限与定量限分别为 1.31μg/mL 和 3.79μg/mL,氯霉素的检测限与定量限分别为2.28μg/mL和7.33μg/mL。
稳定性试验:精密量取甲硝唑与氯霉素质量浓度均为0.404 g/L的混合贮备液,加甲醇制成两药质量浓度均分别为 40.40,52.52,64.64μg/mL的混合溶液各2份,1 份常温放置,1 份冰箱(4 ℃)放置,分别于 0,24,48 h时各取10μL注入高效液相色谱仪,记录甲硝唑与氯霉素的峰面积,并计算 RSD。结果见表3。

表3 稳定性试验结果(n=3)
加样回收试验:分别配制甲硝唑和氯霉素高、中、低质量浓度(67.80μg/mL 和 65.92μg/mL,55.12μg/mL和 53.56μg/mL,42.40μg/mL和 41.20μg/mL)对照品溶液。称取复方氯霉素乳膏样品132.5 mg,精密称定,依法制备供试品溶液,取0.5 mL,加至3种质量浓度的甲硝唑及氯霉素混合对照品液0.5 mL中,混匀,4 000 r/min离心10 min,取10μL注入高效液相色谱仪,计算回收率。结果见表4和表5。
2.2.5 样品含量测定
用甲醇分别配制甲硝唑和氯霉素质量浓度均为52.00μg/mL的对照品溶液;取5批次的乳膏样品0.1 g,用甲醇溶解并定容至25 mL,超声10 min,4 000 r/min离心10 min,取上清液,即得供试品溶液。取甲硝唑与氯霉素对照品混合液、供试品溶液各10μL,注入高效液相色谱仪,记录甲硝唑与氯霉素相应的峰面积。计算供试品溶液中甲硝唑与氯霉素的质量浓度,进而计算复方氯霉素乳膏中甲硝唑与氯霉素的含量。结果见表6。

表4 甲硝唑加样回收试验结果(n=9)
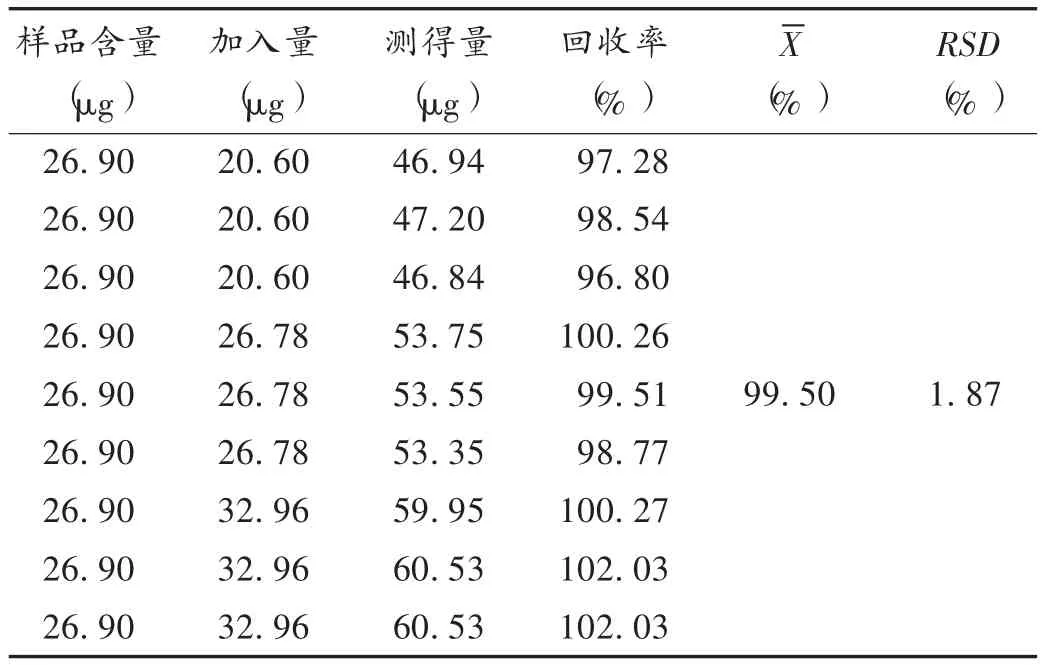
表5 氯霉素加样回收试验结果(n=9)
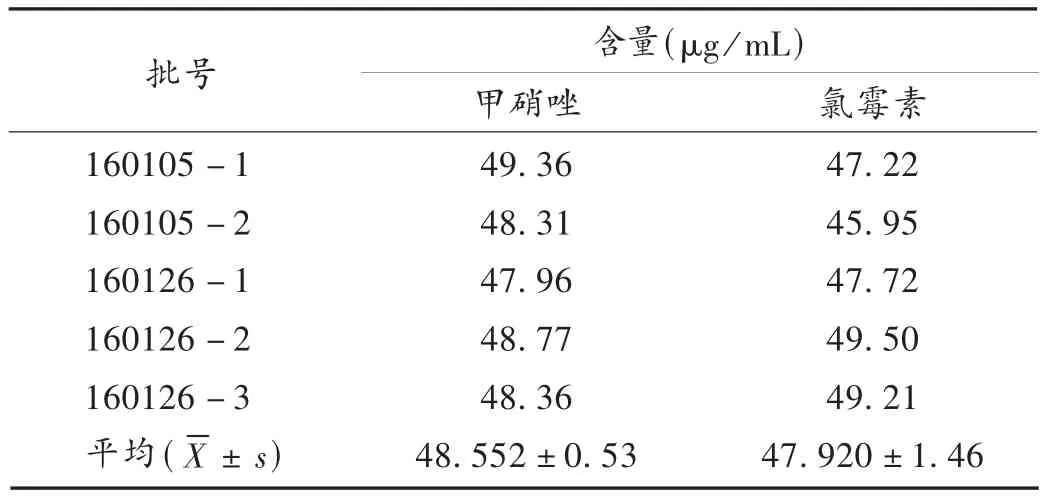
表6 样品含量测定结果(n=5)
3 讨论
本研究中以对痤疮致病菌有效的氯霉素和甲硝唑为主药[9-11],设计出7种不同乳膏的处方,根据质量评价体系,对制剂外观、粒度、4 000 r/min离心 10 min后的稳定性、晶体析出时间等重要质量控制指标进行考察[12],以获得最佳处方。
本研究中曾选择甲醇-水(50∶50)为流动相,结果甲硝唑与氯霉素峰的保留时间分别为1.85min和3.60min,两者无法完全分离;流动相为甲醇-水(45∶55)和(40 ∶60)[13-14]时,甲硝唑与氯霉素峰分离效果较好,但甲醇保留时间为1.40 min,与甲硝唑峰分离度不好;当流动相为甲醇 -水(35 ∶65)[15]时,甲醇、甲硝唑、氯霉素的分离效果均较好。
在处理复方氯霉素乳膏样品时,可对其进行超声处理[15],增加溶解;样品进样前,溶液需离心,取上清液,消除基质的干扰;由精密度及稳定性试验结果可见,甲硝唑与氯霉素相应项目下的 RSD值均小于2%,表明甲硝唑与氯霉素溶液较稳定;测定样品时,因流动相中甲醇易挥发,流动相必须使用当天配制。

