2007—2016年《中华皮肤科杂志》随机对照临床试验文献报告质量评价
张建红 刘子艳 刘玉媛 刘学茗 苗婷 马胜男 王瑜
300140天津市第四中心医院药剂科
随机对照试验(RCT)是公认的临床治疗性试验的金标准方法,可对临床决策产生重要而深远的影响[1]。但是,一些RCT报告质量较低,影响了研究结果评价的准确性和真实性。客观、准确地评价RCT报告的质量,为临床医学的发展提供更多、更有价值的证据意义重大。临床试验报告的统一标准(CONSORT)于1996年首次发表,经过几次修订,已形成一套规范的报告格式和要求,被许多国际主流医学期刊所认可[2-4]。我们依据2010版CONSORT声明设计临床RCT文献质量评价表,对《中华皮肤科杂志》2007—2016年发表的RCT文献进行质量评价,旨在发现该刊RCT文献存在的问题,进一步提高RCT报告的质量。
一、资料和方法
1.资料来源:《中华皮肤科杂志》2007—2016年刊登的全部临床RCT文献。
2.检索方法:手工逐篇筛选2007—2016年《中华皮肤科杂志》发表的全部临床RCT文献,通过阅读全文对每篇文献的各部分内容进行评价。
3.评价表设计及评价方法:基于CONSORT声明并结合国内RCT的实际情况设计评价表,保留CONSORT声明中核心评价指标,省略国内RCT文献普遍缺失或重要性相对较低的部分项目,如文题(提示为随机试验)和摘要(用结构式摘要概括设计、方法、结果和结论)、方法(试验设计)、结果(分析的人数、辅助分析)、其他信息(注册登记、试验方案、资助情况)。因临床试验应遵循两大基本原则即研究的科学性和伦理的合理性,本文增加伦理评价条目“伦理委员会同意”及“患者知情同意”。针对每篇文献前言、方法、结果及讨论部分对纳入文献报告质量进行评价。最后依据各指标报告率评价《中华皮肤科杂志》RCT文献质量情况。所有文献评价均由2位研究者独立完成,再交叉核对结果。如2位研究者结果不一致,则由熟悉RCT研究的第三方专家介入判定。
4.统计学方法:采用SPSS16.0统计软件包处理数据,不同阶段报告质量差异采用列联表卡方检验分析,P<0.05示差异有统计学意义。
二、结果
1.一般情况:共纳入2007—2016年《中华皮肤科杂志》刊出的 RCT文献94篇,其中2007—2011年45篇,2012—2016年49篇。
2.前言部分报告质量:前言部分评价指标为科学背景和研究目的。该刊近10年发表的RCT文献基本对这两项内容作了阐述,仅少量文献表达不清楚或不明确。其中,科学背景表达清楚的比例在2007—2011年文献中为53.33%,2012—2016年升高至79.59%,两组间差异有统计学意义(P<0.05)。见表1。
3.方法部分报告质量:该部分共9项评价指标,结果显示,随机方法、盲法、样本量计算、主要结局指标和次要结局指标明确报告比例较低,而纳入及排除标准、干预措施、统计学方法的明确报告比例较高,均高于80%。其中,正确描述随机方法的比例在2007—2011年为48.89%,2012—2016年升高至77.55%,两组间差异有统计学意义(P<0.05)。2007—2011年文献中明确报告纳入及排除标准的比例为71.11%,2012—2016年为91.84%,两组间差异有统计学意义(P<0.05)。见表2。
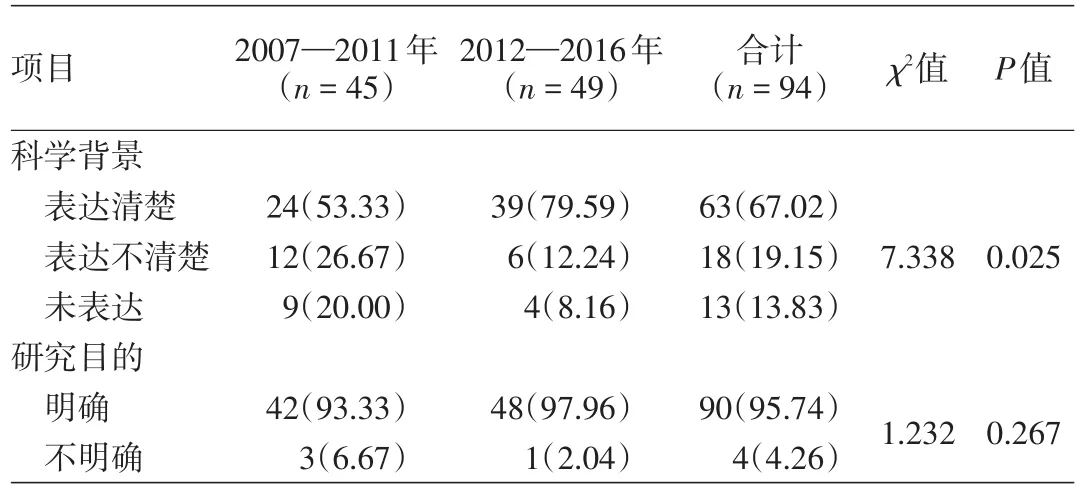
表1 《中华皮肤科杂志》2007—2016年随机对照临床试验文献前言部分报告质量评价[篇(%)]
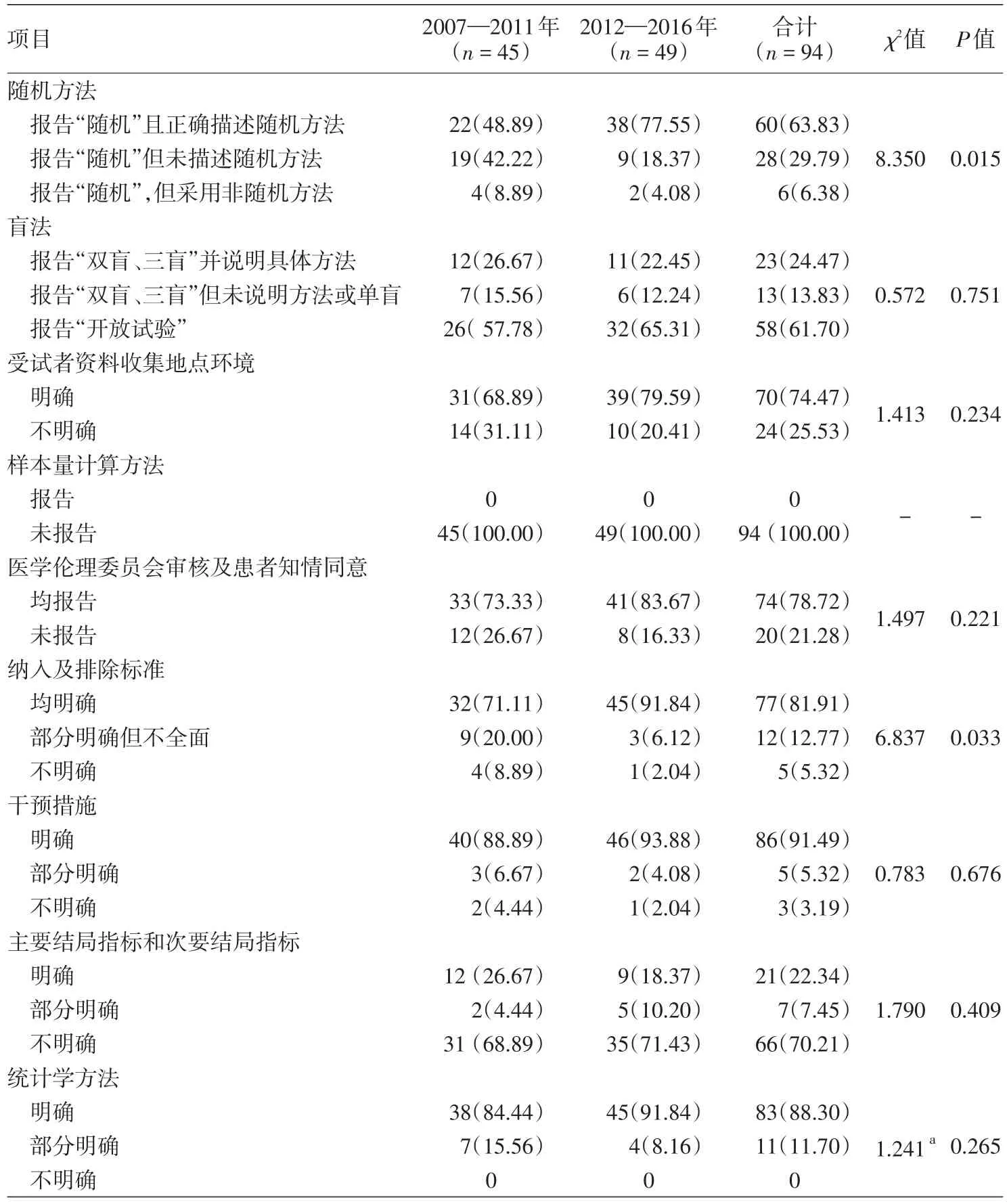
表2 《中华皮肤科杂志》2007—2016年随机对照临床试验文献方法部分报告质量评价[篇(%)]
4.结果部分报告质量:表3显示,对随访起止时间、基线资料的明确报告比例较高,达80%以上;列出受试者流程图及报告依从性的文献比例较低;重要不良事件或不良反应发生原因分析不够充分,提及但未分析原因者占24.47%,另有3.19%未提及。
5.讨论部分报告质量:大部分文献作者在该部分中结合国内外相关研究解释结果,报告试验可推广性的文献比例达到92.55%,但详细分析或提及试验局限性的文献比例较低。见表4。
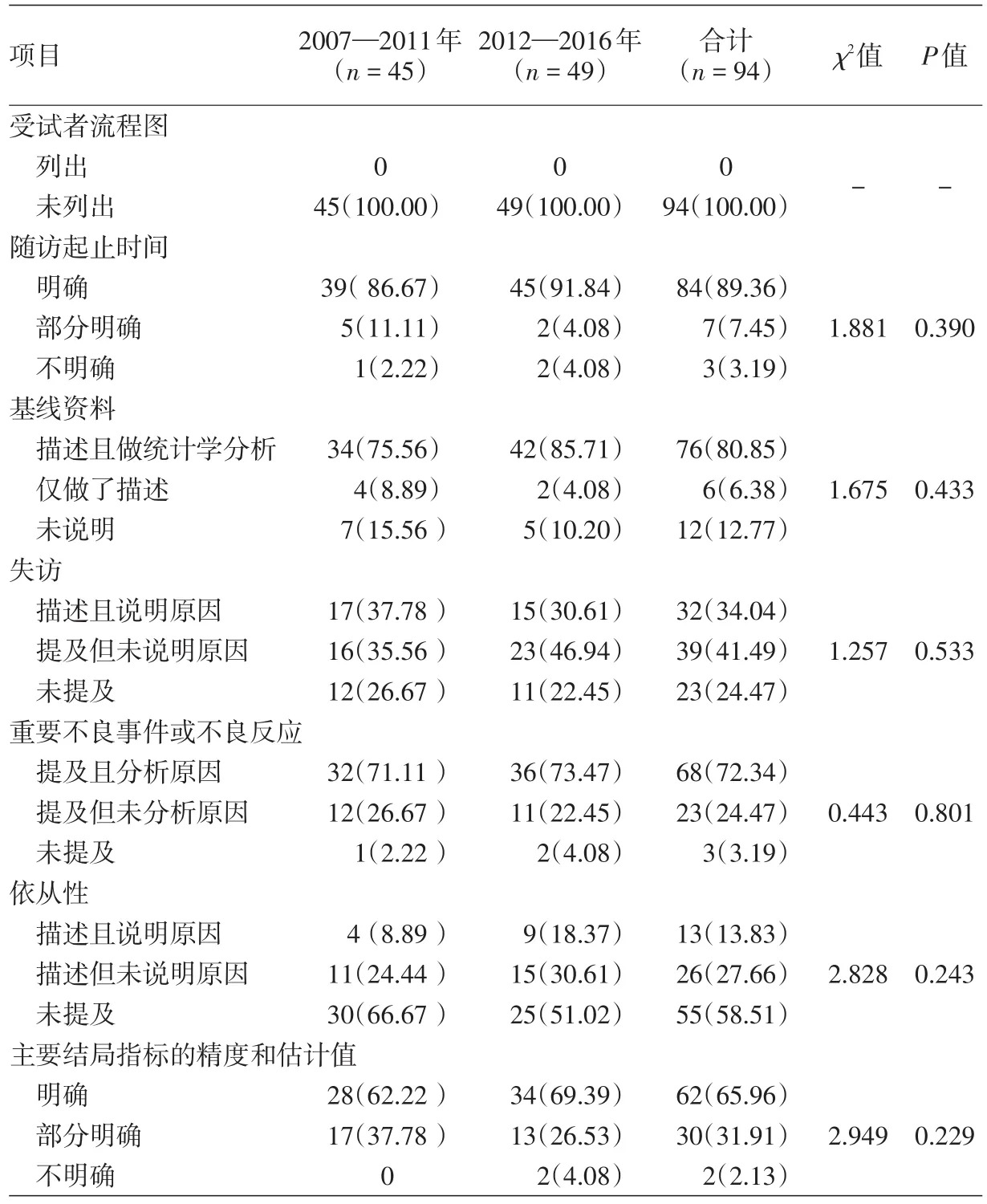
表3 《中华皮肤科杂志》2007—2016年随机对照临床试验文献结果部分报告质量评价[篇(%)]
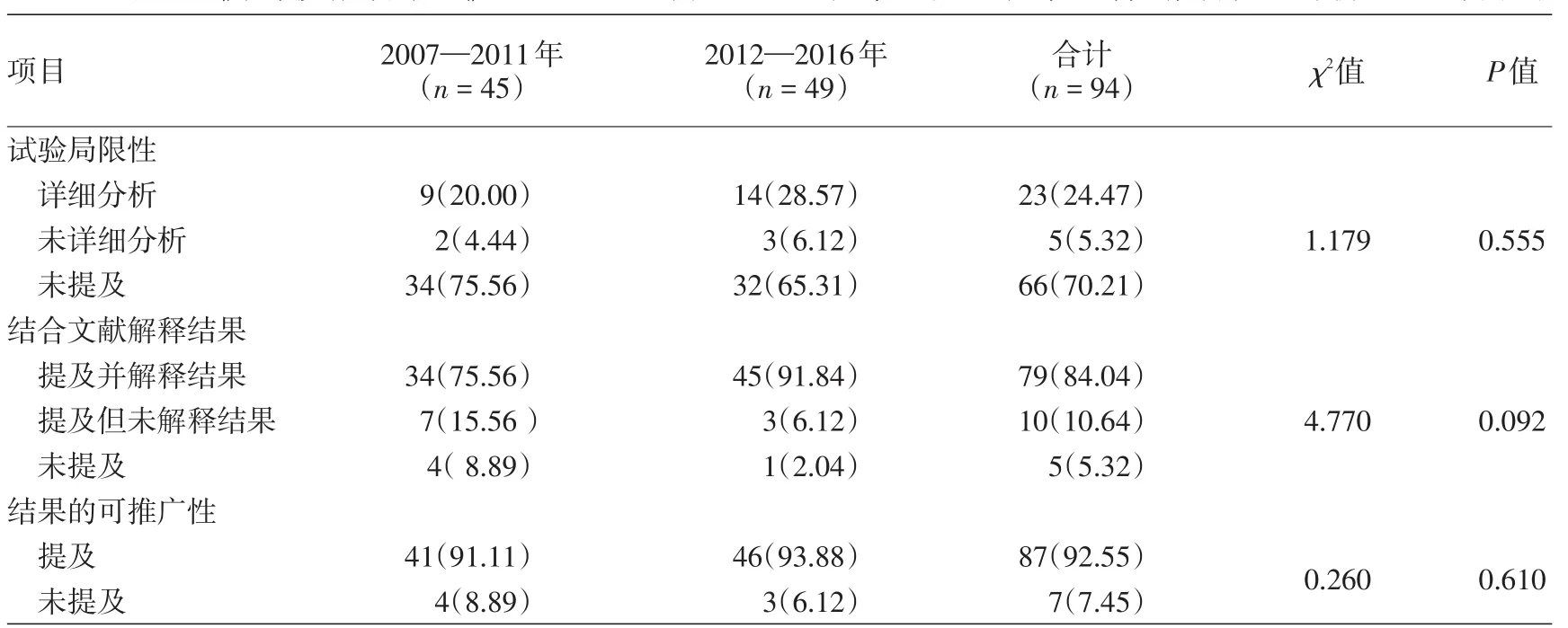
表4 《中华皮肤科杂志》2007—2016年随机对照临床试验文献讨论部分报告质量评价 篇(%)
三、讨论
CONSORT声明的出版和推广,旨在指导研究者提高RCT的报告质量。研究表明,采纳CONSORT的期刊所发表的RCT报告质量获得了显著提高[5]。我们基于CONSORT声明中各项指标对《中华皮肤科杂志》刊出的RCT文献进行评价后发现,2007—2016年RCT报告整体水平稳定,部分指标报告质量显著提高。
在前言部分,多数作者对科学背景和研究目的进行描述,但是一些文献对科学背景表达不清楚,部分作者将科学背景的介绍写为疾病定义、分型介绍或技术应用,忽略了对研究依据的说明。建议科学背景部分主要描述研究的国内外进展、已取得的成果以及研究的不足等,这样将有助于读者更好地理解研究的科学性。
RCT核心部分为试验的随机化过程。要正确地实施随机化,避免选择性和混杂性偏倚,首先应保证随机化顺序产生方法的科学性[6]。本研究中28篇文献虽提到随机,但随机化方法说明过于简单,导致读者难以判断随机方法是否合理、正确实施。还有个别文献尽管使用了“随机”一词,但实际研究却采用非随机方法,如通过就诊顺序、轮流交替分组、出生日期来确定处理组别。盲法是减少偏倚的重要方法,尤其是在评价主观性结局指标时,盲法可防止实施偏倚和测量偏倚[7]。本研究中23篇(24.47%)文献提及盲法并说明具体方法,13篇(13.83%)文献提及盲法但未说明具体方法,虽高于蒋献等[8]报道的22.9%,但盲法的应用比例仍然明显偏低。
本次研究中5篇(5.32%)文献未提及受试者的纳入和排除标准,12篇(12.77%)对受试者纳入或排除标准描述不够全面,一些文献仅有纳入标准而未明确排除标准,说明研究者对排除标准未予重视,而明确排除标准是有效避免过多、过杂的临床症状干扰,并保证研究对象重要特性均质性的重要方法[9]。临床试验报告中有无预先估计样本量是评价临床试验质量的重要依据之一[10],而我们发现所有纳入文献均未提及样本量计算。伦理委员会与知情同意书是保障受试者权益的主要措施,因此,开展临床试验时,应遵循伦理原则,维护受试者的尊严、权利、安全、健康[11-12]。本研究中20篇(21.28%)文献没有报告伦理审查情况,说明仍有部分研究者缺乏伦理意识。
CONSORT声明强烈推荐使用受试者流程图来表示受试者在研究中的流向,尤其应报告每组随机分配、接受预定治疗、完成研究方案及进行主要结局指标分析的例数。本次研究显示,所有纳入文献均未列出受试者流程图。研究组间基线资料的可比性,对于保证研究结果的真实性和可靠性具有重要意义[13]。本研究中少量文献描述不够全面,主要表现在仅对研究对象的性别、年龄等基本情况进行介绍,而忽略了对各试验组对象病情严重程度、疾病史、分型、临床症状、生理生化指标等可比性的说明,或缺少对组间基线资料是否具有一致性的统计学描述。
临床研究中出现无统计学意义的结果时,并不能排除存在重要临床差异的可能,而可信区间能显示出差别的程度,并由此判断差别有无临床意义或实际价值。本研究中,62篇(65.96%)文献报告主要结局指标的估计值及精度(均为95%可信区间)。我们发现,受试者的失访描述比例(34.04%)和依从性(13.83%)均较低,提示作者应加强对该方面的描述,避免造成偏倚,影响结果的可靠性。
不良事件的报告和不良事件报告系统是提高医疗质量,促进患者安全的重要手段[14]。本研究中23篇(24.47%)文献虽提及但未分析重要不良事件或不良反应,只是简单地描述出现某种症状,无法判断发生的不良事件是否为不良反应,3篇(3.19%)文献未提及重要不良事件或不良反应,可见作者在写作时对安全性问题重视不足。
在讨论部分,结合国内外相关研究解释结果和报告试验结果可推广性的文献比例较高。不足之处在于对试验的局限性讨论不够,仅有23篇(24.47%)文献详细描述试验的局限性,另有5篇(5.32%)文献描述局限性不够充分,使试验缺乏客观的评价。作者如能在为其RCT研究的结论提供支持性观点的同时,评价研究的局限性,将有助于读者判断研究的价值和可信度,为以后进一步研究提供依据。
综上所述,《中华皮肤科杂志》RCT文献大部分项目报告规范、清楚,近年来在整体报告水平保持稳定的基础上有所提高,但对随机、盲法、样本量计算及失访和局限性的报告仍需加强。建议研究者采用CONSORT声明作为写作RCT报告的指导工具,规范报告临床试验,提高国内皮肤科领域RCT报告的质量。

