银纳米/氨基硫脲复合物的合成、表征及光学性质研究
王 聪,朱鑫玉,李胜利
(安徽大学 化学化工学院,功能无机材料实验室,安徽 合肥 230601)
非线性光学(nonlinear optics, 简称NLO)材料作为一类重要的光电功能材料,因具有独特的性质,在很多领域特别是现代医学领域拥有非常广泛的应用前景[1],引起了人们极大的兴趣.纳米金属与有机分子相互作用得到功能性配合物是制备非线性光学材料的重要方法[2-3].在过去几十年中,有机分子和金属纳米粒子之间的相互作用已经成为研究的热点,学者们并致力于提高其整体应用性能的探索[4-6].仔细选择有机物和金属物质种类,通过对其尺寸、形状的调整和优化可有助于获得具有高稳定性的银纳米颗粒(Ag NPs)[7].它们之间的相互作用可导致光物理性质的增强或淬灭,甚至为金属纳米粒子提供全新的性能,如单光子发射荧光,非线性光学性质.因此,这类材料可以应用于光学切换[8]、3D荧光成像[9]、3D光学数据存储等方面[10].
金属纳米粒子在光电学、催化和生物医学应用领域所具有的显著特性,近年来备受人们关注[11-12].Ag NPs凭借其独特的光学和电子性质以及表面等离子体特性和固有的电导率而具有吸引力[13].金属纳米颗粒通过使用小的有机分子、聚合物或生物模板的简单方法合成,将它们稳定在溶液中[14],表现出类似分子的性质[15]、近红外吸收和大的双光子激发性能.
微波法制备纳米颗粒是制备纳米复合材料的热门手段之一[16-17],笔者课题组采用微波加热反应,以AgNO3、氨基硫脲为原料,在PVP保护下采用一步合成法制备银纳米-氨基硫脲复合物(Ag NPs-TSC).
1 实验部分
1.1 主要试剂
硝酸银,上海化学试剂有限公司;聚乙烯吡咯烷酮(PVP)、N,N-二甲基甲酰胺(DMF),国药集团化学试剂有限公司; 氨基硫脲(TSC), 阿拉丁试剂有限公司;试剂均为分析纯;实验中所用的水为去离子水.
1.2 主要仪器
实验使用的是WBFY-201型微电脑微波化学反应器、KQ2200DE型数控超声波清洗器和TG16W台式高速离心机.紫外光谱(UV-Vis)在SHIMADZU UV-3600 UV-VIS-NIR分光光度计上测试;荧光光谱在HITACHIF-4500荧光谱仪上室温下测得,1.0 cm×1.0 cm的四面通光的石英比色皿为样品池.红外光谱测试是在NexuS870型傅里叶变换红外光谱仪上进行,采用KBr压片法,拉曼光谱测试使用英国Renishaw公司的inVia Reflex型拉曼光谱仪.TEM照片在JEOL JEM 2011(300 kV)高分辨透射电镜上完成;X射线粉末衍射(XRD) 选用18 kW 多晶X射线衍射仪,采用高强度CuKα射线 (λ=1.540 56 Å).复合物的非线性研究使用全自动协调飞秒钛蓝宝石脉冲激光器 (Coherent ultra II,波长690~1 080 nm,频率80 MHz,脉冲140 fs)进行.粒度分析使用英国 Malvern Instruments公司马尔文激光粒度仪 Mastersizer Micro型测定.热重分析(TG)在德国耐驰公司449F3型同步热分析仪测定,N2环境中升温速率为20 ℃·min-1,温度范围从室温到800 ℃.
1.3 微波还原法一步合成Ag NPs-TSC复合物
用精密分析天平称量0.085 0 g(0.50 mmol)AgNO3,用去离子水定容5 mL;称量0.20 g PVP (PVP与Ag+质量比约4∶1)配成15 mL水溶液.依次将这2种溶液加入100 mL微波炉配套反应发生烧瓶中,并稀释溶液到50 mL.称取0.136 7 g氨基硫脲(1.5 mmol)配成10 mL的DMF溶液.烧瓶放入微波炉进行反应,微波功率调整到100%,从冷凝管上口逐滴加入氨基硫脲的DMF溶液,反应时间为3 min(为防止溶液温度升高太快,采取间断加热的加热方式,每次加热30 s停10 s).产物溶胶用高速离心机进行离心分离(1 200 r,15 min),取离心管底部沉淀用去离子水/DMF洗涤2次,真空干燥后用石英皿研磨,获得棕黑色的银-氨基硫脲纳米复合颗粒粉末——Ag NPs-TSC复合物.
1.4 反应过程及机制分析
当混合液置于微波环境中进行反应时,首先,在微波作用下,具有极性的水分子快速旋转产生(·H)和(·OH)以及溶剂化电子,同时激发PVP分子中N和O上的孤对电子形成自由基,从而对银离子进行还原[18];此外PVP末端的活性官能团也具有一定的还原作用,此步反应得到的反应液呈亮黄色.粒度分析测试表明,在PVP保护作用下形成的银纳米颗粒(前驱纳米颗粒)粒径在5 nm左右.逐步滴加氨基硫脲的DMF溶液时,由于氨基硫脲与银离子的配位作用,使其与反应体系中的未反应银离子形成配合物(Ag+-TSC),然后在微波的作用下,氨基硫脲N上的孤对电子形成自由基,快速还原Ag+,并在前驱纳米颗粒的基础上继续生长成较大的纳米颗粒;与此同时,氨基硫脲也不断与银纳米颗粒进行配位形成复合物;且由于氨基硫脲的加入也起到一定的分散作用,不至于使银纳米颗粒过大而形成沉淀.反应后溶胶显棕黄色,经TEM表征显示纳米复合物颗粒为球形或类球形,粒径在30 nm左右,且配体均匀结合在银纳米颗粒表面.反应机制如图1所示.
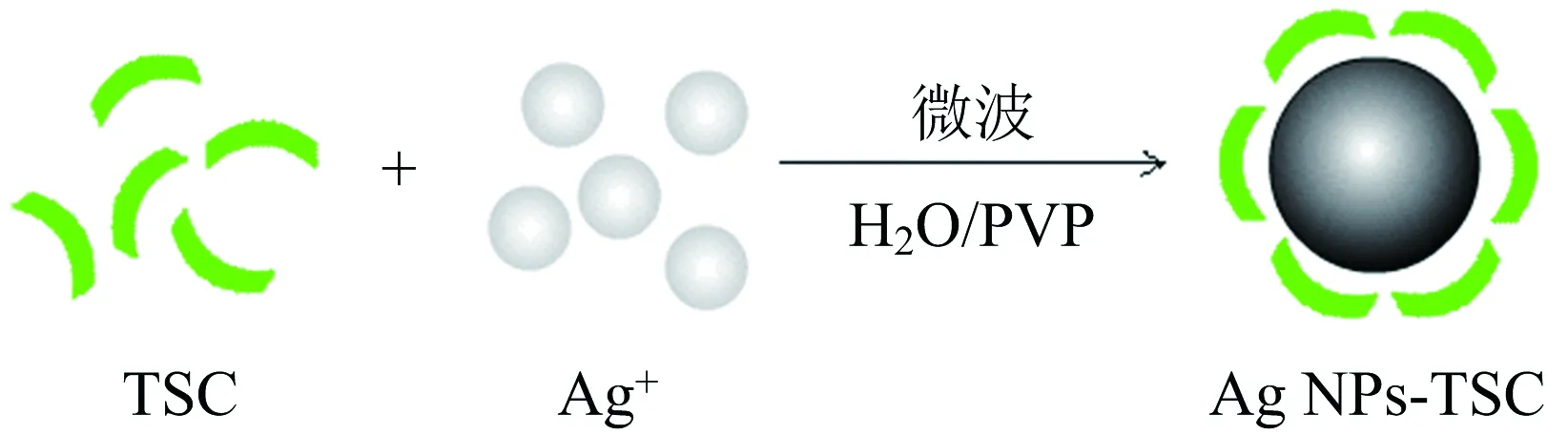
图1 反应机制示意图
2 表征、性质与分析
2.1 紫外可见吸收光谱分析
2.1.1 微波反应时间的选择
在其他反应条件一致的情况下,取M(TSC)∶M(AgNO3)=3∶1的条件分别在不同时间下进行实验,对反应后得到的溶胶进行紫外吸收光谱分析.混合物的反应时间分别为:0,60,120,180,240,300,600 s.紫外吸收测试时样品浓度为1×10-5mol·L-1,结果如图2所示.
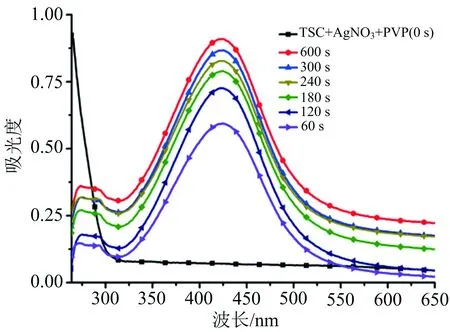
图2 不同反应时间后溶胶的紫外吸收光谱表征
图2显示,420 nm左右出现了明显的紫外吸收峰,经分析为银纳米的表面等离子共振吸收峰,与文献[19]报道的银纳米的紫外吸收峰(430 nm)基本相符.同时,随着微波反应时间的增加,紫外吸收峰并没有发生明显的红移,表明微波反应时间的长短对Ag NPs-TSC的形成影响不大,为可忽略条件,经考虑为使反应充分,选取反应时间为3 min.
2.1.2 硝酸银与氨基硫脲的比例对Ag NPs-TSC形成的影响
在其他条件一致情况下,取硝酸银与氨基硫脲不同摩尔比在相同时间下进行实验,对反应后的溶胶进行紫外吸收表征得到紫外吸收光谱.混合物反应的摩尔比分别为:M(TSC)∶M(AgNO3)=1∶1,M(TSC)∶M(AgNO3)=2∶1,M(TSC)∶M(AgNO3)=3∶1,M(TSC)∶M(AgNO3)=5∶1;微波反应时间为3 min(间断加热).紫外吸收测试时样品浓度为1×10-5mol·L-1.测试结果如图3所示.
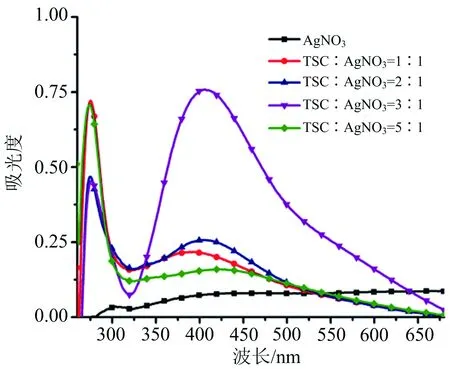
图3 TSC和AgNO3不同摩尔比下混合反应后溶胶的紫外吸收光谱表征
图3显示,随着配体量的增加,产物吸收峰出现红移,说明配体与银纳米之间产生作用,银纳米粒子的半径正生长,逐渐变大而发生红移,当M(TSC)∶M(AgNO3)=3∶1时产物吸收峰最强.配体数量过高时,复合物吸收峰宽化,表明产物粒径过大或是小颗粒团簇发生了聚集,对实验结果造成了负面影响.
2.2 粒径分析
微波反应30 s后,取反应液(前驱纳米颗粒)进行粒径分析,结果如图4所示.
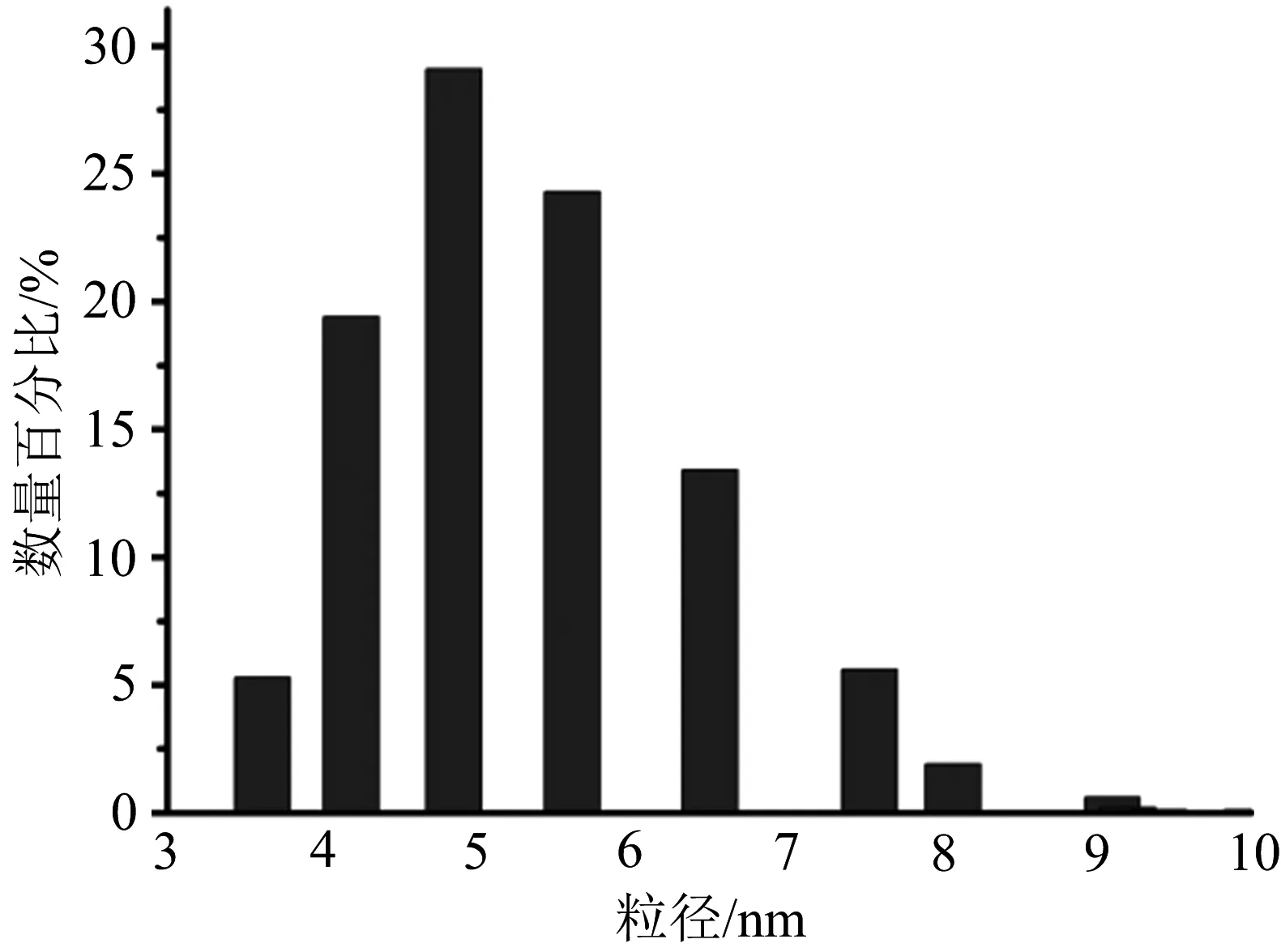
图4 前驱纳米粒子粒径分析
图4显示,初级产物纳米颗粒正态分布在3~10 nm之间,大多分布在5 nm左右.
随后所进行的1组对比实验显示,在PVP存在的状态下,反应得到的复合物纳米颗粒比较均匀,粒径大约在30 nm左右(如图5A所示);图5B是未加入PVP所得到的复合物纳米粒子,由图中可以看出纳米粒径分散在100~300 nm之间,颗粒较大且比较分散.
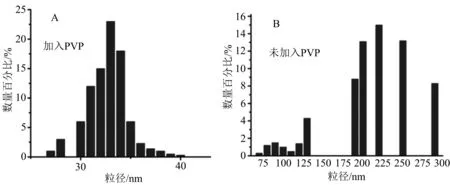
A 加入PVP B 未加入PVP图5 PVP的加入对纳米粒子粒径的影响
2.3 高分辨透射电子显微电镜图(TEM)
硝酸银与氨基硫脲在M(TSC)∶M(AgNO3)=3∶1,微波反应3 min时,取反应溶胶进行高分辨透射电子显微镜表征,得到透射电镜图,测试时样品浓度为1×10-8mol·L-1,纳米颗粒为球形或近球形,粒径在30 nm左右,且周围已经附着了配体,结果如图6所示.

图6 Ag NPs-TSC的透射电镜图
2.4 X射线衍射(XRD)
图7为Ag NPs-TSC的XRD图.
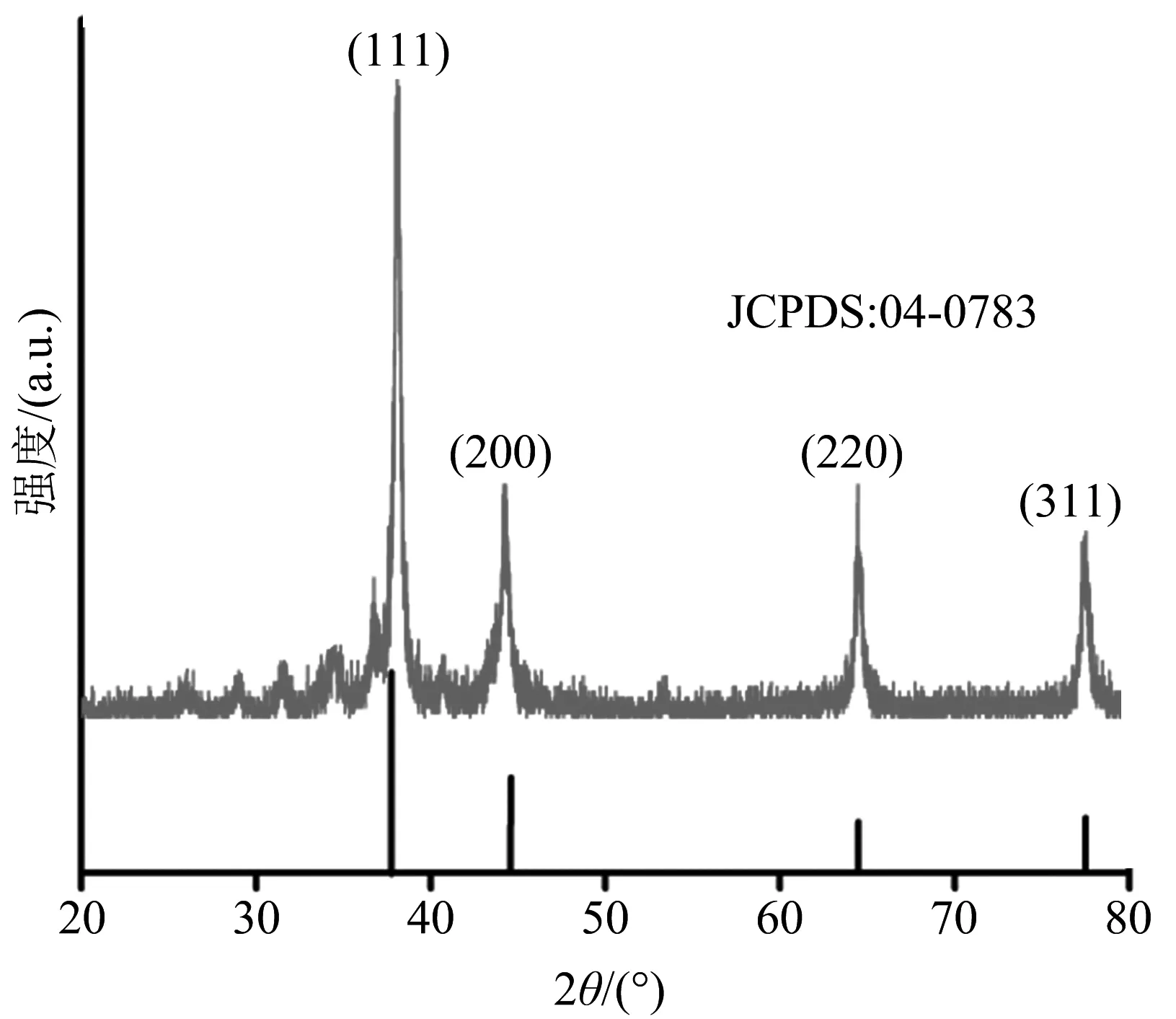
图7 Ag NPs-TSC的XRD图
图7显示,复合纳米颗粒的XRD图中有氨基硫脲的无定形峰,并且在2θ= 38,44,65,78°处的特征峰对应于Ag NPs 的(111) (200) (220) (311)晶面,其峰位置与粉晶衍射卡片(JCPDS 04-0783)匹配.在2θ= 29,32,34,37,53°有较弱的Ag2S的衍射峰对应于(111) (112) (120) (121) (213)晶面Ag2S(JCPDS 14-0072).可能是氨基硫脲与AgNO3在微波加热反应下有少量的Ag2S的产生,Ag2S可能被银纳米壳紧密地包封[20].Ag NPs-TSC的快速生长可能与Ag2S微晶的存在密切相关.
2.5 红外光谱(FT-IR, KBr压片法)分析
取Ag NPs-TSC干燥后进行红外分析,采用KBr压片法,得到红外光谱,如图8所示.

图8 TSC、Ag NPs-TSC的红外光谱
图8显示,银纳米颗粒上已经附着配体,其中,波数为3 185~3 367 cm-1的NH2以及3 264 cm-1的NH特征峰因氨基硫脲分子中N与银纳米的配位作用而明显发生红移.1 285~1 317 cm-1的C=S双键的伸缩振动峰,1 150 cm-1左右的S=C—NH变形峰等也能很好匹配.
2.6 拉曼光谱(Raman) 分析
取Ag NPs-TSC复合物干燥后进行拉曼光谱分析,得到拉曼光谱,如图9所示.
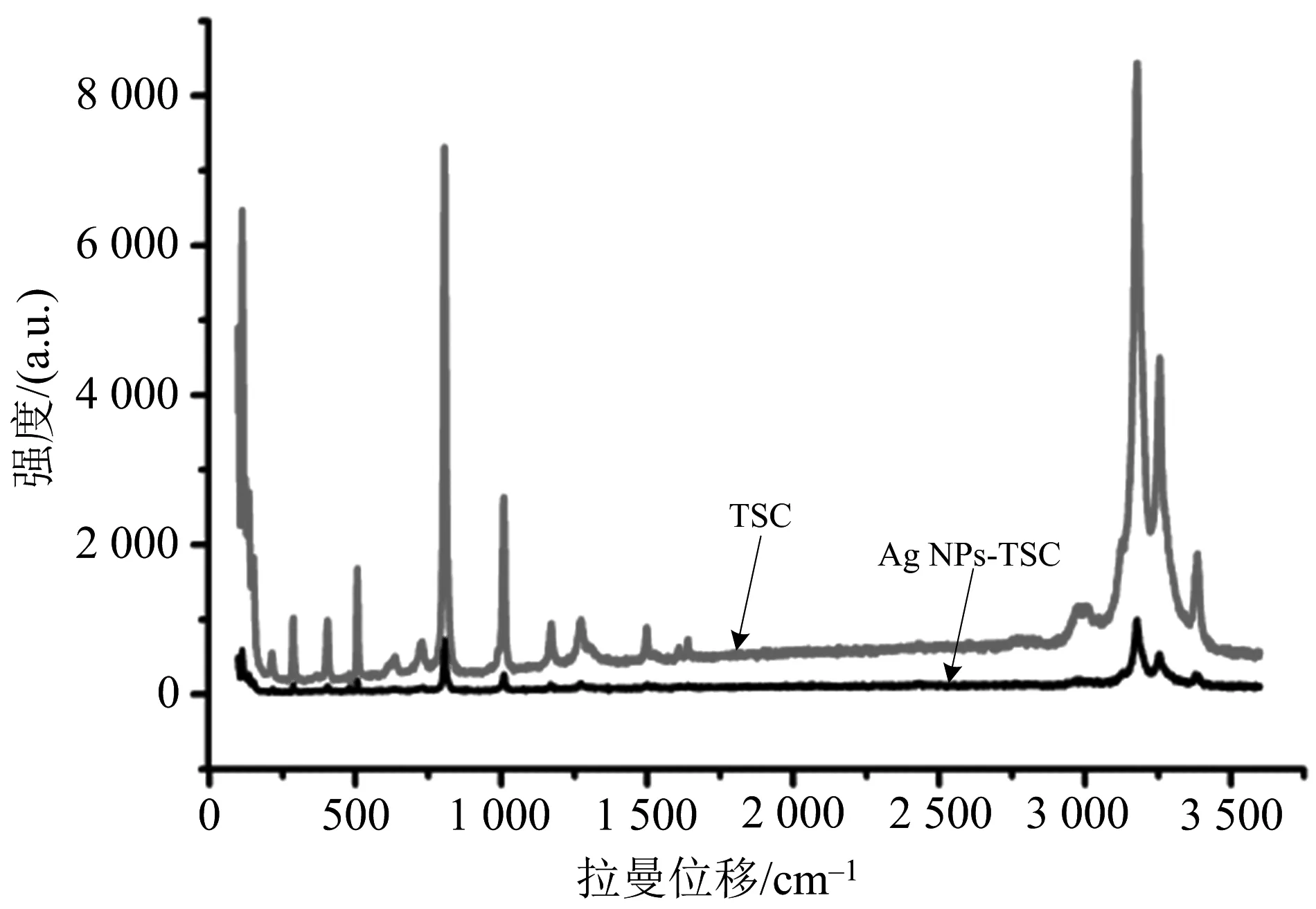
图9 TSC、Ag NPs-TSC的拉曼光谱
图9显示,复合物与配体的峰型基本保持一致,虽未见明显的拉曼增强效应,但可以证明配体已经复合到银纳米颗粒上.
2.7 热重分析(TG)
取真空干燥过的Ag NPs-TSC样品做热重分析(TG),图10是Ag NPs-TSC复合物的热重分析图.
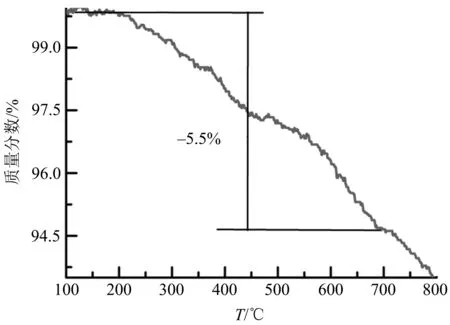
图10 Ag NPs-TSC的热重分析图
图10显示,180~700 ℃温度范围内的失重(质量分数5.5%)是银纳米颗粒表面的有机分子氨基硫脲的热解造成的,质量分数5.5%的失重量应该对应于氨基硫脲在复合粒子中的平均含量.另外,180 ℃以前的失重非常小,可能是由于复合纳米材料进行过充分干燥,表面吸附极少量的溶剂受热挥发造成的.
2.8 荧光光谱分析
取M(TSC)∶M(AgNO3)=3∶1在微波条件下反应3 min,分别取反应前后的溶胶进行荧光光谱表征得到荧光光谱,如图11所示.荧光发射光谱测试时样品浓度为1×10-5mol·L-1,λex=385 nm.
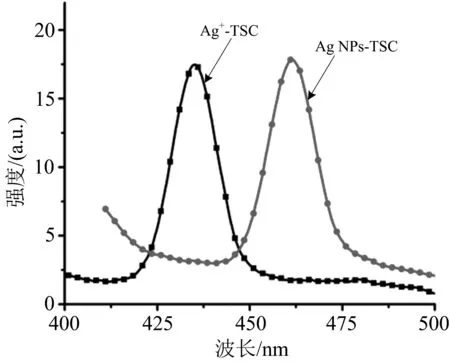
图11 TSC复合前后荧光发射光谱
如图11所示,反应前Ag+-TSC的荧光发射峰在435 nm,Ag NPs-TSC的荧光发射峰在462 nm,荧光激发发射峰出现了红移,说明氨基硫脲与银纳米颗粒复合后,分子内电荷转移能力增强,出现红移[21].
3 非线性光学性质
在信息技术高速发展的时代,为适应进一步发展的需要,用光子做信息载体的研究日益受到重视[22].随着1906年激光器的发明与应用[23],以非线性光学(NLO)效应为特征的光电材料的研究和开发应运而生.光和物质相互作用会产生光的吸收、反射、散射和发光等现象,其效应一般与光的强度无关而只和入射光的波长(或光子能量)有关.当使用高强度的电磁场(包括激光)和物质相互作用时会产生与光强有关的光学效应,成为非线性光学效应.Z-扫描技术是一种基于光畸变原理的纵向扫描测量材料非线性极化率的方法,它是由M. Sheik-Bache于1989年首次提出[24-25].该方法借助光束的空间畸变,不仅可以测量非线性折射率的大小、确定其正负,还能测量材料的非线性吸收系数.非线性吸收通常包括饱和吸收、反饱和吸收以及双光子吸收等.
3.1 开孔Z-扫描
激发光源为钛宝石激光器680~1 080 nm的激光,脉宽140 fs,重复频率80 MHz,D1、D2和D3为能量计.D1监测光源能量,D2测量入射光通过样品后的透射光能量(称为开孔测量).样品在透镜的焦点(z=0)前后移动,定义D2/D1为透过率T(z),并归一化(z位置远离焦点处取T=1),作T(z)~z的曲线即为开孔Z扫描曲线,如图12所示.
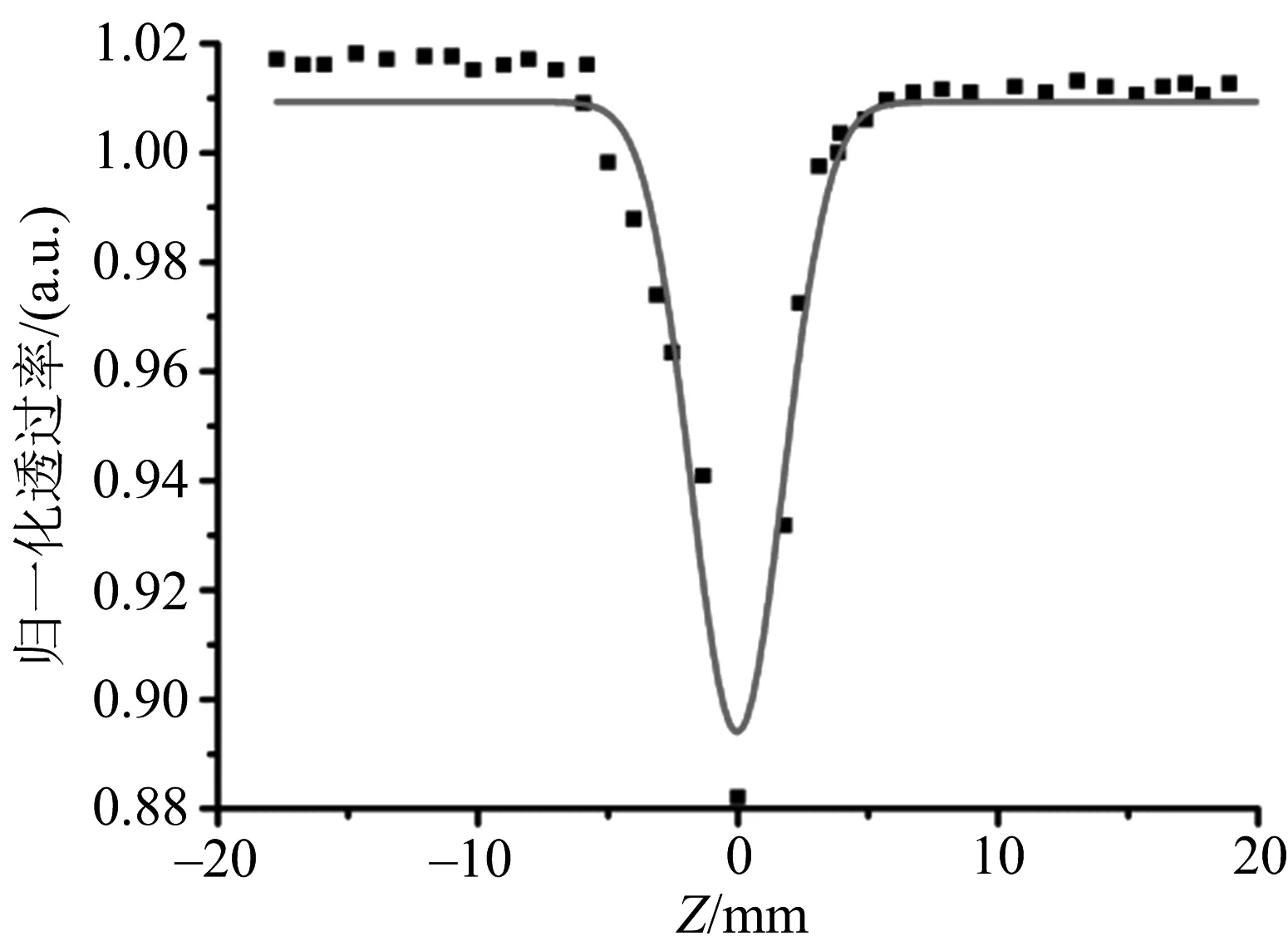
图12 Ag NPs-TSC的开孔Z-扫描曲线
图12显示,归一化后的透过率在入射光焦点z=0处出现一个明显的谷.
在开孔处测量多个数据点(z/z0,D2/D1),再通过下面的方程式拟合,从而推算出β值.
(1)
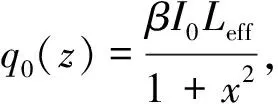
x=Z/Z0,z0=πω02/λ,
(2)
其中:I0=(入射光能量/焦斑面积),为焦点处的入射光峰值光强或光功率密度;Leff为样品池的有效厚度;Z为样品距离焦点的位移,是Z扫描曲线的横坐标;ω0为入射光束腰的半径;λ为入射光波长.拟合曲线后可以得到双光子吸收系数β,对其双光子吸收截面可以依据下面公式计算得到
σ=hγβ/NAd0×10-3,
(3)
其中:h为普朗克常数,γ为入射光频率,NA为阿伏伽德罗常数,d0为样品浓度.通过以上分析和计算可以得到双光子吸收系数β,进而求出双光子吸收截面σ.
3.2 闭孔Z-扫描
闭孔测量时:非线性吸收和折射都影响到小孔的透过能量曲线.Z-扫描曲线虽然表现为前谷后峰,但峰谷形状不对称,峰的高度被压低,而谷的深度被加深.为扣除非线性吸收的影响, 将闭孔测量的Z-扫描曲线逐点对应地除以开孔测量的Z-扫描曲线,就可得到闭孔Z-扫描曲线,如图13所示.
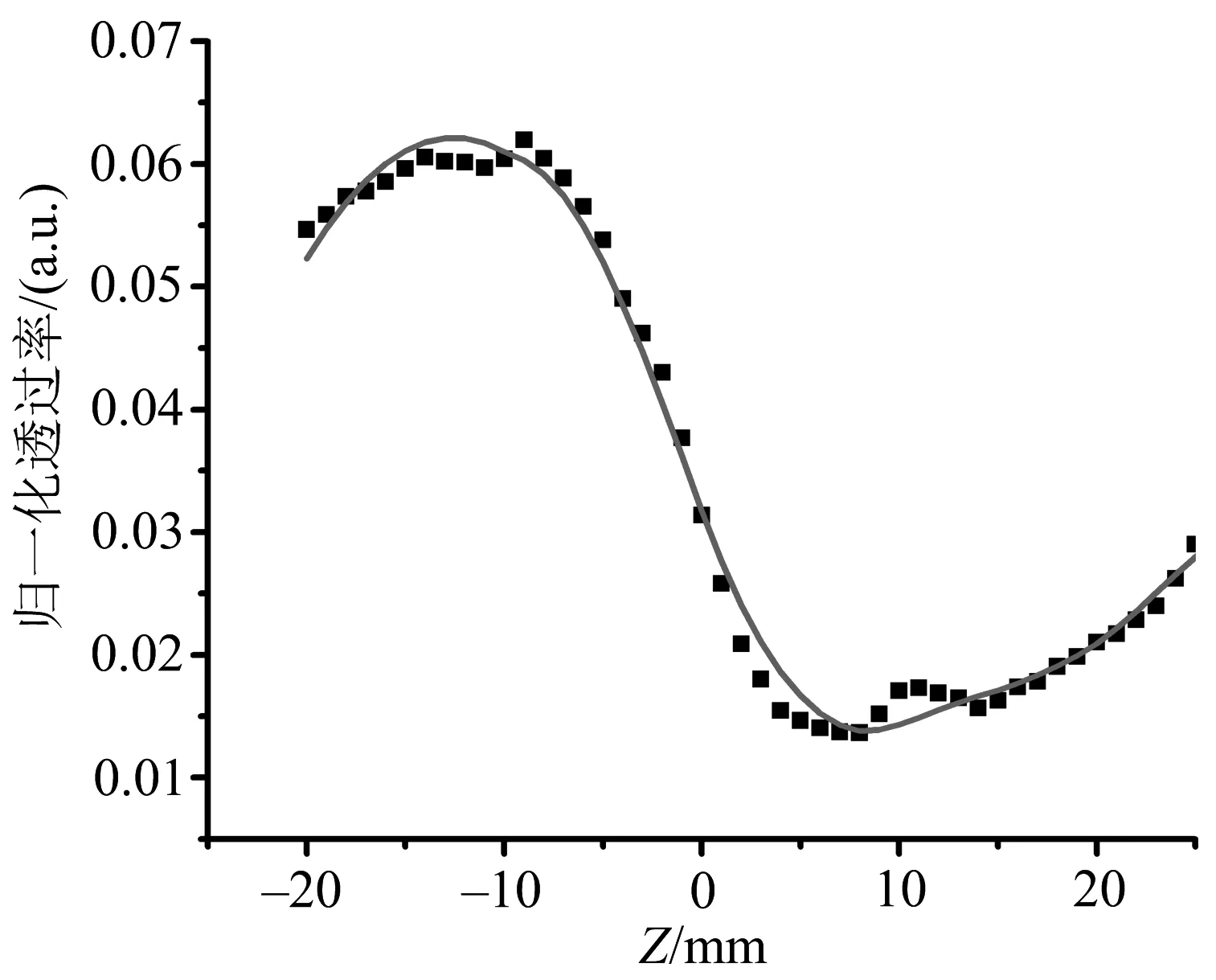
图13 Ag NPs-TSC的闭孔Z-扫描曲线
闭孔扫描透射曲线峰谷差
(1)
其中:ΔTp-v为透射曲线峰谷差,s为小孔光阑的线性透过率,ΔΦ为非线性相移,γ为样品的非线性折射率,Leff= [1-exp(1-αL)]/α为样品有效厚度(α是样品线性吸收系数),L为样品池厚度,I0为焦点处光功率密度.
计算Reχ(3)[esu]和 Imχ(3)[esu]
Reχ(3)[esu]=10-4ε0c2n0γ/π,
(2)
(3)
其中:ε0为真空中介电常数;n0为样品线性折射率;c为真空中光速3.0×108m·s-1;λ为入射光波长;β为双光子吸收系数;Reχ(3)为三阶非线性极化率的实部,Imχ(3)为三阶非线性极化率的虚部.
3.3 Ag NPs-TSC的非线性吸收数据
由3.1和3.2计算得到Ag NPs-TSC的非线性吸收数据列于表1.

表1 AgNPs-TSC的非线性吸收数据
注:表中a表示1 GM=1×10-50cm4·s per photon.
图12~13及表1显示,Ag NPs-TSC的双光子吸收截面达到4 658.23 GM,这是由于氨基硫脲与银纳米颗粒之间的耦合作用、协同作用使Ag NPs-TSC有较大的双光子吸收截面,同时表面等离子体作用使得失电子作用增强也导致复合物的双光子吸收截面增强,表明复合材料有较高的双光子吸收活性,其在非线性光学材料领域有较好的潜在应用价值.
4 结束语
(1) 利用硝酸银溶液为前驱体、PVP为保护剂剂、氨基硫脲为配体,采用液相化学还原法,在微波的条件下,同时没有另外加入其他还原剂,成功制备了粒径均匀的银纳米氨基硫脲复合物.该反应周期短,时效性好,便于重复,有利于实验过程中寻求最佳的方法来进行实验.通过微波反应实验,得到粒径较小、形态均匀的近球形银纳米-氨基硫脲复合物颗粒.
(2) 氨基硫脲小分子修饰在纳米颗粒银表面,建立了一个新的非线性光学有机-金属纳米复合体系.并通过TEM、IR、拉曼光谱等表征手段证明了TSC分子是通过配位键的形式覆在银纳米颗粒表面上.
(3) 通过Z-扫描研究了复合后非线性光学性质的变化,由于氨基硫脲和Ag NPs组分的协同效应,它们之间的激子-等离子体相互作用,增加了双光子吸收系数(β),双光子吸收截面(σ),非线性折射率(γ)和三阶非线性极化率(χ(3)).笔者所制备的复合物是一个较好的非线性光学材料.
(4) 实验的不足在于每次实验不能使溶胶浓度太高,同时微波反应温度不能升高过快,否则产物会出现明显的聚集;而且该反应的产率较低,为15%~20%,后期可通过改进实验工艺等提高产率;此外,反应溶剂选用的是水,在进行光学测试时其自吸收明显,后期可通过使用其他溶剂从而改良实验结果.

