GC-MS法分析滁州贡菊中挥发油成分
徐冬青,张从宇,张雪梅
(1.安徽科技学院 分析测试中心,安徽 凤阳 233100;2.安徽科技学院 化学与材料工程学院,安徽 凤阳 233100)
菊,是多年生菊科草本植物,在我国,其品种已达3 000多种,其在安徽比较著名的当属滁州贡菊和黄山贡菊.这里所说的菊花是菊科植物菊花(DendranthemamorifoliumRamat.)的干燥头状花序,是我国常用的传统中药,研究表明菊花具有清肝明目、散风清热作用,可用于风热感冒、头痛眩晕、眼目昏花等症[1-2].菊花挥发油中含有的大量萜烯及其衍生物具有良好的生物活性[3-4],并且菊花中含有的大量黄酮类[5-6]化合物具有降低血压[7]、扩张冠状动脉、预防高血脂等多种生理活性,其在临床上主要用于治疗高血压和冠心病[8-9].
近年来,随着保健品和化妆品行业的不断发展,精油产品越来越受到人们的追捧,其中菊花精油具有清热解毒、抗衰老和美容等多重功效而广泛受人喜爱.菊花精油的主要成分为菊花中的易挥发成分,由于我国菊花种类较多,不同地区的挥发性成分略有不同;而在安徽滁州贡菊种植面积广和产量较大,故鉴定出滁州贡菊中挥发性成分对滁州贡菊的进一步推广及在中药、保健品和日化行业中的应用具有重要的意义.笔者通过水蒸气蒸馏提取滁州贡菊的挥发油,并运用气质联用仪鉴定其中的化学成分.
1 实验部分
1.1 仪器和材料
气质联用仪(GC-MS)为 Agilent5975C-7890A,色谱柱型号: HP-5MS,30 m×0.25 mm×0.25 μm;滁州贡菊采自安徽科技学院中药园,经中药实验室鉴定为正品,植物标本现存放于安徽科技学院,所用溶剂均为色谱纯.
1.2 滁州贡菊中挥发油的提取
取干燥的滁州贡菊的花朵100 g放至1 000 mL的三口烧瓶中,内加700 mL饱和的氯化钠水溶液和沸石;另配油浴、油水分离器及水蒸气发生装置,先80 ℃加热4 h,后全回流4 h,分去油水分离器的水相,得到菊花挥发油,经无水硫酸镁干燥后,称重得到淡黄绿色油状液体0.38 g(提取率为0.38%).
1.3 挥发油 GC-MS 测定与分析
取2滴提取的挥发油样品用色谱纯环己烷溶解后得到样品,然后进行GC-MS检测,得总离子流图,并将所得色谱峰的质谱图信息经计算机处理在质谱库中进行检索( 相似度大于 80% ),结合人工解析,鉴定滁州贡菊中挥发油的化学成分,按照面积归一化法确定各成分的质量分数.
气相色谱条件:色谱柱为HP-5MS, 5% Phenyl Methyl Silox 30 m×250 μm×0.25 μm; 进样量1. 0 μL,分流比10∶1,载气为高纯氦气,流速1.0 mL·min-1,进样口温度 250 ℃ ,程序升温: 初始温度60 ℃,以5 ℃·min-1速率升温至220 ℃,保留10 min.
质谱条件:离子源温度230 ℃,四级杆温度150 ℃;接口温度250 ℃,电离方式为 EI 源,电子能量70 eV,离子源温度200 ℃,离子扫描范围45~400(m/Z),溶剂延迟时间4 min.
2 结果与讨论
提取的滁州贡菊挥发油样品,经GC-MS检测后,其结果如图1和表1所示.
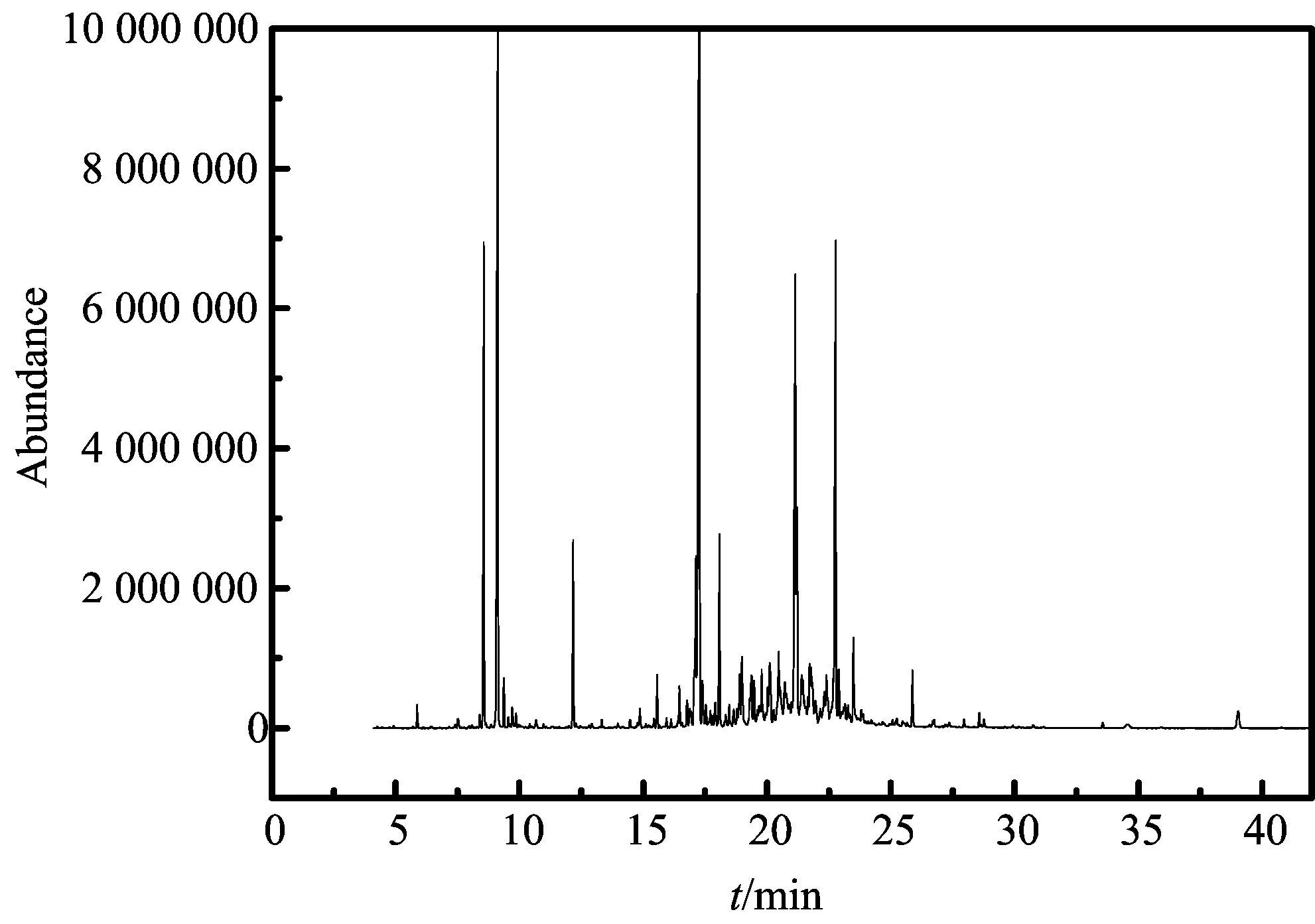
图1 滁州贡菊挥发油成分的总离子流图

No.t/minCompoundsFormulaMWArea/%15.861桉叶油醇 (1,8-cineol)C10H18O1540.26527.405罗勒烯 (ocimene)C10H161360.0538.4032-蒈烯-4-醇 (2-caren-4-ol )C10H16O1520.15348.561樟脑 (bornanone)C10H16O1525.56859.128冰片 (endo-borneol)C10H18O15412.75669.373萜品烯-4-醇 (terpinen-4-ol)C10H18O1540.47679.706α-萜品醇 (α-terpineol)C10H18O1540.24189.863桃金娘烯醇 (myrtenol)C10H16O1520.15912.168乙酸冰片酯 (bornyl acetate)C12H20O21962.0531014.466α-古巴烯 (α-copaene)C15H242040.1051114.870β-橄香烯 (β-elemen)C15H242040.261215.559石竹烯 (caryophyllene)C15H242040.6391315.943α-香柑油烯 (α-bergamotene)C15H242040.1421416.015β-古芸烯 (-)-β-gurjuneneC15H242043.1881516.140β-倍半水芹烯(β-sesquiphellandren)C15H242040.0881616.463(E)-β-金合欢烯 (cis-β-farnesene)C15H242040.4981716.771β-檀香烯 (β-santalene)C15H242040.3551816.877(+)-香橙烯 (aromandendrene)C15H242040.241916.9332-异丙烯基-4a,8-二甲基-1,2,3,4,4a,5,6,7-八氢萘(2-isopropenyl-4a,8-dimethyl-1,2,3,4,4a,5,6,7-octahydronaphthalene)C15H242040.2382017.066β-古巴烯 (β-copaene)C15H242040.062117.075α-衣兰油烯 (α-muurolene)C15H242040.042217.128α-姜黄烯 (α-curcumene)C15H222023.0472317.265(+)-β-芹子烯 ( (+)-β-selinene)C15H2420418.7092417.389α-芹子烯 (α-selinene)C15H242040.8432517.403β-愈创木烯β-guaieneC15H242040.7292617.5349,10-脱氢异长叶烯(9,10-dehydro-isolongifolene)C15H222020.3042717.695β-红没药烯 (β-bisabolene)C15H242040.2242817.788β-姜黄烯 (β-curcumene)C15H222020.1332917.854α-荜澄茄烯 (β-cadinene)C15H242040.2493017.907异戊酸冰片酯 (bornyl isovalerate)C15H26O22380.443118.083β-倍半水芹烯 (β-sesquiphellandren)C15H242040.8443218.2158,9-脱氢异长叶烯(8,9-dehydro-isolongifolene)C15H222021.0513318.665γ-古芸烯环氧化合物 (γ-gurjunenepoxide)C15H24O2200.6963418.796脱氢异长叶烯氧化物(dehydro-cyclolongifolene oxide)C15H22O2180.2313518.9853-蒈烯-4-醇乙酰乙酸酯(3-caren-4-olacetocacetate)C14H20O32360.2493619.184斯巴醇 (spathulenol)C15H24O2200.542
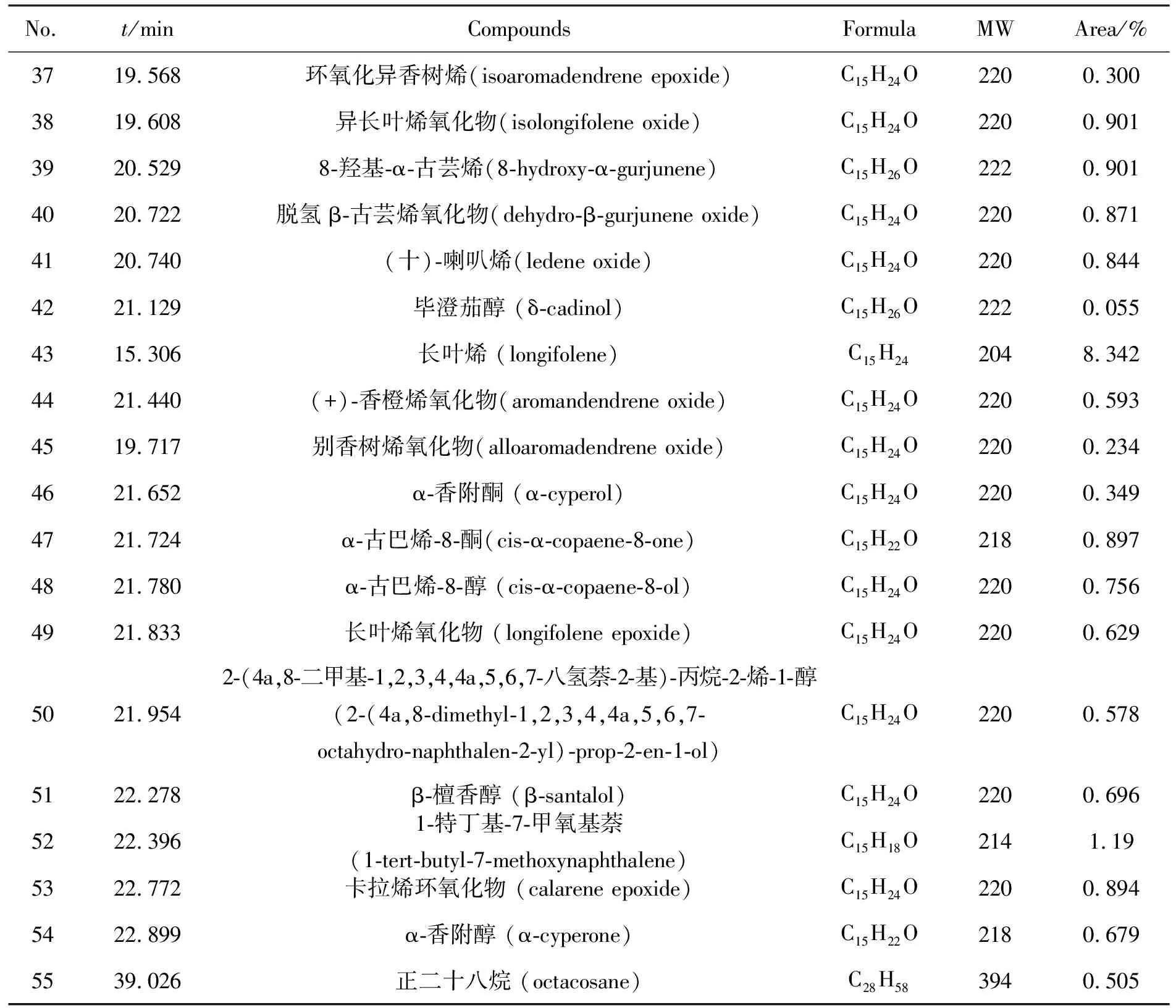
续表1
由图1和表1可知,检测的各组分质谱数据经NIST 和Wiley 数据库检索,并与标准谱图及相对保留时间分析和比较,用面积归一化法计算各组分的相对百分含量,提取出的挥发油经气相分离出156个色谱峰,鉴定了其中55种化合物(相似度大于80%并与标准谱图比对),占挥发油总质量的76.07%,已鉴定成分包括脂肪族及其含氧衍生物和萜烯类及其含氧衍生物,从分析的结果可以看出:樟脑(bornanone)、冰片(endo-borneol)、(+)-β-芹子烯((+)-β-selinene)、长叶烯(longifolene)、卡拉烯环氧化物(calarene epoxide)分别占挥发油的5.800%,13.288%,19.489%,8.690%,8.074%,这4种物质在提取的挥发油中相对含量较高;在已鉴定的化合物中,其中有11种化合物在菊花提取物中未曾报道过,分别为α-香柑油烯 (α-bergamotene)、α-衣兰油烯(α-muurolene)、9,10-脱氢异长叶烯(9,10-dehydro-isolongifolene)、(+)-氧化喇叭烯(ledene oxide)、加氢环长叶烯氧化物(dehydro-cyclolongifolene oxide)、斯巴醇(spathulenol)、8-羟基-α-古芸烯(8-hydroxy-α-gurjunene)、脱氢β-古芸烯氧化物(dehydro、β-gurjunene oxide )、8,9-脱氢异长叶烯(8,9-dehydro-isolongifolene)、α-香附醇(α-cyperol)、α-古巴烯-8-酮(cis-α-copaene-8-one),它们占提取挥发油的5.622%,占已鉴定化合物的7.237%.
3 结束语
滁州贡菊在安徽滁州地区栽培范围广,产量大.笔者对滁州贡菊的药用部分挥发油进行了GC-MS 分析,从滁州贡菊的药用部分挥发油中分离出156个色谱峰,鉴定了其中的55种化合物,占挥发油总质量的76.07%,其中有11种化合物在菊花提取物中未曾报道;从解析的化合物结构看,滁州贡菊挥发油中大多数为萜烯类及其衍生物,而且相关化合物都具有特殊的香气或生物活性,今后将进一步对其进行深入研究,为滁州贡菊提取物在精油、中药和食品领域中的广泛应用提供一定的依据.

