深静脉血栓形成与肺栓塞危险因素及临床特点的对比分析
杨鹏云 党永康 杨 柳 姜学超
1 内蒙古医科大学研究生院,呼和浩特 010110
2 赤峰市医院血管外科,内蒙古 赤峰市 024000
下肢深静脉血栓形成(deep vein thrombosis, DVT)和肺动脉栓塞(pulmonary embolism, PE)统称静脉血栓栓塞症(venous thromboembolism, VTE)。在我国DVT与PE的发病率明显低于西方国家,国内一项多中心临床流行病学调查显示,肿瘤患者中DVT的发病率仅为2.8%,而欧洲的数据则为40%~50%,我国中风患者DVT的发病率为6.7%,而加拿大报道中风患者中DVT的而发病率为28%[1],出现此现象的原因由于国内医师对VTE的认识不足,导致调查存在局限性。蔡柏蔷等对肺栓塞基础病因的变迁从1950年至2000年分为四个时期进行阐述,1950年至1982年间,PE病因的主要构成为心脏病,占比40%,DVT占比仅为13%;1983年至1990年,DVT成为PE病因的主要构成,占比52%,而心脏病在此期后的病因构成比上均有所下降;1991年至1997年DVT有所增加占比65%;直到1998年至2000年第四时期,DVT均为PE病因的主要构成,同时以外伤、手术、肾脏疾病、结缔组织病因素等引发PE的构成比也有所增加[2]。据报道中显示近些年PE的发病有所增加,但仍未达到西方国家的发病水平,随着不同时期的发展,目前DVT已经成为PE发生的主要基础病因,国内众多学者认为PE和DVT是同种疾病在不同阶段的表现[3],但是两者在危险因素及临床特点上是否存在着差异仍有待于研究。
1 资料与方法
1.1 一般资料
抽取2010年1月至2016年12月赤峰市医院住院患者中通过临床查体与辅助检查确诊VTE患者2268例,占同期住院患者总数的0.60%(2268/378 018)。DVT患者1443例,占同期住院患者总数的0.38%(1443/378 018),PE患者825例,占同期住院患者总数的0.22%(825/378 018)。分别选取同期住院诊断为DVT与PE的患者并排除其他干扰因素进行匹配,病例选取原则:⑴通过下肢彩色超声多普勒(CDFI)、下肢静脉造影(CV)、下肢CT静脉造影(CTV)、单纯多普勒血管检查中的任意一项确诊的DVT患者;通过肺动脉血管造影(CTPA)、肺动脉造影(PAA)、磁共振血管造影(MRV)中的肺部平扫CT(PCT)、核素肺通气/灌注扫描(V/Q)或超声心动图检查发现肺动脉内有血栓,其中一项确诊的PE患者;⑵病历记录完整,内容详细。⑶对照组选择同医院,同一住院时间,相同年龄及性别构成,排除与实验组相同或相似疾病及干扰因素进行匹配,本研究对照组病例有限故采用成组匹配。
1.2 统计学分析
采用SSPS 21.0统计学软件进行统计学分析,所有资料均为计数资料,采用构成比表示,χ2检验进行统计分析;危险因素分析采用Logistic回归模型,采用似然比前进法进行分析,P<0.05时差异有统计学意义。
2 结果
2.1 DVT与PE的性别分布特点
本院2010年至2016年住院患者中DVT与PE的性别分布对比,PE患者中男性370例,女性455例,男∶女=0.81∶1。DVT患者中男性724例,女性719例,男∶女=1.01∶1。分组的性别比较差异具有统计学意义(χ2=5.96,P<0.05)。
2.2 DVT与PE的年龄构成对比
DVT与PE的发病人数的分布呈现正态分布规律。统计分析显示,DVT与PE比较,两者在10~29岁、70~89岁比较差异有统计学意义。见表1。
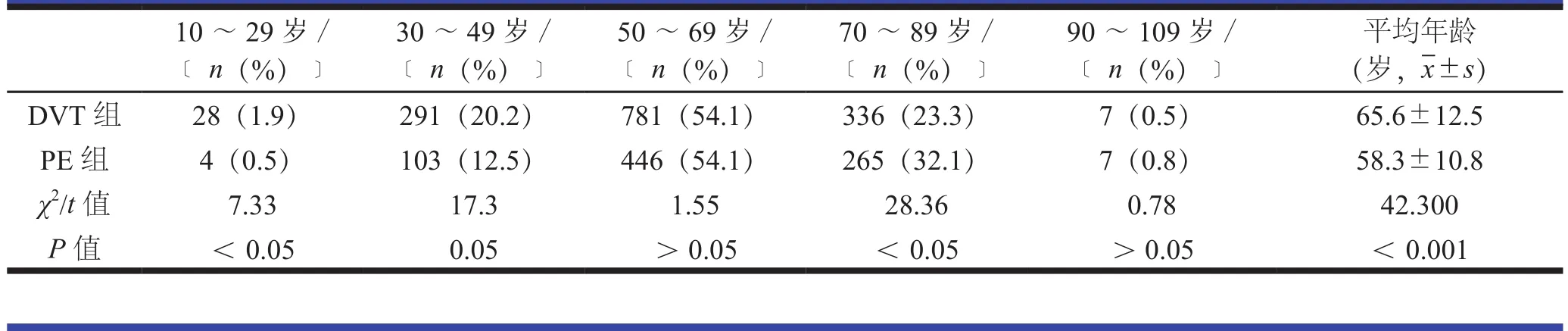
表1 DVT与PE不同年龄段差异性分析
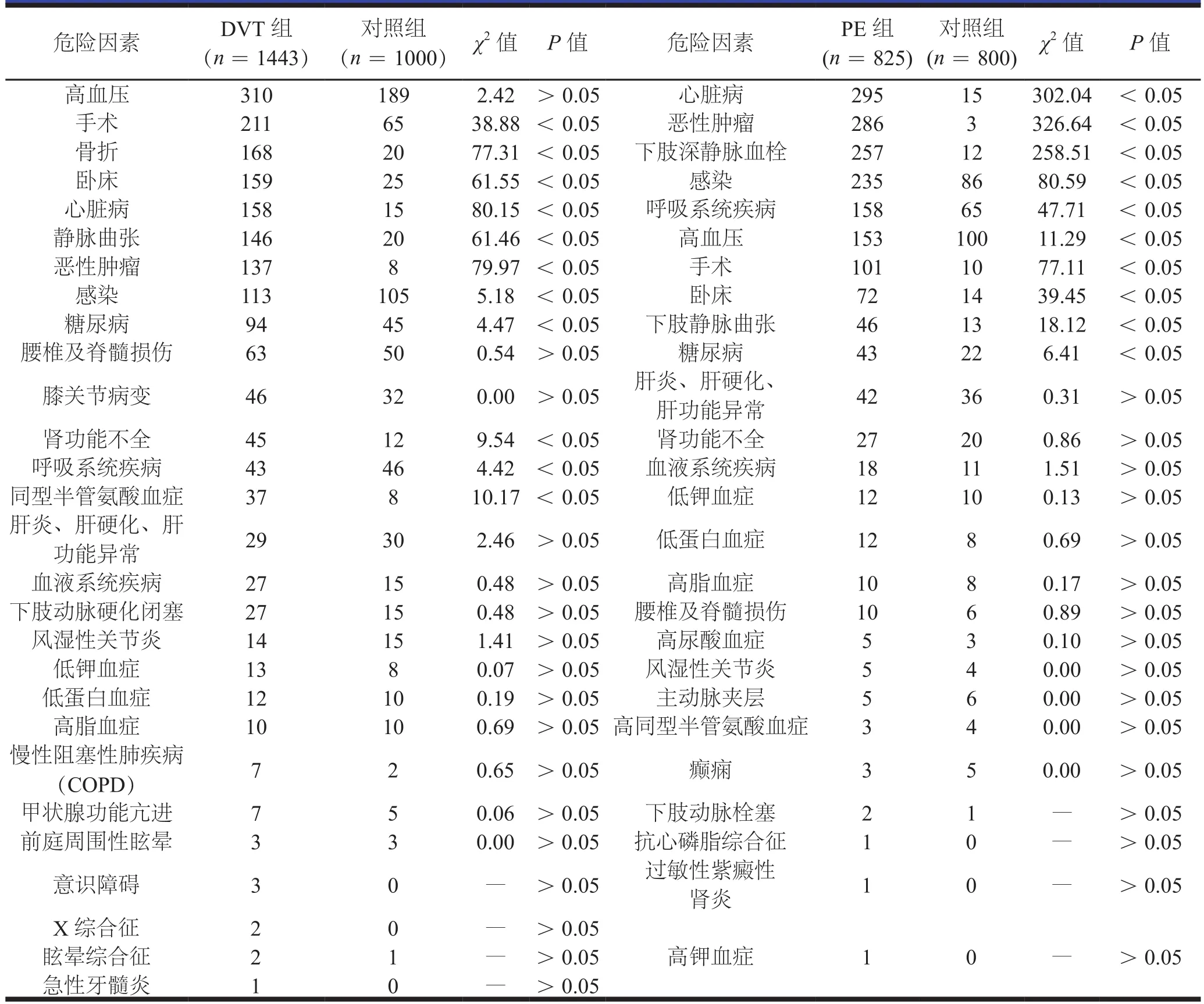
表2 DVT与PE的危险因素
2.3 DVT与PE的危险因素分析
DVT组与对照组危险因素的比较、PE组与对照组危险因素的比较见表2。将单因素分析具有统计学意义的变量共10个引入Logistic回归模型,采用似然比前进法筛选变量,α=0.10,其中手术(OR=1.29,95%CI=0.82-12.56,P<0.05)、骨折(OR=1.55,95%CI=0.24-6.21,P<0.05)、心脏病(OR=9.15,95%CI=6.27-30.17,P<0.05)、恶性肿瘤(OR=8.57,95%CI=5.50-16.29,P< 0.05)、 卧 床(OR=1.03,95%CI=0.33-3.60,P<0.05)均为DVT发生的独立危险因素,见表3。同样方法对PE进行分析心脏病(OR=9.23,95%CI= 4.56-16.33,P<0.05)、 恶 性 肿 瘤(OR=6.39,95%CI=4.83-12.61,P<0.05)、下肢静脉血栓(OR=5.52,95%CI=3.25-16.20,P<0.05)、感染(OR=2.33,95%CI=1.57-5.69,P<0.05)、呼吸系统疾病(OR=1.71,95%CI=0.39-6.57,P<0.05)、手 术(OR=1.25,95%CI= 0.82-10.27,P< 0.05)、卧床(OR=1.00,95%CI=0.32-4.50,P<0.05)均为PE发生的独立危险因素,见表4。
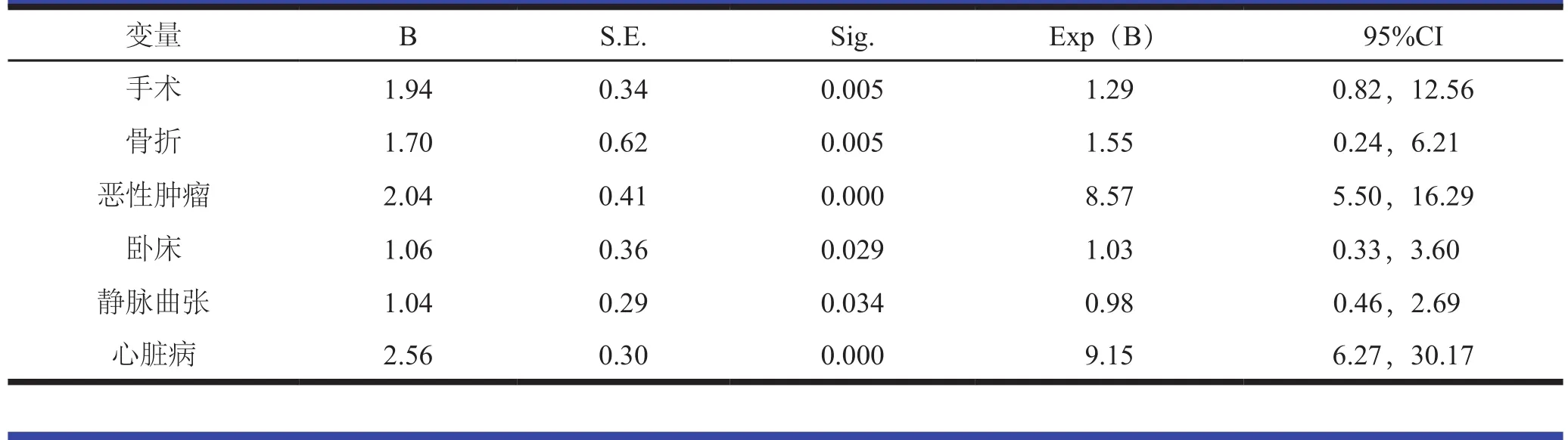
表3 DVT的独立危险因素
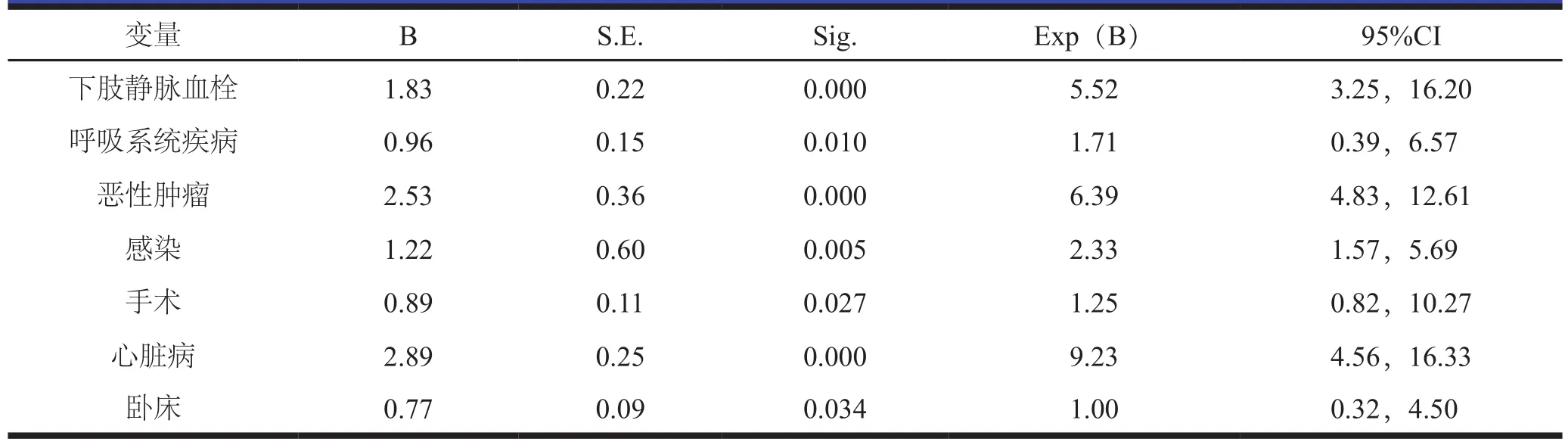
表4 PE的独立危险因素表
3 讨论
在美国,术后DVT的发病率可达45%~70%,其中3%可引起致命的PE,且PE在西方国家的发病率可达30%~50%。但研究者表明因此无论在西方国家还是我国DVT与PE发病率的报道的数据明显低于实际发病率。在近期研究中,有学者对意大利11家医院PE患者进行分析,结果显示PE的患病率为17.3%[4]。
本院自2010年开始DVT与PE的患者数在同期住院患者所占比例中呈逐年上升的趋势。通过对文献的检索,从1998年至2000年国内杂志发表有关VTE的文章不足200篇,而到目前2017年国内杂志发表的有关VTE的文章已达2万余篇,因此,随着医生对DVT与PE认知水平的提高以及检测技术上的完善使得该疾病的发病率出现逐年上升。但是,根据报道[5]近几年我国的发病率仍明显低于西方国家,而且在病因和临床特征上也略有不同,导致这一结果的原因可能由于我国一直欠缺大规模的人群调查研究,因此,我国医生对DVT与PE临床特点与危险因素的认知度的提高以及本院院内VTE的诊断策略的普及与完善仍是当前的重点。同时对于我国国民对于深静脉血栓的危险性认识以及肺栓塞的严重程度认识也需要医生的宣教、媒体的宣传。
3.1 DVT与PE的性别特点
在所查阅的文献中未见DVT与PE患者在性别上的差异比较,在本研究中,DVT与PE比例的比较有统计学差异。在对国外学者Bauersachs RM等的研究中表明在对DVT进行诊断中,女性患病人数比男性多。然而,在确诊的DVT患者中男性的患病率高于女性,这可能与男女双方在DVT上的得分同样受到歧视有关。因此男性的DVT患病率更高,而血栓性事件则更为严重[6]。
3.2 DVT与PE的年龄特点
通过对国内及国外文献的查找,年龄已经作为深静脉血栓形成的独立危险因素存在[7],研究中DVT与PE比较,两者在10~29岁差异有统计学意义、70~89岁差异有统计学意义,具体原因需要近一步分析。在研究中,统计结果显示≥80岁患者DVT与PE的反而呈现下降的趋势,这种现象可能与年龄较大导致凝血系统的反应性下降有关[8],也可能因为年龄较大,病情较重虽然有发病但是未能就诊有关,但具体原因需要进一步分析。
3.3 危险因素分析
研究中手术、骨折、恶性肿瘤、静脉曲张、脑血管疾病、心脏病均为DVT的独立危险因素;下肢深静脉血栓、呼吸系统疾病、恶性肿瘤、感染、手术、心脏病、脑血管疾病均为PE的独立危险因素,与国外危险因素分析结果基本相同[9-10]。对国外相关文献进行研究,其中报道手术与骨折、关节的制动以及卧床被认为是DVT形成的独立危险因素[11],此结论与本研究结果相符。此外本研究中统计结果显示,感染因素在作为PE形成的独立危险因素,其中以肺感染最多见,Francesca Monn于2014年报道中表明感染与静脉血栓栓塞有一定关联,感染时间的长短与静脉血栓栓塞的发生率之间有明显的相关性。感染使深静脉血栓栓塞的风险在增加,这可能与炎症反应能激活多种细胞因子与炎症因子(包括VIII因子,CPR,组织因子,纤维蛋白原和IL-8的激活或增加有关)[12]。PE的形成与肺部感染因素明显相关,通过文献查阅国内未查到肺栓塞与感染因素相关性的报道,对于肺部感染引起肺栓塞可能与感染导致的脓毒性肺栓塞有关,国外近几年对脓毒性肺栓塞(Septic pulmonary embolism,SPE)的研究相对较多,而我国的相关报道较少可能由于目前对SPE诊断的定义仍不明确有关。若在临工作中,出现肺栓塞伴严重感染的患者,临床医生不仅要针对肺血栓栓塞进行治疗,同时也要分析其血栓形成的原因,进一步控制感染,通过研究的深入与进步,对于深静脉血栓与肺栓塞病因的预防与治疗将会成为治疗中的重点。
深静脉血栓与肺栓塞一直被认为是静脉血栓栓塞形成在不同时期的两种不同表现形式,本研究中通过对DVT与PE的危险因素分别进行分析得出下肢深静脉血栓确实是导致肺栓塞的主要危险因素,在以往的研究中此结论均得到证实,但是,针对于二者在危险因素上仍然存在着不同,例如本研究中感染与呼吸系统疾病是肺栓塞形成的独立危险因素,但是并不是深静脉血栓形成的独立危险因素,因此对DVT与PE 的临床特点与危险因素分别进行分析,有助于对我国人群危险因素的统计,将来随着临床研究的深入将引导未来预防指南的发展并降低DVT与PE的发病率。

