浓香型白酒蒸馏过程中挥发性风味物质的变化规律
张琦,沈才洪,孙啸涛,敖宗华,敖灵,郭凯,杨建刚,5
(1.四川理工学院生物工程学院,四川自贡 643000)(2.泸州老窖股份有限公司,四川泸州 646000)(3.国家固态酿造工程技术研究中心,四川泸州 646000)(4.北京工商大学食品学院,北京 100048)(5.酿酒生物技术及应用四川省重点实验室,四川自贡 643000)
中国白酒属于世界六大蒸馏酒之一,无论是在其生产技术上还是产品风格上,都具有独特的地位[1]。白酒按照香型可以分为四大香型:酱香型、浓香型、清香型和米香型[2]。其中浓香型白酒在我国市场上产量最大,根据国家统计局发布2016年我国白酒行业数据显示:1~12月全国规模以上白酒企业完成酿酒总产量1358.36万千升。而白酒产量位居前三的地区分别是:四川省位居全国第一,白酒年产量402.67万千升,其中泸州老窖为代表实现销量17.79万千升;河南省位居全国第二,白酒年产量117.50万千升;山东省位居全国第三,白酒年产量112.64万千升。近年来,虽然浓香型、酱香型和清香型白酒都有较快增长,但浓香型白酒优势更明显,一直占据白酒消费市场约70%左右的份额。
浓香型白酒是原料经与大曲发酵、蒸馏而获得的含有其他风味物质的乙醇水合物,由水、乙醇和微量的风味物质组成[3]。而浓香型白酒在蒸馏过程中,各种风味物质由于其化学特性的不同,导致其在蒸馏过程中的馏出特性和蒸馏结束后的残留量不同[4]。同时在蒸馏过程中由于热化学反应,某些风味物质发生热分解或重组形成新的风味物质[5]。虽然这些风味物质含量极少,但对酒质却有极大的影响。目前,对于浓香型白酒风味化合物的检测方法主要有:液液萃取[6]、固相萃取(solid phase extraction,SPE)[7]、吹扫捕集[8]、固相微萃取(solid phase microextraction,SPME)[9]等,李贺贺等[10]采用顶空固相微萃取和搅拌棒吸附萃取技术分析古井贡酒中香气成分,共定性出190种化合物,其中用标准品准确定性143种。胡格等[11]分析3种不同发酵期基酒在贮存过程中主要酸、醛、醇以及酯含量的变化情况。李学思等[12]利用 GB/T 10345-2007标准分析浓香型白酒蒸馏过程不同馏分酒中风味物质的变化规律,其中在蒸馏过程中总酯随酒精度的降低呈“下降-平衡-上升-下降”趋势。影响白酒风味的因素有原辅料、糖化发酵剂、生产工艺和蒸馏过程等。本实验主要就蒸馏过程中不同窖池酒醅蒸馏出的馏分酒风味物质变化进行探讨。
本研究利用直接进样法,样品前处理简单,避免样品处理中微量成分的损失,具重现性好、检测准确性高的优点[13,14],结合GC-MS测定100年和300年窖龄酒醅蒸馏过程中馏分酒的挥发性物质,得到浓香型馏分酒的挥发性风味物质。因此,本文建立了直接进样结合气相色谱-质谱对浓香型白酒蒸馏过程中主要挥发性物质变化规律的快速检测方法,并系统分析了100年和300年窖池蒸馏过程中馏分酒的含量变化规律。初步阐释了不同窖龄馏分酒中风味物质的含量差异,发掘了不同馏分酒蒸馏过程中风味物质含量与流酒时间之间的关系,该工作为酒企科学蒸馏、质量摘酒和分级贮存提供了科学数据。
1 材料和方法
1.1 材料
1.1.1 原料与试剂
本研究蒸酒所用酒醅来源于原窖法工艺的100年和300年不同窖龄窖池酒醅,利用甑桶固态蒸馏。在酒企生产过程中进行实时采样,采样频率为:2 min取一个酒样,编号分别为:A-1-1、A-1-2、A-1-3、A-1-4、A-1-5、A-1-6、A-1-7、A-1-8、A-1-9、A-1-10、A-1-11、A-1-12、A-1-13、A-1-14、A-1-15、A-1-16、A-1-17是 100年馏分酒(其中A-1-1为酒头,即 1段酒;A-1-2~A-1-7为2段酒;A-1-8为3段酒;A-1-9~A-1-17为酒尾,即4段酒);编号为:A-3-1、A-3-2、A-3-3、A-3-4、A-3-5、A-3-6、A-3-7、A-3-8、A-3-9、A-3-10、A-3-11、A-3-12、A-3-13、A-3-14、A-3-15、A-3-16、A-3-17是300年的馏分酒(其中A-3-1为酒头,即1段酒;A-3-2~A-3-7为 2段酒;A-3-8为 3段酒;A-3-9~A-3-17为酒尾,即4段酒),摘酒时间为32 min,每个酒样取200 mL。
标准品:乙酸乙酯、丁酸乙酯、异丁醇、乙酸异戊酯、戊酸乙酯、正丁醇、丁酸丁酯、2-甲基丁醇、异戊醇、己酸乙酯、戊醇、乳酸乙酯、己醇、己酸丁酯、丁酸己酯、辛酸乙酯、乙酸、壬酸乙酯、辛醇、2,3-丁二醇、丙二醇、丁酸、苯乙酸乙酯、己酸、十四酸乙酯、棕榈酸乙酯、油酸乙酯、亚油酸乙酯和戊酸乙酯购于日本东京化成工业株式会社(TCI);正构烷烃(C7~C30,色谱纯)购于美国Accustandard公司;2-羟基-4-甲基戊酸乙酯购买于百灵威科技有限公司;无水乙醇(色谱纯)购买于天津市光复科技发展有限公司;10000 mg/L 4-辛醇购买于上海安谱有限公司。
1.1.2 仪器
7890B气相色谱和7890A-5975C MSD质谱联用仪(GC-MS)美国Agilent科技有限公司生产。
1.2 实验方法
1.2.1 直接进样
分别取上述34种酒样各980 µL加入20 µL 4-辛醇作为内标物于进样小瓶中,混匀、直接通过气相色谱-质谱法(GC-MS)进样分析。
1.2.2 标准溶液的配置
取适量体积质量浓度的标准溶液,用无水乙醇(色谱纯)稀释至质量浓度分别为5000 mg/L乙酸乙酯、2000 mg/L丁酸乙酯、500 mg/L异丁醇、100 mg/L乙酸异戊酯、500 mg/L戊酸乙酯、500 mg/L正丁醇、100 mg/L丁酸丁酯、100 mg/L 2-甲基丁醇、1000 mg/L异戊醇、4000 mg/L己酸乙酯、100 mg/L乙酸己酯、100 mg/L己酸丙酯、200 mg/L庚酸乙酯、100 mg/L戊醇、9000 mg/L乳酸乙酯、100 mg/L己醇、100 mg/L己酸丁酯、100 mg/L丁酸己酯、200 mg/L辛酸乙酯、9000 mg/L乙酸、100 mg/L壬酸乙酯、100 mg/L 2-羟基-4-甲基戊酸乙酯、100 mg/L辛醇、100 mg/L 2,3-丁二醇、200 mg/L丙二醇、9000 mg/L丁酸、200 mg/L苯乙酸乙酯、500 mg/L己酸、100 mg/L十四酸乙酯、100 mg/L棕榈酸乙酯、100 mg/L油酸乙酯、100 mg/L亚油酸乙酯的混合标准溶液,然后取一定量的体积质量浓度混合标准溶液分别进行0倍、2倍、5倍、10倍、20倍、80倍、100倍、200倍、400倍、800倍和1000倍、10000倍、50000倍和100000倍梯度稀释,制备系列标准工作溶液,将标准溶液储存于-4 ℃备用。
1.2.3 色谱条件
色谱柱:DB-FFAP(40 ℃~250 ℃)毛细管柱(60 m×250 µm×0.25 µm);载气He(99.999%);恒流:柱流速1.0 mL/min;分流比3:1;进样量:1 µL;进样口温度:250 ℃;升温程序:初始温度40 ℃,保持0.5 min;以10 ℃/min升至50 ℃,保持8 min;以3 ℃/min升至70 ℃,保持5 min;以3 ℃/min升至187 ℃,保持1 min;以5 ℃/min升至230 ℃,保持4 min,总时间为73.767 min。
1.2.4 质谱条件
电子电离源:电子轰击(EI)源;电子能量70 eV;离子源温度230 ℃;四级杆温度150 ℃;传输线温度:250 ℃。定性采用全扫描模式(full scan);扫描质量范围:50~500m/z;定量采用选择离子扫描模式(SIM),选择离子对。调谐文件为标准调谐。
1.2.5 定性定量方法
采用NIST11谱库检索、标准品比对,并结合保留指数进行定性。
标准品比对:在同样的色谱条件下,分析酒样和标准品,若两张色谱图所对应谱峰的保留时间和特征离子峰相同,可确定为同一个化合物。
NIST11谱库检索:首先将谱图进行本底扣除,然后根据有机质谱裂分规律进行谱库检索。一般认为,相似度>90%表明与标准谱图的匹配得很好,相似度>80%~90%表明与标准谱图的匹配得较好,相似度>70%~80%表明与标准谱图的匹配可行,相似度<60%表明与标准谱图的匹配得不好。
保留指数(retention index,RI)定性:将C7-C30正构烷烃作为标准物,在与酒样相同的色谱条件下进样分析,通过保留时间直接可计算保留指数,计算公式如(1)所示:
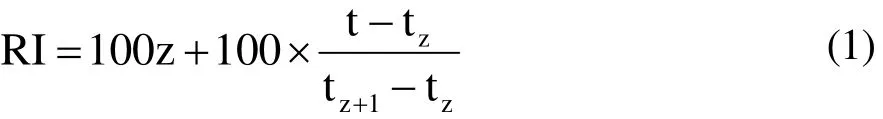
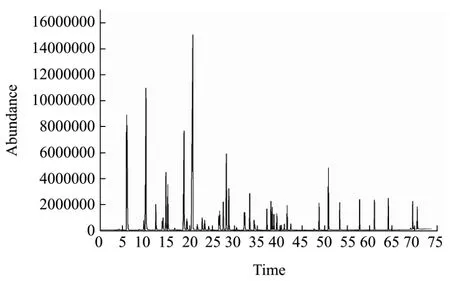
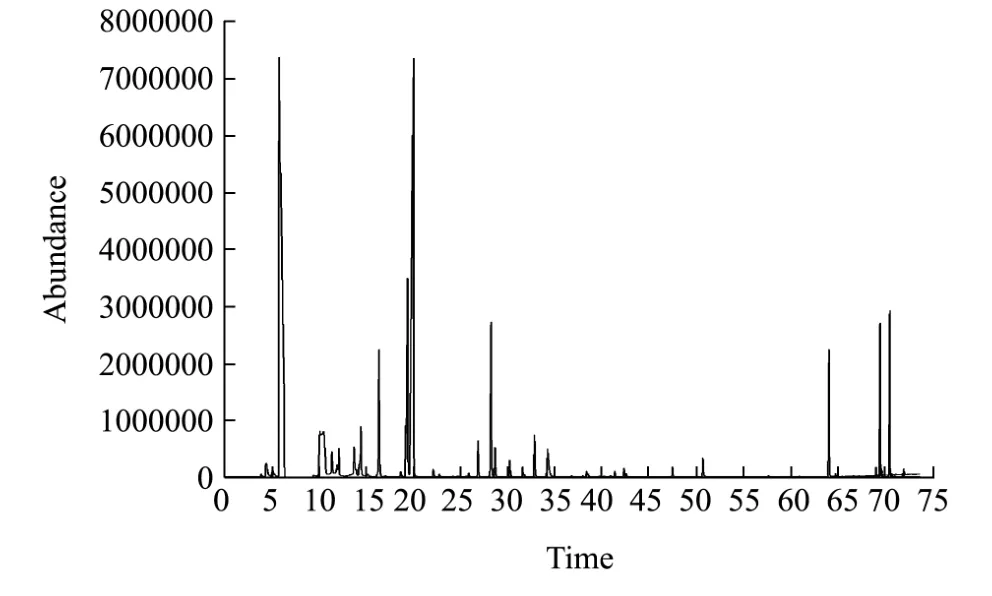
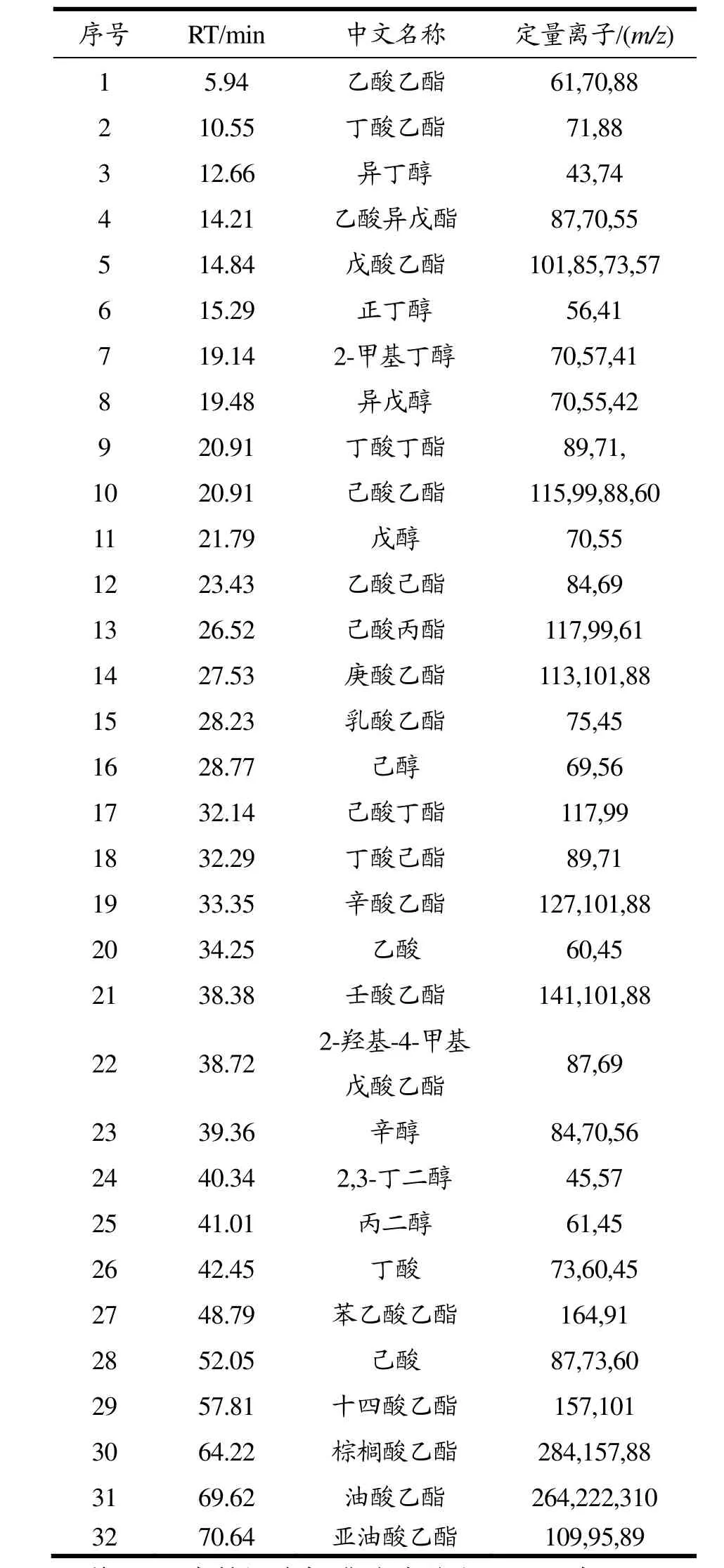
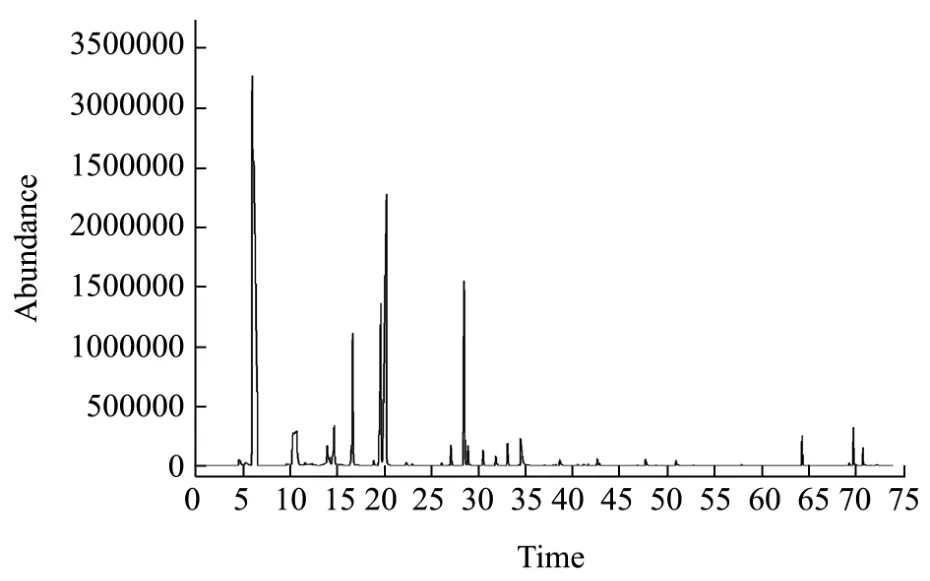
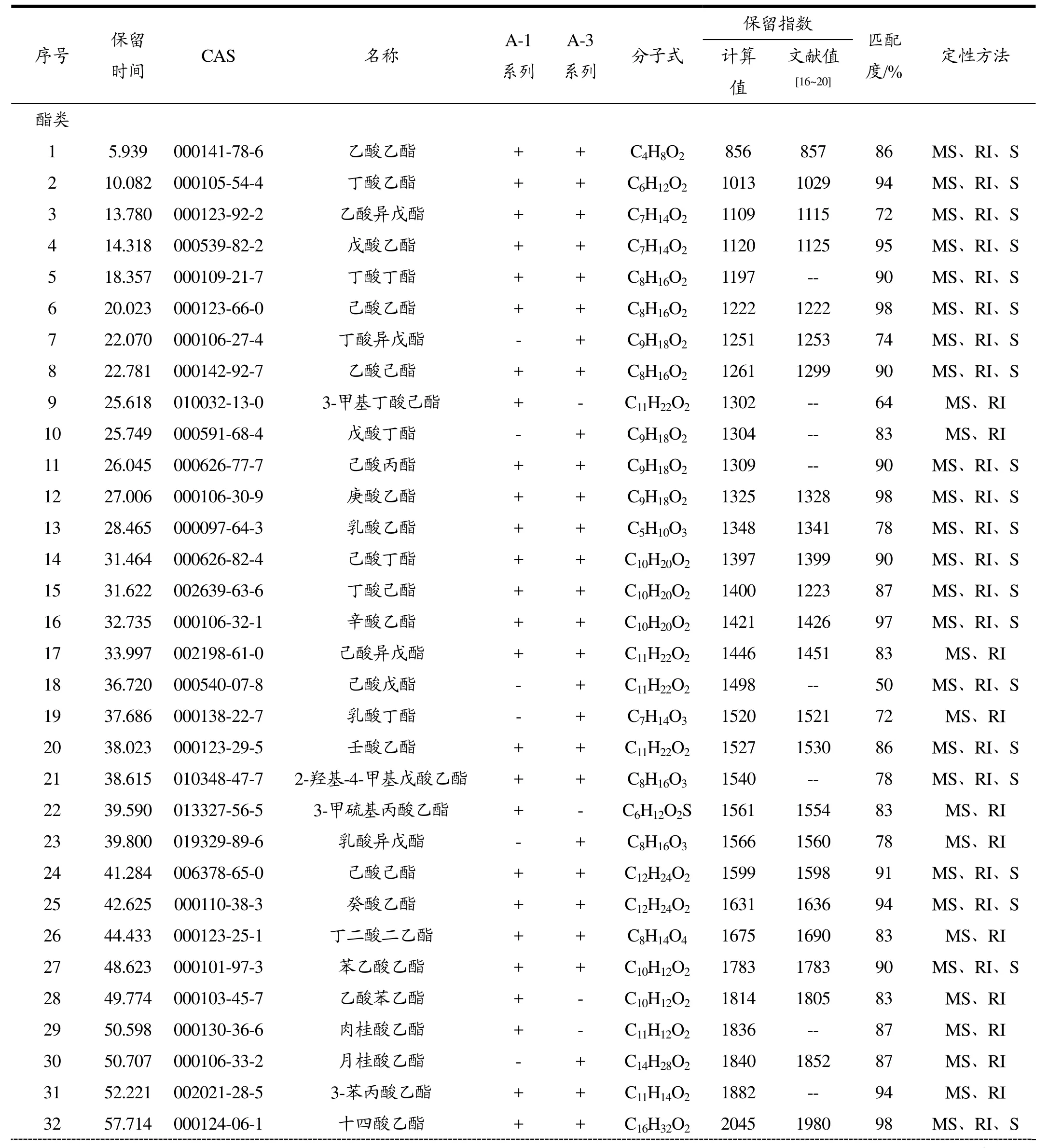
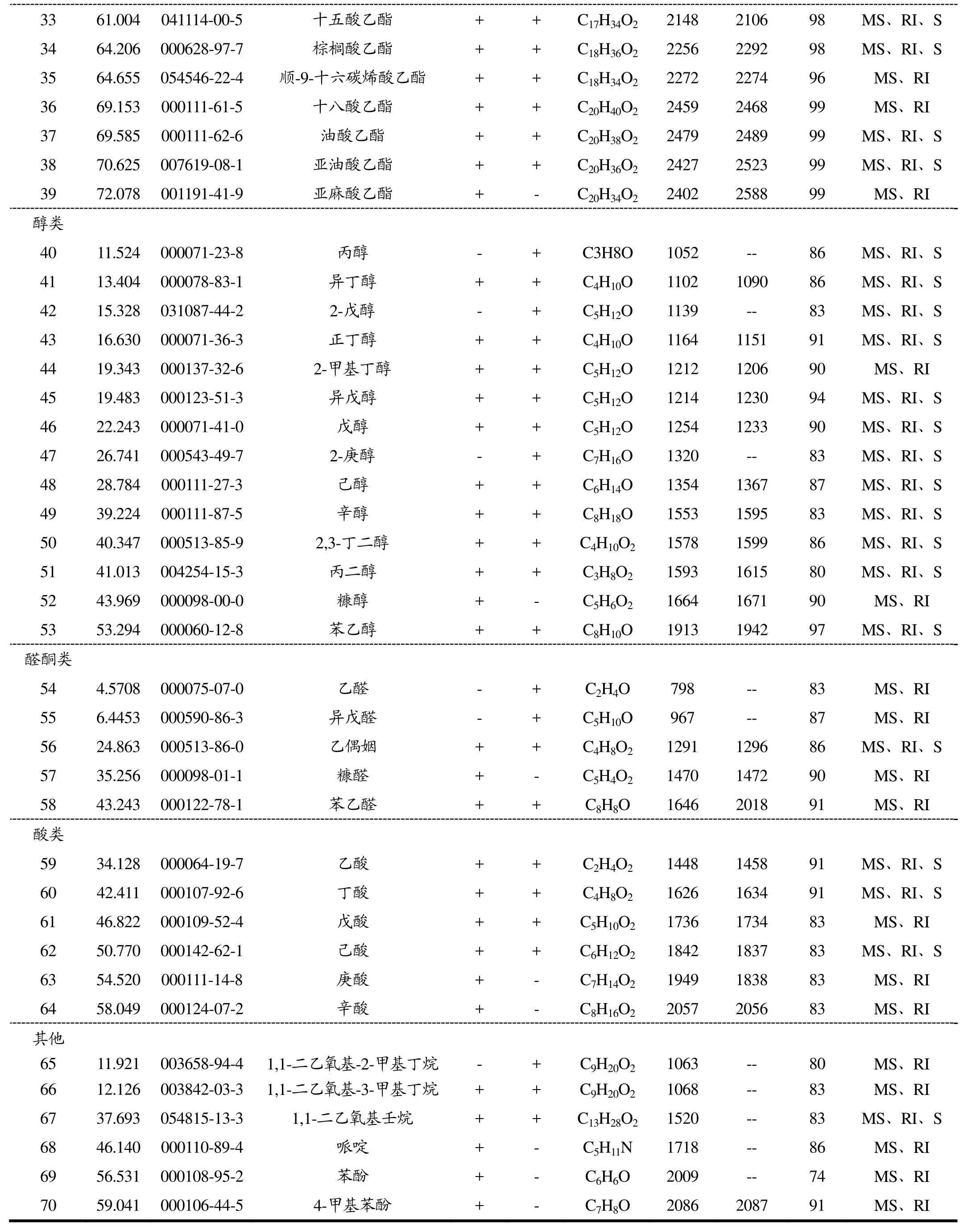
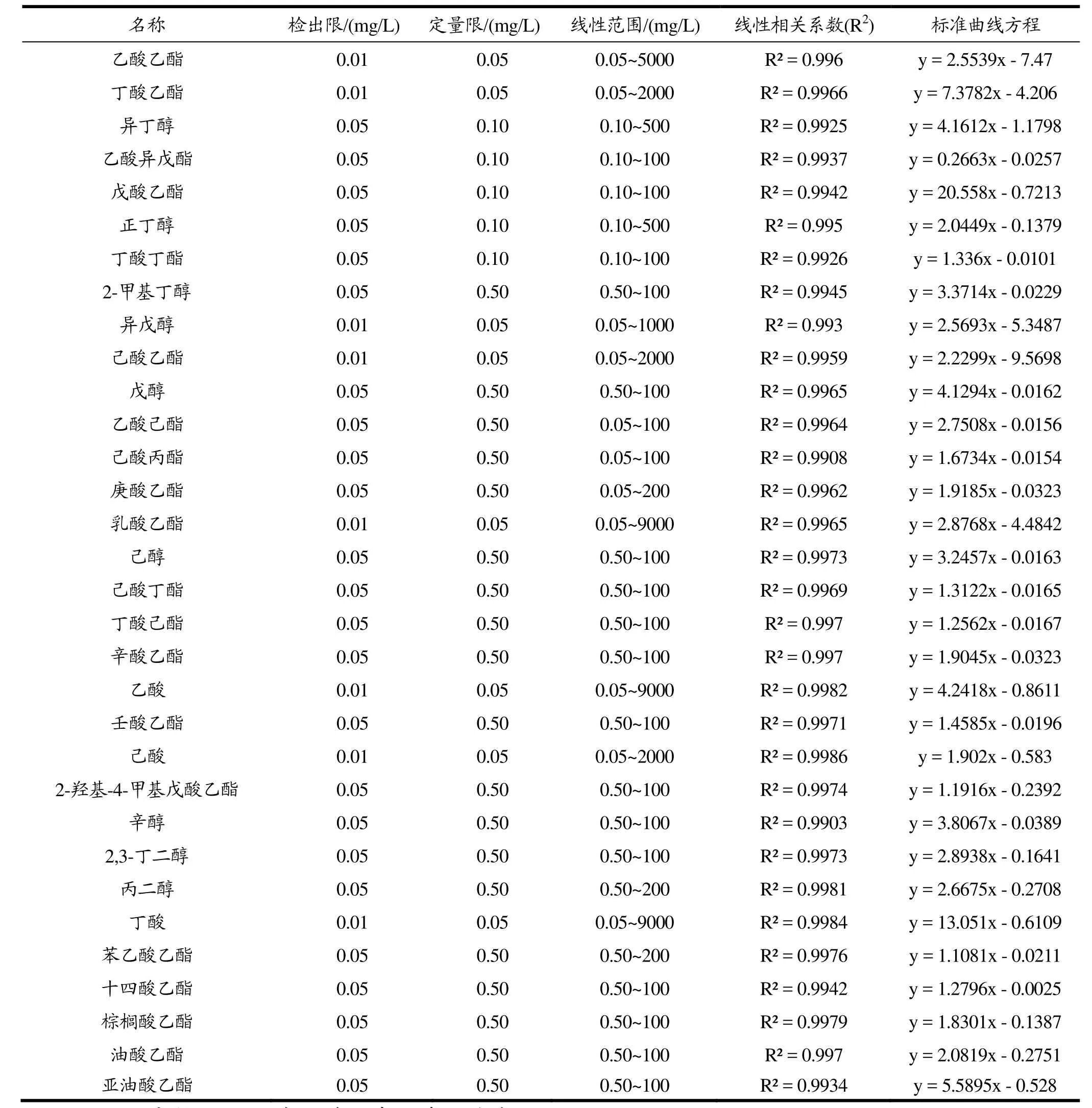
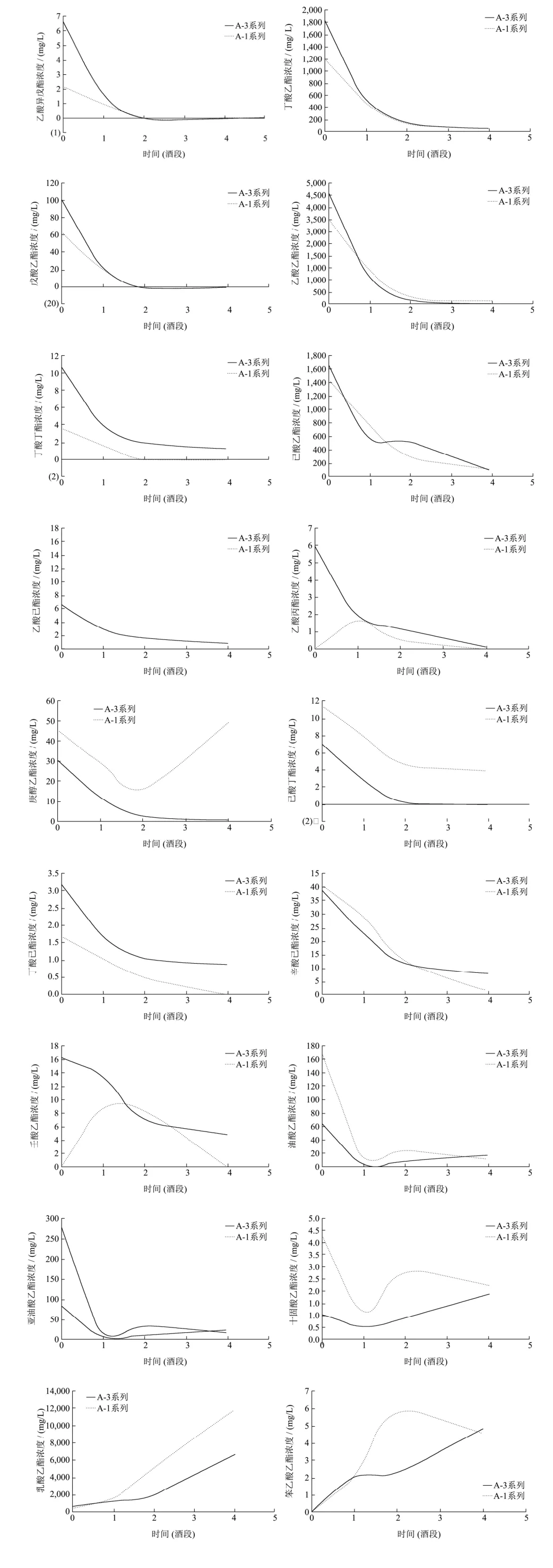
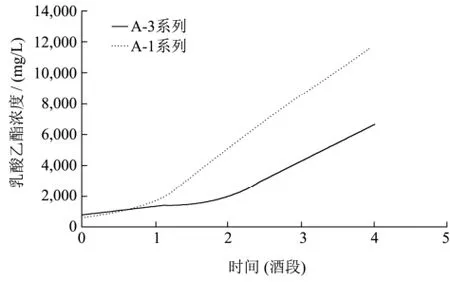
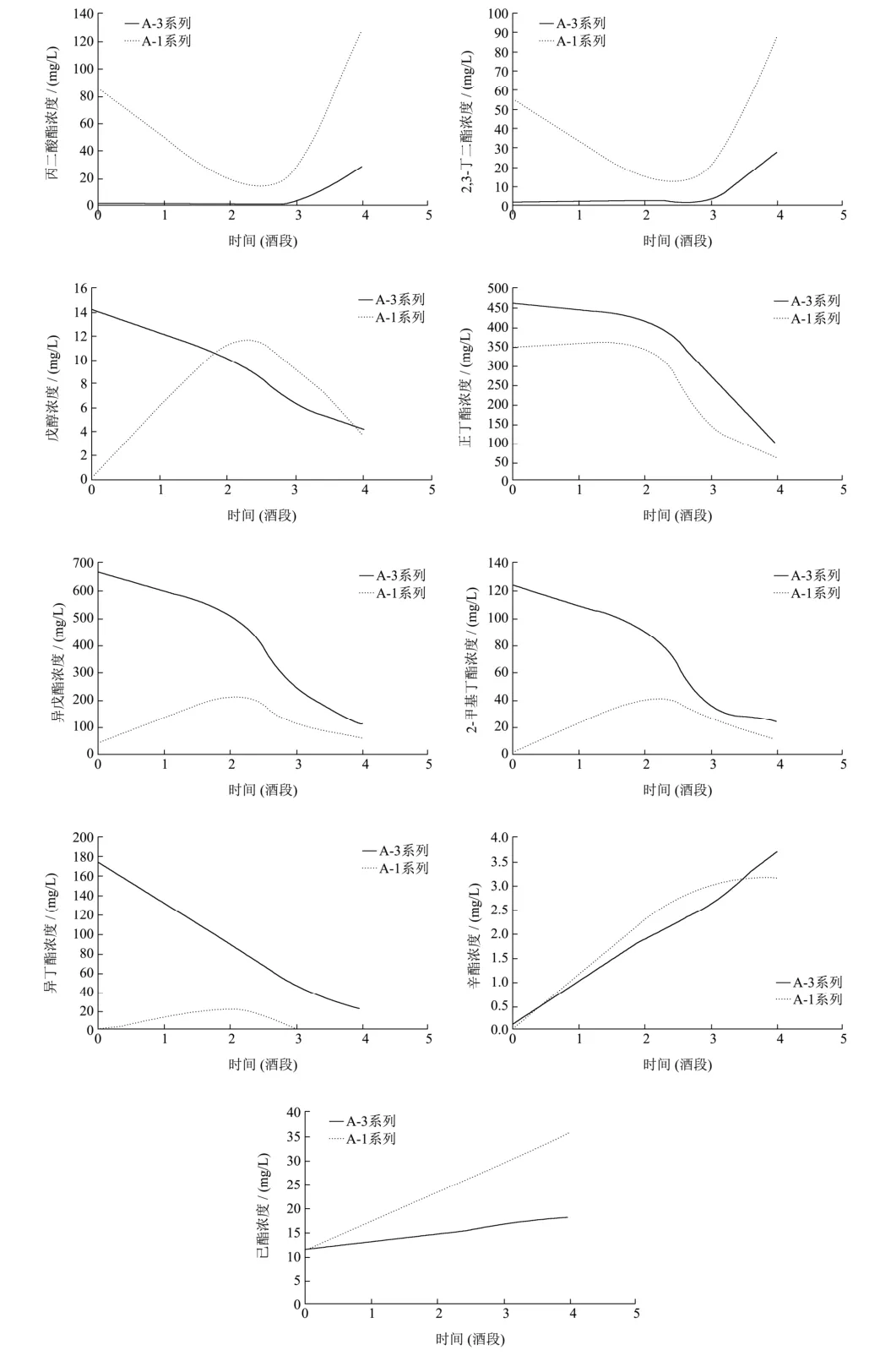
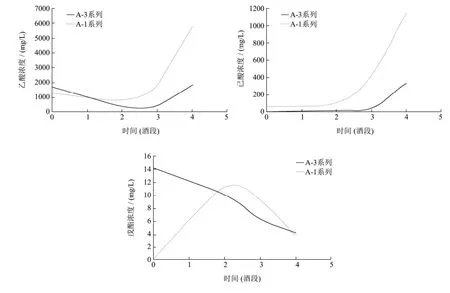
式中:RI为保留指数;z和z+1分别为未知物流出前后正构烷烃碳原子数,tz和tz+1分别为相应正构烷烃的保留时间;t为未知物在气相色谱中的保留时间(tz 采用内标法进行定量分析,以待定量物质的质量浓度与对应内标物质质量浓度之比为横坐标,以待定量物质的峰面积与样品中该物质峰面积之差与内标物质峰面积之比为纵坐标建立标准曲线,计算不同窖龄窖池酒醅蒸馏过程中馏分酒挥发性成分的含量。 将 1.2.2中所稀释不同倍数的体积质量浓度混合标准溶液分别进行GC-MS分析,以物质质量浓度/内标质量浓度-物质峰面积/内标峰面积进行线性回归,绘制标准曲线;将色谱峰信噪比(S/N)大于3的质量浓度确定为检出限,信噪比(S/N)大于10确定为定量限。 图1 32种混合标准品的典型TIC图Fig.1 Typical TIC diagram of 32 mixed standards 图2 白酒样中的典型TIC图Fig.2 Typical TIC diagram of baijiu samples 表1 32种挥发性成分的SIM参数Table 1 SIM parameters of 32 volatile components 将1.2.2中的混合标准溶液移取980 µL加入20 µL 10000 mg/L的4-辛醇作为内标,按照1.2.3和1.2.4的方法进行全扫描分析,其总离子流色谱图(TIC)如图1所示,图2为酒样的典型TIC图,经NIST谱库检索,结合混合标准溶液的总离子流色谱图保留时间,最终确定以下物质的保留时间。以下化合物在色谱中的保留时间、定性定量离子如表1所示。图3所示为酒样中的典型SIM图,可以达到基线分离。 图3 酒样中的典型SIM图Fig.3 Typical SIM chromatogram of baijiu samples 用色谱乙醇将配置的混合标准溶液进行 0倍、2倍、5倍、10倍、20倍、80倍、100倍、200倍、400倍、800倍和1000倍、10000倍、50000倍和100000倍梯度稀释,制备系列标准工作溶液,进行 GC-MS分析,以质量浓度-峰面积进行线性回归,绘制标准曲线,结果如表2所示。每种挥发性风味化合物在各自的线性范围内,线性关系均大于0.99,线性关系良好。同时,将信噪比大于3确定为检出限(LODm);信噪比大于10确定为定量限(LOQm),32种挥发性风味化合物的LODm和LOQm如表2所示。 2.3.1 不同窖龄馏分酒风味物质分析结果 采用直接进样法结合GC-MS技术对不同窖龄馏分酒(A-1、A-3系列)进行分析,共检测到70种化合物,包括酯类39种,醇类14种,酸类6种、烷烃类3种,醛酮类5种,其他3种。其中用标准品准确定性41种化合物。结果如表3所示。 由表3可见浓香型白酒的两个不同窖龄(A-1系列和A-3系列)的馏分酒中共有挥发性风味化合物46种,占全部检出风味物质的66.7%,其中酯类28种,占全部检出风味物质的40.6%;醇类10种,占全部检出风味物质的14.5%;酸类4种,占全部检出风味物质的5.8%;醛酮类2种,占全部检出风味物质的2.9%;其他2种,占全部检出风味物质的2.9%。在这些挥发性风味物质中,酯类和醇类为主要的挥发性化合物。在A-1系列的挥发性风味物质成分中检出12种不同的挥发性风味物质化合物,包括酯类5种,分别为3-甲基丁酸乙酯、3-甲硫基丙酸乙酯、乙酸苯乙酯、肉桂酸乙酯、亚麻酸乙酯;醇醛类2种,分别为糠醇和糠醛;酸类挥发性化合物为庚酸和辛酸2种;其他类有3种,分别为哌啶、苯酚和4-甲基苯酚。而A-3系列中的挥发性风味物质成分检出11种不同的化合物,包括酯类5种,分别为丁酸异戊酯、己酸戊酯、乳酸丁酯、乳酸异戊酯和月桂酸乙酯;醇类3种,为丙醇、2-戊醇和2-庚醇;醛类物质有2种,乙醛和异戊醛;其他类1种,为1,1-二乙氧基-2-甲基丁烷。酯类化合物是检测出来化合物中最多的一类化合物,占全部检出风味物质的56.5%。 同时由表3得出酯类物质和醇类物质是浓香型白酒固态发酵蒸馏酒中最重要的挥发性风味物质成分,给酒体提供了怡人的香气,使酒体变得清甜醇香、舒适优雅。 表2 32种挥发性化合物的线性方程、线性范围、相关系数、检出限和定量限Table 2 Linear equation, linear range, correlation coefficient, LODm and LOQm of 32 volatile compounds 注:+表示有,-表示无;--表示未见文献报道;MS采用NIST谱库检索定性;RI采用保留指数法定性;S采用标准品定性。 表3 不同窖龄馏分酒挥发性风味物质成分GC-MS鉴定结果Table 3 GC-MS identification of volatile flavor compounds in different pit ages 2.3.2 不同窖龄馏分酒蒸馏过程中酯类化合物含量的变化规律 采用直接进样结合GC-MS联用技术方法定量分析了不同窖龄的馏分酒在蒸馏过程中酯类的含量变化情况,结果见图4。 比较同一种酯在同一窖龄不同时间段下馏分酒中的含量和同一种酯类在不同窖龄相同蒸馏时间下馏分酒中的含量变化,容易发现,在分析所有酯类化合物中,它们的含量均跟馏分酒时间和窖龄密切相关。 从上述图中可以看出,窖龄不同(实线为A-3系列和虚线为A-1系列,下同)的馏分酒,其丁酸乙酯、乙酸异戊酯、乙酸乙酯和戊酸乙酯在二段、三段酒和酒尾含量稳定且相差不大,但是对于酒头而言,其含量变化较大。丁酸乙酯、乙酸异戊酯和戊酸乙酯含量在整个蒸馏过程中窖龄为A-3系列的馏分酒均大于窖龄为A-1系列的馏分酒。 图4 窖龄A-1系列与窖龄A-3系列不同蒸馏阶段馏分中酯类含量的比较Fig.4 Comparison of esters content in different distillated fractions between A-1 and A-3 图4显示了丁酸丁酯、己酸乙酯、乙酸己酯、己酸丙酯、庚酸乙酯、己酸丁酯、丁酸己酯、辛酸乙酯、壬酸乙酯、棕榈酸乙酯、油酸乙酯、亚油酸乙酯、十四酸乙酯、2-羟基-4-甲基戊酸乙酯、苯乙酸乙酯和乳酸乙酯在蒸馏过程中的含量变化情况: ①丁酸丁酯、己酸丁酯和丁酸己酯的含量在同一窖龄不同时间是逐渐降低,丁酸丁酯和丁酸己酯在相同时间不同窖龄下的含量A-3系列均大于A-1系列,己酸丁酯含量A-3系列小于A-1系列; ②己酸丙酯和壬酸乙酯含量在A-3系列中随着时间的变化依次降低,而在A-1系列中含量是先增加到二段酒,达到最大值,然后依次减少,从整体来看A-3系列的含量除在三段的时间内小于A-1系列,其它时间里均大于A-1系列; ③庚酸乙酯、十四酸乙酯、棕榈酸乙酯、油酸乙酯和亚油酸乙酯波动较大,含量A-1系列大于A-3系列; ④己酸乙酯和辛酸乙酯含量呈下降趋势,己酸乙酯含量在1段含量刚开始由A-3系列大于A-1系列到随着时间的变化变为A-1系列大于A-3系列,2段时间内基本稳定,3段和酒尾又逐渐降低,但从2段后半时间开始A-3系列大于A-1系列; ⑤2-羟基-4-甲基戊酸乙酯、苯乙酸乙酯和乳酸乙酯含量随着时间的变化呈上升趋势,A-1系列大于A-3系列。 另外,值得注意的一点是,比较同一种酯在不同窖龄中其含量波动较大,窖龄越大的馏分酒在蒸馏过程中波动弧度较为稳定,这在十四酸乙酯含量变化曲线中可以明显看出。在四大酯中己酸乙酯、乙酸乙酯和丁酸乙酯属于醇溶性,均表现出了与特性相符的溜出趋势,即含量趋于下降。而乳酸乙酯表现出不同的馏出特性,随着酒精度下降的变化,乳酸乙酯的含量逐渐上升,这是由乳酸乙酯的特性所决定的。乳酸乙酯同时具有羟基和羧基,难以挥发,而且是水溶性的,因此含量是逐渐增加的,这与张鹏[21]等人在研究浓香型大曲白酒蒸馏过程中四大酯馏出特性分析时,也得出了类似结果。 2.3.3 不同窖龄馏分酒蒸馏过程中醇类化合物含量的变化规律 定量分析了两个不同窖龄(A-3系列和A-1系列)馏分酒在蒸馏过程中醇类物质的变化情况,结果见图5。比较同一种醇,同一蒸馏时间在不同窖龄馏分酒样和同一窖池酒醅蒸馏的不同时间段馏分酒酒样中的含量,可以得出,在分析的9种醇中含量变化规律如下: 图5 窖龄A-1系列与窖龄A-3系列不同蒸馏阶段馏分中醇类含量的比较Fig.5 Comparison of alcohol content in different distillated fractions between A-1 and A-3 从图5可以看出: ①在蒸馏过程中,风味化合物丙二醇和 2,3-丁二醇含量变化趋势相似,A-3系列均呈上升趋势,而A-1系列呈现出先下降后上升,在3段酒中达到含量最低的变化趋势。从整体来看A-1系列各个时间段的含量均大于A-3系列各时间段的含量; ②图3中A-3系列戊醇含量逐渐降低,A-1系列中呈现先上升后降低的趋势,含量在3段馏分酒中达到最大值。在同一时间不同窖龄中,A-3系列在酒头和2段馏分酒酒样中的含量大于A-1系列,2段后变化为A-1系列中的含大于A-3系列中的含量。 ③含量上升的醇类:各酒样辛醇和己醇的含量随蒸馏的时间呈逐渐上升的趋势,在同一时间不同窖龄中A-1系列中己醇的含量均大于A-3系列,而辛醇在刚开始出酒和出酒结束的两个时间点中A-3系列中的含量大于A-1系列的含量。 ④含量下降的醇类:各酒样正丁醇的含量随蒸馏时间呈现下降的趋势,在不同的窖龄中含量A-3系列均大于A-1系列; ⑤异戊醇、2-甲基丁醇和异丁醇在A-3系列酒样中含量均逐渐降低,而在A-1系列酒样中均是先上升后下降的趋势变化,都在2段馏分酒中含量达到最大值;从不同窖龄上来看,A-3系列含量均大于A-1系列。 从上面的分析可以看出,醇类含量的变化因窖龄不同和蒸馏时间的变化而存在差异。 2.3.4 不同窖龄馏分酒蒸馏过程中酸类化合物含量的变化规律 定量分析了两个不同窖龄(A-3系列和A-1系列)馏分酒在蒸馏过程中醇类物质的变化情况,结果见图6。比较同一种酸,在同一蒸馏时间不同窖龄馏分酒蒸馏过程中酒样和同一窖龄不同时间馏分酒蒸馏过程中酒样的含量,可以得出,在分析的3种酸中含量变化来看,虽然蒸馏的时间不同,但丁酸和己酸的含量在不同窖龄中的变化趋势却是大致相同的与酒样的时间无关。 图6 窖龄A-1系列与窖龄A-3系列不同蒸馏阶段馏分中酸类含量的比较Fig.6 Comparison of acids content in different distillated fractions between A-1 and A-3从图6可以看出: ①在蒸馏过程中乙酸含量呈现先降后上升的变化趋势,在同一时间不同窖龄下,A-3系列酒头乙酸的含量均大于A-1系列,之后A-1系列乙酸的含量在2段、3段和酒尾中均大于A-3系列; ②含量上升的酸类:各酒样丁酸和己酸的含量随着蒸馏时间的变化呈逐渐上升的趋势,从不同窖龄的角度来看,在 A-1系列中丁酸和己酸的含量均大于A-3系列。 风味物质的馏出规律与其在乙醇或水中的溶解性密切相关,随蒸馏过程进行,水溶性物质乙酸、丁酸和己酸的浓度逐渐增加,这与李海龙[22]人研究水溶性物质的浓度随加热蒸汽量的变化与乙醇变化规律相反的结果一致。 本研究通过分析两种不同窖龄酒醅在蒸馏过程中馏分酒的酯类、醇类和酸类的含量变化。结果表明,浓香型馏分酒在蒸馏过程中不同时间段酸类、醇类和酯类的含量变化趋势很明显,在不同窖龄相同时间下含量差异较大。具体来讲,不同窖龄馏分酒在蒸馏过程中存在如下变化: 3.1 酯类物质在不同窖龄酒醅蒸馏过程馏分酒中的己酸乙酯、乙酸乙酯和丁酸乙酯的含量均是逐渐呈下降的变化趋势,酒尾达到最低,在100年窖池酒醅蒸馏过程中馏分酒中己酸乙酯在酒尾的含量为 111.99mg/L,在300年窖池酒醅蒸馏过程中馏分酒中己酸乙酯在酒尾的含量为97.56 mg/L。而乳酸乙酯的含量逐渐上升,在酒尾所占比例较大。 3.2 对不同窖龄酒醅蒸馏过程馏分酒中的乙酸、丁酸和己酸含量进行了跟踪检测。结果表明,蒸馏过程中丁酸和己酸的含量均呈逐渐上升的趋势,在100年窖池酒醅蒸馏过程中馏分酒含量在酒头最低,丁酸为418.56 mg/L,己酸的含量为60.86 mg/L;在300年窖池酒醅蒸馏过程中丁酸的含量为100.96 mg/L,己酸的含量为4.00 mg/L。乙酸在刚开始出酒时的含量较大,随着酒度的降低呈先下降后上升的趋势,在100年和300年窖池酒醅蒸馏中乙酸的含量在二段时达到最低,含量分别为831.87 mg/L和431.05 mg/L。从整体的酸类物质含量变化来看均呈现出上升的趋势,总酸有较大幅度的增加,并且越靠后的酒段增加就越明显。通过本次研究还得出窖龄较大的馏分酒其酸类含量较低。这与李俊刚[23]等在研究对不同窖龄下浓香型白酒风味物质的研究时,也得出了类似的结果。 3.3 醇类物质在不同窖龄酒醅蒸馏过程中的变化情况,辛醇和己醇含量在蒸馏过程中逐渐上升,但是辛醇、己醇、丙二醇和 2,3-丁二醇含量随着窖龄的含量增加反而降低;正丁醇、异戊醇、2-甲基丁醇和异丁醇含量随着窖龄的增加而增加。 在不同窖龄馏分酒蒸馏过程中,随着窖龄的增加,窖泥微生物数量的增加,酒体挥发性物质中酯类化合物种类增多,挥发性组分的相对含量也有明显的变化,而随着窖池窖龄的减少其波动性越大。掌握白酒蒸馏过程中风味物质的变化规律,在酿造中根据蒸馏时间以及乙醇浓度适时摘酒,对提高白酒品质有着重要意义。2 结果与讨论
2.1 GC-MS选择离子扫描参数(SIM)的确定
2.2 检出限、定量限和标准曲线的考察
2.3 定性分析结果
3 结论

