2,4-表油菜素内酯和赤霉素对微拟球藻产油率及脂肪酸组成的影响
凌婷 杨树萍 魏煜凡 张琳
(宁波大学海洋学院,宁波 315211)
改变微藻的培养条件(如氮磷硅等营养成分、pH、温度、光强等)既可调控微藻的脂肪酸组成,又可调控微藻的总脂含量[1-4]。添加植物生长调节剂也是其中一种有效手段。据报道,2,4-表油菜素内酯(2,4-Epibrassinosteroid,EBR)、赤霉素(Gibberellin A3,GA3)、吲哚乙酸(Indole-3-acetic acid,IAA)、水杨酸(Salicylic acid,SA)等植物生长调节剂对促进微藻生长、优化脂肪酸组成、增加抗逆性等有显著功效[5]。该结论在小球藻(Chlorella sp.)、球等鞭金藻(Isochrysis galbana)等微藻中得以印证[6]。微拟球藻(Nannochloropsis sp.),属于真眼点藻纲(Eustigmatophyceae),是一类具有巨大开发潜力的经济微藻。其富含多糖、蛋白和多不饱和脂肪酸(PUFAs)等高附加值产物,被广泛用作水产饵料及心脏病、糖尿病等疾病的预防[7]。此外,微拟球藻油脂含量高,被视为最有发展前景的生物柴油原材料之一[8]。
目前,植物生长调节剂对微拟球藻产油率及脂肪酸组成影响的研究较少,本实验着重分析了EBR、GA3对微拟球藻大洋种(Nannochloropsis oceanica)生长、产油率和脂肪酸组成的影响,拟找出最适浓度,为微拟球藻的研究和应用提供借鉴。
1 材料与方法
1.1 材料
微拟球藻藻种编号为N. oceanica LAMB0001,由中国海洋大学应用微藻生物学实验室提供。培养基选用f/2海水培养基[9]。培养温度(24±1)℃,光 周 期(L∶D)12 h∶12 h, 光 照 强 度 60 μmol photons/(m2·s)。每天固定时间摇瓶4次,防止细胞贴壁。EBR和GA3购自美国Sigma公司,使用微孔膜过滤除菌配制成母液,低温保存。
1.2 方法
1.2.1 实验流程 将微拟球藻培养至指数生长中期,分别取60 mL接种于新鲜f/2培养基中至总体积300mL,并分别添加EBR和GA3至相应的终浓度。EBR和GA3分别设置4个浓度梯度0、5、15和50 mg/L,每个浓度设置3个平行。培养10 d,收集细胞,测定干重、脂肪酸组成及总脂含量。期间,每天监测藻液光密度变化。
1.2.2 光密度及干重测定 光密度测定方法:本实验使用750 nm波长下藻液的吸光度来表示藻液光密度。光密度值代表细胞密度。干重测定方法:离心收集一定体积的藻液,冷冻干燥后称取藻粉重量。
1.2.3 总脂含量测定分析 取30 mg冷冻干燥的藻粉至密封性良好的螺口玻璃管中,加入氯仿-甲醇(体积比2∶1)剧烈震荡15 min,离心(4 000 r/min,10 min)后吸取上清液至新的螺口玻璃管中。重复抽提3次。向装有上清液的玻璃管中加入适量NaCl溶液(0.9%),充分震荡混匀,静置30 min。吸取下层有机相至新玻璃管中,50℃水浴待氯仿全部挥发,称重并计算总脂含量。
1.2.4 脂肪酸组成测定分析 取20 mg冷冻干燥的藻粉置于密封性良好的螺口玻璃管中,加入2 mL KOH-CH3OH溶液(2 mol/L)于75℃水浴锅中皂化和甲酯化30 min;冷却至室温后加入2 mL HCl-CH3OH溶液(3 mol/L),75℃水浴酸化30 min;冷却后再加入1 mL色谱级正己烷和适量蒸馏水,充分震荡促进分层;吸取正己烷相待测。
脂肪酸组成分析:采用Agilent 6890 Series GC System 气相色谱仪(US10251016,USA),色谱柱为 HP-5毛 细 管 柱(30 m×320 μm×0.25 μm,5%Phenyl Siloxane),检测器为氢火焰离子化检测器(FID)。使用安捷伦化学工作站数据处理系统(Agilent Chemsation)分析结果,以面积归一化法计算脂肪酸组分的相对百分含量。
2 结果
2.1 EBR和GA3对生长的影响
添加不同浓度EBR的微拟球藻生长状况如图1所示。曲线使用Origin 7.0软件非线性拟合得到,光密度值代表细胞密度,曲线斜率变化代表生长速率。当EBR浓度小于15 mg/L时,随着EBR浓度升高,微拟球藻对数生长期不断延长。培养至第10天,15 mg/L EBR处理组光密度较5 mg/L处理组和对照组分别提高了6.44%和17.45%。由此可见,15 mg/L EBR对其生长促进最明显。而50 mg/L EBR对微拟球藻生长产生了抑制作用,培养仅至第4天,光密度就下降至初始值的47%,显微观察发现藻细胞已裂解。
与EBR不同,较对照组,本实验中所设3种浓度的GA3均能促进微拟球藻生长,对数生长期延长(图2)。培养10 d后,添加了5、15和50 mg/L GA3的处理组光密度分别比对照组高出 14.54%,17.51%和29.28%;50 mg/L GA3处理下光密度达到最大。说明GA3对微拟球藻的细胞增殖十分有效。

图1 不同浓度EBR对微拟球藻藻液光密度的影响
2.2 EBR和GA3对生物量、总脂含量及产油率的影响
本实验所设50 mg/L EBR显著抑制微拟球藻生长,藻液浓度过低,以致无法收集测定后续指标。如表1所示,添加较低浓度(5、15 mg/L)的EBR后,该藻生物量较对照组显著增加,分别增加了9.19%、13.97%,而总脂含量并未发生显著变化。综合生物量和总脂含量来看,添加5和15 mg/L EBR后该藻产油率较对照组分别增加了7.85%和13.97%。生物量增幅与产油率增幅相近,由此推测EBR对微拟球藻产油率的提高主要归功于其对该藻生物量积累的促进,并不影响单位质量藻细胞的总脂含量。
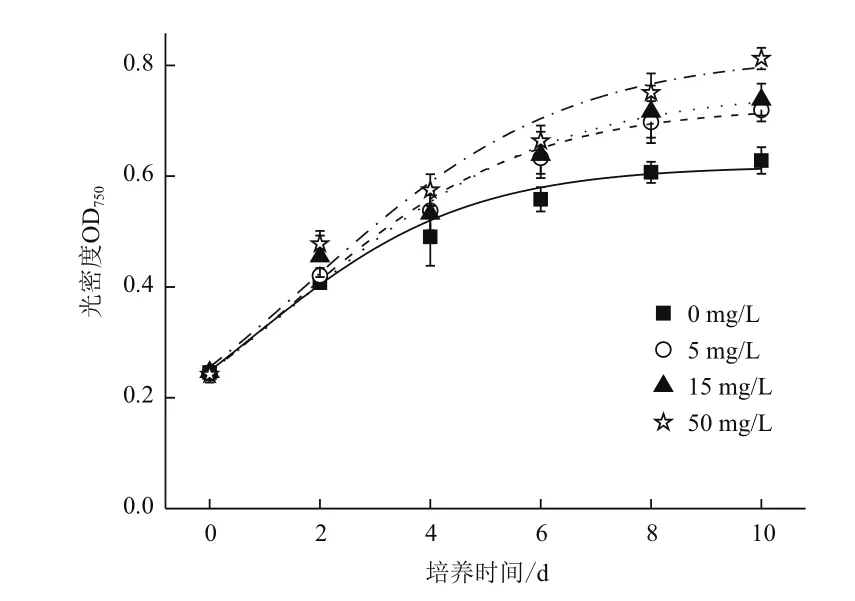
图2 不同浓度GA3对微拟球藻液光密度的影响
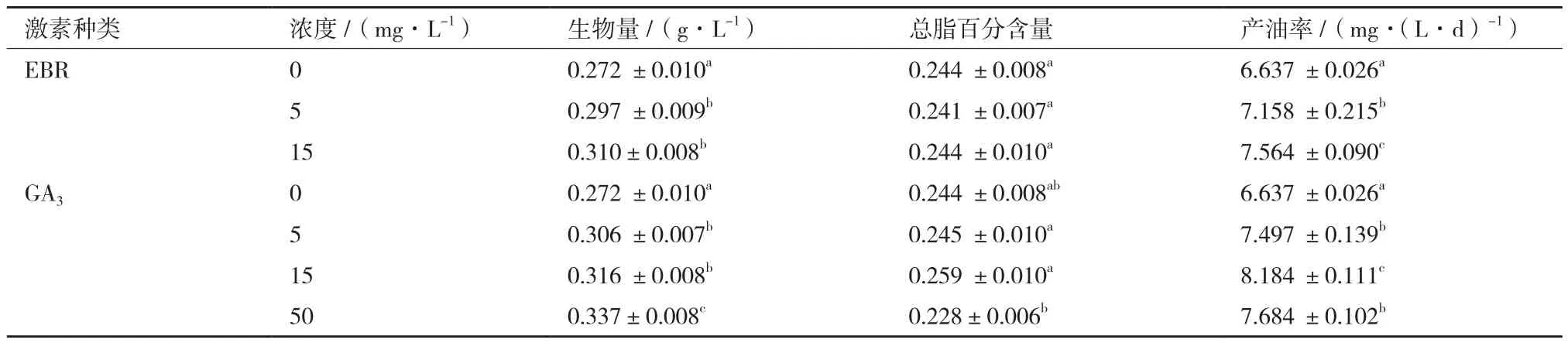
表1 EBR和GA3对微拟球藻生物量及总脂含量的影响
由表1可知,在实验浓度范围内,GA3处理组微拟球藻生物量较对照组显著提高,且随GA3浓度增加而增加;当GA3为50 mg/L时,生物量最高达0.337 g/L。而总脂含量与之不同,5、15、50 mg/L处理组较对照组均没有显著变化。综合生物量和总脂含量分析,产油率在GA3为15 mg/L时达到最大值(8.184 mg/(L·d)),显著高于对照组及5和50mg/L处理组。以上结果表明,实验所设浓度GA3均显著促进了微拟球藻生物量的积累,而对总脂含量影响不大。产油率的差异主要是来自GA3对微拟球藻生长的影响。总体来看,15 mg/L GA3对产油率提高效果最显著。
2.3 EBR和GA3对脂肪酸组成的影响
不同浓度EBR和GA3对微拟球藻脂肪酸组成的影响如表2和表3所示。与对照相比,不同浓度的EBR和GA3对14∶0(十四烷酸,其中14代表脂肪酸碳链长度,0代表双键的数量;以此类推)所占比例基本无影响,16∶0、16∶1、18∶1所占比例随着EBR和GA3浓度升高而显著降低,而18∶2、20∶4、20∶5(EPA)所占比例显著提高。特别是EPA含量显著提高,培养仅10 d,15和50 mg/L GA3处理组中其含量即分别达到了34.96%和36.34%。
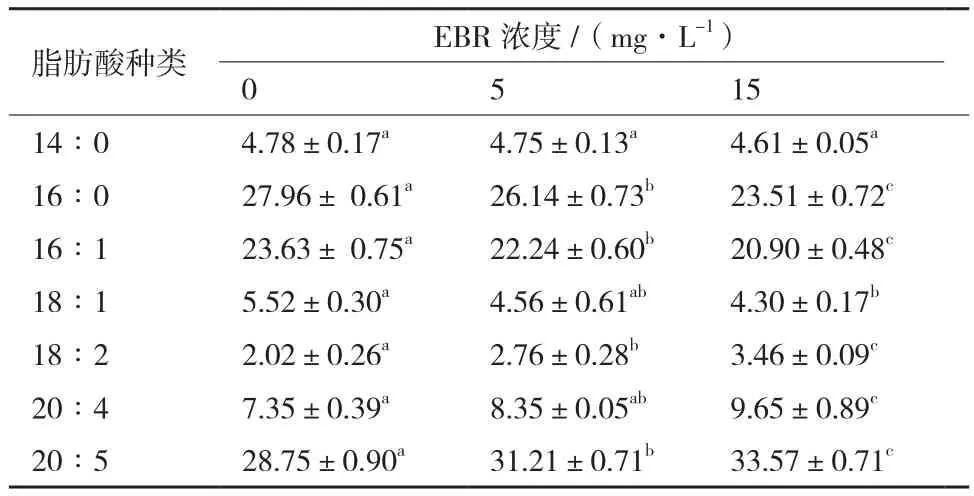
表2 EBR浓度对微拟球藻脂肪酸组成的影响
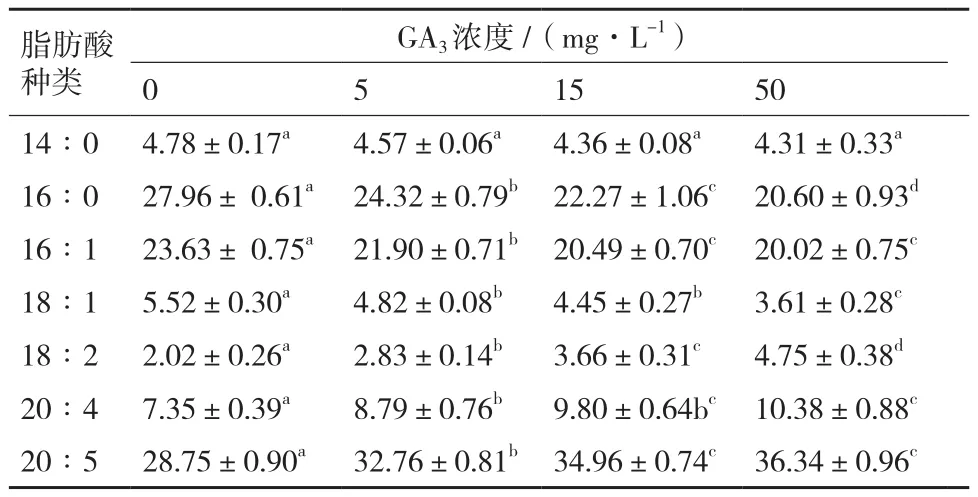
表3 GA3浓度对微拟球藻脂肪酸组成的影响
3 讨论
3.1 EBR和GA3对微拟球藻生长的影响
EBR是一种广谱、无毒的高活性植物激素,其最突出的作用是促进细胞伸长与分裂、促进植物光合作用及增加植物抗逆性[10-12]。范新照等[13]认为2 μmol/L EBR即可显著促进微茫藻(Micractinium sp.)生长;而10 μmol/L EBR则显著抑制其生长,最大生物量较对照组减少了72.83%。王小飞等[14]研究表明,在0-0.2 mg/L范围内,随EBR浓度升高,三角褐指藻(Phaeodactylum tricornutum)生物量呈先增后减之趋势。本实验发现,在5、15 mg/L时,EBR显著促进微拟球藻生长;而50 mg/L EBR则会抑制该藻生长。这与前人研究结果相似,但因不同藻种对EBR敏感性有差异,其最适作用浓度也不同。
GA3是重要的植物激素之一,其主要作用是促进细胞分裂。Falkowska等[15]研究了GA3对镉铅胁迫条件下普通小球藻(Chlorella vulgaris)的影响,结果表明,GA3可促进细胞增殖和光合色素及单糖的积累。Park等[16]发现,1 mg/L GA3对莱茵衣藻(Chlamydomonas reinhardtii)生长促进效果最显著。范新照等[13]使用GA3处理微茫藻后发现,1 μmol/L GA3对藻株生长有明显促进作用;增加GA3浓度至5 μmol/L 则会显著抑制该藻生长,其最大生物量比对照组减少了60.70%。据报道,在一定浓度范围(0.01-10 mg/L)内,随GA3浓度升高,其对铜绿微囊藻(Microcystis aeruginosa)生长促进越明显;浓度过高则会抑制其生长[17]。在本实验浓度范围内,GA3对微拟球藻生长促进效果也随GA3浓度增大而增强,这与低浓度EBR在其他藻中的作用效果相似。但本实验中浓度尚未达到抑制微拟球藻生长的临界值,更高浓度GA3的作用效果有待后期探索。
3.2 EBR和GA3对微拟球藻总脂含量及产油率的影响
除调节微藻生长外,适宜浓度EBR和GA3对其总脂含量也有显著影响。郝宗娣等[6]研究表明,EBR能显著提高原始小球藻(Chlorella protothecoides)的总脂含量。王小飞等[14]认为0.1 mg/L EBR能显著提高三角褐指藻的产量和总脂含量。本实验发现,EBR处理下的微拟球藻产油率和生物量是同步增加的,而单位质量藻细胞的总脂百分含量并未发生明显改变,推测EBR提高微拟球藻产油率是通过促进其细胞增殖实现的。
目前,GA3对微藻总脂含量影响的研究较少。据报道,1.0 μmol/L GA3处理下,微茫藻油脂含量较对照组有所降低;GA3浓度为5.0 μmol/L 时,其生物量降低但油脂含量却显著提高[13]。在本研究中,50 mg/L GA3虽促进了微拟球藻生物量积累,但显著抑制了单位质量藻细胞的总脂含量,而15 mg/L GA3处理下总脂含量和产油率达到最高,效果较好,且优于EBR处理组的效果。综上,适宜浓度GA3对于促进该藻生长、总脂积累作用显著。
3.3 EBR和GA3对微拟球藻脂肪酸组成的影响
多不饱和脂肪酸是形成生物膜的必备条件之一,在维持生物膜流动性中起关键作用[18]。此外,参与多个重要生理过程,如物质转运[19]和叶绿体形成[20]等。本实验中,添加EBR(5和15 mg/L)和GA3(5、15和50 mg/L)后,微拟球藻中饱和及单不饱和脂肪酸(16∶0、16∶1、18∶1)占比随浓度升高而逐渐下降,多不饱和脂肪酸(18∶2、20∶4、20∶5)占比则显著提高。培养10 d后,15和50 mg/L GA3处理组中EPA含量即分别达到了34.96%和36.34%。结果表明,一定浓度EBR和GA3可促进微拟球藻生长和油脂积累并优化其脂肪酸组成。EPA属于ω3系长链多不饱和脂肪酸,具有维持生物膜的结构和功能、预防心脑血管疾病、提高机体免疫力和改善视力等功效[21]。作为EPA主要来源,现有鱼油难以满足人们的持续需求[22],微拟球藻作为一类重要的经济微藻,在EPA生产上潜力巨大。
4 结论
本研究发现,5、15 mg/L EBR能显著促进微拟球藻生长和提高其产油率,但对单位质量藻细胞总脂含量影响不大。50 mg/L EBR则显著抑制该藻生长。5、15和50 mg/L GA3均显著促进微拟球藻生物量积累。15 mg/L GA3对微拟球藻产油率提升效果最显著。50 mg/L GA3处理组生物量最高,但总脂积累受到一定抑制。添加EBR和GA3浓度后,饱和和单不饱和脂肪酸占比下降,多不饱和脂肪酸占比显著提高。
[1]陈程浩, 吴嘉仪, 汤明星, 等. 八株海洋微藻Nannochloris sp. 生长及生化性状评价[J]. 生物技术通报, 2016(6):231-237.
[2]郭兵, 龚阳, 万霞, 等. 光强和温度对球等鞭金藻(Isochrysis sphaerica)生长及其脂肪酸的影响[J]. 中国油料作物学报,2011, 33(3):295-301.
[3]陈传红, 吴洪, 李青, 等. 三株栅藻属藻株光合自养产油脂的比较研究[J]. 生物技术通报, 2016, 32(6):238-243.
[4]刘菲菲, 冯慕华, 尚丽霞, 等. 温度对铜绿微囊藻(Microcystis aeruginosa)和鱼腥藻(Anabaena sp.)生长及胞外有机物产生的影响[J]. 湖泊科学, 2014, 26(5):780-788.
[5]Salama ES, Kabraa N, Ji MK, et al. Enhancement of microalgae growth and fatty acid content under the influence of phytohormones[J]. Bioresource Technology, 2014, 172:97-103.
[6]郝宗娣, 刘平怀, 时杰, 等. 不同植物激素对原始小球藻生长及油脂含量的影响[J]. 广东农业科学, 2012, 39(8):104-107.
[7]Ferreira M, Coutinho P, Seixas P, et al. Enriching rotifers with“premium” microalgae. Nannochloropsis gaditana[J]. Marine Biotechnology, 2009, 11(5):585-595.
[8]何文栋, 朱葆华, 等. 微拟球藻富油藻株筛选及柱状光生物反应器培养评价研究[J]. 水生生物学报, 2017, 4(5):1112-1117.
[9]Guillard RRL, Ryther JH. Studies of marine planktonic diatoms.I. Cyclotella nana Hustedt, and Detonula confervacea(cleve)Gran[J]. Canadian Journal of Microbiology, 1962, 8:229-239.
[10]张琳. 油菜素内酯的生理效应及发展前景[J]. 北方园艺,2011, 20:188-191.
[11]郑洁, 王磊. 油菜素内酯在植物生长发育中的作用机制研究进展[J]. 中国农业科技导报, 2014, 16(1):52-58.
[12]李辉, 左钦月, 涂升斌. 油菜素内酯生物合成和代谢研究进展[J]. 植物生理学报, 2015, 51(11):1787-1798.
[13]范新照, 费小雯, 吴小霞, 等. 植物生长调节剂EBR和GA3对微茫藻18A8(Micractinium sp.)生长和油脂积累的影响[J].热带农业科学, 2013, 33(2):4-8.
[14]王小飞, 张问, 等. 2, 4-表油菜素内酯对三角褐指藻生长及有机质积累的影响[J]. 植物生理学报, 2015, 9:1482-1488.
[15]Falkowska M, Pietryczuk A, Piotrowska A, et al. The effect of gibberellic acid(GA3)on growth, metal biosorption and metabolism of the green algae Chlorella vulgaris(Chlorophyceae)beijerinck exposed to cadmium and lead stress[J]. Polish Journal of Environmental Studies, 2011, 20(1):53-59.
[16]Park WK, Yoo G, Moon M, et al. Phytohormone supplementation significantly increases growth of Chlamydomonas reinhardtii cultivated for biodiesel production[J]. Applied Biochemistry &Biotechnology, 2013, 171(5):1128-1142.
[17]王勤. 植物生长调节剂对铜绿微囊藻(Microcystis aeruginosa)生长特性影响的研究[D]. 南京:南京农业大学, 2009.
[18]Chang YT, Chang MC, et al. Distinctive roles of unsaturated and saturated fatty acids in hyperlipidemic pancreatitis[J]. World J Gastroenterol, 2015, 21(32):9534-9543.
[19]Xiao YF, Ke Q, Wang SY, et al. Single point mutations affect fatty acid block of human myocardial sodium channel alpha subunit Na+channels[J]. Proc Natl Acad Sci USA, 2001, 98:3606-3611.
[20]Wallis JG, Browse J. Mutants of Arabidopsis reveal many roles for membrane lipids[J]. Prog Lipid Res, 2002, 41:254-278.
[21]李文宗, 王磊. 长链多不饱和脂肪酸EPA、DHA 的基因工程研究进展[J]. 生物技术通报, 2016, 32(8):1-7.
[22]胡亚平, 吴刚, 张丽, 等. 长链多不饱和脂肪酸的替代来源——转基因油料作物[J]. 生物技术通报, 2016, 6:1-6.

