热重-示差扫描量热法研究水热温度和浓度对CeO2结晶效果和模板炭化效率的影响
唐远征, 陈 丰, 陈志刚*
(1.苏州科技大学江苏省环境功能材料重点实验室,江苏苏州 215009;2.苏州科技大学化学生物与材料工程学院,江苏苏州 215009)
我国稀土元素储量丰富,而对稀土元素的研发与应用,促进了稀土资源的有效利用[1]。CeO2因晶型单一、光学性能和电学性能良好[2],被广泛应用于光催化材料[3]、防腐涂层、气体传感器、固体氧化物燃料电池等方面[4]。
生物炭是以生物物质为原料[5],在无氧或厌氧条件下进行热解产生含碳丰富的物质[6]。生物炭具备比表面积大、容量小、通气性好等优点[7]。CeO2负载在生物炭上可以同时具备CeO2和碳材料的各自优点[8],之前在此方面已有过报道[9]。然而如何控制条件以获得炭化效果好、CeO2结晶度高和保持生物形貌的材料仍是目前研究的难点[10]。针对此问题,本研究在之前的研究基础上,采用热重-示差扫描法量热(TG --DSC)技术研究了生物材料负载CeO2前驱体后,在氮气氛围中炭化分解的趋势和规律[11 - 12],研究了不同浓度的Ce(NO3)3与六次亚甲基四胺在不同温度下的水热结晶效果,以便为制备性能优异的CeO2/碳复合材料提供可靠的实验数据[13]。
1 实验部分
1.1 仪器、试剂及材料
SDTQ-600 TG -DSC联用仪(美国,TA仪器公司);GSL-1600r-Ⅲ管式炉(中美合资合肥科晶材料技术有限公司);S-4800场发射扫描电镜(SEM)(日本,Hitachi公司);D8 Advanced X-射线衍射仪(XRD)(德国,Bruke公司)。
无水乙醇(分析纯,国药集团化学试剂有限公司);HCl(分析纯,国药集团化学试剂有限公司);Ce(NO3)3·6H2O(分析纯,国药集团化学试剂有限公司);六次亚甲基四胺(分析纯,国药集团化学试剂有限公司);高纯N2(99.999%,苏州金宏气体股份有限公司)。实验用水为去离子水。
新鲜的竹叶(来自于校园)。
1.2 样品的制备
将新鲜的竹叶浸渍于50%的乙醇中,加入适量的HCl,调节溶液pH=2后,浸渍48 h。取出竹叶用去离子水清洗数次,重复浸渍2次。然后将竹叶浸泡在一定浓度的Ce(NO3)3及六次亚甲基四胺(Ce(NO3)3与六次亚甲基四胺摩尔比为2∶1)溶液中,并水热一定的时间。然后用去离子水清洗数次,在60 ℃的烘箱中烘干,留下部分样品进行TG -DSC测试。将其余样品在管式炉中于550 ℃(N2气氛,升温速率5 ℃/min)保温120 min进行煅烧,对所得到的样品进行SEM测试。分别制备了Ce(NO3)3前驱体浓度为0.05 mol/L、0.1 mol/L、0.15 mol/L和水热温度为80 ℃、120 ℃、160 ℃的样品。
1.3 TG -DSC实验
实验在TG -DSC 联用仪上进行。温度范围为20~800 ℃,升温速率为20 ℃/min,N2气流速为100 mL/min,试样测试前经过6 h的干燥。
2 结果与讨论
2.1 80 ℃水热温度下不同浓度试样的TG、DSC及SEM分析

图1 不同前驱体浓度下所制备样品的热重(TG)(a)和示差扫描量热(DSC)曲线(b)Fig.1 TG curves(a) and DSC curves(b) of the samples synthesized with different precursor concentrations

图2 前驱体浓度为0.1 mol/L(a)和0.15 mol/L(b)样品的扫描电镜(SEM)图Fig.2 SEM images of the samples synthesized with precursors at concentrations of 0.1 mol/L(a) and 0.15 mol/L(b)
图1(a)中所显示的是水热温度均为80 ℃,不同浓度Ce(NO3)3样品的TG曲线。图中可见,样品的失重主要分三个阶段:20 ℃到100 ℃左右为第一阶段,此阶段失重是由于试样中吸附的水分蒸发;第二阶段失重过程在250 ℃到370 ℃,试样的大部分失重主要发生在这个阶段,失重原因是由于试样中有机质的分解;最后一个失重阶段紧接着第二阶段到550 ℃,这个阶段失重是由试样发生炭化所引起。图1(b)是试样的DSC曲线,所有样品均在100 ℃的位置出现吸收峰,主要缘于模板内吸附水蒸发需要吸收热量。负载CeO2的试样在560 ℃位置出现放热峰,比空白样品放热峰的出峰位置提前大约100 ℃,这表明CeO2可以降低植物炭化反应温度。图1(a)中可以看到Ce(NO3)3为0.1 mol/L与0.15 mol/L的试样TG曲线基本重合。图1(b)可以得出两个不同浓度试样的DSC曲线形状基本相似。这说明80 ℃水热条件下,Ce(NO3)3浓度为0.1 mol/L与0.15 mol/L的竹叶模板负载CeO2数量相差不多,从图2的SEM图像也可以证实这一点。0.1 mol/L和0.15 mol/L浓度下获得的样品形貌几乎相同,复制了原模板的结构,且无颗粒分散在模板表面,因此选择0.1 mol/L作为合适的反应浓度,以避免原料的浪费。
2.2 120 ℃水热温度下不同浓度试样的TG、DSC及SEM分析
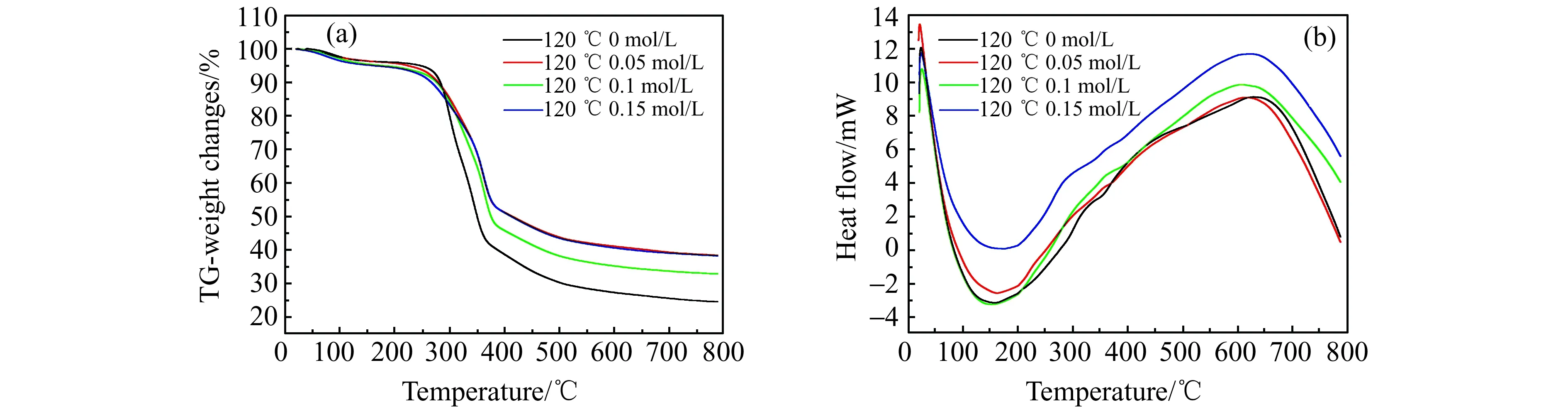
图3 不同前驱体浓度下所制备样品的热重(TG)(a)和示差扫描量热(DSC)曲线(b)Fig.3 TG curves(a) and DSC curves(b) of the samples synthesized with different precursor concentrations

图4 前驱体浓度为0.1 mol/L(a)和0.15 mol/L(b)样品的扫描电镜(SEM)图片Fig.4 SEM images of the samples synthesized with concentrations of 0.1 mol/L(a) and 0.15 mol/L(b)
图3(a)是水热温度为120 ℃,不同Ce(NO3)3浓度试样的TG曲线。失重过程同样主要分为水分蒸发、有机质分解和有机质炭化三个主要过程。图3(b)是水热温度为120 ℃,不同浓度Ce(NO3)3试样的DSC曲线。图中吸热峰的出峰位置在150 ℃,因为水热过程中Ce(NO3)3生成结晶的CeO2,模板已经被部分炭化,在碳和CeO2共同作用下使得部分细胞内的吸附水生成结晶水,结晶水的失去需要更高的温度。空白竹叶模板的DSC曲线放热峰的位置大概在625 ℃,负载CeO2的模板出峰位置在610 ℃左右,负载CeO2试样的放热峰出峰位置比起空白试样有少量提前,说明CeO2的负载可以提前模板的炭化温度。图4(a)是浓度为0.1 mol/L的试样的SEM图,可以看出竹叶表面有颗粒状的CeO2,且分布较均匀。图4(b)是浓度为0.15 mol/L的试样的SEM图,CeO2在竹叶的表面发生了团聚现象且分布的不均匀,CeO2的结晶效果不佳。通过图4(a)与图4(b)对比,可以得知水热温度为120 ℃,Ce(NO3)3浓度控制在0.1 mol/L,可以得到炭化后形貌较好且分布均匀的CeO2复合材料。
2.3 160 ℃水热温度下不同浓度试样的TG、DSC及SEM分析

图5 不同前驱体浓度下所制备样品的热量(TG)(a)和示差扫描量热(DSC)曲线(b)Fig.5 TG curves(a) and DSC curves(b) of the samples synthesized with different precursor concentrations
图5(a)所示是水热温度为160 ℃时,不同Ce(NO3)3浓度试样的TG曲线。失重包括三个阶段,第一阶段从起始温度到100 ℃左右,所有的试样的失重情况基本相同。比较失重的第二阶段,可以看出前驱体浓度高的试样失重起始点较早,失重的速率小,最终失重的比例小。这主要是水热温度为160 ℃,竹叶模板炭化量增多,较多的碳也促进了CeO2的生成,CeO2促进了植物内部有机质的分解,因此提前了植物有机质分解的温度。图5(b)是水热温度为160 ℃,不同浓度试样的DSC曲线。所有试样吸热峰的出峰位置大概在180 ℃,这是由于较高的水热温度促使试样炭化量增加,较多的碳与CeO2的结合从而使得试样内形成了较多的结晶水。浓度为0.05 mol/L和0.1 mol/L的试样在380 ℃有一个较小的吸热峰,浓度为0.15 mol/L的试样的吸收峰推后至500 ℃,原因是在160 ℃水热时,部分竹叶模板生成了无定型碳,这部分碳在高温的作用下渗透到CeO2晶格内,Ce(NO3)3浓度较低时形成的CeO2颗粒较小,碳容易渗透到CeO2晶格内,而Ce(NO3)3浓度较高时形成的CeO2颗粒较大,碳渗透到CeO2晶格内需要更高的能量,因此浓度为0.15 mol/L的试样的吸热峰会有所后移。图6(a)和图6(b)分别是浓度为0.1 mol/L和0.15 mol/L试样的SEM图,与图2和图4相比,可以看出较高的水热温度容易导致CeO2的团聚,不利于生物形貌的保留。
2.4 0.1 mol/L浓度下不同水热温度试样的TG和DSC曲线
图7(a)是浓度为0.1 mol/L,水热温度分别是80 ℃、120 ℃和160 ℃试样的TG曲线。失重可以分为水分蒸发、有机质分解和有机质炭化三个阶段。图中可以看出水热温度为80 ℃的试样在第一阶段的失重量最大,这可能是由于试样干燥未彻底所导致。图7(b)是浓度为0.1 mol/L,水热温度分别是80 ℃、120 ℃和160 ℃试样的DSC曲线。图中可以得知水热温度高的试样在100~200 ℃吸热峰出峰位置后移,这是因为越高的水热温度会使得竹叶模板发生炭化量增多,从而会有较多的吸附水形成结晶水,因此需要一个较高的温度才能使得结晶水去除。水热温度120 ℃和160 ℃的试样在400~700 ℃之间的放热峰出峰位置较水热温度为80 ℃试样的出峰位置推后,这也是由于水热温度高,已经使得试样中生物模板表面发生部分炭化,新的炭化要在材料内部进行,需要更高的能量,从而推后了炭化温度。水热温度为120 ℃和160 ℃的试样放热峰出峰位置大致相同,主要是由于较高的水热过程使模板发生了部分碳化和CeO2结晶,改变了材料的二次碳化能量。

图7 不同温度下所制备样品的热重(TG)(a)示差扫描量热(DSC)(b)曲线Fig.7 TG curves(a) and DSC curves(b) of the samples synthesized at different precursor temperatures

图8 不同温度条件下制备样品的X-射线衍射(XRD)图谱Fig.8 XRD images of the samples synthesized at different temperatures
2.5 0.1 mol/L浓度下不同水热温度试样的XRD谱图
图8所示的是浓度为0.1 mol/L,水热温度分别是80 ℃、120 ℃和160 ℃试样的XRD谱图。图中的2θ=28.5°、33.1°、47.5°、56.3°的衍射峰对应于立方萤石结构CeO2的(111)、(200)、(220)、(311) 晶面。材料中没有其它杂峰的出现,说明所获得产物不含其它杂质,纯度较高。水热温度80 ℃和120 ℃的试样与水热温度160 ℃的试样相比较,有较高的峰值,说明这两个温度下产物的结晶度相对较好。
3 结论
应用TG -DSC技术研究了生物模板负载CeO2的热解过程和热流变化情况,热解主要经历了3个阶段:水分蒸发阶段、有机质分解阶段和有机质炭化阶段。水分蒸发阶段伴随着热量的吸收过程,有机质分解和炭化阶段伴随着热量放出过程。水热温度高,试样在水热过程中发生炭化量增加,形成越多的结晶水。负载的CeO2可以降低植物发生炭化反应的温度。过高的水热温度不利于CeO2的结晶,过高的水热温度会使模板在水热过程中产生过多的炭化,使得所得到的CeO2发生团聚现象,不利于较好形貌的形成。过低的水热温度虽然可以得到结晶相对较高的CeO2,但也不能得到形貌较好的复合材料。因此,水热温度为120 ℃,浓度为0.1 mol/L的条件下,所制备的样品经炭化后能获得负载CeO2较均匀、结晶度较高且保持生物形貌的材料。
参考文献:
[1] ZHONG Q,HE Z,DAI A Q,et al.Journal of Agro-Environment Science(钟秋,何桢,戴安琪,等.农业环境科学学报),2012,31(2):299.
[2] Du X J,Jiang D,Chen S B,Dai L M,Zhou L,Hao N,You T Y,Mao H P,Wang K.Biosensors & Bioelectronics,2015,89(2017):682.
[3] Chen F,Wang W,Chen Z G,Wang T B.Journal of the Chinese Rare Earth Society,2012,30(4):350.
[4] Yang X P,Pan H P,Wang P,Zhao F J.Journal of Hazardous Materials,2012,322(2017):293.
[5] WANG R,HOU S L,ZHAO L X,et al.Renewable Energy Resources(王茹,侯书林,赵立欣,等.可再生能源),2013,31(6):91.
[6] LIN L Y,CHEN Z L,FU F.World Forestry Research(林兰英,陈志林,傅峰.世界林业研究),2007,20(5):22.
[7] LIU Z K,YE L J.Biomass Chemical Engineering(刘志坤,叶黎佳.生物质化学工程),2007,41(5):28.
[8] CHEN F,CHEN Z G,QIAN J C.Journal of Inorganic Materials(陈丰,陈志刚,钱君超.无机材料学报),2012,27(1):69.
[9] ZHAO X B,QIAN Q,CHEN Z G.Journal of the Chinese Ceramic Society(赵晓兵,钱前,陈志刚.硅酸盐学报),2011,39(2):263.
[10] Cao J,Xiao G,Xu X,Shen D K,Jin B S.Fuel Processing Technology,2012,106(2013):41.
[11] Xavier S,Periandy S,Carthigayan K,Sebastian S.Journal of Molecular Structure,2016,1125(2016):204.
[12] WANG L.Journal of Yunnan Nationalities University(王琳.云南民族大学学报),2014,23(1):35.
[13] Cui M Y,Yao X Q,Dong W J.Journal of Crystal Growth,2010,312(2):287.

