碳酸二甲酯与苯酚酯交换反应动力学研究
顾凯杰,朱志庆,沈卫华,方云进
(1.华东理工大学 化学工程联合国家重点实验室,上海 200237;2.华东理工大学 化工学院,上海 200237)
甲基苯基碳酸酯(MPC)与苯酚反应或者经自身歧化反应可以合成碳酸二苯酯(DPC)[1-2],而DPC是一种重要的有机化工中间体,用于合成许多重要的有机化合物及高分子材料,也可广泛用作溶剂、增塑剂和载热体等,特别是能替代光气与双酚A反应合成性能优良的聚碳酸酯(PC)[3]。目前,合成MPC的主要方法是碳酸二甲酯(DMC)与苯酚经酯交换反应合成[4-5]。该酯交换反应的平衡常数很小(约10-4),即使提高温度,其转化率和选择性也不高[6]。因此,目前大多数研究者采用反应精馏的方法,打破反应平衡,从而得到较高的产率。
对于DMC与苯酚的酯交换反应,众多研究者着重于催化剂的研究[7-10],对其动力学研究少有报道。Haubrock等[11-12]以钛酸四丁酯为催化剂,研究DMC与苯酚在160~200 ℃的反应动力学,分别求解得到DMC与苯酚生成MPC的反应和MPC与苯酚生成DPC反应的Van’t Hoff方程,以及上述反应的活化能,但文中涉及的反应较多,产物复杂,得出两个反应的熵都为负值。Yin等[13-14]以二丁基氧化锡为催化剂,采用反应精馏的方法探究了酯交换反应的动力学,由于有多种催化剂与反应物生成了中间体,导致DMC与苯酚酯交换反应的动力学更加复杂,没有求得反应的活化能以及相关的平衡数据。
本工作通过增大DMC的浓度,简化酯交换反应过程,研究了DPC与苯酚反应生成MPC的反应动力学,对于研究酯交换两步法合成DPC具有重要的指导意义。
1 实验部分
1.1 原料
苯酚:分析纯,上海凌峰化学试剂有限公司;DMC:纯度大于等于99.5%(w),山东东营海科新源化工有限责任公司。
1.2 实验方法和步骤
反应在配有取样器的2 L密闭高压反应釜(QCF型反应釜,山东威海环宇化工机械有限公司)中进行。在反应釜中加入一定量的DMC与苯酚,检漏确保密闭,通入氮气置换反应釜内的空气。开启搅拌,转速控制在500 r/min,加热升温至所需的反应温度时,用氮气将催化剂压入釜内并开始计时,同时充氮气至反应釜压力为1.5 MPa,若压力升高,可通过调节阀排出一些氮气,使得反应釜压力稳定在1.5 MPa。在反应过程中定时取液相试样(由于反应液体积约占反应釜总体积的2/3,通过估算得知气相中的组分量可以忽略),取样时慢慢打开高压釜上的取样阀,阀后接冷凝管,使得液相试样不闪蒸汽化,先放掉一定体积的液相物料(取样管中的液体),取反应釜中的物料,分析液相中各组分浓度的变化。
1.3 分析方法
GC7900型气相色谱仪:上海天美科学仪器有限公司。分析条件:OV-1701型毛细管柱(30 m×0.32 mm×0.3 μm),FID检测,载气为高纯氮气,压力0.03 MPa,空气压力0.015 MPa,氢气压力0.01 MPa,尾吹0.03 MPa,柱温200 ℃,汽化室温度260 ℃,检测器温度260 ℃,进样量0.4 μL。以苯乙酮为内标物进行定量分析。
2 动力学分析
DMC与苯酚合成MPC的反应方程见式(1)。

采用钛酸四丁酯为原料,通过乙酰化法制得有机钛化合物(简称钛催化剂),将其作为苯酚与DMC反应的催化剂。该钛催化剂具有以下优点:1)均相催化剂,不存在内外扩散的影响。2)该催化剂对生成MPC的选择性高达99%以上,在动力学实验中可忽略生成副产物的影响。3)该催化剂耐水性好,稳定不易水解。
从反应热力学分析,DMC与苯酚生成MPC的化学平衡常数约为10-4,相比之下MPC与苯酚生成DPC的化学平衡常数约为10-5。而MPC歧化生成DPC的化学平衡常数约为10-1,也是个可逆反应,移走产物能促进歧化反应的进行,因此MPC的歧化反应在负压下进行有利于移走产物之一的DMC,能大大提高MPC的转化率;而本实验采用加压,并且DMC过量,可以保证在动力学上对MPC歧化反应不利,避免生成DPC。在实验过程中通过对液相试样的气相色谱分析,只发现痕量的DPC。因此,综合反应的热力学和动力学分析,在DMC与苯酚摩尔比为10∶1的情况下,主要以生成MPC的酯交换反应为主,其他副反应可以忽略。
3 结果与讨论
3.1 催化剂用量的影响
在原料配比n(DMC)∶n(苯酚)= 10∶1、反应温度为443 K条件下,通过改变催化剂用量测定苯酚转化率随反应时间的变化,结果见图1。由图1可见,在催化剂用量大于0.28%(w)时,苯酚转换率随时间的变化较小,因此,选择催化剂用量为0.28%(w)。

图1 催化剂用量对苯酚转化率的影响Fig.1 Effects of catalyst dosage on the conversion of PhOH.
3.2 反应温度的影响
改变反应温度测定苯酚转化率随反应时间的变化,结果见图2。在加入催化剂之前,未检测到MPC的生成,表明DMC与苯酚并未发生反应。由图2可见,加入催化剂后,反应速度很快,即使在较低的反应温度下,反应时间大于30 min后即达到了平衡。反应液中各物质的浓度随时间的变化见图3。

图2 反应温度对苯酚转化率的影响Fig.2 Effect of temperature on the conversion of PhOH.
根据反应时间为60 min时各组分浓度随温度的变化及化学反应计算反应的平衡常数,结果见表1。从表1可见,DMC与苯酚生成MPC的反应平衡常数非常小,且随温度的升高增加不显著,因此,在热力学上,非常不利于反应的进行。

图3 反应液中各物质的浓度随时间的变化Fig.3 The concentration of substances in the reaction fluid varies with time.

表1 不同温度下达到反应平衡后各物质的质量分数Table 1 Mass fraction after reaction equilibrium at different temperature
由Van’t Hoff方程(式(2))可得平衡常数与温度的关系(见图4)。

由图4可知,平衡常数与温度的线性相关性良好。由斜率计算得反应热ΔH = 35.95 kJ/mol,表明这是一个吸热反应。由截距计算得反应熵变ΔS =12.72 J/(mol·K)。

图4 温度与反应平衡常数的关系Fig.4 The relationship of temperature and K.
3.3 动力学模型
DMC与苯酚的酯交换反应是一个平衡常数很小的可逆反应。考虑到温度对反应液密度的影响,采用Aspen Plus数据库,物性方法为NRTL,压力为1.5 MPa,根据不同温度下平衡反应液的组成,模拟计算得到的反应液密度见表2。

表2 不同温度下的液相密度Table 2 The liquid density(ρ) at different temperature
在反应过程中MPC与DMC和苯酚的浓度关系见式(3)。

实验采用的动力学模型表达式见式(5)。

采用二级均相动力学模型,则式(5)可化简为:

3.4 模型参数估计
在反应温度为438~463 K、催化剂用量0.28%(w)、反应压力1.5 MPa的动力学实验条件下,采用Matlab中的最小二乘非线性估算方法Lsqnonlin,根据不同时刻苯酚转化率随时间变化的实验值与估算值残差平方和最小的原则,得出不同温度下的反应速率常数,结果见表3。
根据阿伦尼乌斯方程lnk+= lnA-Ea/RT,将反应速率常数k+与1/T作图,结果见图5。从图5可看出,反应速率常数k+与1/T呈线性关系,分别由斜率和截距计算得到反应活化能为57.70 kJ/mol,指数前因子为2.70×103L/(mol·min)。根据平衡常数与反应速率常数的关系K = k+/k-,可得逆反应的活化能和指数前因子分别为21.78 kJ/mol和6.08×102L/(mol·min)。

表3 不同温度下的反应速率常数Table 3 Calculated reaction rate constants at different temperature
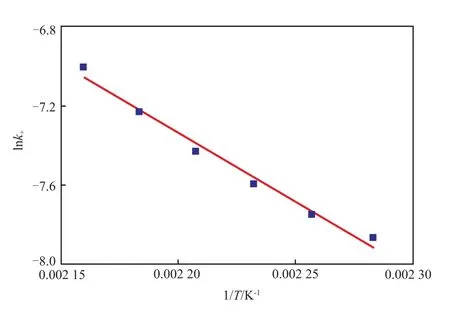
图5 温度与正反应速率常数的关系Fig.5 Relationship of temperature and positive reaction rate constant.
3.5 模型检验
对DMC与苯酚反应生成MPC的动力学进行统计学检验,其回归结果的显著性检验指标采用决定性指标ρ2和F检验来衡量[15-16]。具体计算公式见式(7)~(8)。
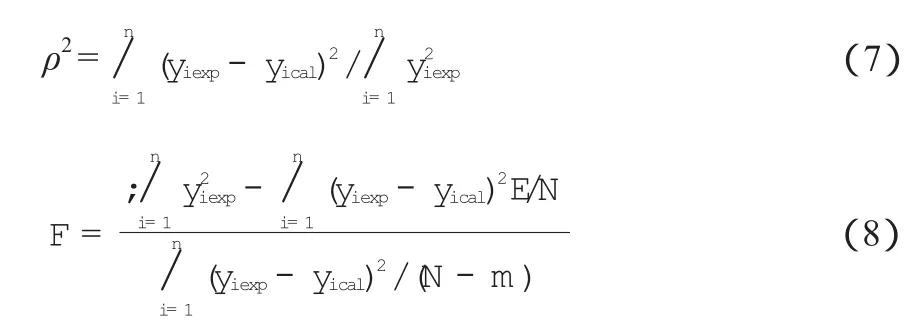
统计结果显示,动力学方程的ρ2= 0.996,F =289,F0.01= 3.53。 一 般 ρ2> 0.90,F > 10F0.01时,可认为拟合的模型方程是显著的。因此,在实验考察的范围内,该动力学模型能较好地描述DMC与苯酚酯交换生成MPC的反应。
4 结论
1)在438~463 K条件下,DMC与苯酚酯交换反应平衡常数的数量级为10-4,反应热为35.95 kJ/mol,是吸热反应。
2)将0.28%(w)的钛催化剂用于DMC与苯酚酯交换生成MPC的反应,所得二级动力学方程对实验数据拟合良好。
3)DMC与苯酚酯交换反应生成MPC的正、逆反应均为二级反应,正反应活化能为57.70 kJ/mol,指数前因子为 2.70×103L/(mol·min);逆反应活化能为21.78 kJ/mol,指数前因子为6.08×102L/(mol·min)。
符 号 说 明
A 指数前因子,L/(mol·min)
a,b,d,e 各物质的反应级数
c 浓度,mol/L
Ea活化能,kJ/mol
ΔH 反应热,kJ/mol
K 反应平衡常数
k+,k-正、负反应速率常数,mol/(L·min)M 摩尔质量,g/mol
m 变量个数
N 实验个数
R 气体常数,J/(mol·K)
ΔS 反应熵,J/(mol·K)
T 温度,K
t 时间,min
w 质量分数,%
X 转化率,%
yiexpi物质的实验值
yicali物质的计算值
ρ 密度,g/mL
下角标
DMC 碳酸二甲酯
MPC 甲基苯基碳酸酯
MeOH 甲醇
PhOH 苯酚
[1] 高俊杰,姚洁,王公应. 钛酸酯催化碳酸二甲酯与苯酚酯交换反应的研究[J].催化学报,2001,15(4):21-24.
[2] 冯东,农洁静,张政. 非光气法合成碳酸二苯酯的热力学与催化剂研究进展[J].材料导报,2015,29(21):68-74.
[3] 殷霞,马飞,李建国. 碳酸二甲酯与苯酚反应动力学及工艺研究进展[J].化学工程,2013,41(12):1-4.
[4] 王胜平,马新宾,刘戈. 碳酸二苯酯合成研究的进展[J].石油化工,2002,31(1):53-57.
[5] 牛红英,杜治平,康涛. 碳酸二甲酯和苯酚酯交换合成碳酸二苯酯的研究进展[J].石油化工,2006,35(2):191-196.
[6] Gong Jinlong,Ma Xinbin,Wang Shengping. Phosgene-free approaches to catalytic synthesis of diphenyl carbonate and its intermediates[J].Appl Catal,A,2007,316(1):1-21.
[7] Wang Qiang,Li Chunhong,Guo Ming,et al. Transesterification of dimethyl carbonate with phenol to diphenyl carbonate over hexagonal Mg(OH)2nanoflakes[J].Inorg Chem Front,2014,2(1):47-54.
[8] Zhou Xi,Ge Xin,Tang Rongzhi,et al. Preparation and catalytic property of modified multi-walled carbon nanotubesupported TiO2for the transesterification of dimethyl carbonate with phenol[J].Chin J Catal,2014,35(4):481-489.
[9] 唐荣芝,王松林,张元卓. 乙酸氧钛对碳酸二甲酯与苯酚酯交换的催化作用[J].高等学校化学学报,2014,35(11):2444-2450.
[10] 范大鸿,朱志庆,方云进. PbO/SiO2催化酯交换合成甲基苯基碳酸酯[J].石油化工,2015,44(5):581-585.
[11] Haubrock J,Raspe M,Versteeg G F,et al. Reaction from dimethyl carbonate to diphenyl carbonate. 1. Experimental determination of the chemical equilibria[J].Ind Eng Chem Res,2008,47(24):9854-9861.
[12] Haubrock J,Wermink W,Versteeg G F,et al. Reaction from dimethyl carbonate(DMC) to diphenyl carbonate(DPC). 2. Kinetics of the reactions from DMC via methyl phenyl carbonate to DPC[J].Ind Eng Chem Res,2008,47(24):9862-9870.
[13] Yin Xia,Zeng Yi,Yao Jie,et al. Kinetic modeling of the transesterification reaction of dimethyl carbonate and phenol in the reactive distillation reactor[J].Ind Eng Chem Res,2014,53(49):19087-19093.
[14] 倪峰,田恒水,朱云峰. 酯交换法合成碳酸二苯酯的工艺进展[J].广东化工,2008,35(8):44-47.
[15] 邵健强,赵玲,奚桢浩. 甲基苯基碳酸酯歧化反应工艺及动力学研究[J].石油化工,2016,45(10):1167-1171.
[16] 张卿,李涛,郑起. FBD变换催化剂反应动力学 Ⅰ. 本征动力学研究[J].华东理工大学学报:自然科学版,2003,29(3):217-220.

