尿微量白蛋白检测试剂盒性能验证
冯洋
尿微量白蛋白(microalbuminuria,mALB)是指尿液中白蛋白超过正常水平、但低于常规试带法可检出的范围,是评价肾功能的常见指标[1-2]。相对分子质量大于70 000的大分子溶质不能通过肾小球滤过膜,69 000的白蛋白则几乎不能通过滤过膜,即便有通过的也在肾小管被全部重吸收;但当肾小球滤过功能受损、肾小管重吸收的能力受限时,尿液中mALB含量就会升高。因此mALB的升高对诊断早期或轻微肾损害具有重要的提示作用。mALB检测方法较多,试剂质量也参差不齐。本研究旨在验证Orion免疫比浊法检测mALB的方法学性能是否满足临床需求。
1 材料与方法
1.1 仪器 采用OLYMPUS公司生产的AU640型全自动生化分析仪。
1.2 试剂、校准品、质控品 Orion附带校准品的微量白蛋白测定试剂盒,批号为1687202和1767794;质控品由上海市临床检验中心提供,批号分别为高值M1303和低值M1301。
1.3 标本来源 采集本院就诊患者或正常体检者的新鲜尿液;生理盐水为市售医用品。
1.4 验证实验方法
1.4.1 精密度验证实验 参考国家卫生和计划生育委员会发布的行业标准(WS/T)492-2016文件《临床检验定量测定项目精密度与正确度性能验证》进行精密度验证[3]。选择2个不同浓度的质控品,每天分析1批,连续测定5 d,每批分高、低2个浓度水平,每个浓度水平同一样品重复测定3次;如果出现失控,则应删除数据并重新测定。将以上检测结果根据公式进行统计分析,分别计算批内变异系数(CV批内)、批间变异系数(CV批间)、批内标准差(S批内)和批间标准差(S批间)。
1.4.2 正确度验证实验 参考WS/T 492-2016文件进行正确度验证。选择2个与定标校正品不同批号的原厂校正品,每天重复测定2次,连续测定5 d,计算均值、标准差以及置信区间,以验证指定值。
1.4.3 线性范围验证实验
1.4.3.1 参照美国临床和实验室标准(the Clinical and Laboratory Standards Institute,CLSI)EP6-A2 文件[4],挑选新鲜高值和低值临床尿液样本各1份,挑选的高值样本白蛋白含量应与试剂盒标称线性范围上限尽可能相符。按照10L、2H+8L、4H+6L、6H+4L、8H+2L、10H将高值和低值样本配制为6个浓度,用OLYMPUS AU640型全自动生化分析仪对6个浓度的尿液样本进行分析,每个浓度在同一批次重复测定2次。
1.4.3.2 对检测结果进行统计,计算每个浓度2次测定的均值。将横坐标定义为理论值,纵坐标定义为实测值的均值,绘制散点图。观察实验所得到的数据,看是否存在较明显的非线性或离群点,如存在,应查找原因。若有明确原因,纠正后修正数据;若无明显原因,则应重新检测全部数据。
1.4.3.3 根据公式计算SDr。
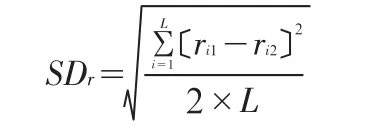
式中,L代表样本数,ri1与ri2代表两次测定的实际结果。
1.4.3.4 将SDr与设定的不精密度目标进行比较,本次试验以美国疾病控制与预防中心(Centers for Disease Control and Prevention,CDC)和美国医疗保险和医疗补助服务中心(Centers for Medicare and Medicaid Services,CMS)发表的临床实验室修正法规1988(CLIA'88)中规定的允许误差的1/4为不精密度目标。如果SDr大于设定目标,则可能是不精密度欠佳,不能可靠地评价线性关系。此时应检查生化仪或操作流程,找到引起不精密度欠佳的原因,
纠正后重新进行实验。如果方法性能与以前评估重复性时一致,重复测量次数增多1倍(4次),这样可以将均值的标准差降低约40%。
1.4.3.5 进行回归分析,计算一阶、二阶、三阶回归方程及回归标准误。利用t检验对二阶(b2)、三阶(b2、b3)回归系数进行检验,如果3个回归系数与0比较差异均无统计学意义(均P>0.05),则可认定其为一级线性,若有统计学意义则判断为非线性。若为非线性,则应比较各标准误大小,选择标准误最小者为最适多项式,并分析最适多项式在各个浓度上的线性偏差(deviation from linearity,DL)。
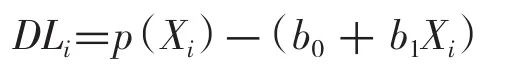
1.4.4 参考区间验证实验 参考CLSI C28-A2文件[5],抽取20例健康体检合格者作为甲组,其测定值如果有18例及以上在设定的参考值范围内,即95%以上,则设定的参考区间便可以接受;如果低于95%,则需重新抽取另外20例健康体检合格者作为乙组再次检测。若乙组的测定结果95%以上在所设定的参考范围内,则仍然可以认为验证有效;若乙组有超过2例在参考区间以外,则应首先判断检测程序、检测系统性能是否可靠,然后再分析人群生物特性是否可能对该项目的参考区间验证产生影响,重新选定合适的生物参考区间,必要时可自建生物参考区间。
1.5 统计学处理 采用SPSS 16.0统计软件和Excel 2003对检测数据进行处理。
2 结果
2.1 精密度验证结果 共检测10个标本。高浓度水平、低浓度水平质控品的CV批内分别为0.7%和1.0%,CV批间分别为1.5%和1.8%。CLIA'88允许误差为10%,CV批内均小于CLIA'88允许误差的1/4;CV批间均小于CLIA'88允许误差的1/3。
2.2 正确度验证结果 共检测10个标本。高浓度水平校正品靶值为87 mg/L,均值为86.8 mg/L,标准差为0.34 mg/L,上置信限为87.1 mg/L,下置信限为86.4 mg/L,置信区间包括靶值;低浓度水平校正品靶值为24 mg/L,均值为23.9 mg/L,标准差为0.29 mg/L,上置信限为24.2 mg/L,下置信限为23.6 mg/L,置信区间包括靶值。因此可以证实正确度。
2.3 线性范围验证结果 共检测12个标本。实验未发现明显的非线性和离群值,SDr小于不精密度目标。对二阶(b2)、三阶(b2、b3)回归系数的 t检验结果显示,回归系数与0比较差异均无统计学意义(均P>0.05),判断为一次方程呈线性。其线性范围评价 r=0.999 5,r2=0.998 9,预期值与实测值之间的相关性良好。回归方程为y=1.001 6x+2.142,说明书的线性范围为6~150 mg/L,验证线性范围为6.45~151.40 mg/L。
2.4 参考区间验证结果 20例实验对象的结果均在现行参考区间内,因此可判定现行参考区间有效。现行参考区间为0~20 mg/L,验证参考区间为7.8~11.7 mg/L。
3 讨论
白蛋白的相对分子质量为69 000,带负电荷,是肾小球在发挥其滤过作用时所能允许通过的最大相对分子质量的蛋白质之一,主要由肝脏分泌,经肾小球滤过的白蛋白在近曲小管基本全部被主动重吸收,重吸收后的尿液中只存有很少的白蛋白,通常在随机尿样本中的含量<20 mg/L。如果肾小球基底膜发生病变,通过肾小球的白蛋白大量增加,使得肾小管无法全部重吸收时,尿中的白蛋白将会增加[6]。mALB对于早期诊断具有重要意义,研究表明,mALB既是评估高血压性肾病[7]和糖尿病性肾病[8]的早期敏感指标,还已被证实是心血管系统疾病的重要危险因子[9-10],同时mALB也是血管内皮细胞功能受损的标志,能够预测大血管病变[11]。另外,mALB对于监控肾移植术后感染[12]及重症过敏性紫癜的治疗[13]也有一定的意义。
当随机尿样本中白蛋白浓度为20~150 mg/L时,由于低于尿常规试带法的可检出范围,常常导致其无法检出,因此需要使用其他方法对mALB进行检测。mALB的检测方法较多,如放射免疫法、化学发光法、酶联免疫吸附试验(enzyme linked immunosorbent assay,ELISA)、免疫比浊法等。目前放射免疫法被认为是检测mALB的金标准,这种方法应用最早,灵敏度和准确性较好[14],但缺点是使用的仪器较贵,且存在放射性污染的问题,在临床应用上具有局限性。化学发光法是近年新兴的方法,这种方法的灵敏度和准确性也较好,但缺点是成本较高。ELISA法虽然成本较低,但操作繁琐,影响因素较多,结果的可靠性较差。免疫比浊法是mALB测定的常用方法,其理论基础是抗原、抗体在特殊缓冲液中能迅速形成抗原-抗体复合物,成为均匀分散于反应体系中的颗粒,这些颗粒具有光学特性,可使反应体系在浊度仪下出现度数,如果在反应体系中加入过量的抗体,随抗原量增加形成的复合物也会增加,反应体系的浊度亦随之增加[15]。免疫比浊法根据浊度仪检测的反应体系是透射光还是散射光而分为免疫透射浊度法和散射浊度法。其中免疫透射浊度法测定透射光,依据的是朗伯-比尔定律;而免疫散射浊度法测定散射光,依据的是雷莱定律。免疫透射比浊法具有仪器构造简单、检测迅速、结果可靠、易实现自动化等优点,可整合在生化分析仪上,目前国内外生产厂商生产的生化分析仪都有免疫透射比浊功能,方法易于普及[16];而免疫散射比浊法需要特殊的免疫散射比浊仪,很难整合在全自动生化分析仪上,目前国内临床检验工作中主要在既时检验(point of care testing,POCT)中使用。
Orion mALB检测试剂盒是利用免疫透射比浊法检测mALB。本资料经过对Orion mALB检测试剂盒性能的验证发现,该试剂盒的正确度高,精密度好,线性范围符合说明书要求,参考区间有效。该试剂盒在OLYMPUS AU640全自动生化分析仪上能满足临床检验的要求。
1 熊立凡.临床检验基础[M]. 3版.北京:人民卫生出版社,2006:132.
2 黄耀东.糖化血红蛋白和尿微量白蛋白的联合检测在2型糖尿病肾病早期诊断中的临床研究[J].实用检验医师杂志,2017,9(2):83-85.
3 中华人民共和国国家卫生和计划生育委员会.WS/T 492-2016临床检验定量测定项目精密度与正确度性能验证[S].北京:中国标准出版社,2016.
4 Clinical and Laboratory Standards Institute. EP6-A2. Evaluation of the linearity of quantitative measurement procedures[S]. Wayne,PA:CLSI,2003.
5 Clinical and Laboratory Standards Institute. C28-A2. How to define and determine reference intervals in the clinical laboratory[S].Wayne,PA:CLSI,2000.
6 刘国娣.尿蛋白分析在肾脏疾病中的临床价值[J].实用检验医师杂志,2017,9(3):159-162.
7 王慧珍.高血压性肾病的早期诊断及临床意义[J].中华危重病急救医学,2000,12(4):216-216.
8 李艳,张家明,卓少贤,等.尿液微量蛋白4项检测对糖尿病肾病的早期诊断价值[J].实用检验医师杂志,2017,9(3):156-158.9 Verdecchia P,Reboldi GP. Hypertension and microalbuminuria: the new detrimental duo[J]. Blood Press, 2004,13(4):198-211.
10 Wang TJ,Evans JC,Meigs JB,et al. Low-grade albuminuria and the risks of hypertension and blood pressure progression[J].Circulation, 2005,111(11):1370-1376.
11 Gschwend S,Pinto-Sietsma SJ,Buikema H,et al. Impaired coronary endothelial function in a rat model of spontaneous albuminuria[J].Kidney Int, 2002,62(1):181-191.
12 涂金鹏,郑虹.肾移植术后丙型肝炎病毒感染的治疗[J/CD].实用器官移植电子杂志,2015,3(4):249-252.
13 黄玉辉,胡宝金,傅睿,等.血液灌流联合血液透析治疗重症过敏性紫癜的临床研究[J].中国中西医结合急救杂志,2010,17(6):349-351.
14 鲍利民,齐若梅,高欣,等.ELISA法检测尿微量白蛋白的临床应用与评价[J].中国卫生检验杂志,2006,16(2):227-228.
15 段玉东,桑俊军,闫海鹏,等.散射比浊法和透射比浊法测定血浆免疫蛋白的比较[J].中国医药导报,2008,5(2):87.
16 贾宁人,吴家明,芮志莲,等.颗粒增强免疫透射比浊测定血中Cyst C全自动分析法的建立与评价[J].放射免疫学杂志,2006,19(5):423-426.

